文档内容
2024年高一上学期化学月考试卷
一、单选题(每题3分,共48分)
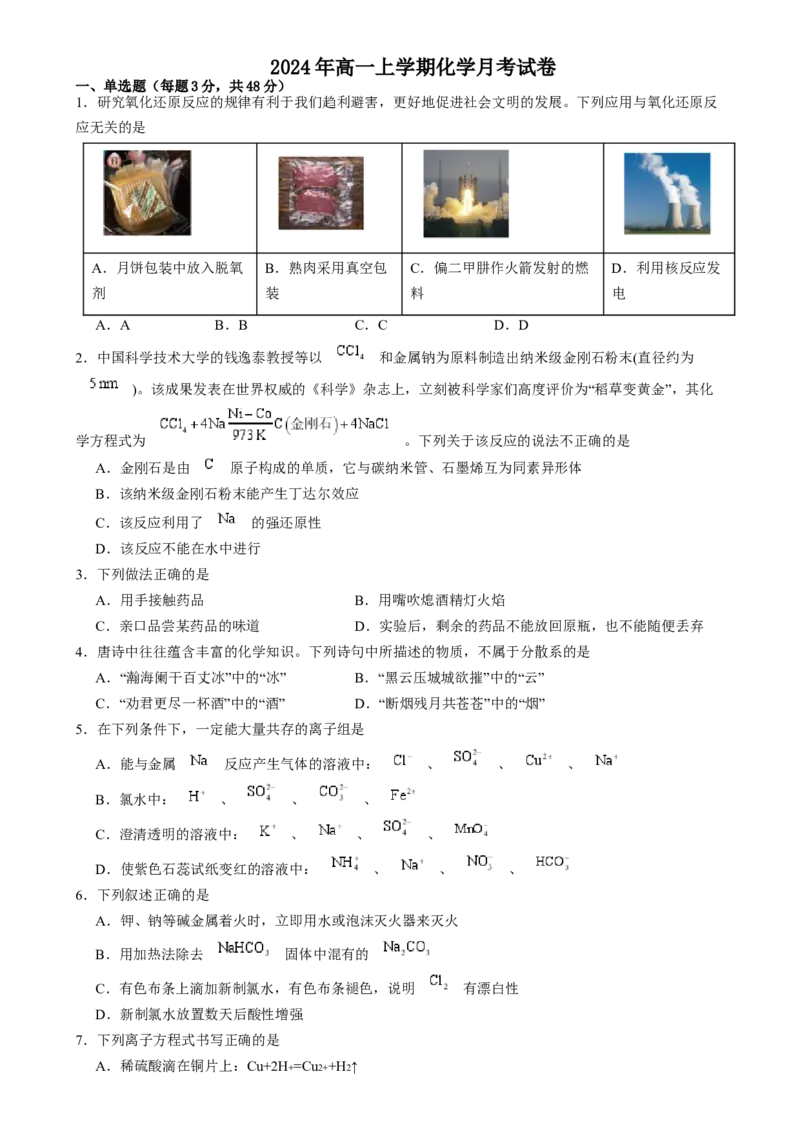
1.研究氧化还原反应的规律有利于我们趋利避害,更好地促进社会文明的发展。下列应用与氧化还原反
应无关的是
A.月饼包装中放入脱氧 B.熟肉采用真空包 C.偏二甲肼作火箭发射的燃 D.利用核反应发
剂 装 料 电
A.A B.B C.C D.D
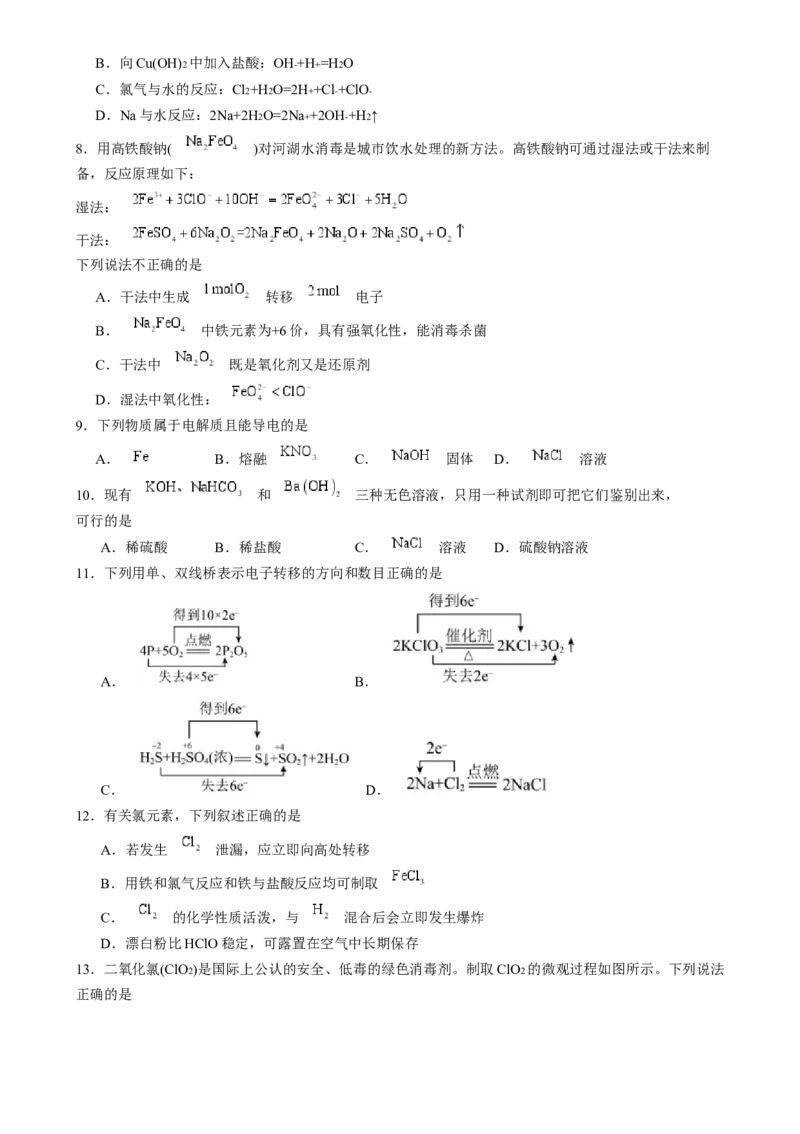
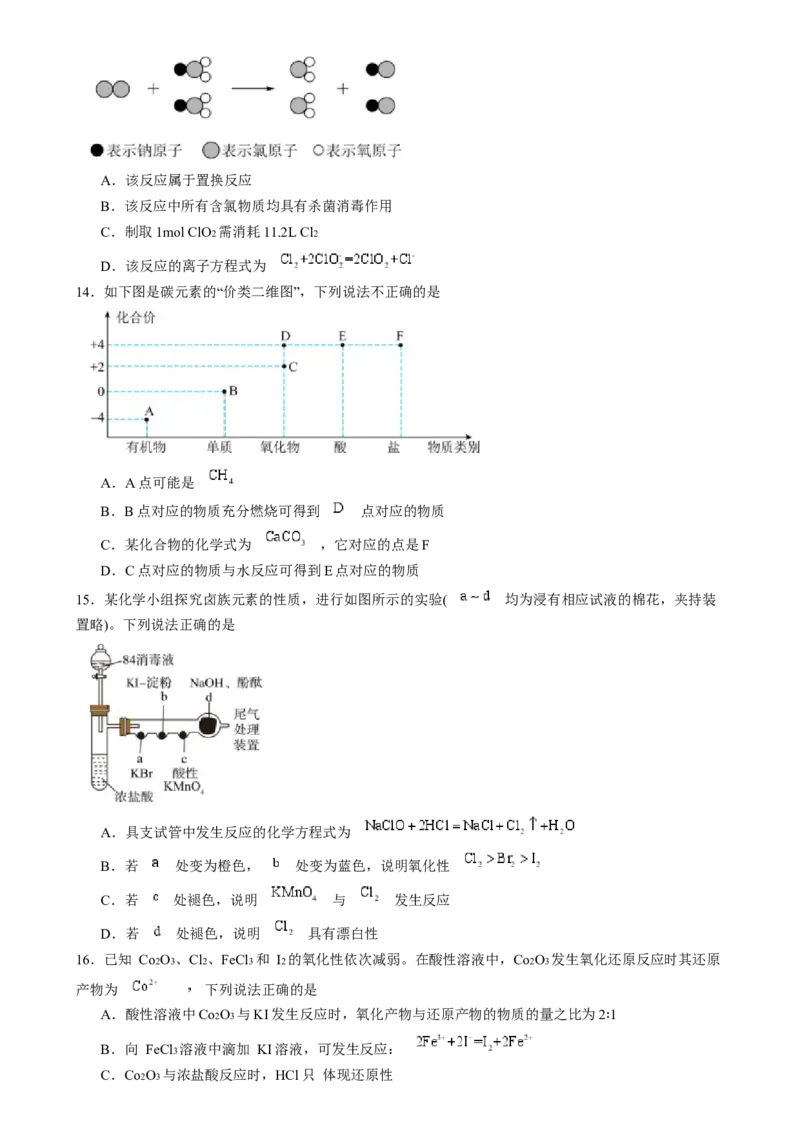
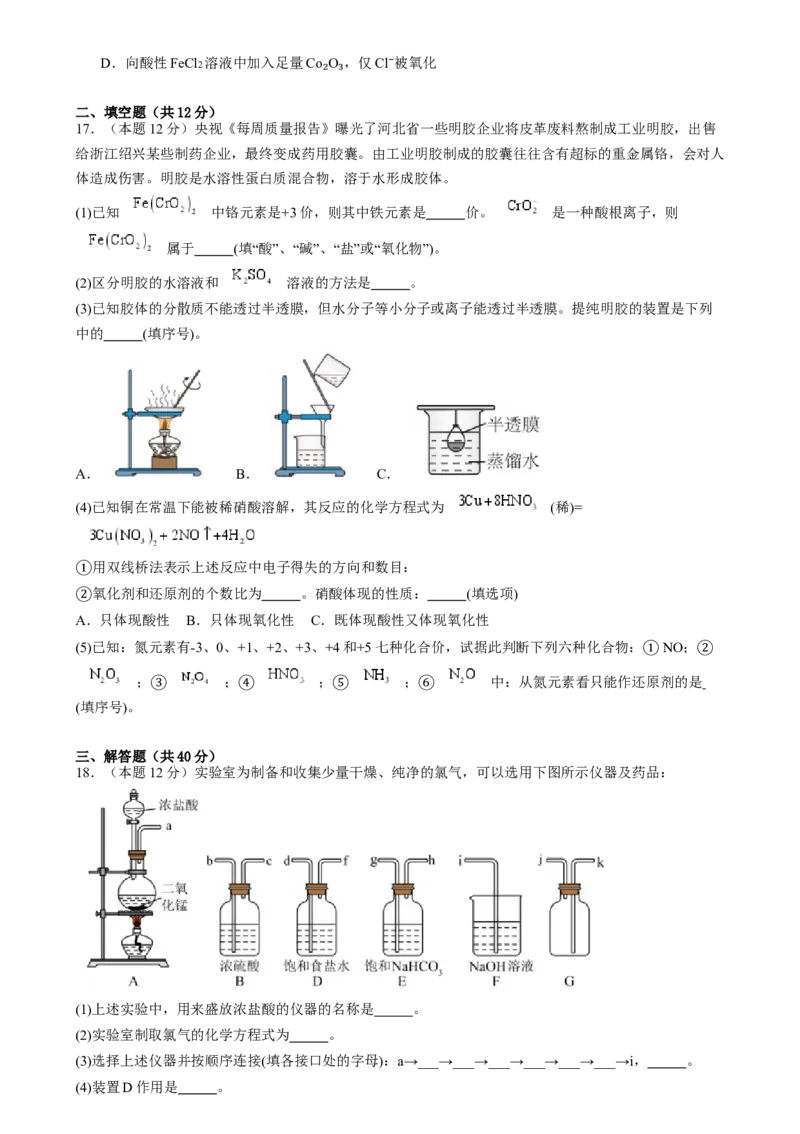
2.中国科学技术大学的钱逸泰教授等以 和金属钠为原料制造出纳米级金刚石粉末(直径约为
)。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”,其化
学方程式为 。下列关于该反应的说法不正确的是
A.金刚石是由 原子构成的单质,它与碳纳米管、石墨烯互为同素异形体
B.该纳米级金刚石粉末能产生丁达尔效应
C.该反应利用了 的强还原性
D.该反应不能在水中进行
3.下列做法正确的是
A.用手接触药品 B.用嘴吹熄酒精灯火焰
C.亲口品尝某药品的味道 D.实验后,剩余的药品不能放回原瓶,也不能随便丢弃
4.唐诗中往往蕴含丰富的化学知识。下列诗句中所描述的物质,不属于分散系的是
A.“瀚海阑干百丈冰”中的“冰” B.“黑云压城城欲摧”中的“云”
C.“劝君更尽一杯酒”中的“酒” D.“断烟残月共苍苍”中的“烟”
5.在下列条件下,一定能大量共存的离子组是
A.能与金属 反应产生气体的溶液中: 、 、 、
B.氯水中: 、 、 、
C.澄清透明的溶液中: 、 、 、
D.使紫色石蕊试纸变红的溶液中: 、 、 、
6.下列叙述正确的是
A.钾、钠等碱金属着火时,立即用水或泡沫灭火器来灭火
B.用加热法除去 固体中混有的
C.有色布条上滴加新制氯水,有色布条褪色,说明 有漂白性
D.新制氯水放置数天后酸性增强
7.下列离子方程式书写正确的是
A.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑B.向Cu(OH)2 中加入盐酸:OH-+H+=H2O
C.氯气与水的反应:Cl2+H2O=2H++Cl-+ClO-
D.Na与水反应:2Na+2H2O=2Na++2OH-+H2↑
8.用高铁酸钠( )对河湖水消毒是城市饮水处理的新方法。高铁酸钠可通过湿法或干法来制
备,反应原理如下:
湿法:
干法:
下列说法不正确的是
A.干法中生成 转移 电子
B. 中铁元素为+6价,具有强氧化性,能消毒杀菌
C.干法中 既是氧化剂又是还原剂
D.湿法中氧化性:
9.下列物质属于电解质且能导电的是
A. B.熔融 C. 固体 D. 溶液
10.现有 和 三种无色溶液,只用一种试剂即可把它们鉴别出来,
可行的是
A.稀硫酸 B.稀盐酸 C. 溶液 D.硫酸钠溶液
11.下列用单、双线桥表示电子转移的方向和数目正确的是
A. B.
C. D.
12.有关氯元素,下列叙述正确的是
A.若发生 泄漏,应立即向高处转移
B.用铁和氯气反应和铁与盐酸反应均可制取
C. 的化学性质活泼,与 混合后会立即发生爆炸
D.漂白粉比HClO稳定,可露置在空气中长期保存
13.二氧化氯(ClO2)是国际上公认的安全、低毒的绿色消毒剂。制取ClO2 的微观过程如图所示。下列说法
正确的是A.该反应属于置换反应
B.该反应中所有含氯物质均具有杀菌消毒作用
C.制取1mol ClO2 需消耗11.2L Cl2
D.该反应的离子方程式为
14.如下图是碳元素的“价类二维图”,下列说法不正确的是
A.A点可能是
B.B点对应的物质充分燃烧可得到 点对应的物质
C.某化合物的化学式为 ,它对应的点是F
D.C点对应的物质与水反应可得到E点对应的物质
15.某化学小组探究卤族元素的性质,进行如图所示的实验( 均为浸有相应试液的棉花,夹持装
置略)。下列说法正确的是
A.具支试管中发生反应的化学方程式为
B.若 处变为橙色, 处变为蓝色,说明氧化性
C.若 处褪色,说明 与 发生反应
D.若 处褪色,说明 具有漂白性
16.已知 Co2O3 、Cl2 、FeCl3 和 I2 的氧化性依次减弱。在酸性溶液中,Co2O3 发生氧化还原反应时其还原
产物为 下列说法正确的是
A.酸性溶液中Co2O3 与KI发生反应时,氧化产物与还原产物的物质的量之比为2 1
B.向 FeCl3 溶液中滴加 KI溶液,可发生反应: ∶
C.Co2O3 与浓盐酸反应时,HCl只 体现还原性D.向酸性FeCl2 溶液中加入足量Co O ,仅Cl 被氧化
₂ ₃ ⁻
二、填空题(共12分)
17.(本题12分)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售
给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人
体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是 价。 是一种酸根离子,则
属于 (填“酸”、“碱”、“盐”或“氧化物”)。
(2)区分明胶的水溶液和 溶液的方法是 。
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列
中的 (填序号)。
A. B. C.
(4)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为 (稀)=
用双线桥法表示上述反应中电子得失的方向和数目:
氧化剂和还原剂的个数比为 。硝酸体现的性质: (填选项)
①
A.只体现酸性 B.只体现氧化性 C.既体现酸性又体现氧化性
②
(5)已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物: NO;
; ; ; ; 中:从氮元素看只能作还①原剂的是②
(填序号)。
③ ④ ⑤ ⑥
三、解答题(共40分)
18.(本题12分)实验室为制备和收集少量干燥、纯净的氯气,可以选用下图所示仪器及药品:
(1)上述实验中,用来盛放浓盐酸的仪器的名称是 。
(2)实验室制取氯气的化学方程式为 。
(3)选择上述仪器并按顺序连接(填各接口处的字母):a→___→___→___→___→___→___→i, 。
(4)装置D作用是 。(5) 可用于制造漂白粉、漂白纸浆和布匹、饮水消毒、合成塑料和农药、提炼稀有金属等多方面,
是一种重要的化工原料,下列关于氯气的说法中不正确的有___________。
A. 具有强氧化性,只可用作氧化剂
B. 是一种黄绿色气体,有刺激性气味,可用于杀菌消毒
C.实验室制备 时,常用向上排空气法收集
D. 可溶于水,故实验室制备 时可以用水吸收 进行尾气处理
(6)如图是一组探究氯气性质的装置。
现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条 (填现象)。
(7) 通入双氧水( )水溶液中会产生使带有火星的木条复燃的气体,写出在水溶液中
和 反应的化学方程式 。
19.(本题14分)氯及其化合物在生产生活中有很多重要的用途。
Ⅰ.亚氯酸钠( )都是漂白织物的漂白剂, 是易溶于水的强电解质,具有较强的
氧化性。
工业上的制备 流程如图所示:
已知: 亚氯酸钠受热易分解; 常温下 为气体。
(1) ① 中 元素的化②合价为 , 作为氧化剂参与反应时会生成 ,下列
试剂中可将 转化为 是 (填字母)。
a. b. c. d.
(2)反应1所得的母液中的含硫微粒只有 ,试写出反应1的离子方程式 。
该反应中氧化剂与还原剂的个数比为 。
(3)“反应2”的化学方程式为 。反应中 作 (填“氧化剂”或“还原剂”)。
Ⅱ.家用泡腾消毒片由 、可溶性固体强酸及辅助剂(辅助剂不参与反应)混合制得,使用时只需
将泡腾片放入水中,5~10分钟即可完全溶解,释放出 气体。
(4)已知上述过程中生成物质 的反应属于歧化反应,另一个产物为 ,请配平这个反应并
标出电子转移的方向和数目 。___________ ___________ ___________ ___________
___________
(5)泡腾片使用时需要加水,水作___________(填字母)。
A.氧化剂 B.还原剂
C.既不是氧化剂,也不是还原剂 D.既是氧化剂,又是还原剂
20.(本题14分)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法
的主要过程如图所示(部分物质已略去):
(1)往饱和食盐水中通入气体时,应先从口 (填“a”或“b”)通入 (填“CO2”或“NH3”)。
(2)根据上图,写出 中发生反应的化学方程式: 。
(3)下列说法中,正确的是 (填字母)。
①
a.CO2 可循环使用
b.副产物NH4Cl可用作肥料
c.整个流程中涉及氧化还原反应
(4)除去Na2CO3 粉末中混有的少量小苏打的方法是 ,所涉及的反应的化学方程式为 。
(5)若制出的纯碱样品中含有的杂质只有NaCl。
检验用该纯碱样品配制的溶液中含有Cl 的方法是 。
①
向mg纯碱样品中加入足量的CaCl2 溶液
⁻
,沉淀经过滤、洗涤、干燥,称其质量为bg。则该纯碱样品的
纯度(质量分数)为 (用m、b来表示)。
②
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 D B D A C D D A B A
题号 11 12 13 14 15 16
答案 A A D D A B
17.(1) +2 盐
(2)丁达尔效应
(3)C
(4) 2 3 C
(5)
∶
18.(1)分液漏斗
⑤
(2)(3)d f b c k j
(4)吸收 或除去
(5)AD
(6)无明显现象/不褪色
(7)
19.(1) +3 ad
(2) 2 +SO2= +2ClO2 2:1
(3) 2ClO2+2NaOH+H2O2=2NaClO2+O2+2H2O 还原剂
(4)
(5)C
20.(1) a NH3
(2)
(3)ab
(4) 加热
(5) 取适量样品于小试管中加水溶解,先加硝酸酸化,再加硝酸银溶液,若产生白色沉淀,则有Cl-