文档内容
株洲市二中教育集团 2024 年上学期高一期末联考
化学试题
命题人:朱文江 审题人:王晶露 时量: 60 分钟 分值: 100 分
温馨提示:
1.本试卷分试题和答题卡两部分,试卷共8页。满分100分,时量60分钟。
2.答案一律在答题卡上书写,在试题卷上作答无效。
3.可能用到的相对原子质量:H:1C:12O:16S:32Na:23
第Ⅰ卷 选择题
一、选择题(共16小题,每小题均只有一个选项符合题意,每小题3分,共48分)
1.化学与生活、科技相关。下列相关说法正确的是
A.株洲李映明剪纸艺术所用纸的主要成分与淀粉互为同分异构体
B.醴陵生产的白瓷闻名于世,白瓷的白色是含氧化铁所致
C.中国建材研制的低渗氦耐辐照高纯石英玻璃首次应用于嫦娥六号上升器激光陀螺仪,其主要成分为
SiO
2
D.华为问界M9是全球最大的一体压铸车体,车身铝合金含量达到80%,铝合金硬度低于铝单质
2.下列有关常见有机物的说法不正确的是
A.乙烯和聚乙烯都能使酸性KMnO 溶液褪色 B.淀粉、纤维素都是天然有机高分子
4
C.福尔马林和医用乙醇均能使蛋白质变性 D.84消毒液中滴加少量醋酸,可增强消毒效果
3.下列化学用语使用正确的是
A.中子数为8的碳原子:❑ 14C
8
B.甲烷分子的空间填充模型:
C.次氯酸的结构式H−Cl−O
D.聚丙烯(CH =CH−CH )的链节:−CH −CH−CH −
2 3 2 3
4.下列除杂试剂选用不正确的是
选项 实验 除杂试剂
A 除去镁粉中少量的铝粉 NaOH溶液
B 除去甲烷中混有的乙烯 酸性高锰酸钾溶液
C 除去FeCl 溶液中少量的FeCl 铁粉
2 3
D 除去乙酸乙酯中少量的乙酸 饱和Na CO 溶液
2 3
5.下列离子方程式与所给事实不相符的是
A.Cl 制备84消毒液(主要成分是NaClO):Cl +2OH− ❑Cl−+ClO−+H O
2 2 2
B.食醋去除水垢中的CaCO :CaCO +2CH COOH❑Ca2++2CH COO−+H O+CO ↑
3 3 3 3 2 2
C.过量CO 通入饱和碳酸钠溶液:2Na++CO2−+CO +H O❑2NaHCO ↓
2 3 2 2 3
D.H SO 溶液中滴入氯化钙溶液:SO2−+Ca2+ ❑CaSO ↓
2 3 3 3
6.硫及其化合物部分转化关系如图(N 为阿伏伽德罗常数)。下列说法正确的是
A
第 1 页
学科网(北京)股份有限公司A.标准状况下,11.2LH S气体中所含有的原子数目为0.5N
2 A
B.反应①中氧化剂与还原剂的物质的量之比为2:1
C.反应②中氧化产物与还原产物的物质的量之比为2:1
D.反应②每生成1mol还原产物,转移电子数目为2N❑
A
7.下列鉴别或检验不能达到实验目的的是
A.用品红溶液检验某无色气体是SO 还是CO
2 2
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的Ba(NO ) 溶液检验Na SO 是否被氧化
3 2 2 3
D.用CaCl 溶液鉴别Na CO 与NaHCO 两种无色溶液
2 2 3 3
8.短周期主族元素A、B、C、D、E的原子序数依次增大,且分布在三个周期,B元素原子的最外层电子
数是内层电子数的2.5倍,C、D两元素同主族,且能形成化合物DC 和DC 。下列说法正确的是
2 3
A.B、C、D元素的简单离子半径由小到大的顺序:BE
C.A与C形成的化合物中只含有极性键
D.D E 分子中,各原子最外层均达到8电子稳定结构
2 2
9.抗坏血酸(维生素C)能被氧化为脱氢抗坏血酸而发挥抗氧化作用,常用作食品抗氧化剂,其抗氧化过
程如图所示。下列说法正确的是
A.抗坏血酸与脱氢抗坏血酸互为同系物
B.脱氢抗坏血酸中所有原子共平面
C.1mol抗坏血酸与H 发生加成反应,可消耗2molH
2 2
D.抗坏血酸含有三种不同的官能团
10.23g某无色液体与足量的金属钠反应完全反应,得到5.6LH (标准状况下),该物质可能是
2
A.H O B.C H OH C.CH COOC H D.CH COOH
2 2 5 3 2 5 3
11.四瓶无色溶液N H NO 、Na CO 、Ba(OH) 、AlCl ,它们之间的反应关系如图所示。其中a、
4 3 2 3 2 3
b、c、d代表四种溶液,e和g为无色气体,g能使澄清石灰水变浑浊,f为白色沉淀。下列叙述正确的是
A.a中溶质常用于实验室制取e B.f不能溶于过量的b中
C.c中通入过量的e也可得到f D.b和d反应生成的沉淀不溶于稀硝酸
12.根据下列实验操作及现象能推出相应结论的是
选项 实验操作及现象 结论
第 2 页
学科网(北京)股份有限公司A 在试管中加0.5g淀粉和4mL2mol/LH SO 溶液,加热,再加 淀粉未发生水解
2 4
少量新制Cu(OH) ,加热无明显现象
2
B 稀硝酸的氧化性比浓硝酸强
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,
后者无明显现象
C Mg(OH) 和Al(OH) 中均分别加入NaOH溶液和盐酸, Mg(OH) 比Al(OH) 碱性强
2 3 2 3
Mg(OH) 只溶于盐酸,Al(OH) 都能溶
2 3
D 向3m5%H O 溶液中滴加几滴FeSO 溶液,观察到有气泡产生 Fe2+对H O 的分解具有催化作
2 2 4 2 2
用
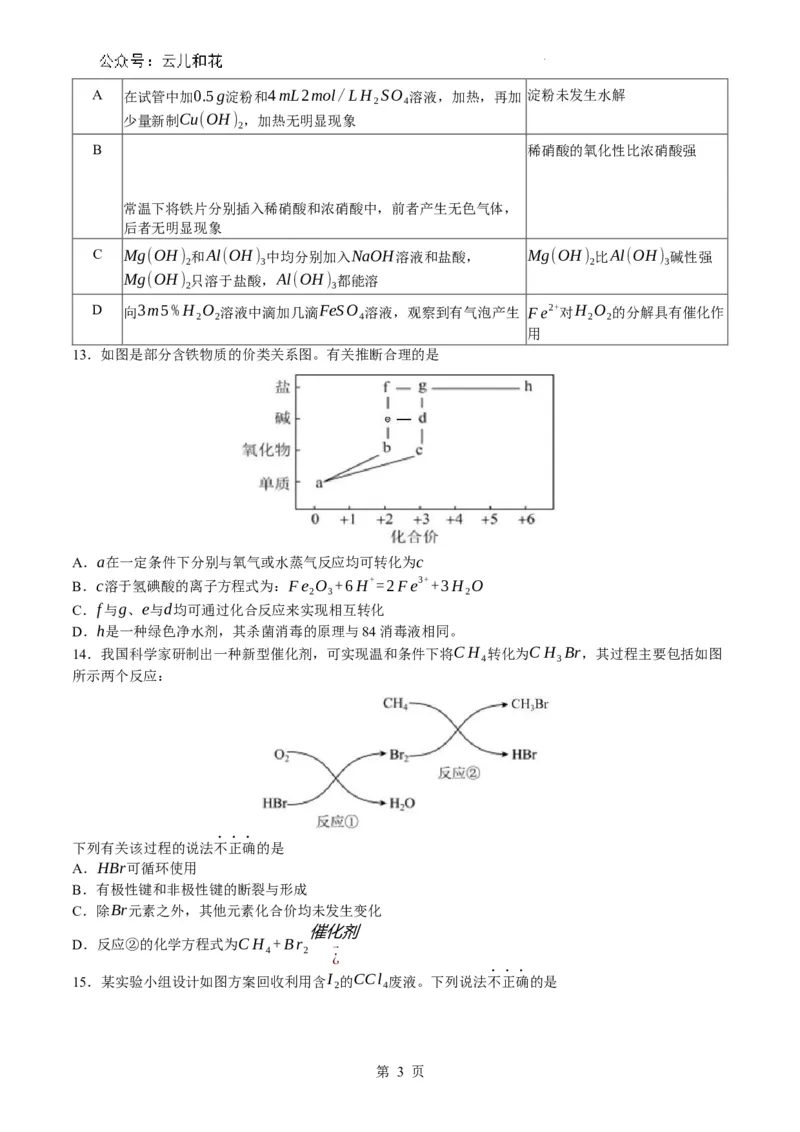
13.如图是部分含铁物质的价类关系图。有关推断合理的是
A.a在一定条件下分别与氧气或水蒸气反应均可转化为c
B.c溶于氢碘酸的离子方程式为:Fe O +6H+=2Fe3++3H O
2 3 2
C.f与g、e与d均可通过化合反应来实现相互转化
D.h是一种绿色净水剂,其杀菌消毒的原理与84消毒液相同。
14.我国科学家研制出一种新型催化剂,可实现温和条件下将CH 转化为CH Br,其过程主要包括如图
4 3
所示两个反应:
下列有关该过程的说法不正确的是
A.HBr可循环使用
B.有极性键和非极性键的断裂与形成
C.除Br元素之外,其他元素化合价均未发生变化
催化剂
D.反应②的化学方程式为CH
4
+Br
2 →
¿
15.某实验小组设计如图方案回收利用含I 的CCl 废液。下列说法不正确的是
2 4
第 3 页
学科网(北京)股份有限公司(已知:Na CO +I =NaI+NaIO+CO ↑)
2 3 2 2
A.步骤Ⅰ中,加入足量Na CO 溶液充分反应后,上下两层均为无色
2 3
B.步骤Ⅰ中,分液时从分液漏斗下口放出CCl
4
C.试剂X可选用稀硫酸,发生的离子反应为:I−+IO−+2H+=I +H O
2 2
D.步骤Ⅱ中,实验操作为蒸馏
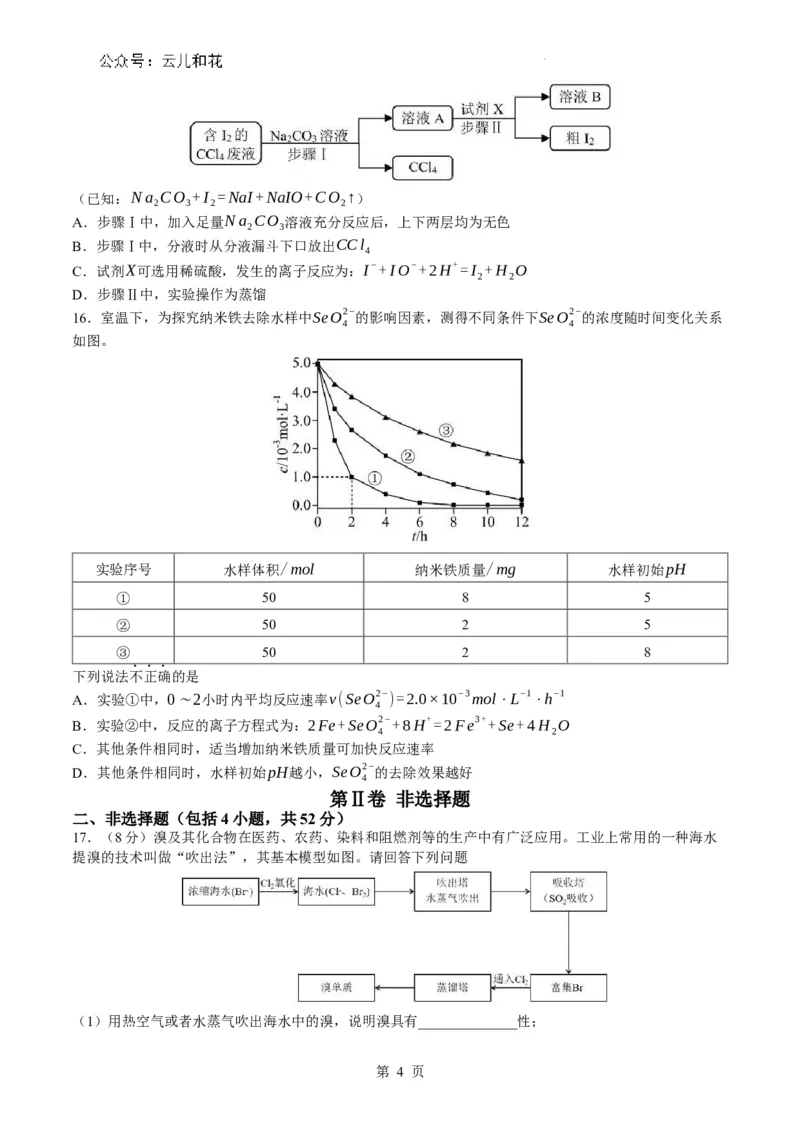
16.室温下,为探究纳米铁去除水样中SeO2−的影响因素,测得不同条件下SeO2−的浓度随时间变化关系
4 4
如图。
实验序号 水样体积/mol 纳米铁质量/mg 水样初始pH
① 50 8 5
② 50 2 5
③ 50 2 8
下列说法不正确的是
A.实验①中,0∼2小时内平均反应速率v(SeO2− )=2.0×10−3mol⋅L−1 ⋅h−1
4
B.实验②中,反应的离子方程式为:2Fe+SeO2−+8H+=2Fe3++Se+4H O
4 2
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始pH越小,SeO2−的去除效果越好
4
第Ⅱ卷 非选择题
二、非选择题(包括4小题,共52分)
17.(8分)溴及其化合物在医药、农药、染料和阻燃剂等的生产中有广泛应用。工业上常用的一种海水
提溴的技术叫做“吹出法”,其基本模型如图。请回答下列问题
(1)用热空气或者水蒸气吹出海水中的溴,说明溴具有______________性;
第 4 页
学科网(北京)股份有限公司(2)吸收塔中所发生反应化学方程式为
____________________________________________________________;
(3)根据以上流程反应可判断SO 、Cl 、Br 三种物质氧化性由强到弱的顺序是:
2 2 2
__________________________________________________________________________;
(4)蒸馏塔中,温度应控制在80∼90∘C。温度过高或过低都不利于生产,请解释原因:
____________________________________________________________________________________________
____________________________________。
18.(16分)某实验小组探究SO 与AgNO 溶液反应的产物。
2 3
Ⅰ.配制100mL0.10mol⋅L−1AgNO 溶液
3
(1)所需玻璃仪器有:烧杯、量筒、胶头滴管、玻璃棒、______________________________________。
(2)在定容时,仰视刻度线将导致所配溶液浓度____________(填“偏高”“偏低”或“无影响”)。
Ⅱ.利用如图所示装置制备SO ,并探究其相关性质。
2
(3)装置A的圆底烧瓶中发生反应的化学方程式为
____________________________________________________________________________________________
____________________________________________________________________________。
(4)装置B中可观察到的现象为________________________________,说明SO 具有____________性。
2
(5)装置C中产生白色沉淀,该小组成员对白色沉淀的成分进行探究。
提出假设
假设1:白色沉淀为Ag SO
2 3
假设2:白色沉淀为Ag SO
2 4
假设3:白色沉淀为Ag SO 和Ag SO 的混合物
2 3 2 4
查阅资料知Ag SO 和Ag SO 均可溶于氨水,其反应如下:
2 3 2 4
Ag SO +4N H ⋅H O=2[Ag(N H ) ] ++SO2−+4H O
2 3 3 2 3 2 3 2
Ag SO +4N H ⋅H O=2[Ag(N H ) ] ++SO2−+4H O
2 4 3 2 3 2 4 2
实验探究
步骤ⅰ:将白色沉淀溶于足量的氨水,过滤得到少量灰黑色固体和滤液;
步骤ⅱ:向步骤ⅰ所得滤液中加入足量Ba(NO ) 溶液,产生白色沉淀,经过滤洗涤后得到白色固
3 2
体,向其中加入足量稀盐酸;
步骤ⅲ:将步骤ⅰ所得灰黑色固体洗涤,并向其中加入足量浓硝酸,固体溶解,产生红棕色气体。
实验结论:
①小组成员通过实验步骤ⅱ得出结论为“假设3”成立。他们观察到的实验现象为
____________________________。
②进一步查阅资料得知探究步骤i中生成的灰黑色固体为Ag,是因为SO 具有较强的还原性,与AgNO 溶
2 3
液发生反应所生成。结合小组探究结论写出反应的离子方程式为
第 5 页
学科网(北京)股份有限公司____________________________________________________________________________________________
____________________________________________________________。
Ⅲ.SO 电化学原理处理制备硫酸
2
(6)可用电化学原理处理SO 制备硫酸,装置如图,电极为多孔材料。电极M为____________极;写出
2
N极的电极方程式:________________________________________________。当M极处理标准状况下
4.48LSO 气体时,该极区域质量增加____________克。
2
19.(14分)金山银山不如绿水青山,实现碳达峰碳中和是贯彻新发展理念的要求,综合利用CO 具有重
2
要的意义。一定条件下,CO 与H 制备气态甲醇(CH OH)的反应方程式为
2 2 3
CO (g)+3H (g)=CH OH(g)+H O(g)。
2 2 3 2
(1)合成甲醇的反应中的能量变化如图所示。该反应是____________反应(填“吸热”或“放热”),
其原因是反应物化学键断裂吸收的总能量____________(填“大于”或“小于”)生成物化学键形成放出
的总能量。
(2)在容积为2L的恒温密闭容器中,充入1molCO 和3molH ,测得CO 和CH OH的物质的量随时
2 2 2 3
间的变化关系如图。
①3∼6min钟内,v(H )= ____________mol⋅L−1min−1
2
第 6 页
学科网(北京)股份有限公司②第3min时v (CH OH)____________第9min时v (CH OH)(填“大于”、“小于”或“等
正 3 逆 3
于”)。第9分钟时往容器中充入1molN ,则此时v(CO )____________(填“增大”、“减
2 2
少”或“不变”)。
(3)12min末时,混合气体中CH OH的物质的量分数为____________________。(已知:B的物质的
3
B的物质的量
量分数= ×100%)
混合气体的总物质的量
(4)一定温度下发生上述反应。下列说法能作为反应是否达到平衡的判断依据的是
______________________________________________________________(填标号)
a.CO 和CH OH的百分含量不再变化
2 3
b.容器内气体的密度不再变化
c.容器内混合气体的平均相对分子质量不再变化
d.断裂3N 个H−H键的同时断裂2N❑ 个H−O键
A A
20.(14分)巴豆酸乙酯(CH CH=CHCOOCH CH )是一种较好的有机溶剂,可由石油裂解气的主
3 2 3
要产物A物质进行合成(A的产量常用于衡量一个国家的石油化工发展水平),合成线路如图所示:
请回答下列有关问题:
(1)物质A的名称是____________,无机物M是____________________________(填化学式)。
(2)化合物D中官能团的名称为________________________________________________________。
(3)A→B,E→F的反应类型分别为__________,__________________________________。
(4)F所具有的化学性质( )
a.既能发生加成反应,又能发生取代反应
b.F能使溴水褪色但不能使酸性高锰酸钾溶液褪色
c.可用NaHCO 溶液检验F中的含氧官能团
3
(5)写出B与F生成G的化学方程式:
____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________。
(6)有机物G自身会发生聚合反应,所得聚合物是一种用途广泛的有机玻璃树脂,该聚合物的结构简式为
____________________________________________________________________________________________
____________________________________________________________________________________________
______________。
(7)写出一种与F具有相同官能团的同分异构体H的结构简式:
____________________________________________________________________________________________
____________________________________________________________________________________________
__________________________________________________________________。
【参考答案】
株洲市二中教育集团 2024 年上学期高一期末联考
第Ⅰ卷 选择题
第 7 页
学科网(北京)股份有限公司一、选择题(共16小题,每小题均只有一个选项符合题意,每小题3分,共48分)
1.C 2.A 3.B 4.B 5.D 6.D 7.C 8.D 9.D 10.B 11.C 12.C
13.D 14.C 15.D 16.D
第Ⅱ卷 非选择题
二、非选择题(包括4小题,共52分)
17.(1) 挥发性(2分)
(2) Br +SO +2H O=2HBr+H SO (2分)
2 2 2 2 4
(3) Cl >Br >SO (2分)
2 2 2
(4) 温度过高大量水蒸气被蒸出,使得溴蒸气中水增加;温度过低,溴不能完全蒸出,吸收率低。(2
分,答案合理均给分)
18.(1) 100mL容量瓶(1分)
(2) 偏低(1分)
(3) ¿(2分)
(4) 酸性高锰酸钾溶液褪色(2分); 还原(1分)
(5) ① 白色沉淀部分溶解(2分)
② 4Ag++SO +2H O=Ag SO ↓+4H++2Ag↓(2分未打沉淀符号不扣分)
2 2 2 4
(6) 负极(1分); O +4H++4e−=2H O(2分); 12.4(2分)
2 2
19.(1) 放热(2分); 小于(2分)
(2) ① 0.075(2分)
② 大于(2分); 不变(2分)
(3) 30%(2分)
(4) ac(2分,不全给1分,有错误选项不给分)
20.(1) 乙烯(1分); H O(1分)
2
(2) 羟基、醛基(2分,写对1个给1分,有错别字不给分)
(3) 加成反应; 氧化反应(2分,写对1个给1分)
(4) a、c(2分,选对1个给1分,有错误选项不给分)
浓硫酸
(5) CH CH=CHCOOH+CH CH OH ⇌ CH CH=CHCOOCH CH +H O(2分,未写
3 3 2 3 2 3 2
△
条件、未写可逆符号扣1分)
(6) (2分)
CH =CHCH COOH
2 2
(7) 或 (任写一种,2分)
第 8 页
学科网(北京)股份有限公司