文档内容
2000 年广东高考化学真题及答案
第Ⅰ卷 (选择题共84分)
可能用到的原子量:H 1 C 12 N 14 O 16 CL 35.5 Fe 56 Br 80
Ag 108 I 127
一、 选择题(本题包括11小题,每小题4分,共44分。每小题只有一个选项符合题
意。)
1.1999年新发现的114号元素的同位素,其子数为184,该同位素原子的质量数为
A.70 B.114 C.228 D.298
2.下列气体不能用浓HSO 干燥的是
2 4
A.CO B.HS C.SO D.HCl
2 2 2
3.室温时,下列液体的密度纯水密度大的是
A.硝基苯 B.浓氛水 C.乙醇 D.汽油
4.只含有一种元素的物质
A.可能是纯净物也可能是混合物
B.可能是单质也可能是化合物
C.一定是纯净物
D.一定是一种单质
5.可以判断油脂皂化反应基本完成的现象是
A. 反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D.反应后静置,反应液不分层
6.在周期表中,第三、四、五、六周期元素的数目分别是
A.8、18、32、32 B、8、18、18、32
C、8、18、18、18 D、8、8、18、18
7.PH=7的盐酸和PH=9的氢氧化纳溶液以体积比11:9混合,混合液的pH
A.为7.2 B.为8 C.为6 D.无法计算
8.在CHN中,N原子以三个单键与其他原子相连接,它具有的同分异构体数目为
2 9
A.1 B.2 C.3 D.4
9.把表面有氧化物的相同大小的铜片和铁片一起放入盐酸中充分反应,所得溶液中的金属离
子
A.是Fe3+和Cu2+ B.是Fe2+和Cu2+
C.是Fe2-和Fe3+ D.只有Fe2+
10.某种解热镇痛药的结构简式为
当它完全水解时,可得到的产物有
A.2种 B.3种 C.4种 D.5种
11.把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干
燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为
A.70% B.52.4% C.47.6% D.30%
参考答案:
第1页 | 共7页1.D 2.B 3.A 4.A 5.D 6.B 7.C 8.D 9.D 10.C 11.A
二.选择题(本题包括10小题,第小题4分,共40分。每小题有一个或两个选项符合题意。
若正确答案只包括一选项,多选时,该题为0分;若正确答案包括两个选项,只选一个
且正确的给2分,选两个且都正确的给4分,但只要选借一个,该小题就为0分。)
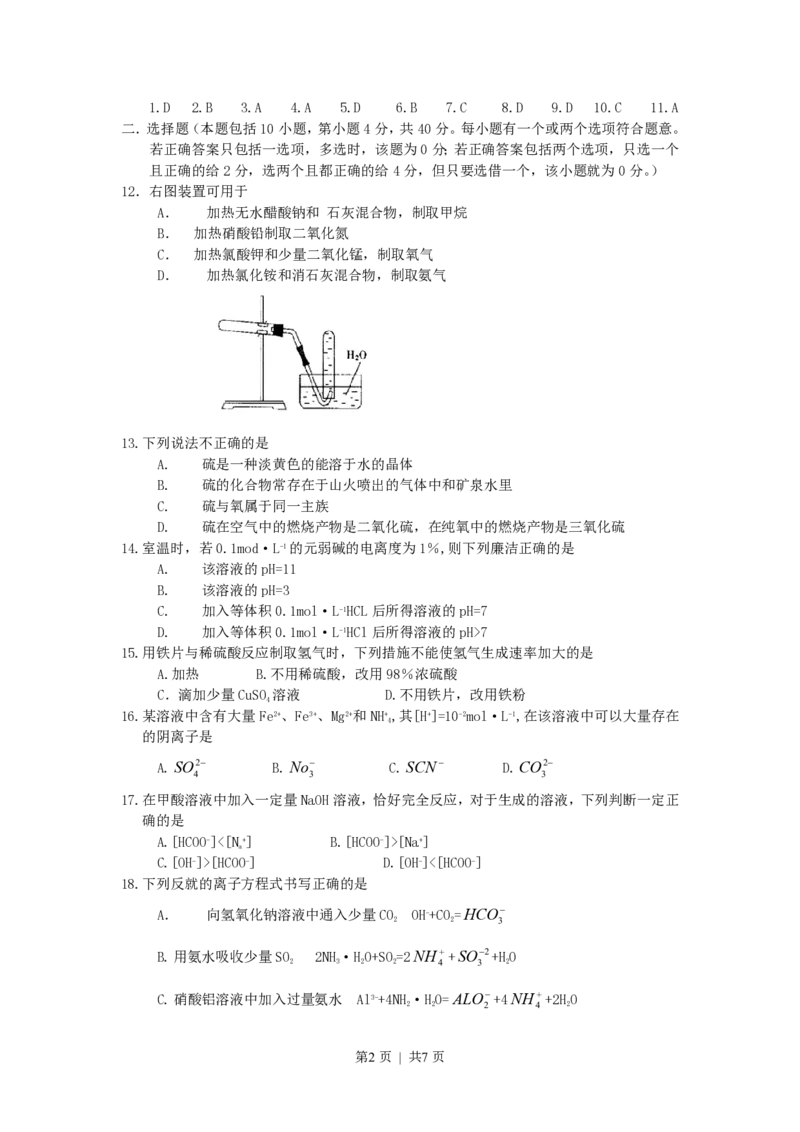
12.右图装置可用于
A. 加热无水醋酸钠和 石灰混合物,制取甲烷
B. 加热硝酸铅制取二氧化氮
C. 加热氯酸钾和少量二氧化锰,制取氧气
D. 加热氯化铵和消石灰混合物,制取氨气
13.下列说法不正确的是
A. 硫是一种淡黄色的能溶于水的晶体
B. 硫的化合物常存在于山火喷出的气体中和矿泉水里
C. 硫与氧属于同一主族
D. 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫
14.室温时,若0.1mod·L-1的元弱碱的电离度为1%,则下列廉洁正确的是
A. 该溶液的pH=11
B. 该溶液的pH=3
C. 加入等体积0.1mol·L-1HCL后所得溶液的pH=7
D. 加入等体积0.1mol·L-1HCl后所得溶液的pH>7
15.用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.不用稀硫酸,改用98%浓硫酸
C.滴加少量CuSO 溶液 D.不用铁片,改用铁粉
4
16.某溶液中含有大量Fe2+、Fe3+、Mg2+和NH+,其[H+]=10-2mol·L-1,在该溶液中可以大量存在
4
的阴离子是
A.SO2 B.No C.SCN D.CO2
4 3 3
17.在甲酸溶液中加入一定量NaOH溶液,恰好完全反应,对于生成的溶液,下列判断一定正
确的是
A.[HCOO-]<[N+] B.[HCOO-]>[Na+]
a
C.[OH-]>[HCOO-] D.[OH-]<[HCOO-]
18.下列反就的离子方程式书写正确的是
A. 向氢氧化钠溶液中通入少量CO OH-+CO=HCO
2 2 3
B.用氨水吸收少量SO 2NH·HO+SO=2NH+SO2+HO
2 3 2 2 4 3 2
C.硝酸铝溶液中加入过量氨水 Al3-+4NH·HO=ALO+4NH+2HO
2 2 2 4 2
第2页 | 共7页D.向Fe(SO) 的酸性溶液中通入足量HS Fe3++HS=Fe2++S↓+2H+
2 4 3 2 2
19.同温同压下两个容积相等的贮气瓶,一个装有CH,另一个装有CH 和CH 的混合气体,
2 4 2 2 2 6
两瓶内的气体一定具有相同的
A.质量 B.原子总数 C.碳原子数 D.密度
20.同温同压下,当反应物分解了8%时,总体积也增加8%的是
A. 2NH(g) N(g)+3H(g)
3 2 2
A.2NO(g) N(g)+O(g)
2 2
B.2NO(g) 4NO(g)+O(g)
2 5 2 2
C.2NO(g) 2NO(g)+O(g)
2 2
21.用铂电极(情性)电解下列溶液时,阴极和阳极上的主要产物分别是H 和O 的是
2 2
A. 稀NaOH溶液
B. HCl溶液
C. 酸性MgSO 溶液
4
D酸性AgNO
3
参考答案:
12.A、C 13.A、D 14.A 15.B 16.A 17.A、D
18.B 19.C 20.A 21.A、C
三、题共两小题,16分。
22.(4分)
(1)在进行沉淀反应的实验时,如何认定沉淀已经完全?
答________________________________________________
(2)中学化学实验中,在过滤器上洗涤沉淀的操作是
23.(12分)某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是a g·cm-3。该RX可
以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的分子量,拟定的
实验步骤如下:
① 准确量取该卤代烷b mL,放入锥形瓶中。
② 在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反反
应。
③ 反应完成后,冷却溶液,加稀NaOH溶液,塞上带有长玻璃的塞子,加热,发生
反应。
④ 过滤、洗涤、干燥后称重,得到固体c g。
回答问题:
(1) 装置中长玻璃管的作用是________________。
(2) 步骤④中,洗涤的目的是为了除去沉淀上吸附的________离子。
(3) 该卤代烷中所含卤素的名称是____________,判断的依据是_____________。
(4) 该卤代烷的分子量是_____________(列出算式)。
(5) 如果在步聚③中,加HNO 的量不足,没有将溶液酸化,则步骤④中测得的c
3
值(填下列选项代码)_______。
A.偏大 B.偏小 C.不变 D.大小不定
参考答案:
22.(1)在上层清液中(或取少量上层清液置于小试管中),滴加沉淀剂,如果不再产
第3页 | 共7页生沉淀,说明沉淀完全。
(2)向漏斗里注入蒸馏水,使水面没过沉淀物,等水流完后,重复操作数次。
23.(1)防止卤代烷挥发(或答 冷疑)
(2)Ag+,Na+和NO
3
(3)氯(1分);得到的卤化银沉淀是白色的(2分)
143.5ab
(4)
c
(5)A
四、本题共两小题, 20分
24.(10分)
(1)分别写出由氧在一定条件下生成下列物质的化学议程式(必须注明反应条件)
①O:_____________________.
3
②NaO____________________________。
2 2
③指出氧在下列各物质中的化合价:
O___________;NaO___________;NaO_________。
3 2 2 2
(2)KO 能吸收CO 生丰收KCO 和O,故可用作特殊情况下的氧气源,试写出该反应的化学
2 2 2 3 2
方程式____________________________。
(3)KO 能吸收CO 生成KCO 和O,故可用作特殊情况下的气氧气源,试写出该反应的化学
2 2 2 3 2
方程式___________________。
(4)人体内O离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,
2
请完成该反应的离子方程式:
O + HO HO + O+
2 2 2 2 2
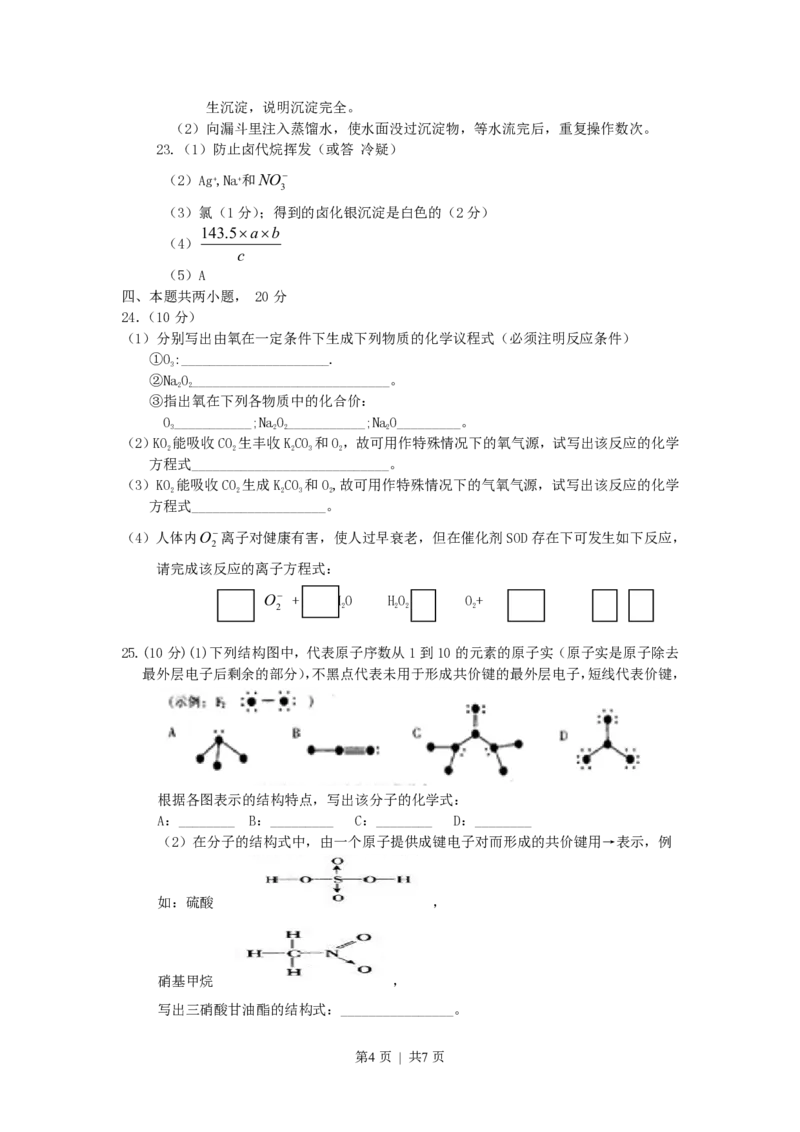
25.(10分)(1)下列结构图中,代表原子序数从1到10的元素的原子实(原子实是原子除去
最外层电子后剩余的部分),不黑点代表未用于形成共价键的最外层电子,短线代表价键,
根据各图表示的结构特点,写出该分子的化学式:
A:________ B:_________ C:________ D:________
(2)在分子的结构式中,由一个原子提供成键电子对而形成的共价键用→表示,例
如:硫酸 ,
硝基甲烷 ,
写出三硝酸甘油酯的结构式:________________。
第4页 | 共7页参考答案:
放电
24.(1)①3O 2O
2 3
点燃
②2Na+O NaO
2 2 2
③4Na+O===2NaO
2 2
(2)0; -1; -2,
(3)4KO+2CO===2KCO+3O
2 2 2 3 2
(4) 2O + 2HO===HO+O+ 2OH-
2 2 2 2 2
25.(1)A:NH B:HCN C:CO(NH) D.BF
3 2 2 3
(2)
五.(本题包括2小题,共14分)
26.(8分)(1)今有A、B、C 3种二甲苯;将它们分别进行一硝化反应,得到的产物分子
式都是CHNO,但A得到两种产物,B得到3种产物,C只得到一种产物。由此可以判断
8 9 2
A、B、C各是下列哪一结构,请将字母填入结构式后面的括号中。
(2)请写出一个化合物的结构式。它的分子式是CHNO,分子中有苯环,苯环上有三个取代
8 9 2
基,其中之一为羧基,但并非上述二甲笨的硝化产物。请任写一个:
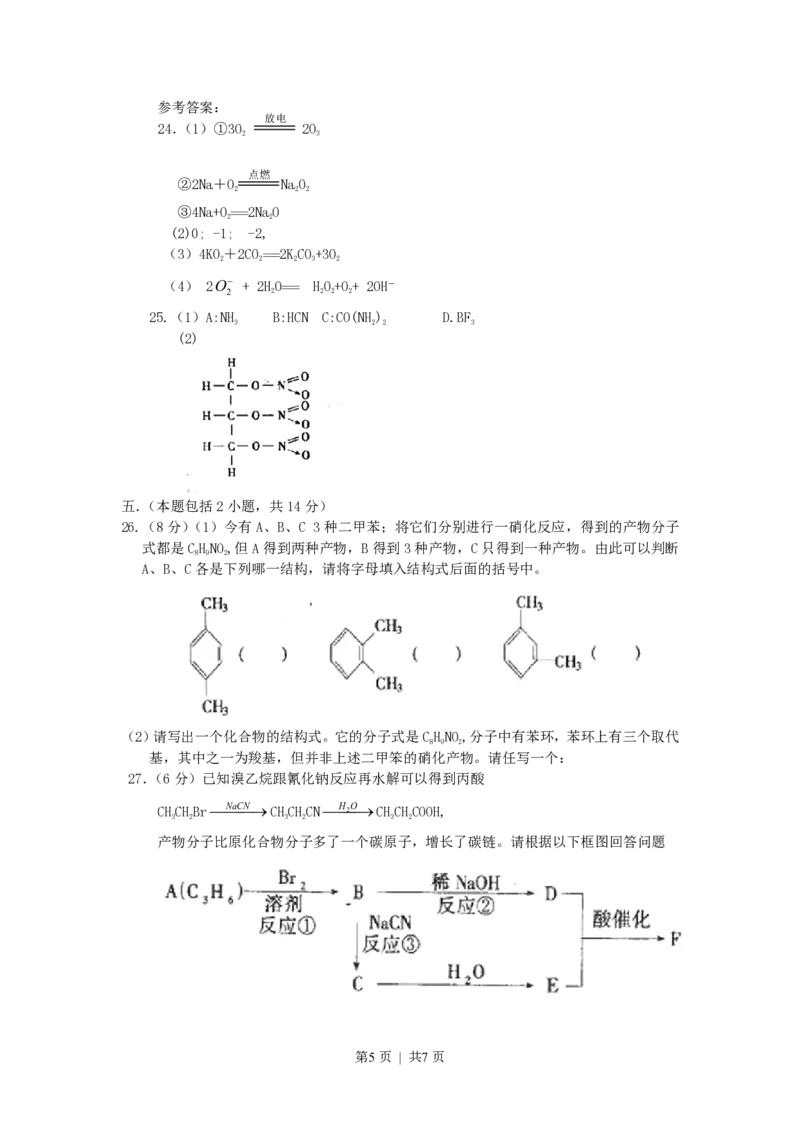
27.(6分)已知溴乙烷跟氰化钠反应再水解可以得到丙酸
CHCHBrNaCNCHCHCNH2 OCHCHCOOH,
3 2 3 2 3 2
产物分子比原化合物分子多了一个碳原子,增长了碳链。请根据以下框图回答问题
第5页 | 共7页F分子中含有8个原子组成的环状结构。
(1)反应①②③中属于取代反应的是__________(填反应代号)。
(2)写出结构简式:E_____________,F__________。
参考答案:
26.(1)(C)(A)(B)
27.(1)②;③
(2)CH—CHCOOH
3
CHCOOH
2
CHCH—COOCH—CH CHCH—COOCH
3 3 3 2
CH—COOCH CH—COOCH—CH
2 2 2 3
六.(本题包括2小题,共16分)
28.(5分)在1.00L 1.00mol·L-1NaOH溶液中通入16.8L标准状况下的CO,计算所得溶液
2
中含有的NaHCO 和NaCO 的物质的量。
3 2 3
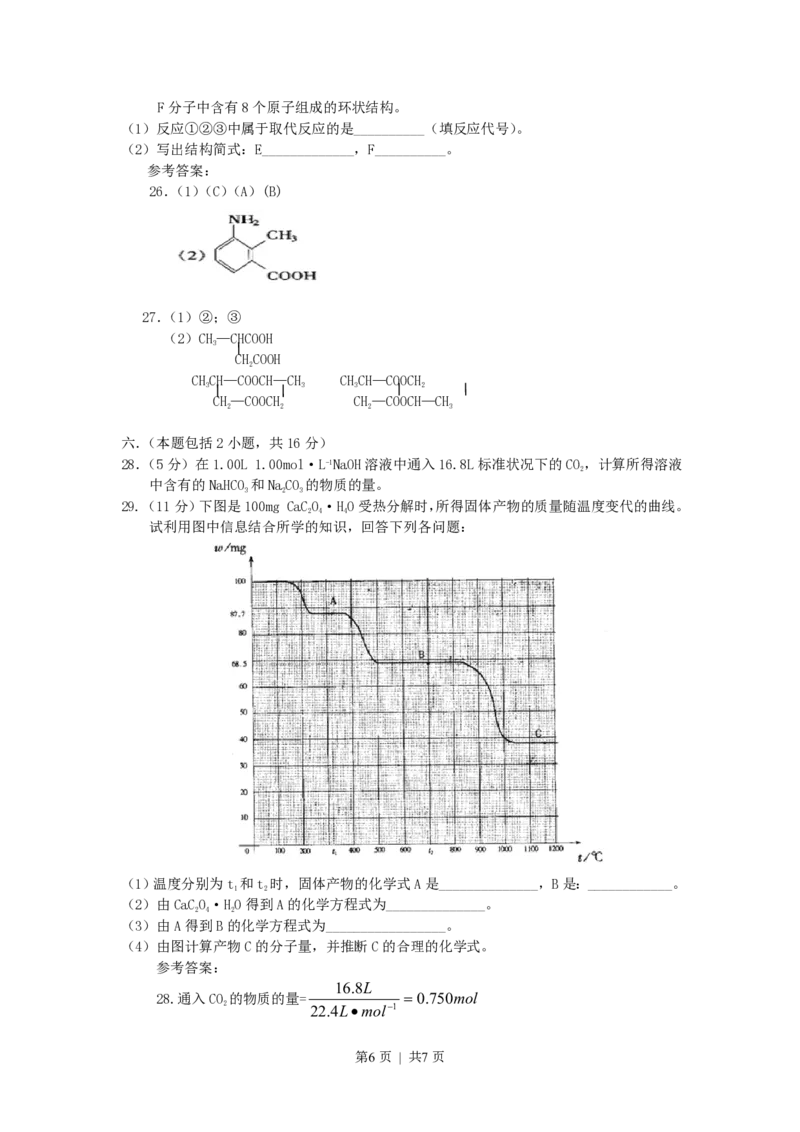
29.(11分)下图是100mg CaCO·HO受热分解时,所得固体产物的质量随温度变代的曲线。
2 4 4
试利用图中信息结合所学的知识,回答下列各问题:
(1)温度分别为t 和t 时,固体产物的化学式A是______________,B是:____________。
1 2
(2)由CaCO·HO得到A的化学方程式为______________。
2 4 2
(3)由A得到B的化学方程式为_________________。
(4)由图计算产物C的分子量,并推断C的合理的化学式。
参考答案:
16.8L
28.通入CO 的物质的量= 0.750mol
2 22.4Lmol1
第6页 | 共7页溶液中NaOH物质的量=1.00L×1.00mol·L-1=1.00mol
根据2NaOH+CO=NaCO+HO
2 2 3 2
2 1
1.00mol
该反应中CO 过量:0.750mol- =0.250mol
2
2
NaCO+CO+HO=2NaHCO
2 3 2 2 3
1 : 1 : 2
反应中NaCO 过量,生成的NaHCO 为n(反应CO)×2=0.500mol
3 3 2
溶液中剩余的NaCO 为0.500mol-0.250mol=0.250mol
2 3
29.(1)CaCO
2 4
CaCO
3
△
(2)CaCO·HO CaCO+HO↑
2 4 2 2 4 2
△
(3)CaCO CaCO+CO↑
2 4 3
(4)由图读得分解产物C的质量约为38mg
14638
C的分子量= =56
100
38100
(或= 56)
68.5
由此推断C的化学式是CaO
第7页 | 共7页