文档内容
第三章 水溶液中的离子反应与平衡
第一节 电离平衡
一、强电解质和弱电解质
1、电解质:在水溶液中或__________能导电的化合物。
2、非电解质:在水溶液中和__________均以分子形式存在,因而不能导电的化合物。
3、强电解质和弱电解质
(1)实验探究盐酸和醋酸的电离程度
酸 0.1 mol·L-1盐酸 0.1 mol·L-1醋酸
pH 较__________ 较__________
导电能力 较__________ 较__________
与镁条反应的现象 产生无色气泡__________ 产生无色气泡__________
实验表明盐酸中c(H+) __________ ,说明盐酸的电离程度 __________ 醋酸的
实验结论
电离程度
(2)强电解质与弱电解质的比较
强电解质 弱电解质
概念 在水溶液中能_________电离的电解质 在水溶液中只能__________电离的电解质
电解质在溶液
只有__________ 既有__________,又有电解质__________
中的存在形式
化合物类型 离子化合物、部分共价化合物 共价化合物
① __________ , 如 CHCOOH 、 HClO
3
①多数盐(包括难溶性盐);
等;
实例 ②__________,如HCl、HSO 等;
2 4
② __________ ,如NH ·H O等;
3 2
③ __________ ,如KOH、Ba(OH) 等
2
③水
二、弱电解质的电离平衡
1、电离平衡状态
(1)概念:在一定条件(如温度、浓度)下,弱电解质分子__________与 __________ 相等,溶液中各分子
和离子的__________都不再发生变化,电离过程就达到了电离平衡状态。
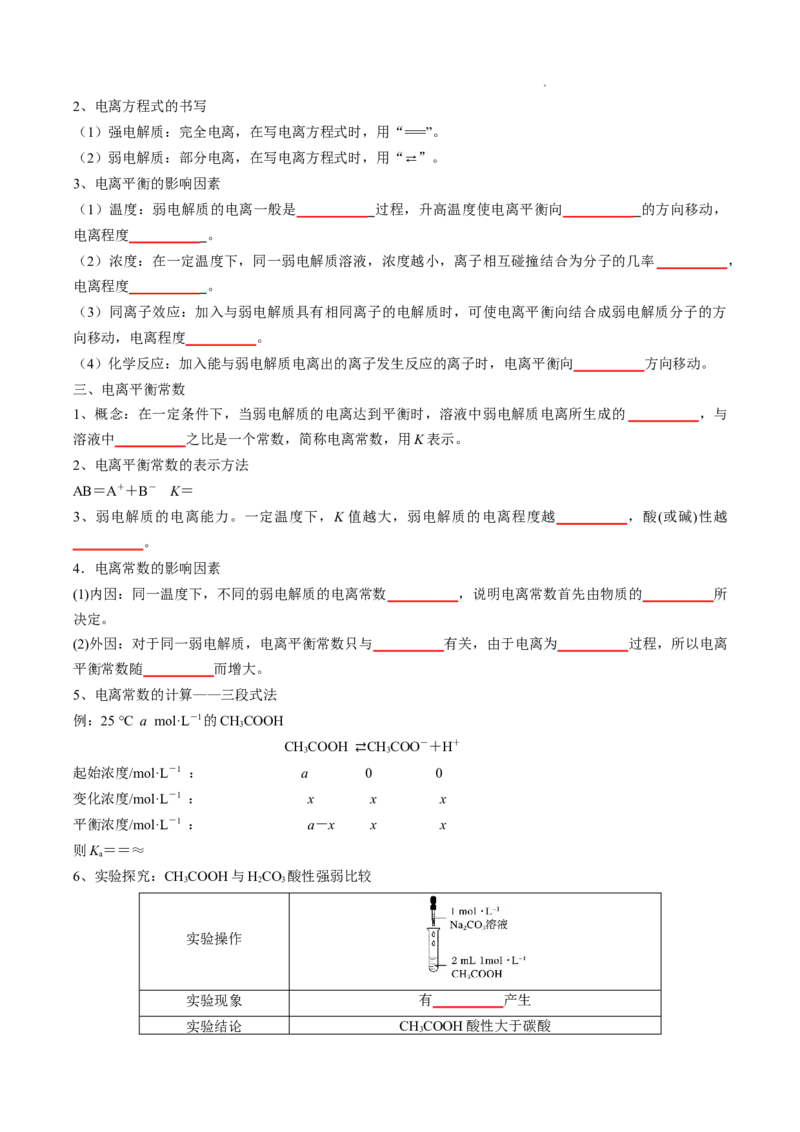
(2)建立过程
学科网(北京)股份有限公司2、电离方程式的书写
(1)强电解质:完全电离,在写电离方程式时,用“===”。
(2)弱电解质:部分电离,在写电离方程式时,用“
⇄
”。
3、电离平衡的影响因素
(1)温度:弱电解质的电离一般是 __________ 过程,升高温度使电离平衡向 __________ 的方向移动,
电离程度 __________ 。
(2)浓度:在一定温度下,同一弱电解质溶液,浓度越小,离子相互碰撞结合为分子的几率__________,
电离程度 __________ 。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方
向移动,电离程度__________。
(4)化学反应:加入能与弱电解质电离出的离子发生反应的离子时,电离平衡向__________方向移动。
三、电离平衡常数
1、概念:在一定条件下,当弱电解质的电离达到平衡时,溶液中弱电解质电离所生成的__________,与
溶液中__________之比是一个常数,简称电离常数,用K表示。
2、电离平衡常数的表示方法
AB=A++B- K=
3、弱电解质的电离能力。一定温度下,K值越大,弱电解质的电离程度越__________,酸(或碱)性越
__________。
4.电离常数的影响因素
(1)内因:同一温度下,不同的弱电解质的电离常数__________,说明电离常数首先由物质的__________所
决定。
(2)外因:对于同一弱电解质,电离平衡常数只与__________有关,由于电离为__________过程,所以电离
平衡常数随__________而增大。
5、电离常数的计算——三段式法
例:25 ℃ a mol·L-1的CHCOOH
3
CHCOOH CHCOO-+H+
3 3
起始浓度/mol·L-1 : a 0 0
⇄
变化浓度/mol·L-1 : x x x
平衡浓度/mol·L-1 : a-x x x
则K==≈
a
6、实验探究:CHCOOH与HCO 酸性强弱比较
3 2 3
实验操作
实验现象 有__________产生
实验结论 CHCOOH酸性大于碳酸
3
学科网(北京)股份有限公司K 大小比较 K(CHCOOH)__________K (H CO)
a a 3 a1 2 3
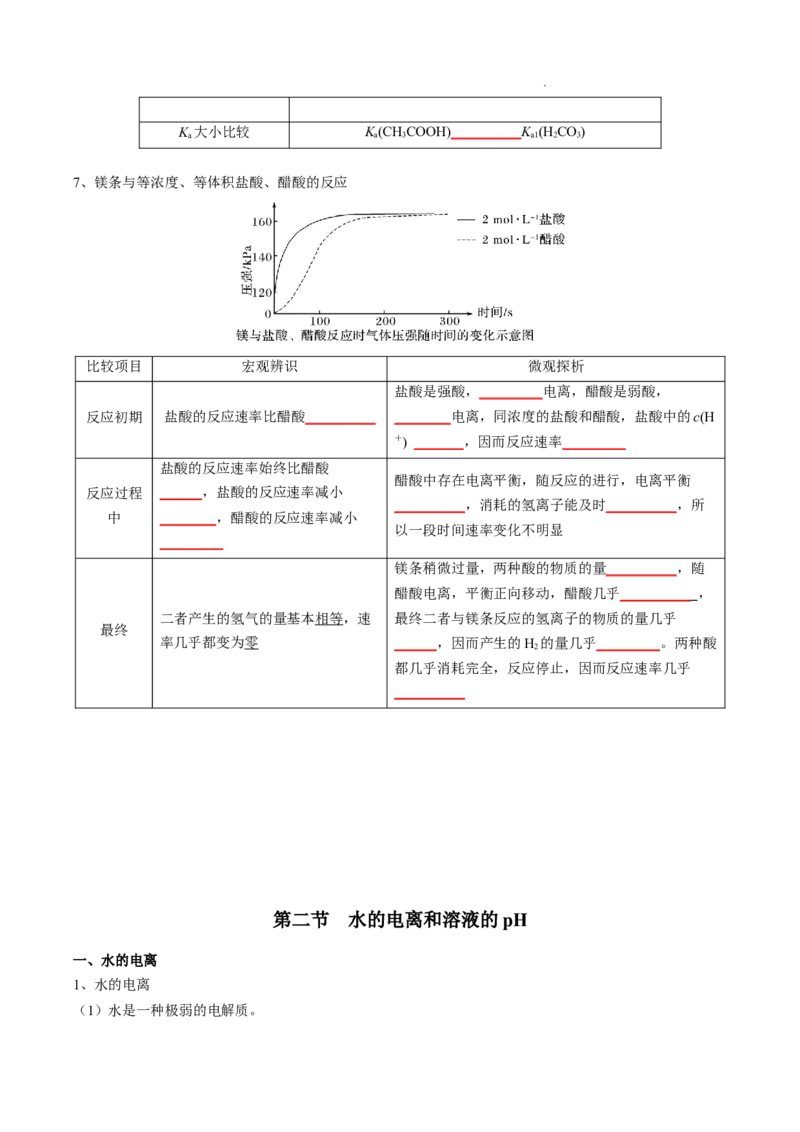
7、镁条与等浓度、等体积盐酸、醋酸的反应
比较项目 宏观辨识 微观探析
盐酸是强酸,_________电离,醋酸是弱酸,
反应初期 盐酸的反应速率比醋酸__________ ________电离,同浓度的盐酸和醋酸,盐酸中的c(H
+) _______,因而反应速率_________
盐酸的反应速率始终比醋酸
醋酸中存在电离平衡,随反应的进行,电离平衡
反应过程 ______,盐酸的反应速率减小
__________,消耗的氢离子能及时__________,所
中 ________,醋酸的反应速率减小
以一段时间速率变化不明显
_________
镁条稍微过量,两种酸的物质的量__________,随
醋酸电离,平衡正向移动,醋酸几乎 __________ ,
二者产生的氢气的量基本相等,速 最终二者与镁条反应的氢离子的物质的量几乎
最终
率几乎都变为零 ______,因而产生的H 的量几乎_________。两种酸
2
都几乎消耗完全,反应停止,因而反应速率几乎
__________
第二节 水的电离和溶液的pH
一、水的电离
1、水的电离
(1)水是一种极弱的电解质。
学科网(北京)股份有限公司(2)水的电离方程式为HO+HO HO++OH-,简写为HO H++OH-。
2 2 3 2
(3)水的电离平衡常数K =。
电离 ⇄ ⇄
2、水的离子积常数
(1)含义:因为水的浓度可看作常数,所以水中的__________可看作常数,称为水的__________,简称
水的离子积,用K 表示。
W
(2)表达式与数值:表达式K =__________,室温时,K =1.0×10-14。
W W
(3)影响因素:K 只受温度影响,由于水的电离是__________过程,温度升高,K 增大。
W W
3、外界条件对水的电离平衡的影响
分析下列条件的改变对水的电离平衡HO H++OH- ΔH>0的影响,并填写下表:
2
改变条件 平衡移动方向 c(H+) c(OH-) 水的电离程度 K
⇄ w
升高温度 __________ __________ __________ __________ __________
加入HCl(g) __________ __________ __________ __________ __________
加入NaOH(s) __________ __________ __________ __________ __________
加入金属Na __________ __________ __________ __________ __________
加入NaHSO(s) __________ __________ __________ __________ __________
4
二、溶液的酸碱性与pH
1.25 ℃时,分析下列溶液的氢离子和氢氧根离子浓度
纯水 0.1 mol·L-1 NaOH溶液 0.1 mol·L-1盐酸
c(H+)/mol·L-1 __________ __________ __________
c(OH-)/mol·L-1 __________ __________ __________
c(H+) 、c(OH-)
__________ c(H+)< c(OH-) c(H+)> c(OH-)
的相对大小
溶液的酸碱性 __________ __________ __________
2、溶液的酸碱性与溶液中c(H+)、c(OH-)的关系
c(H+)与c(OH-)的关系 c(H+)的范围(室温下)
酸性溶液 c(H+)>c(OH-) c(H+)>__________mol·L-1
中性溶液 c(H+)=c(OH-) c(H+)=__________ mol·L-1
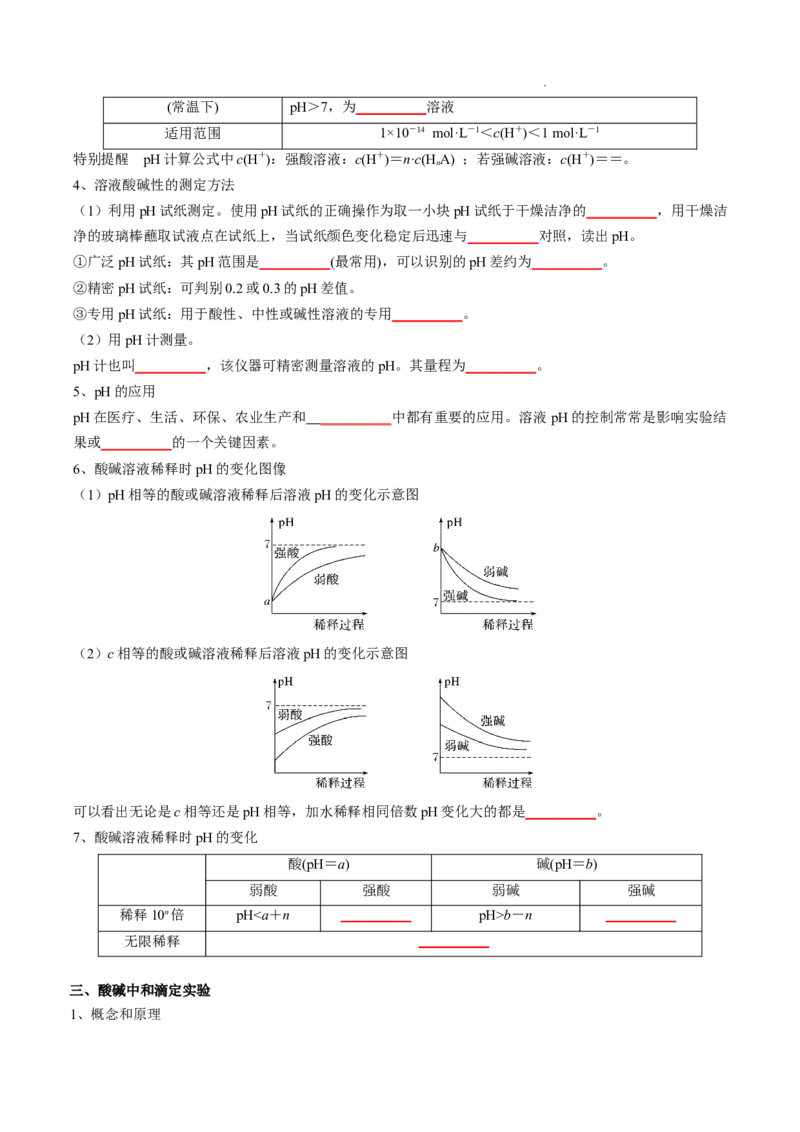
碱性溶液 c(H+)b-n __________
无限稀释 __________
三、酸碱中和滴定实验
1、概念和原理
学科网(北京)股份有限公司(1)概念:依据中和反应,用已知浓度的__________来测定未知浓度的__________的方法。
(2)原理:在中和反应中,酸提供的H+与碱提供的OH-之间的__________相等 。
即:__________,则c(H+)=或c(OH-)=。
2、主要仪器使用
(1)仪器:滴定管,铁架台,滴定管夹,__________,__________。
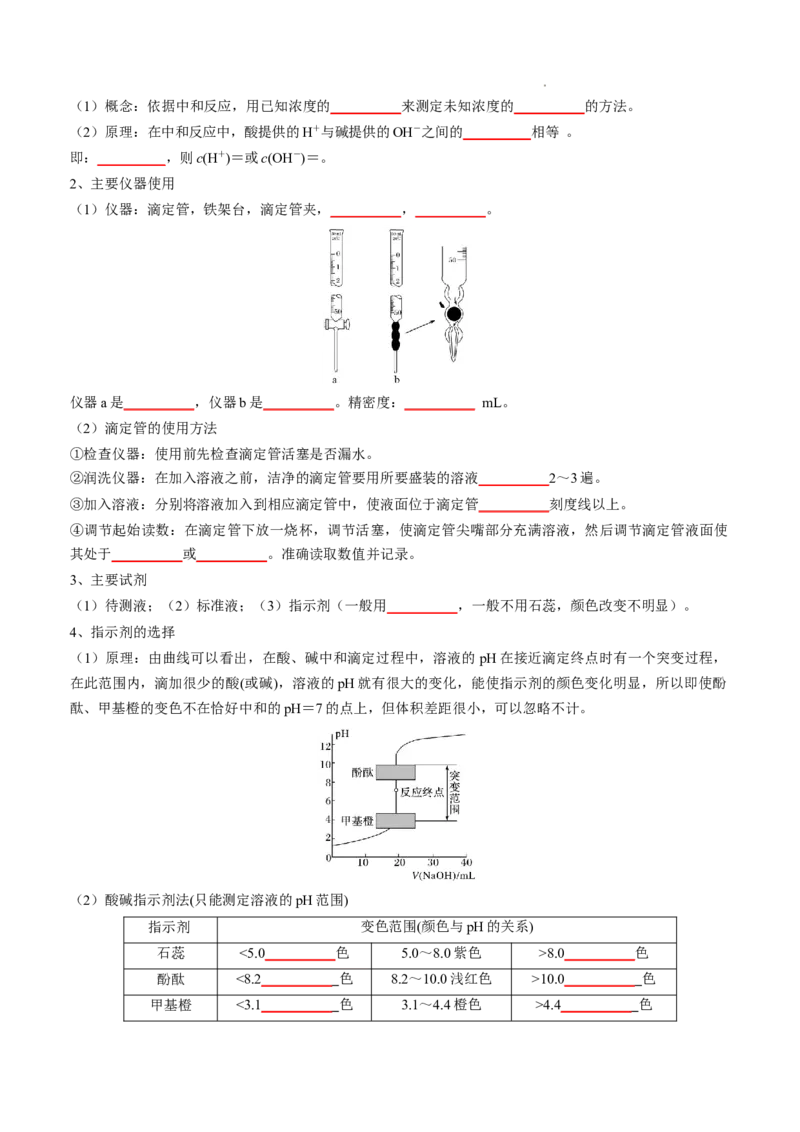
仪器a是__________,仪器b是__________。精密度:__________ mL。
(2)滴定管的使用方法
①检查仪器:使用前先检查滴定管活塞是否漏水。
②润洗仪器:在加入溶液之前,洁净的滴定管要用所要盛装的溶液__________2~3遍。
③加入溶液:分别将溶液加入到相应滴定管中,使液面位于滴定管__________刻度线以上。
④调节起始读数:在滴定管下放一烧杯,调节活塞,使滴定管尖嘴部分充满溶液,然后调节滴定管液面使
其处于__________或__________。准确读取数值并记录。
3、主要试剂
(1)待测液;(2)标准液;(3)指示剂(一般用__________,一般不用石蕊,颜色改变不明显)。
4、指示剂的选择
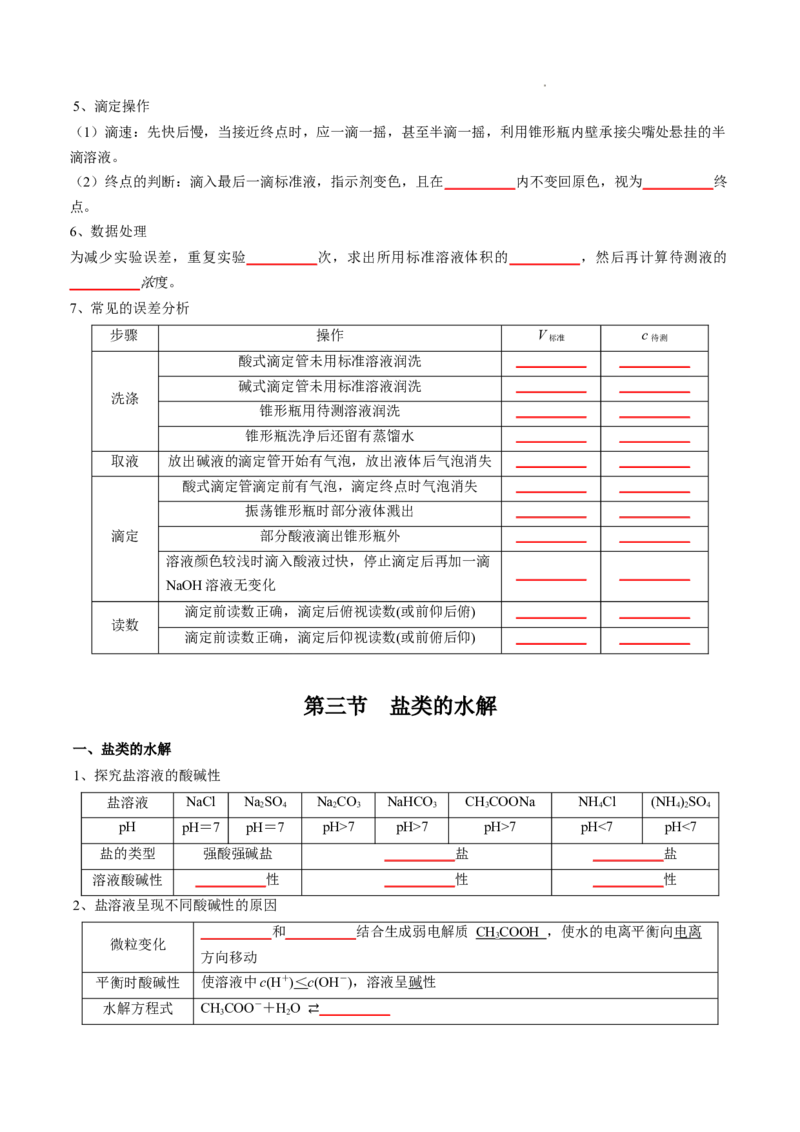
(1)原理:由曲线可以看出,在酸、碱中和滴定过程中,溶液的pH在接近滴定终点时有一个突变过程,
在此范围内,滴加很少的酸(或碱),溶液的pH就有很大的变化,能使指示剂的颜色变化明显,所以即使酚
酞、甲基橙的变色不在恰好中和的pH=7的点上,但体积差距很小,可以忽略不计。
(2)酸碱指示剂法(只能测定溶液的pH范围)
指示剂 变色范围(颜色与pH的关系)
石蕊 <5.0__________色 5.0~8.0紫色 >8.0__________色
酚酞 <8.2 __________ 色 8.2~10.0浅红色 >10.0 __________ 色
甲基橙 <3.1 __________ 色 3.1~4.4橙色 >4.4 __________ 色
学科网(北京)股份有限公司5、滴定操作
(1)滴速:先快后慢,当接近终点时,应一滴一摇,甚至半滴一摇,利用锥形瓶内壁承接尖嘴处悬挂的半
滴溶液。
(2)终点的判断:滴入最后一滴标准液,指示剂变色,且在__________内不变回原色,视为__________终
点。
6、数据处理
为减少实验误差,重复实验__________次,求出所用标准溶液体积的__________,然后再计算待测液的
__________浓度。
7、常见的误差分析
步骤 操作 V c
标准 待测
酸式滴定管未用标准溶液润洗 __________ __________
碱式滴定管未用标准溶液润洗 __________ __________
洗涤
锥形瓶用待测溶液润洗 __________ __________
锥形瓶洗净后还留有蒸馏水 __________ __________
取液 放出碱液的滴定管开始有气泡,放出液体后气泡消失 __________ __________
酸式滴定管滴定前有气泡,滴定终点时气泡消失 __________ __________
振荡锥形瓶时部分液体溅出 __________ __________
滴定 部分酸液滴出锥形瓶外 __________ __________
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴
__________ __________
NaOH溶液无变化
滴定前读数正确,滴定后俯视读数(或前仰后俯) __________ __________
读数
滴定前读数正确,滴定后仰视读数(或前俯后仰) __________ __________
第三节 盐类的水解
一、盐类的水解
1、探究盐溶液的酸碱性
盐溶液 NaCl NaSO NaCO NaHCO CHCOONa NH Cl (NH )SO
2 4 2 3 3 3 4 4 2 4
pH pH=7 pH=7 pH>7 pH>7 pH>7 pH<7 pH<7
盐的类型 强酸强碱盐 __________盐 __________盐
溶液酸碱性 __________性 __________性 __________性
2、盐溶液呈现不同酸碱性的原因
__________和__________结合生成弱电解质 CHCOOH ,使水的电离平衡向电离
3
微粒变化
方向移动
平衡时酸碱性 使溶液中c(H+)<c(OH-),溶液呈碱性
水解方程式 CHCOO-+HO __________
3 2
⇄
学科网(北京)股份有限公司NH 和__________结合生成弱电解质__________,使水的电离平衡向__________的
微粒变化
方向移动
平衡时酸碱性 使溶液中c(H+)>c(OH-),溶液呈__________性
水解方程式 NH+HO __________
2
水解方程式 HO H++OH-,NaCl===Cl-+Na+
2 ⇄
理论解释:溶液中不生成__________,水的电离平衡未受影响,溶液中 c(H+)=c(OH-),溶液呈
⇄
__________性。
3、盐类的水解
(1)概念:在溶液中,由盐电离出来的弱离子跟水电离出来的H+或OH-结合生成弱电解质的反应。
(2)实质:生成弱酸或弱碱,使水的电离平衡被破坏而建立起新的平衡。
(3)特征:①一般是可逆反应,在__________条件下达到化学平衡;②盐类水解反应是__________反应
的逆反应。
③盐类水解是__________反应。
二、影响盐类水解的主要因素
1、反应物本身性质的影响
盐类水解程度的大小主要由__________所决定的,生成盐的弱酸(或弱碱)越难__________(电离常数越小),
盐的水解程度__________,即越弱越水解。
2、实验探究反应条件对盐类水解程度的影响
已知FeCl 发生水解反应的离子方程式:Fe3++3HO Fe(OH) +3H+,根据实验操作填写下表:
3 2 3
影响因素 实验步骤 实验现象 解释
⇄
加入FeCl 固
3 溶液颜色变_________, 加入FeCl 固体,c(Fe3+)增大,水解平
3
盐的浓度 体,再测溶液的
溶液的pH__________ 衡向__________方向移动
pH
加入盐酸,c(H+)增大,水解平衡向
加盐酸后,测溶 溶液颜色变_________,
__________方向移动,但c(H+)仍比原
液的pH 溶液的pH_________
溶液的酸碱度 平衡中c(H+)大
加入少量NaOH 加入氢氧化钠后,OH-消耗H+,c(H+)
产生________色沉淀
溶液 减小,水解平衡向__________方向移动
温度 升高温度 溶液颜色变深 升高温度,水解平衡正向移动
3、盐的水解常数
(1)表达式
以CHCOONa为例:CHCOO-+HO CHCOOH+OH-
3 3 2 3
K =,只与__________有关。
h ⇄
(2)与对应弱酸电离常数的关系
K= 所以,K ·K=K 或K =。
a h a w h
学科网(北京)股份有限公司弱酸或弱碱的电离常数__________(越弱),其生成的盐水解的程度就__________。
三、盐类水解的应用
1、在化学实验中的应用
应用 举例
判断溶液的酸碱性 FeCl 溶液显酸性,原因是Fe3++3HO===Fe(OH) +3H+
3 2 3
相同浓度的NaX、NaY、NaZ溶液的pH分别为8、9、10,则酸性:
判断酸性强弱
__________
配制或贮存易水解 配制CuSO 溶液时,加入少量__________,抑制Cu2+水解;贮存NaCO 溶液
4 2 3
的盐溶液 不能用__________玻璃塞
胶体的制取 制取Fe(OH) 胶体的离子反应:Fe3++3HO=====Fe(OH) (胶体)+3H+
3 2 3
制备无水盐 将挥发性酸的弱碱盐如AlCl 、FeCl 溶液蒸干时,在通HCl的气流中加热蒸干
3 3
Al3+与CO、HCO、S2-、HS-、AlO;Fe3+与HCO、CO、AlO;NH与AlO、
判断离子是否共存
SiO因相互促进水解强烈而 _________ _共存。
判断中和反应至中 如NH ·H O与HCl反应至中性,__________过量,CHCOOH与NaOH反应
3 2 3
性的试剂用量 至中性时__________过量。
如用TiCl 制备TiO,其反应的化学方程式为:
4 2
制备无机化合物 TiCl +(x+2)H O===TiO·xHO↓+4HCl
4 2 2 2
加入大量的水,同时加热,促使水解趋于完全。
2、在生产生活中的应用
泡沫灭火器中药品成分为NaHCO 与Al (SO ),发生的反应为:
3 2 4 3
泡沫灭火器原理
Al3++3HCO===Al(OH) ↓+3CO↑
3 2
作净水剂 明矾可作净水剂,原理为Al3++3HO===Al(OH) (胶体)+3H+
2 3
化肥的使用 铵态氮肥与草木灰不得混合施用
NH Cl溶液与ZnCl 溶液可作焊接时的除锈剂,原理为:
4 2
除锈剂
NH+HO===NH ·H O+H+、Zn2++2HO===Zn(OH) +2H+
2 3 2 2 2
热纯碱去污能力强 加热,促进NaCO 的水解,使c(OH-)增大,去污能力增强
2 3
四、溶液中的守恒关系
1、电荷守恒:电解质溶液中__________所带的电荷总数与__________所带的电荷总数 相等 。即电荷
守恒,溶液呈__________。
2、元素质量守恒:
在电解质溶液中,由于某些离子发生水解或电离,__________的存在形式发生了变化,就该 __________
所含的某种元素来说,其质量在反应前后是__________的,即__________守恒。
如:NaCO 溶液中:
2 3
①=,即n(Na+)=2c(CO),CO在水中部分会水解成HCO、HCO,共三种含碳元素的存在形式。
2 3
学科网(北京)股份有限公司②c(Na+)=2[c(CO)+c(HCO)+c(H CO)]。
2 3
3、质子守恒
方法一:可以由电荷守恒与元素质量守恒推导出来。
如NaCO 中将电荷守恒和元素质量守恒中的金属阳离子消去得c(OH-)=c(H+)+c(HCO)+2c(H CO)。
2 3 2 3
方法二:质子守恒是依据水的电离平衡:HO=H++OH-,水电离产生的H+和OH-的物质的量总是相等
2
的,无论在溶液中由水电离出的H+和OH-以什么形式存在。
如:NaCO 溶液中即:c(OH-)=2c(H CO)+c(HCO)+c(H O+)或c(OH-)=2c(H CO)+c(HCO)+c(H+)。
2 3 2 3 3 2 3
第四节 沉淀溶解平衡
一、难溶电解质的沉淀溶解平衡
1、25 ℃时,溶解性与溶解度的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 >10 g 1~10 g __________ __________
2、难溶电解质的沉淀溶解平衡
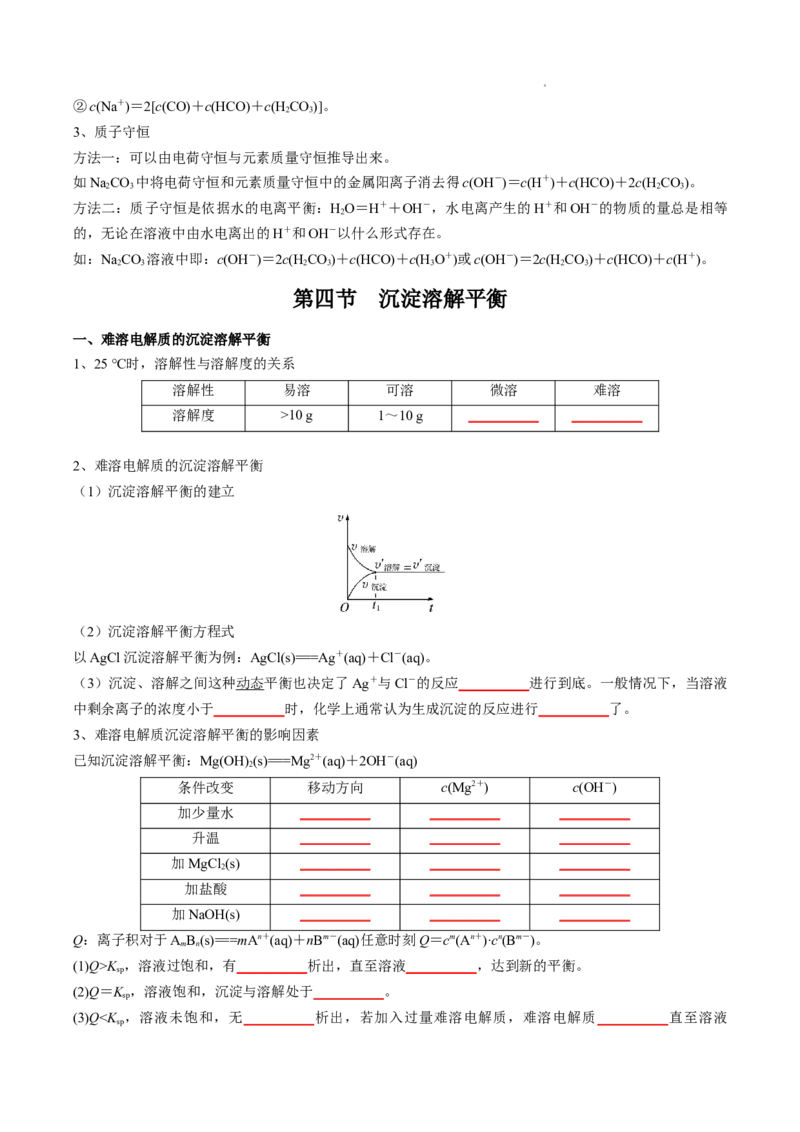
(1)沉淀溶解平衡的建立
(2)沉淀溶解平衡方程式
以AgCl沉淀溶解平衡为例:AgCl(s)===Ag+(aq)+Cl-(aq)。
(3)沉淀、溶解之间这种动态平衡也决定了Ag+与Cl-的反应__________进行到底。一般情况下,当溶液
中剩余离子的浓度小于__________时,化学上通常认为生成沉淀的反应进行__________了。
3、难溶电解质沉淀溶解平衡的影响因素
已知沉淀溶解平衡:Mg(OH) (s)===Mg2+(aq)+2OH-(aq)
2
条件改变 移动方向 c(Mg2+) c(OH-)
加少量水 __________ __________ __________
升温 __________ __________ __________
加MgCl (s) __________ __________ __________
2
加盐酸 __________ __________ __________
加NaOH(s) __________ __________ __________
Q:离子积对于A B (s)===mAn+(aq)+nBm-(aq)任意时刻Q=cm(An+)·cn(Bm-)。
m n
(1)Q>K ,溶液过饱和,有__________析出,直至溶液__________,达到新的平衡。
sp
(2)Q=K ,溶液饱和,沉淀与溶解处于__________。
sp
(3)Q