文档内容
人教版(2019)高一必修第一册 第三章 铁 金属材料 第一
节 铁及其化合物
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列反应中,产物有氧化铁的是( )
A.加热Fe(OH) B.Fe在纯O 中燃烧
3 2
C.灼热的Fe与水蒸气反应 D.加热蒸发Fe (SO ) 溶液至干
2 4 3
2.下列离子方程式书写不正确的是
A.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++HO===I +2HO
2 2 2 2
B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO -+Ba2++OH-===BaCO ↓+HO
3 3 2
C.向Al (SO ) 溶液中加入过量的氨水:Al3++4NH ·H O===AlO -+4NH ++2HO
2 4 3 3 2 2 4 2
D.用铁棒作阴极,碳棒作阳极电解饱和氯化钠溶液:2Cl-+2HO H↑+Cl↑+
2 2 2
2OH-
3.在给定条件下,下列选项所示的物质均能实现的是
A.SiO SiCl Si
2 4
B.Al O NaAlO (aq) Al(OH)
2 3 2 3
C.FeS SO HSO
2 3 2 4
D.Fe O FeCl (aq) 无水FeCl
3 4 3 3
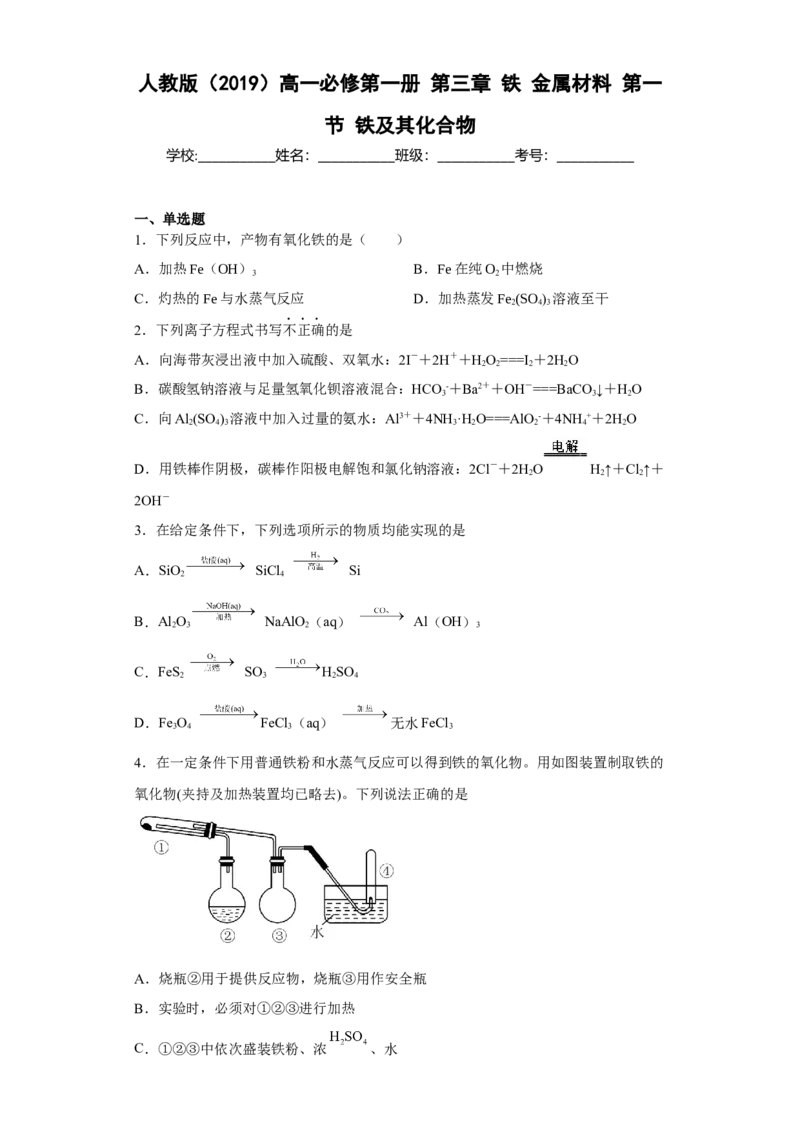
4.在一定条件下用普通铁粉和水蒸气反应可以得到铁的氧化物。用如图装置制取铁的
氧化物(夹持及加热装置均已略去)。下列说法正确的是
A.烧瓶②用于提供反应物,烧瓶③用作安全瓶
B.实验时,必须对①②③进行加热
C.①②③中依次盛装铁粉、浓 、水D.④处的气体收集方法也可用于收集氨气和甲烷
5.已知反应:①
②
③
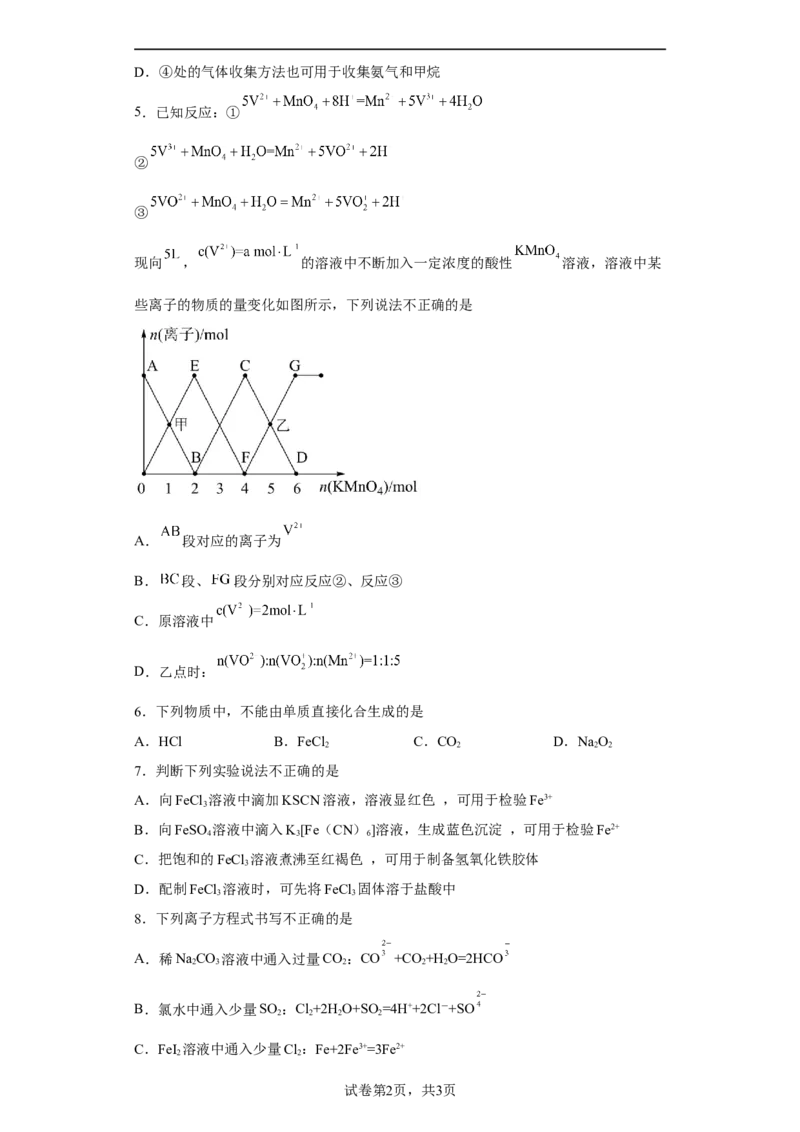
现向 , 的溶液中不断加入一定浓度的酸性 溶液,溶液中某
些离子的物质的量变化如图所示,下列说法不正确的是
A. 段对应的离子为
B. 段、 段分别对应反应②、反应③
C.原溶液中
D.乙点时:
6.下列物质中,不能由单质直接化合生成的是
A.HCl B.FeCl C.CO D.NaO
2 2 2 2
7.判断下列实验说法不正确的是
A.向FeCl 溶液中滴加KSCN溶液,溶液显红色 ,可用于检验Fe3+
3
B.向FeSO 溶液中滴入K[Fe(CN)]溶液,生成蓝色沉淀 ,可用于检验Fe2+
4 3 6
C.把饱和的FeCl 溶液煮沸至红褐色 ,可用于制备氢氧化铁胶体
3
D.配制FeCl 溶液时,可先将FeCl 固体溶于盐酸中
3 3
8.下列离子方程式书写不正确的是
A.稀NaCO 溶液中通入过量CO:CO +CO +H O=2HCO
2 3 2 2 2
B.氯水中通入少量SO :Cl+2H O+SO =4H++2Cl-+SO
2 2 2 2
C.FeI 溶液中通入少量Cl:Fe+2Fe3+=3Fe2+
2 2
试卷第2页,共3页D.铜粉加入稀硝酸溶液中:3Cu+8H++2NO =3Cu2++2NO↑+4HO
2
9.将铁片投入下列溶液,溶液质量增加,但无气体产生的是( )
A.AgNO B.Cu(NO ) C.稀HSO D.FeCl
3 3 2 2 4 3
10.某合金粉末11 g,加入到足量的稀硫酸中,在标准状况下产生的气体体积为11.2
L,此合金可能是( )
A.Mg-Al合金 B.Cu-Zn合金 C.Zn-Fe合金 D.Mg-Zn合金
11.下列物质露置于空气中易与氧气作用而变质的是
A.NaHCO B.NaOH C.FeSO D.漂白粉
3 4
12.已知2A-+B ===A+2B-,2A-+C ===A+2C-,2B-+C ===B +2C-,2C-+
2 2 2 2 2 2
D=== C +2D-。则各种单质氧化性由强到弱的顺序是
2 2
A.A>C >B >D B.B >C >A>D
2 2 2 2 2 2 2 2
C.D>C >B >A D.C >B >A>D
2 2 2 2 2 2 2 2
13.化学与生活、环境和生产密切相关。下列叙述不涉及氧化还原反应的是
A.使用添加氟化物牙膏预防龋齿 B.绿化造林助力实现碳中和目标
C.用氯化铁溶液制作铜印刷电路板 D.用 泡腾片杀灭新型冠状病毒
二、实验题
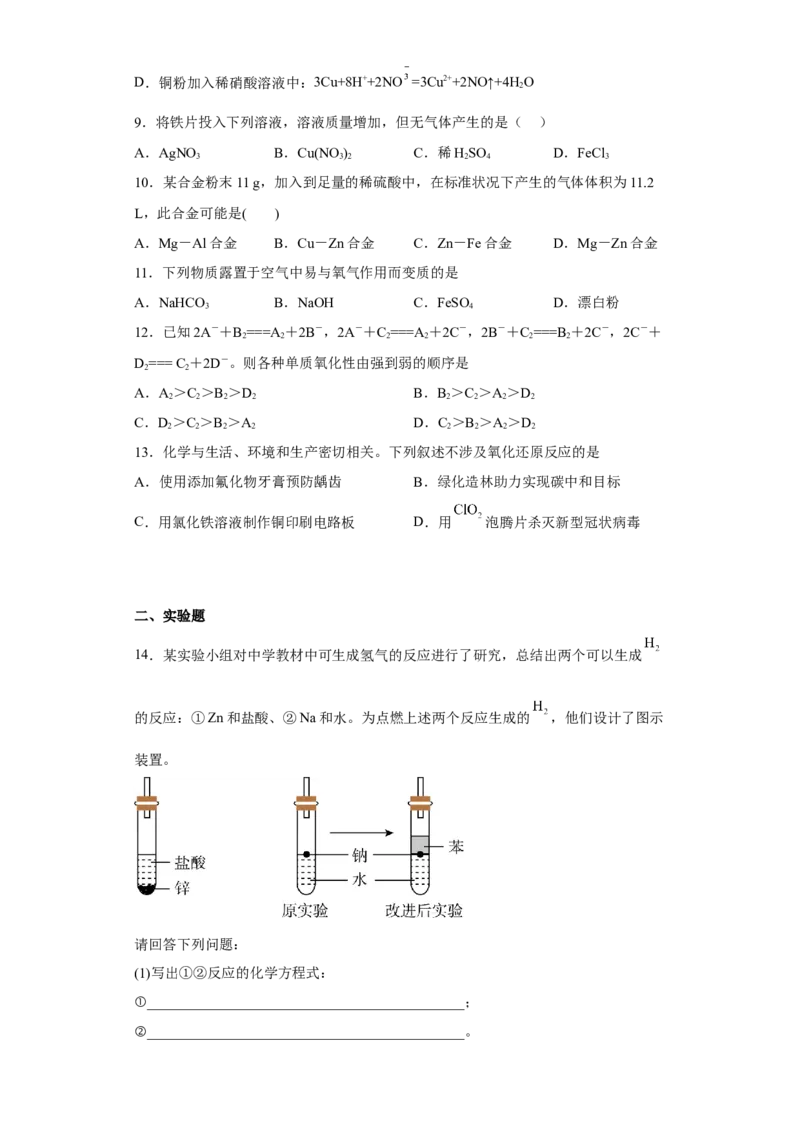
14.某实验小组对中学教材中可生成氢气的反应进行了研究,总结出两个可以生成
的反应:①Zn和盐酸、②Na和水。为点燃上述两个反应生成的 ,他们设计了图示
装置。
请回答下列问题:
(1)写出①②反应的化学方程式:
①_____________________________________________;
②_____________________________________________。(2)在点燃 之前必须先_________________________
(3)实验小组在点燃用上述装置制得的 时,①实验获得成功,②实验却失败了。他们
分析认为失败的原因是 与 的反应速率太快, 的用量太少。于是他们准备增
加钠的用量,可老师说太危险,你认为产生危险的原因为
_____________________________________________。
(4)实验小组查阅得钠、苯、水的密度分别为0.97 、0.88 、1.00 ,
并据此对实验进行了改进。在改进后的实验中 的生成速率会_______(填“加快”或
“减缓”)。改进后的实验现象为
____________________________________________________。
三、元素或物质推断题
15.铁是人体内含量最多的必需微量元素,缺铁性贫血患者应补充含Fe2+的亚铁盐。
“速力菲”(主要成分:琥珀酸亚铁)是一种常见的补铁药物。某兴趣小组为了检验“速
力菲”药片中Fe2+的存在并测定铁元素的含量,设计如下实验(假设反应过程无铁元素
损耗):
请回答下列问题:
(1)写出 的一种常见用途_______;
(2)操作Ⅰ的名称是_______,试剂1是_______(填试剂名称)。
(3)证明药片中含有Fe2+的依据_______。
(4)淡红色溶液中加入氯水,发生反应的离子方程式为_______。
(5)“速力菲”药片中铁元素的含量为_______(用含有a、b的式子表示)。
16.已知A是一种淡黄色固体,可做供氧剂,C为具有磁性的黑色晶体,E的焰色反
应为黄色,F为红褐色固体(部分产物已略去)。
试卷第4页,共3页(1)物质A、F的化学式分别是_____________、_____________。
(2)C→D的过程中第②步反应的离子方程式是
____________________________________。
(3)如何检验D中的金属阳离子,说明具体的操作和实验现象
________________________。
(4)E溶液与地壳中含量最多的金属元素的单质发生反应的化学方程式为
______________。
(5)G与D溶液也能发生反应,其反应的类型为___________________(填序号)。
a.化合反应 b.置换反应 c.复分解反应 d.氧化还原反应参考答案:
1.A
【详解】A.氢氧化铁不稳定,灼烧分解得到氧化铁,故A正确;B.铁在纯氧中燃烧生成
四氧化三铁,不能生成氧化铁,故B错误;C.灼热的Fe与水蒸气反应生成四氧化三铁和
氢气,不能生成氧化铁,故C错误;D.加热蒸干Fe (SO ) 溶液,硫酸铁水解生成硫酸和
2 4 3
氢氧化铁,加热蒸干,硫酸是难挥发性酸,水挥发,得到硫酸铁固体,不能得到氧化铁,
故D错误;答案为A。
2.C
【详解】A.向海带灰浸出液中加入硫酸、双氧水发生氧化还原反应,离子方程式为:2I-+
2H++HO=I +2HO,故A正确;
2 2 2 2
B. 碳酸氢钠溶液与足量氢氧化钡溶液混合,化学方程式为:
Ba(OH) +NaHCO=BaCO ↓+NaOH+HO,所以离子方程式为:HCO -+Ba2++OH-
2 3 3 2 3
═BaCO↓+H O,故B正确;
3 2
C.Al(OH) 与过量的氨水不反应,故C错误;
3
D.电解饱和氯化钠溶液反应方程式:2NaCl+2H O 2NaOH+H ↑+Cl↑,所以离子方程
2 2 2
式为:2Cl-+2HO H↑+Cl↑+2OH-,故D正确。
2 2 2
故选C。
【点睛】C项为易错点,注意氢氧化铝只能溶于强碱不能溶于氨水等弱碱。
3.B
【详解】A.SiO 不与HCl反应,A错误;
2
B.Al O 与NaOH反应得到NaAlO ,NaAlO 溶液中通入过量的CO,可得到Al(OH) ,化
2 3 2 2 2 3
学方程式分别为Al O+2NaOH=2NaAlO +HO,NaAlO +CO+2HO=NaHCO +
2 3 2 2 2 2 2 3
Al(OH) ↓,B正确;
3
C.FeS 与O 反应生成二氧化硫,得不到SO ,C错误;
2 2 3
D.FeCl 溶液加热后得不到无水FeCl ,由于Fe3+会水解,加热促进水解,最终得到氢氧化
3 3
铁,D错误;
答案选B。
4.A
【分析】烧瓶②中盛水,加热烧瓶②提供水蒸气,水蒸气和铁粉在①中反应生成四氧化三铁和氢气,烧瓶③用作安全瓶,④处收集氢气。
【详解】A.试管①是铁粉和水蒸气反应装置,烧瓶②用于提供反应物水蒸气,烧瓶③用
作安全瓶,防倒吸,故A正确;
B.反应需要高温,需要水蒸气,故需要对①②进行加热,故B错误;
C.①②中依次盛装铁粉、水,③中不需要加试剂,故C错误;
D.④处收集的是氢气,用排水法,因为甲烷不易溶于水,可用此法收集,而氨气极易溶
于水,不能用排水法,故D错误;
故答案为A。
5.D
【分析】根据分析得到AB段或0E段发生反应: ,
EF段或BC段发生反应 ,CD段或FG段发生反应
。
【详解】A.向 , 的溶液中不断加入一定浓度的酸性 溶液,说
明开始时 浓度不断降低, 浓度不断增大,因此 段对应的离子为 ,故A正确;
B.B点 恰好反应完,E点 浓度达到最大值,向溶液中继续加高锰酸钾溶液,则
段发生反应②的反应,F点 全部反应完, 达到最大值,所以 段发生反应③,
故B正确;
C.根据A选项和方程式 ,得到原溶液中
,则 ,故C正确;
D.根据前面分析得到FG发生 反应,根据质量
答案第2页,共2页守恒F点 ,乙点 物质的量消耗了5mol,生成 物质的量为5mol,
整个溶液中 物质的量为5mol,即乙点时: ,故D错误。
综上所述,答案为D。
6.B
【详解】A. ,HCl可以直接化合生成,A正确;
B. ,因此FeCl 不能由单质直接化合而成,B错误;
2
C. ,CO 可以由C与O 直接化合而得,C正确;
2 2
D. ,NaO 可以由Na与O 直接化合得到,D正确。
2 2 2
故本题选B。
7.C
【详解】A. 向FeCl 溶液中滴加KSCN溶液,溶液显红色 ,所以可用KSCN溶液检验
3
Fe3+,故A正确;B. 向FeSO 溶液中滴入K[Fe(CN)]溶液,生成蓝色沉淀 ,故K[Fe
4 3 6 3
(CN)]溶液可用于检验Fe2+;故B正确;C. 把饱和的FeCl 溶液滴加到沸水中至溶液呈
6 3
红褐色 ,可制得氢氧化铁胶体,若直接把饱和氯化铁溶液煮沸会生成氢氧化铁沉淀,C不
正确;D. 配制FeCl 溶液时,为防止氯化铁水解,可先将FeCl 固体溶于盐酸中,再加适量
3 3
的蒸馏水稀释到所需要的浓度即可,故D正确;答案:C。
8.C
【详解】A.向碳酸钠溶液中通入二氧化碳,溶液中的碳酸根与水和二氧化碳反应生成碳
酸氢根,反应的离子方程式为CO +CO +H O=2HCO ,A正确;
2 2
B.氯单质具有氧化性,可以和二氧化硫反应生成硫酸根,反应的离子方程式为
Cl+2H O+SO =4H++2Cl-+SO ,B正确;
2 2 2
C.氯气具有氧化性,可以与I-和Fe2+发生反应,因I-的还原性强于Fe2+,则向FeI 溶液中
2
通入少量的Cl,Cl 先与I-反应,反应的离子方程式为2I-+Cl=2Cl-+I ,C错误;
2 2 2 2D.硝酸具有氧化性,可以和Cu反应生成一氧化氮,反应的离子方程式为3Cu+8H++2NO
=3Cu2++2NO↑+4HO,D正确;
2
故答案选C。
9.D
【详解】A.Fe置换出Ag,溶液质量减小,故A错误;
B.Fe置换出Cu,溶液质量减小,故B错误;
C.反应生成硫酸亚铁和氢气,溶液质量增加,但生成气体,故C错误;
D.反应生成氯化亚铁,无固体析出,溶液质量增加,且没有气体生成,故D正确;
答案选D。
10.A
【详解】标准状况下11.2L氢气的物质的量为n(H )= =0.5mol,则转移电子
2
的物质的量n(e-)=2n(H)=2×0.5mol=1mol。11g混合金属反应过程中失去1mol电子,则金属
2
产生1mol电子需要质量一种大于11g,一种小于11g。
A.Mg是+2价金属,摩尔质量是24g/mol,所以产生1mol电子需要质量为24g÷2=12g;Al
是+3价金属,摩尔质量是27g/mol,所以产生1mol电子需要质量为27g÷3=9g;
9g<11g<12g,符合题意;
B.Zn是+2价金属,摩尔质量是65g/mol,所以产生1mol电子需要质量为65g÷2=32.5g;Cu
与稀硫酸不能反应,所以可认为是无穷大,两种金属需要的质量都大于11g,B不符合题意;
C.Zn是+2价金属,摩尔质量是65g/mol,所以产生1mol电子需要质量为65g÷2=32.5g;Fe
是+2价金属,摩尔质量是56g/mol,所以产生1mol电子需要质量为56g÷2=28g;两种金属
产生1mol电子需要质量都大于11g,C不符合题意;
D.Mg是+2价金属,摩尔质量是24g/mol,所以产生1mol电子需要质量为24g÷2=12g;Zn
是+2价金属,摩尔质量是65g/mol,所以产生1mol电子需要质量为65g÷2=32.5g;;两种
金属产生1mol电子需要质量都大于11g,D不符合题意;
故合理选项是A。
11.C
【详解】A.NaHCO 在空气中较稳定,不易变质,故A不选;
3
B.NaOH易与空气中的二氧化碳反应最终生成碳酸钠,NaOH不和氧气反应,故B不选;
C.FeSO 具有还原性,易被空气中的氧气氧化而变质,故C选;
4
答案第4页,共2页D.漂白粉中的Ca(ClO) 可以和空气中的水蒸气、二氧化碳反应:
2
Ca(ClO) +CO +H O=CaCO +2HClO,生成的HClO不稳定,容易分解生成HCl和氧气,漂
2 2 2 3
白粉露置在空气中会变质,但不是和氧气反应而变质的,故D不选;
故选C。
12.C
【详解】在氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,根据2A-+B ===A
2 2
+2B-可知氧化剂是B ,氧化产物是A,则氧化性是B >A;根据2A-+C ===A+2C-
2 2 2 2 2 2
可知氧化剂是C ,氧化产物是A,则氧化性是C >A;根据2B-+C ===B +2C-可知氧
2 2 2 2 2 2
化剂是C ,氧化产物是B ,则氧化性是C >B ;根据2C-+D===C +2D-可知氧化剂是
2 2 2 2 2 2
D,氧化产物是C ,则氧化性是D>C ,所以各种单质氧化性由强到弱的顺序是D>C >
2 2 2 2 2 2
B >A,答案选C。
2 2
13.A
【详解】A.使用添加氟化物牙膏预防龋齿,该过程中是发生沉淀的转化,将牙釉质转化
为含氟的更坚硬的沉淀,发生的是复分解反应,故不涉及元素化合价变化,不属于氧化还
原反应,A符合题意;
B.绿化造林助力实现碳中和目标,即让绿色植物进行光合作用,故涉及C、O元素化合价
变化,属于氧化还原反应,B不合题意;
C.用氨化铁溶液制作铜印刷电路板,发生的反应为:2FeCl +Cu=CuCl +2FeCl ,涉及Fe
3 2 2
元素化合价变化,属于氧化还原反应,C不合题意;
D.用ClO 泡腾片杀灭新型冠状病毒,利用ClO 的强氧化性,使蛋白质被氧化而发生变性,
2 2
自身被还原为Cl-,故有元素化合价变化,属于氧化还原反应,D不合题意;
故答案为:A。
14.
检验 的纯度 大块的钠与水反应剧烈,放出大量的热,可能将试管内 和
的混合气点燃而发生爆炸 减缓 钠处于苯和水的交界处,钠与水反应产
生的 使钠浮起,脱离水面,反应停止,当钠表面的 逸出,钠又回落水层,如此反复,
钠间歇与水反应
【分析】本实验通过Zn与稀盐酸的反应和Na与水的反应制取氢气,并验证产物是否为氢气;在点燃氢气前需要验纯,据此分析。
【详解】(1)锌与盐酸反应生成氯化锌和氢气,化学方程式为 ;钠
与水反应生成氢氧化钠和氢气,化学方程式为 。
(2)在点燃 之前必须先检验 的纯度,以免发生爆炸。
(3)大块的钠与水反应剧烈,放出大量的热,可能将试管内 和 的混合气点燃而发生爆
炸。
(4)钠处于苯和水的界面处,钠与水反应产生的 使钠浮起,脱离水面,反应停止;当钠
表面的 逸出,钠又回落水层,如此反复,减缓了 与 的反应速率。
15.(1)作红色油漆(或红色颜料、涂料、油墨,答案合理即可)
(2) 过滤 硫氰化钾溶液(或硫氰化钾)
(3)淡黄色溶液中加入KSCN溶液,溶液颜色变为淡红色,再加入氯水,溶液变为红色
(4)
(5)
【分析】某同学为了检测“速力菲”药片中Fe2+的存在,将药片破碎研细后加入盐酸溶解、
过滤,过滤得到淡黄色溶液和不溶物,淡黄色溶液中加入KSCN溶液,变为淡红色溶液,
说明部分亚铁离子被氧化为铁离子,加入氯水溶液变为血红色,亚铁离子全部被氧化生成
铁离子,所以得到红色溶液,然后经过多步反应,铁离子全部转化为bg氧化铁固体,据此
分析回答。
(1)
Fe O 是红色固体,常见用途作红色油漆,故答案为:作红色油漆;
2 3
(2)
根据分析可知操作1是分离固体和溶液,操作Ⅰ的名称是过滤;淡黄色溶液中加入试剂Ⅰ
为KSCN溶液,变为淡红色溶液,故答案为:过滤;硫氰化钾溶液;
(3)
答案第6页,共2页淡黄色溶液中加入KSCN溶液,变为淡红色溶液,说明部分亚铁离子被氧化为铁离子,再
加入氯水溶液变为血红色,亚铁离子全部被氧化生成铁离子,得到红色溶液,故答案为:
淡黄色溶液中加入KSCN溶液,溶液颜色变为淡红色,再加入氯水,溶液变为红色;
(4)
因Fe2+与Cl 反应生成Fe3+和Cl-,反应为:Cl+2Fe2+=2Cl-+2Fe3+,故答案为:Cl+2Fe2+=2Cl-
2 2 2
+2Fe3+;
(5)
根据铁元素守恒,a g“速力菲”药片中铁元素最后全部转化为b g氧化铁中的铁元素,所以
“速力菲”药片中铁元素的含量为 ,故答案为: 。
16. NaO Fe(OH) 2Fe2++Cl=2Fe3++2Cl- 取少量D溶液于试管
2 2 3 2
中,滴加KSCN溶液,溶液显血红色(其它合理答案也得分 2Al+2NaOH+2HO
2
=2NaAlO +3H↑ ad
2 2
【分析】已知A是一种淡黄色固体,可做供氧剂,应为NaO,C为具有磁性的黑色晶体,
2 2
应为Fe O,E的焰色反应为黄色,则由转化关系可知E为NaOH,B为O,D为FeCl ,F
3 4 2 3
为红褐色固体,应为Fe(OH) ,以此解答该题。
3
【详解】(1)由以上分析可知A为NaO ,F为Fe(OH) ,故答案为:NaO ;Fe(OH)
2 2 3 2 2 3
;
(2)C→D的过程中第②步反应的离子方程式是2Fe2++Cl=2Fe3++2Cl-;
2
(3)D为FeCl ,阳离子为铁离子,检验铁离子,可取少量D溶液于试管中,滴加KSCN
3
溶液,可观察到溶液显血红色,故答案为:取少量D溶液于试管中,滴加KSCN溶液,溶
液显血红色;
(4)地壳中含量最多的金属为铝,与氢氧化钠反应的方程式为
2Al+2NaOH+2H O=2NaAlO +3H ↑;
2 2 2
(5)铁与氯化铁反应生成氯化亚铁,为化合反应和氧化还原反应,故答案为:ad。
【点睛】题目涉及浓硫酸、硝酸的性质,物质的颜色、反应现象及特殊反应是推断突破口,
注意对基础知识的全面掌握。答案第8页,共2页