文档内容
济宁市第一中学 2024 届高三 3 月份定时检测
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
可能用到的相对原子质量:H1 N14 O16 Cl35.5 Ca40 Br80 I127
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.2023年10月26日11时14分,神舟十七号载人飞船点火升空成功发射,我国航天航空事业再次迎来
飞速发展。下列有关说法正确的是
A.飞船返回舱逃逸系统复合材料中的酚醛树脂属于合成纤维
B.飞船舱体外壳部件材料是铝合金材料制成,主要是利用了其密度大、硬度大的特性
C.制造5G芯片的氮化铝晶圆属于传统无机非金属材料
D.新型火箭燃料航空煤油是石油分馏产品
2.下列实验操作正确的是
A.用酒精清洗试管内壁附着的硫
B.蒸发浓缩冷却结晶时,应加热至有大量晶体析出时,停止加热
C.用pH计监测乙酸乙酯的水解程度
D.液溴沾到皮肤上,立即用苯洗涤,然后用水冲净,涂上甘油
3.有机金属氯化物由原子序数依次增大的短周期主族元素X、Y、Z、M、N组成,部分结构如图所示,
基态原子M核外电子所占据原子轨道全充满,N元素的价层电子排布式为nsn-1np2n-1,下列说法正确的是
A.氢化物的沸点:Z>Y
B.Z与N可形成化合物ZN 、ZN
3 5
C.M元素的第一电离能比同周期相邻元素的大
D.YX +、YX -离子中Y的杂化类型相同
3 3
4.在允许加热的前提下,只用一种试剂不能鉴别对应溶液的是
A.用Ba(OH) 溶液鉴别NH Cl、(NH ) SO 、NaCl、Na SO
2 4 4 2 4 2 4
B.用红色石蕊试纸鉴别Na SO 、浓HNO 、NaHCO 、氯水
2 3 3 3
C.用NaOH溶液鉴别MgCl 、FeCl 、Al (SO ) 、(NH ) SO
2 2 2 4 3 4 2 4
D.用FeCl 溶液鉴别NaI、Ba(OH) 、Na S、NaHCO
3 2 2 3
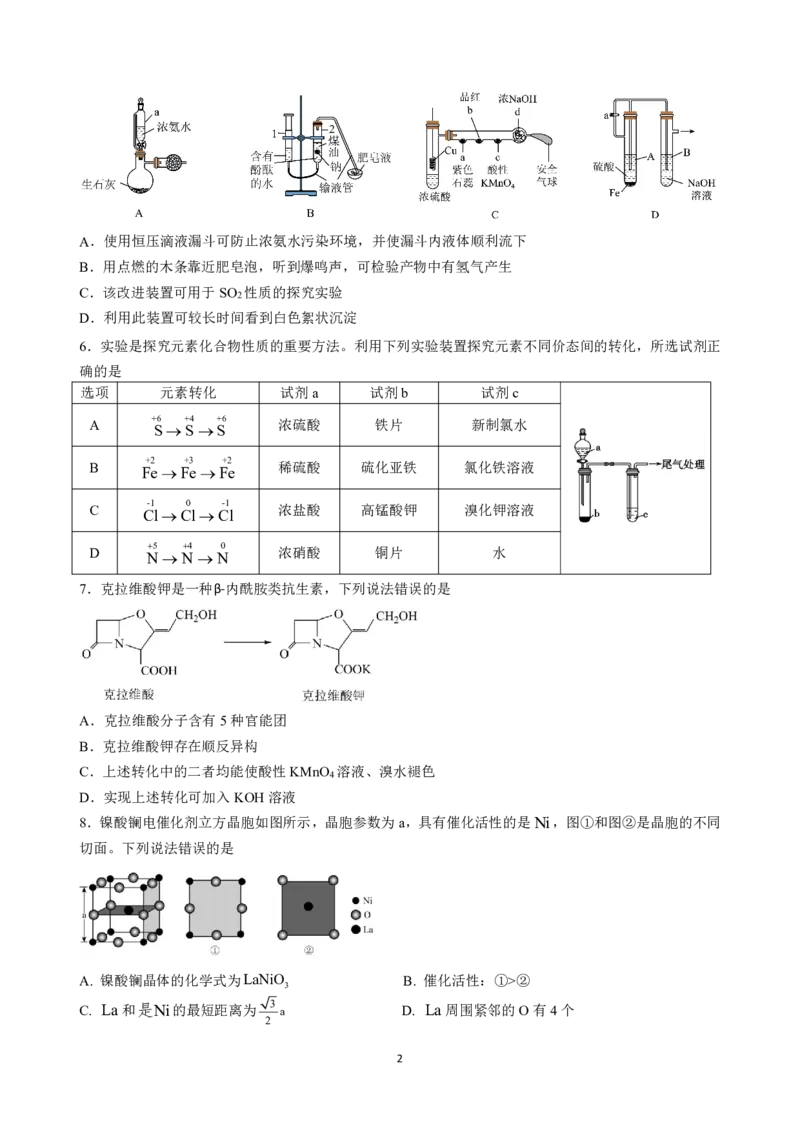
5.实验改进与优化应遵循科学性、直观性、易操作性、安全性的原则,提升化学实验效率。下列有关实
验改进分析不正确的是
1
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}A.使用恒压滴液漏斗可防止浓氨水污染环境,并使漏斗内液体顺利流下
B.用点燃的木条靠近肥皂泡,听到爆鸣声,可检验产物中有氢气产生
C.该改进装置可用于SO 性质的探究实验
2
D.利用此装置可较长时间看到白色絮状沉淀
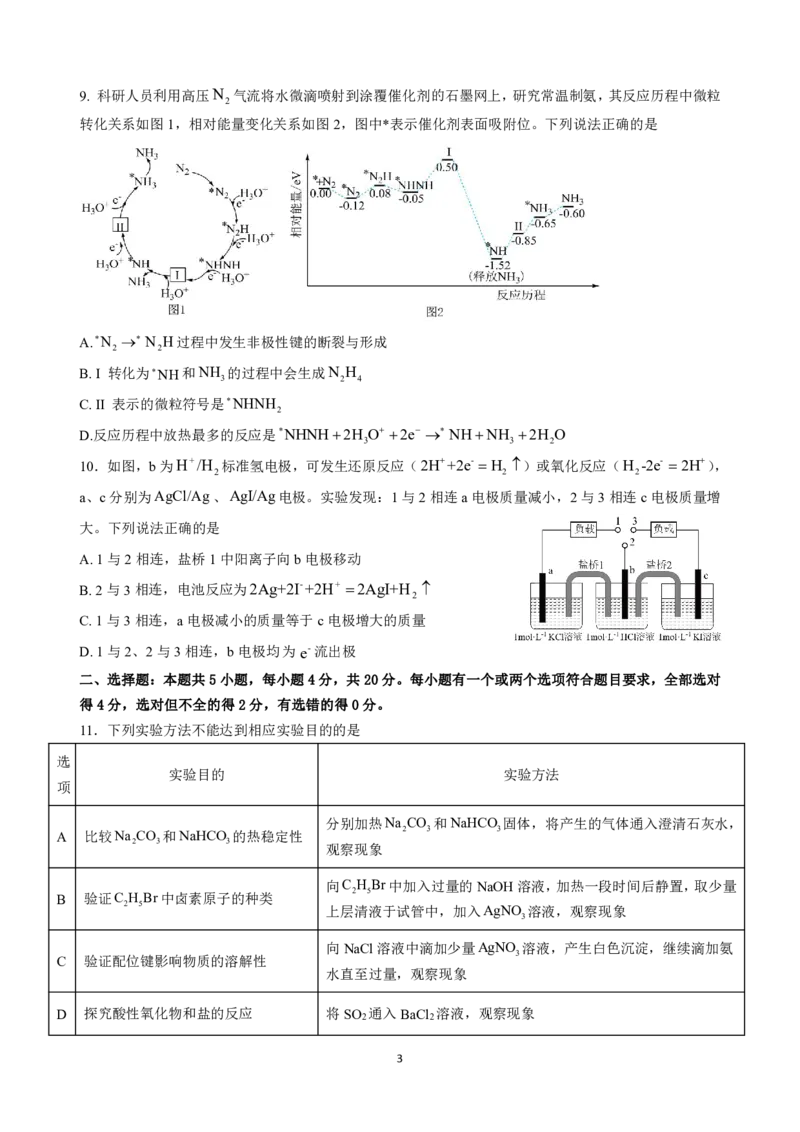
6.实验是探究元素化合物性质的重要方法。利用下列实验装置探究元素不同价态间的转化,所选试剂正
确的是
选项 元素转化 试剂a 试剂b 试剂c
A + S 6 + S 4 + S 6 浓硫酸 铁片 新制氯水
B F +2 eF +3 eF +2 e 稀硫酸 硫化亚铁 氯化铁溶液
C C -1 lC 0 lC -1 l 浓盐酸 高锰酸钾 溴化钾溶液
D N 5 N 4 N 0 浓硝酸 铜片 水
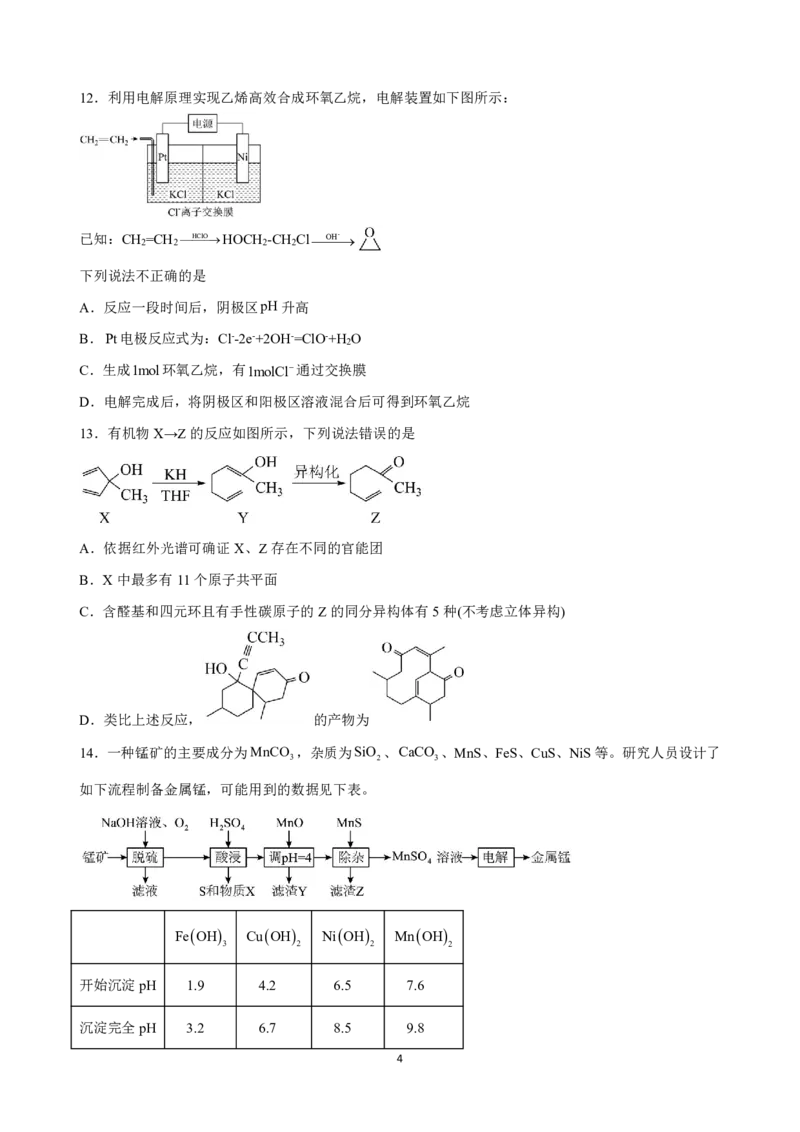
7.克拉维酸钾是一种β-内酰胺类抗生素,下列说法错误的是
A.克拉维酸分子含有5种官能团
B.克拉维酸钾存在顺反异构
C.上述转化中的二者均能使酸性KMnO 溶液、溴水褪色
4
D.实现上述转化可加入KOH溶液
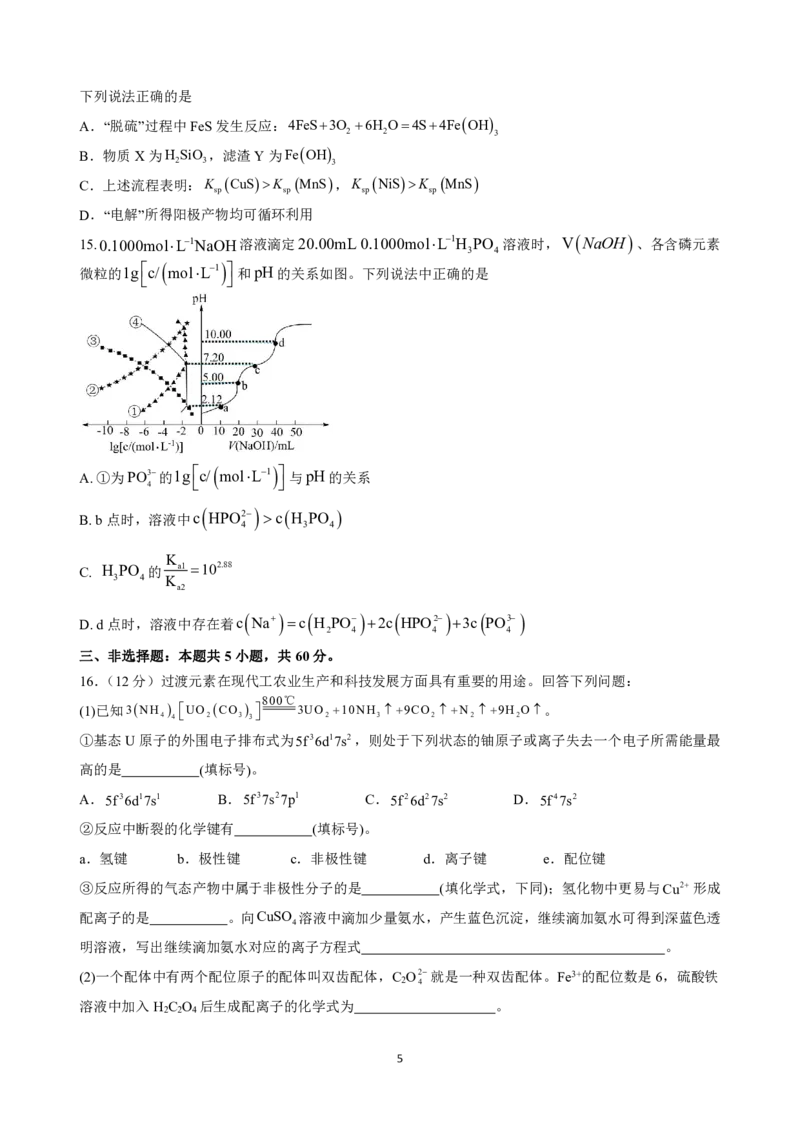
8.镍酸镧电催化剂立方晶胞如图所示,晶胞参数为a,具有催化活性的是Ni,图①和图②是晶胞的不同
切面。下列说法错误的是
A. 镍酸镧晶体的化学式为LaNiO B. 催化活性:①>②
3
C. La和是Ni的最短距离为 3 a D. La周围紧邻的O有4个
2
2
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}9. 科研人员利用高压N 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒
2
转化关系如图1,相对能量变化关系如图2,图中*表示催化剂表面吸附位。下列说法正确的是
A. N N H过程中发生非极性键的断裂与形成
2 2
B.Ⅰ 转化为NH和NH 的过程中会生成N H
3 2 4
C.Ⅱ
表示的微粒符号是NHNH
2
D.反应历程中放热最多的反应是NHNH2H O 2e NHNH 2H O
3 3 2
10.如图,b为H+/H 标准氢电极,可发生还原反应(2H++2e- H )或氧化反应(H -2e- 2H+),
2 2 2
a、c分别为AgCl/Ag、AgI/Ag电极。实验发现:1与2相连a电极质量减小,2与3相连c电极质量增
大。下列说法正确的是
A.1与2相连,盐桥1中阳离子向b电极移动
B.2与3相连,电池反应为2Ag+2I-+2H+ 2AgI+H
2
C.1与3相连,a电极减小的质量等于c电极增大的质量
D.1与2、2与3相连,b电极均为 e-流出极
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对
得4分,选对但不全的得2分,有选错的得0分。
11.下列实验方法不能达到相应实验目的的是
选
实验目的 实验方法
项
分别加热Na CO 和NaHCO 固体,将产生的气体通入澄清石灰水,
2 3 3
A 比较Na CO 和NaHCO 的热稳定性
2 3 3
观察现象
向C H Br中加入过量的NaOH溶液,加热一段时间后静置,取少量
2 5
B 验证C H Br中卤素原子的种类
2 5
上层清液于试管中,加入AgNO 溶液,观察现象
3
向NaCl溶液中滴加少量AgNO 溶液,产生白色沉淀,继续滴加氨
3
C 验证配位键影响物质的溶解性
水直至过量,观察现象
D 探究酸性氧化物和盐的反应 将SO 通入BaCl 溶液,观察现象
2 2
3
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}12.利用电解原理实现乙烯高效合成环氧乙烷,电解装置如下图所示:
已知:CH
2
=CH
2
HClOHOCH
2
-CH
2
ClOH-
下列说法不正确的是
A.反应一段时间后,阴极区pH升高
B.Pt电极反应式为:Cl--2e-+2OH-=ClO-+H O
2
C.生成1mol环氧乙烷,有1molCl通过交换膜
D.电解完成后,将阴极区和阳极区溶液混合后可得到环氧乙烷
13.有机物X→Z的反应如图所示,下列说法错误的是
A.依据红外光谱可确证X、Z存在不同的官能团
B.X中最多有11个原子共平面
C.含醛基和四元环且有手性碳原子的Z的同分异构体有5种(不考虑立体异构)
D.类比上述反应, 的产物为
14.一种锰矿的主要成分为MnCO ,杂质为SiO 、CaCO 、MnS、FeS、CuS、NiS等。研究人员设计了
3 2 3
如下流程制备金属锰,可能用到的数据见下表。
FeOH CuOH NiOH MnOH
3 2 2 2
开始沉淀pH 1.9 4.2 6.5 7.6
沉淀完全pH 3.2 6.7 8.5 9.8
4
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}下列说法正确的是
A.“脱硫”过程中FeS发生反应:4FeS3O 6H O4S4FeOH
2 2 3
B.物质X为H SiO ,滤渣Y为FeOH
2 3 3
C.上述流程表明:K CuSK MnS,K NiSK MnS
sp sp sp sp
D.“电解”所得阳极产物均可循环利用
15.0.1000molL1NaOH溶液滴定20.00mL 0.1000molL1H PO 溶液时,V NaOH 、各含磷元素
3 4
微粒的1gc/ molL1 和pH的关系如图。下列说法中正确的是
A.①为PO3的1gc/ molL1 与pH的关系
4
B.b点时,溶液中c HPO2 c H PO
4 3 4
K
C. H PO 的 a1 102.88
3 4 K
a2
D.d点时,溶液中存在着c Na c H PO 2c HPO2 3c PO3
2 4 4 4
三、非选择题:本题共5小题,共60分。
16.(12分)过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
800℃
(1)已知3NH
4
4
UO
2
CO
3
3
3UO
2
10NH
3
9CO
2
N
2
9H
2
O。
①基态U原子的外围电子排布式为5f36d17s2,则处于下列状态的铀原子或离子失去一个电子所需能量最
高的是 (填标号)。
A.5f36d17s1 B.5f37s27p1 C.5f26d27s2 D.5f47s2
②反应中断裂的化学键有 (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是 (填化学式,下同);氢化物中更易与Cu2形成
配离子的是 。向CuSO 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透
4
明溶液,写出继续滴加氨水对应的离子方程式 。
(2)一个配体中有两个配位原子的配体叫双齿配体,C O2就是一种双齿配体。Fe3+的配位数是6,硫酸铁
2 4
溶液中加入H C O 后生成配离子的化学式为 。
2 2 4
5
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}(3)四羰基镍NiCO 是制备铂镍合金的重要原料之一,NiCO 为无色有挥发性的剧毒液体,呈四面体
4 4
构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是 。
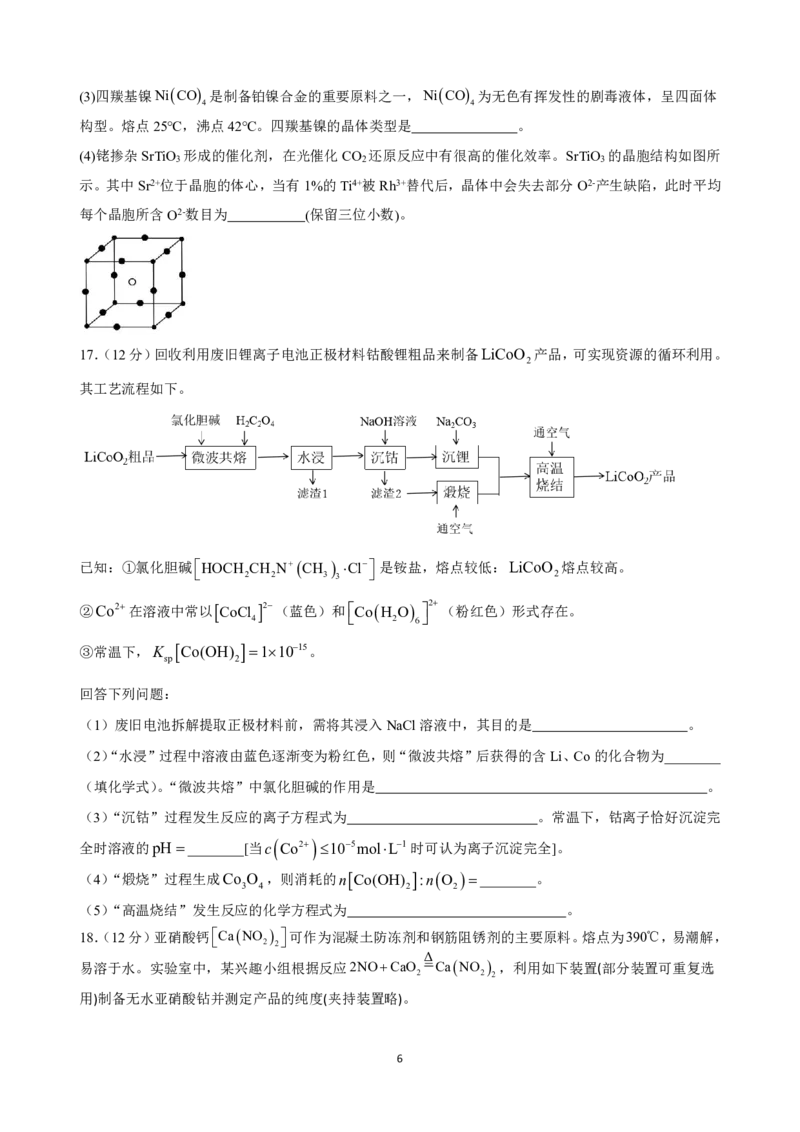
(4)铑掺杂SrTiO 形成的催化剂,在光催化CO 还原反应中有很高的催化效率。SrTiO 的晶胞结构如图所
3 2 3
示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均
每个晶胞所含O2-数目为 (保留三位小数)。
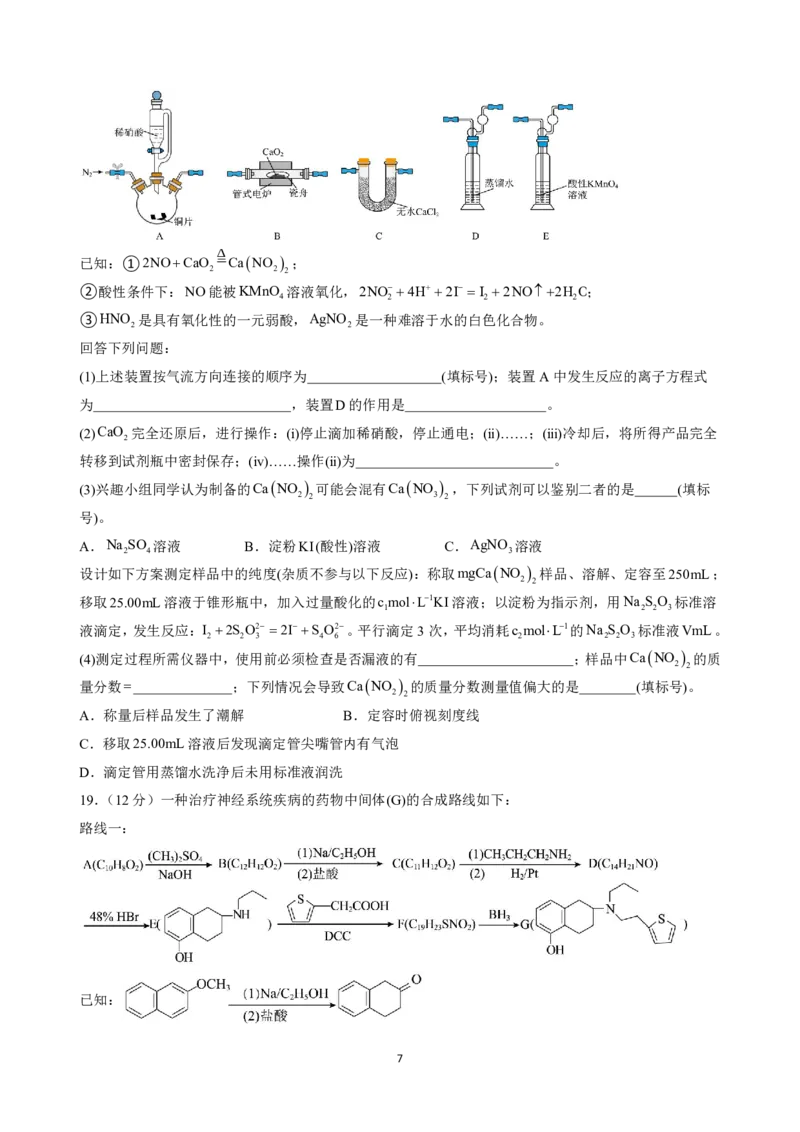
17.(12分)回收利用废旧锂离子电池正极材料钴酸锂粗品来制备LiCoO 产品,可实现资源的循环利用。
2
其工艺流程如下。
已知:①氯化胆碱HOCH CH NCH Cl 是铵盐,熔点较低:LiCoO 熔点较高。
2 2 3 3 2
②Co2在溶液中常以 CoCl 2(蓝色)和Co H O 2 (粉红色)形式存在。
4 2 6
③常温下,K Co(OH) 11015。
sp 2
回答下列问题:
(1)废旧电池拆解提取正极材料前,需将其浸入NaCl溶液中,其目的是 。
(2)“水浸”过程中溶液由蓝色逐渐变为粉红色,则“微波共熔”后获得的含Li、Co的化合物为________
(填化学式)。“微波共熔”中氯化胆碱的作用是 。
(3)“沉钴”过程发生反应的离子方程式为 。常温下,钴离子恰好沉淀完
全时溶液的pH ________[当c Co2 105molL1 时可认为离子沉淀完全]。
(4)“煅烧”过程生成Co O ,则消耗的n Co(OH) :n O ________。
3 4 2 2
(5)“高温烧结”发生反应的化学方程式为 。
18.(12分)亚硝酸钙
CaNO
2
2
可作为混凝土防冻剂和钢筋阻锈剂的主要原料。熔点为390℃,易潮解,
Δ
易溶于水。实验室中,某兴趣小组根据反应2NOCaO CaNO ,利用如下装置(部分装置可重复选
2 2 2
用)制备无水亚硝酸钻并测定产品的纯度(夹持装置略)。
6
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}Δ
已知:①2NOCaO CaNO ;
2 2 2
②酸性条件下:NO能被KMnO 溶液氧化,2NO4H2I I 2NO2H O;
4 2 2 2
③HNO 是具有氧化性的一元弱酸,AgNO 是一种难溶于水的白色化合物。
2 2
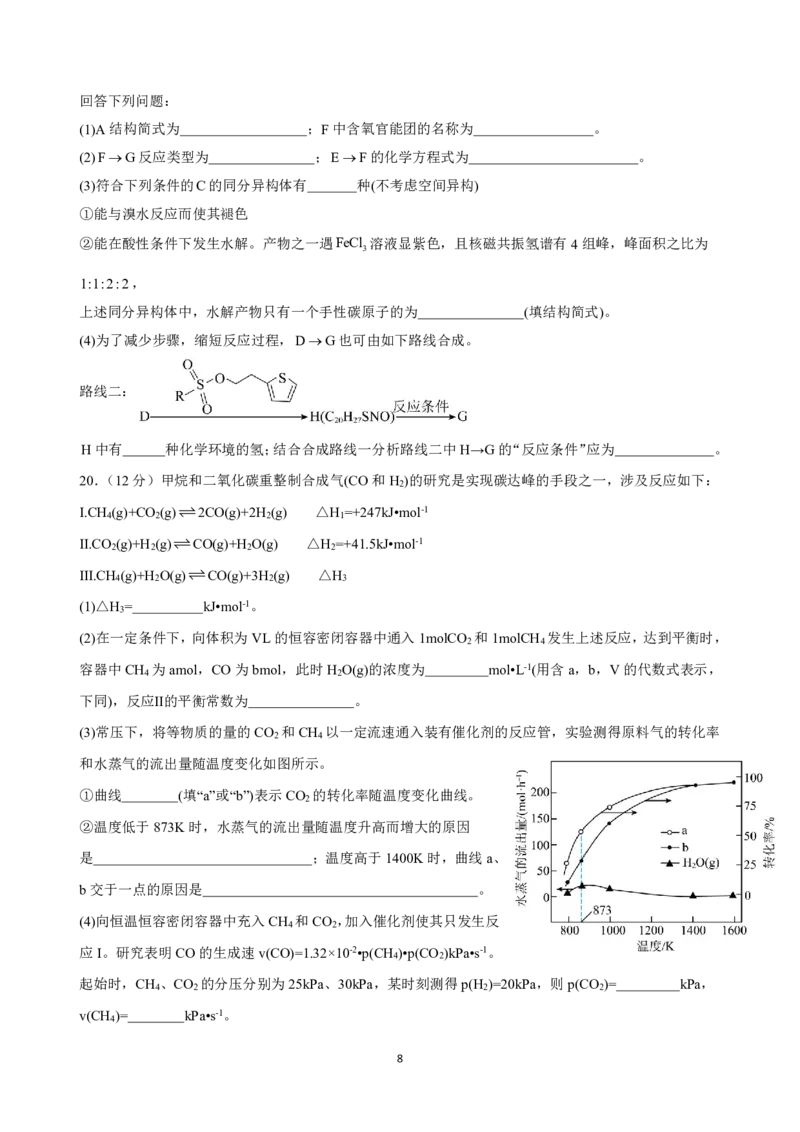
回答下列问题:
(1)上述装置按气流方向连接的顺序为 (填标号);装置A中发生反应的离子方程式
为 ,装置D的作用是 。
(2)CaO 完全还原后,进行操作:(ⅰ)停止滴加稀硝酸,停止通电;(ⅱ)……;(ⅲ)冷却后,将所得产品完全
2
转移到试剂瓶中密封保存;(ⅳ)……操作(ⅱ)为 。
(3)兴趣小组同学认为制备的CaNO 可能会混有CaNO ,下列试剂可以鉴别二者的是 (填标
2 2 3 2
号)。
A.Na SO 溶液 B.淀粉KI(酸性)溶液 C.AgNO 溶液
2 4 3
设计如下方案测定样品中的纯度(杂质不参与以下反应):称取mgCaNO 样品、溶解、定容至250mL;
2 2
移取25.00mL溶液于锥形瓶中,加入过量酸化的cmolL1KI溶液;以淀粉为指示剂,用Na S O 标准溶
1 2 2 3
液滴定,发生反应:I 2S O2 2IS O2。平行滴定3次,平均消耗c molL1的Na S O 标准液VmL。
2 2 3 4 6 2 2 2 3
(4)测定过程所需仪器中,使用前必须检查是否漏液的有 ;样品中CaNO 的质
2 2
量分数 ;下列情况会导致CaNO 的质量分数测量值偏大的是 (填标号)。
2 2
A.称量后样品发生了潮解 B.定容时俯视刻度线
C.移取25.00mL溶液后发现滴定管尖嘴管内有气泡
D.滴定管用蒸馏水洗净后未用标准液润洗
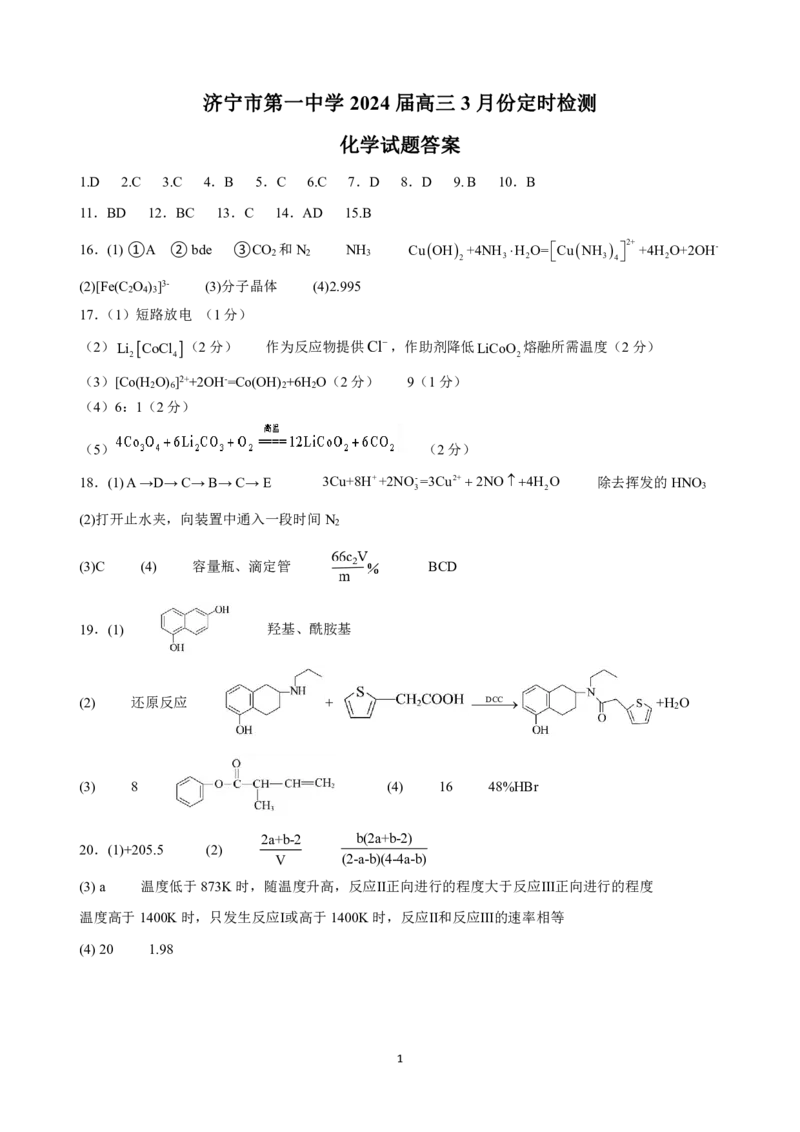
19.(12分)一种治疗神经系统疾病的药物中间体(G)的合成路线如下:
路线一:
已知:
7
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}回答下列问题:
(1)A结构简式为 ;F中含氧官能团的名称为 。
(2)FG反应类型为 ;EF的化学方程式为 。
(3)符合下列条件的C的同分异构体有 种(不考虑空间异构)
①能与溴水反应而使其褪色
②能在酸性条件下发生水解。产物之一遇FeCl 溶液显紫色,且核磁共振氢谱有4组峰,峰面积之比为
3
1:1:2:2,
上述同分异构体中,水解产物只有一个手性碳原子的为 (填结构简式)。
(4)为了减少步骤,缩短反应过程,DG也可由如下路线合成。
路线二:
H中有 种化学环境的氢;结合合成路线一分析路线二中H→G的“反应条件”应为 。
20.(12分)甲烷和二氧化碳重整制合成气(CO和H )的研究是实现碳达峰的手段之一,涉及反应如下:
2
I.CH (g)+CO (g)2CO(g)+2H (g) △H =+247kJ•mol-1
4 2 2 1
Ⅱ.CO (g)+H (g)CO(g)+H O(g) △H =+41.5kJ•mol-1
2 2 2 2
Ⅲ.CH (g)+H O(g)CO(g)+3H (g) △H
4 2 2 3
(1)△H = kJ•mol-1。
3
(2)在一定条件下,向体积为VL的恒容密闭容器中通入1molCO 和1molCH 发生上述反应,达到平衡时,
2 4
容器中CH 为amol,CO为bmol,此时H O(g)的浓度为 mol•L-1(用含a,b,V的代数式表示,
4 2
下同),反应Ⅱ的平衡常数为 。
(3)常压下,将等物质的量的CO 和CH 以一定流速通入装有催化剂的反应管,实验测得原料气的转化率
2 4
和水蒸气的流出量随温度变化如图所示。
①曲线 (填“a”或“b”)表示CO 的转化率随温度变化曲线。
2
②温度低于873K时,水蒸气的流出量随温度升高而增大的原因
是 ;温度高于1400K时,曲线a、
b交于一点的原因是 。
(4)向恒温恒容密闭容器中充入CH 和CO ,加入催化剂使其只发生反
4 2
应I。研究表明CO的生成速v(CO)=1.32×10-2•p(CH )•p(CO )kPa•s-1。
4 2
起始时,CH 、CO 的分压分别为25kPa、30kPa,某时刻测得p(H )=20kPa,则p(CO )= kPa,
4 2 2 2
v(CH )= kPa•s-1。
4
8
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}济宁市第一中学 2024届高三 3月份定时检测
化学答题卡
姓名:
班级:
贴条形码区
学校:
考场: 座号:
选择题(共15个题,1-10每小题2分,11-15每小题4分,共40分)
1.[A][B][C][D] 6. [ A ] [ B ] [ C ] [ D ] 11.[A][B][C][D]
2.[A][B][C][D] 7. [ A ] [ B ] [ C ] [ D ] 12.[A][B][C][D]
3.[A][B][C][D] 8. [ A ] [ B ] [ C ] [ D ] 13.[A][B][C][D]
4.[A][B][C][D] 9. [ A ] [ B ] [ C ] [ D ] 14.[A][B][C][D]
5.[A][B][C][D] 10. [ A ] [ B ] [ C ] [ D ] 15.[A][B][C][D]
非选择题(5个题,共60分)
16.(共12分)
(1)① (1分) ② (2分)
③ (1分) (1分)
(2分)
(2) (2分)
(3) (1分) (2分)
17.(共12分)
(1) (1分)
(2) (2分) (2分)
(3) (2分) (1分)
(4) (2分)
(5) (2分)
- 1 -
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}18.(共12分)
(1分)
((15)) (2分)
(1分)
(2) (1分)
(3) (1分)
(4) (2分) (2分) (2分)
19.(共12分)
(1) (1分) (2分)
(2) (1分)
(2分)
(3) (2分) (2分)
(4) (1分) (1分)
20.(共12分)
(1) (1分)
(2) (2分) (2分)
(3)① (1分)
② (2分)
(2分)
(4) (1分) (1分)
- 2 -
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}济宁市第一中学 2024 届高三 3 月份定时检测
化学试题答案
1.D 2.C 3.C 4.B 5.C 6.C 7.D 8.D 9.B 10.B
11.BD 12.BC 13.C 14.AD 15.B
16.(1)①A ②bde ③CO 和N NH CuOH +4NH H O=CuNH 2+ +4H O+2OH-
2 2 3 2 3 2 3 4 2
(2)[Fe(C O ) ]3- (3)分子晶体 (4)2.995
2 4 3
17.(1)短路放电 (1分)
(2)Li CoCl (2分) 作为反应物提供Cl,作助剂降低LiCoO 熔融所需温度(2分)
2 4 2
(3)[Co(H O) ]2++2OH-=Co(OH) +6H O(2分) 9(1分)
2 6 2 2
(4)6:1(2分)
(5) (2分)
18.(1)A→D→C→B→C→E 3Cu+8H++2NO-=3Cu2+2NO4H O 除去挥发的HNO
3 2 3
(2)打开止水夹,向装置中通入一段时间N
2
(3)C (4) 容量瓶、滴定管 BCD
19.(1) 羟基、酰胺基
(2) 还原反应 + DCC +H O
2
(3) 8 (4) 16 48%HBr
2a+b-2 b(2a+b-2)
20.(1)+205.5 (2)
V (2-a-b)(4-4a-b)
(3)a 温度低于873K时,随温度升高,反应Ⅱ正向进行的程度大于反应Ⅲ正向进行的程度
温度高于1400K时,只发生反应Ⅰ或高于1400K时,反应Ⅱ和反应Ⅲ的速率相等
(4)20 1.98
1
{#{QQABLQiUggAgAJAAARgCAQEACEAQkBCACIoOBAAIoAAAyQFABAA=}#}