文档内容
第一单元 物质及其变化
第二节 离子反应(一)
一、基础巩固
1.下列物质属于非电解质,但其水溶液能导电的是( )
A.BaSO B.SO C.NaOH D.Cl
4 2 2
2.既不是电解质,又不是非电解质的是( )
A.氯气 B.二氧化硫 C.酒精 D.冰醋酸
3.下列有关电解质的说法正确的是( )
A.强电解质一定是离子化合物
B.易溶性强电解质的稀溶液中不存在溶质分子
C.强电解质溶液的导电能力一定比弱电解质强
D.由于硫酸钡难溶于水,所以硫酸钡是弱电解质
4.能发生离子反应,但是不会产生沉淀的是( )
A.澄清石灰水中通入CO
2
B.NaHCO 溶液中滴加NaOH溶液
3
C.Na CO 溶液中滴加NaOH溶液
2 3
D.氯化钠溶液中滴加硝酸银溶液
5.下列各项操作中发生“先产生沉淀,然后沉淀又溶解”现象的是( )
向澄清石灰水中逐渐通入CO 至过量
2
①向NaAlO
2
溶液中逐渐通入CO
2
至过量
②向AlCl
3
溶液中逐滴加入NaOH至过量
③向硅酸钠溶液中逐滴加入盐酸至过量
④向Fe(OH)
3
胶体中逐滴加入稀盐酸至过量
⑤向Ca(ClO)
2
溶液中逐渐通入CO
2
至过量
⑥A. B. C. D.
6.下列①方③程式正确的是( ①)②⑤ ①③⑤⑥ ①②⑥A.NaHS的电离:NaHS═H++S2﹣+Na+
B.NaHCO 的水解:HCO ﹣+H O═H O++CO 2﹣
3 3 2 3 3
C.HF的电离:HF+H O═H O++F﹣
2 3
D.(NH ) SO 的电离:(NH ) SO ═2NH ++SO 2﹣
4 2 4 4 2 4 4 4
7.根据题设的条件判断离子共存情况。
A:Na+、Cu2+、SO 2﹣、Cl﹣
4
B:H+、Cl﹣、CO 2﹣、Na+
3
C:H+、Cl﹣、Fe3+、NO ﹣
3
D:CH COO﹣、H+、Na+、SO 2﹣
3 4
E:Al3+、Ag+、Cl﹣、NO ﹣
3
F:NH +、Na+、S2﹣、ClO﹣
4
(1)因生成沉淀而不能共存的是 ;
(2)因生成弱电解质而不能共存的是 ;
(3)因生成气体而不能共存的是 。
二、拓展提升
8.写出下列反应的化学方程式:
(1)Na O 与CO 反应 ;
2 2 2
(2)将氯气与通入冷的消石灰中反应制漂白粉 ;
(3)将铜粉溶解在浓FeCl 溶液中: ;
3
(4)向FeCl 溶液中滴加氨水: 。
3
9.写出下列过程的离子反应方程式:
(1)向氯化铝溶液中加入少量氨水: 。
(2)用强碱溶液吸收工业废气中的NO :
2
(3)氯化铁溶液的水解反应: 。
10.电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。下列方法中,可以使醋酸稀溶液中 CH COOH 电离程度增大的是
3
(填字母序号)。
a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)白醋是常见的烹调酸味辅料,白醋总酸度测定方法如下。
a.量取20.00 mL白醋样品,用100 mL容量瓶配制成待测液。
b.将滴定管洗净、润洗,装入溶液,赶出尖嘴处气泡,调整液面至0刻度线。c.取20.00 mL配制的待测液于洁净的锥形瓶中,加3滴酚酞溶液,用0.1000 mol•L﹣1的NaOH溶液
滴定至终点,记录数据。
d.重复滴定实验3次并记录数据。
e.计算白醋样品中醋酸总酸度。回答下列问题:
实验a中量取20.00 mL白醋所用的仪器名称是 。
①若实验b中碱式滴定管未用NaOH标准溶液润洗,会造成测定结果比准确值 (填“偏大”、
②“偏小”或“不变”)。
实验C中判断滴定终点的现象是 。
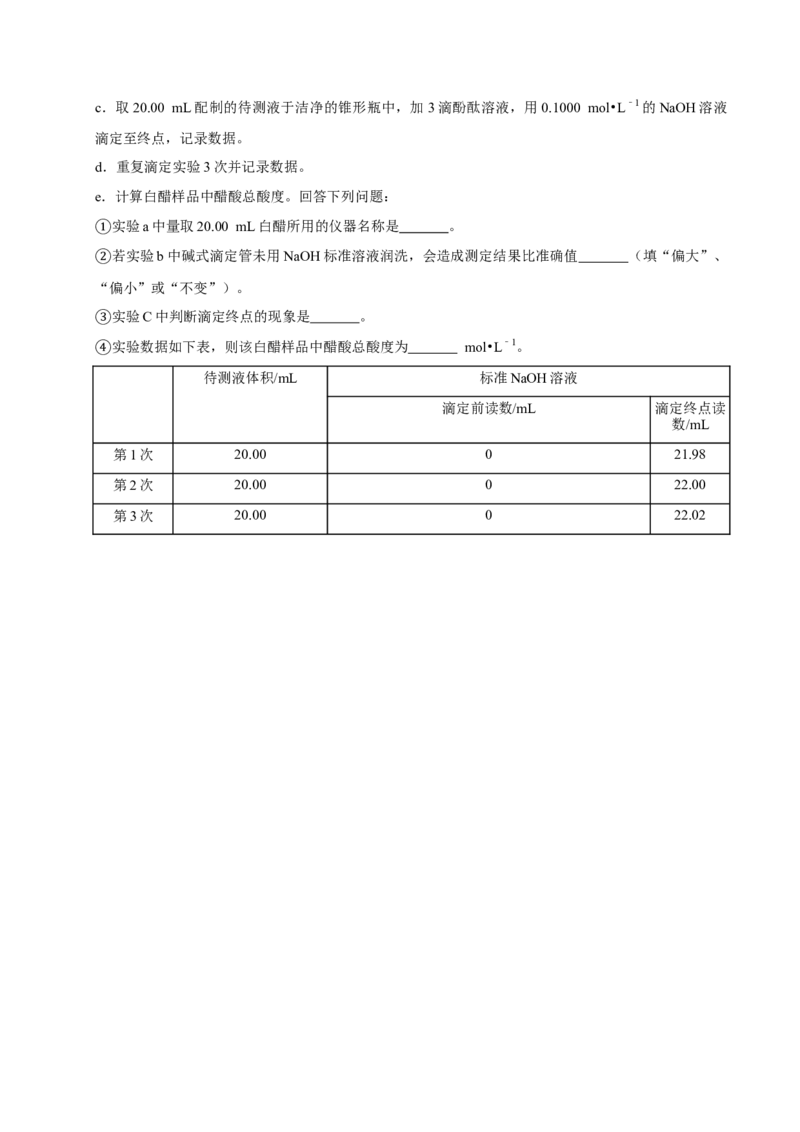
③实验数据如下表,则该白醋样品中醋酸总酸度为 mol•L﹣1。
④ 待测液体积/mL 标准NaOH溶液
滴定前读数/mL 滴定终点读
数/mL
第1次 20.00 0 21.98
第2次 20.00 0 22.00
第3次 20.00 0 22.02