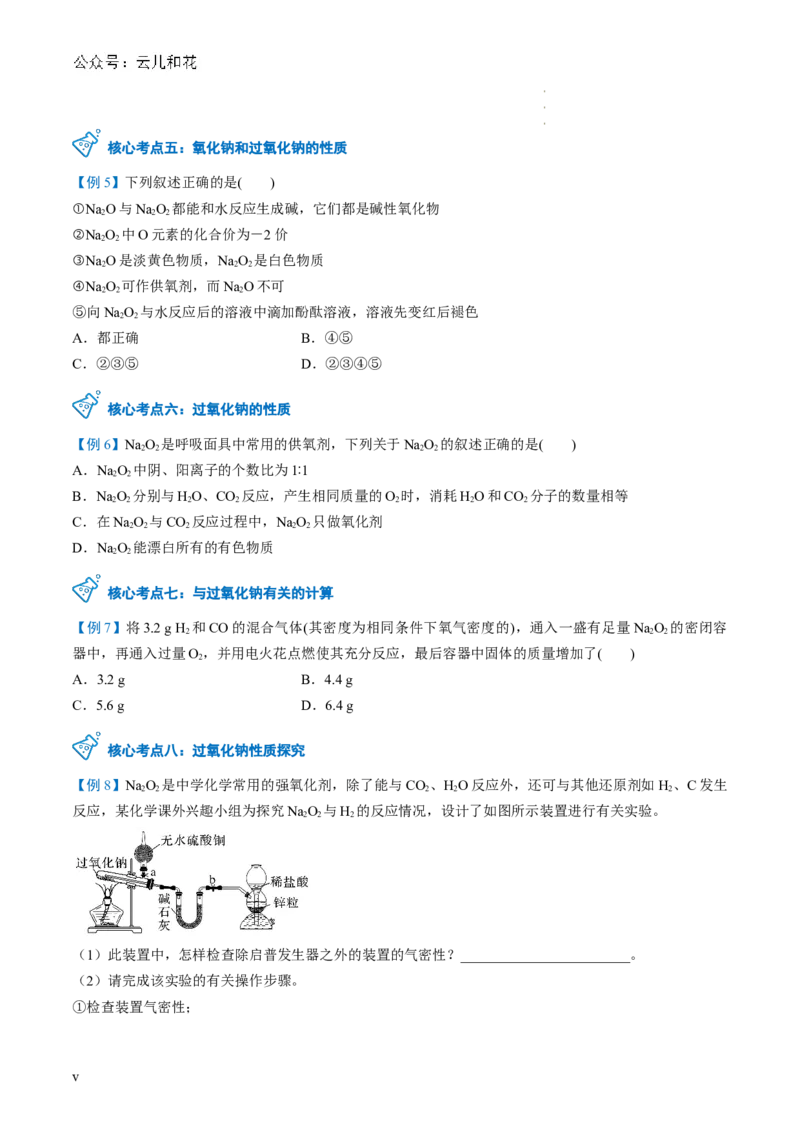
文档内容
第 06 讲 钠及钠的氧化物
模块一 思维导图串知识 1.能从钠原子的结构分析认识钠具有很强的还原性。
模块二 基础知识全梳理(吃透教材) 2.设计实验探究钠与氧气、水的反应,学会分析钠与
模块三 教材习题学解题 酸、碱、盐溶液的反应。
模块四 核心考点精准练(8大考点) 3.认识氧化钠与过氧化钠的性质,熟知过氧化钠与水
模块五 小试牛刀过关测 和二氧化碳反应的应用。
(基础练10题) 4.会设计实验探究过氧化钠与水的反应,掌握NaO 的
2 2
(提升练6题) 相关计算。
一、钠的性质
1.钠元素的原子结构及存在
v
学科网(北京)股份有限公司2.钠的物理性质
状态 颜色 硬度 密度 熔点
固态 银白色 质软 ρ(煤油)<ρ(钠)<ρ(水) 较低
思考与交流:能否把钠保存在汽油或四氯化碳中?
3.钠的化学性质
(1)钠与氧气的反应
条件 常温 加热
实验
步骤
实验 新切开的钠具有 色的金属光泽,在空 钠受热后先 ,然后剧烈燃烧,火焰呈
现象 气中很快 ,生成 固体
①钠具有 色的金属光泽,硬度 ,熔点 ,密度比煤油的大,通常保存在
或 中
②钠与氧气的反应(写出反应的化学方程式)
结论
常温下: (生成物为 固体)
加热时: (生成物为 固体)
反应条件不同,钠与氧气反应的生成物不同
【特别提醒】
①取金属钠时应用镊子,不能用手直接接触,一般取绿豆大小即可,不能太大,以免实验时发生危险。
②剩余的钠要放回原试剂瓶。
(2)钠与氯气的反应
钠与其他非金属单质化合生成的化合物中钠只显+1价,如Na与Cl 在点燃条件下可发生反应,化学方程
2
式:2Na+Cl=====2NaCl。
2
【归纳总结】钠露置在空气中的变化
(1)金属钠长期露置于空气中最终完全转变为NaCO 粉末,此过程中的主要变化与现象有:
2 3
――→――→――→――→――→
(2)发生的主要变化的化学方程式
v
学科网(北京)股份有限公司①4Na+O=2NaO;②NaO+HO=2NaOH;④2NaOH+CO=NaCO+HO,NaCO+10HO=
2 2 2 2 2 2 3 2 2 3 2
NaCO·10H O;⑤NaCO·10H O=NaCO+10HO。
2 3 2 2 3 2 2 3 2
二、钠与水的反应
1.实验探究
预测:从物质组成及氧化还原反应的角度,预测钠与水反应的生成物: NaOH 、 H 。
2
实验操作 实验现象 结论或解释
①钠 在水面上 ①钠的密度比水
②钠 成闪亮的小球 ②钠的熔点 ,反应放热
③小球在水面上 ③反应产生的 推动小球运动
④与水反应发出“嘶嘶”的响声,逐渐变小,最后消
④钠与水 反应,产生气体
失
⑤反应后溶液的颜色逐渐变 ⑤有 物质( )生成
2.实验结论
钠与水剧烈反应,生成 。
(1)化学方程式是 ;
离子方程式是 。
其中氧化剂为 ,还原剂为 。
(2)实质:钠与水电离出的H+发生 反应生成H。
2
(3)简单识记
遇水记五点,浮熔游响红,遇酸酸优先,遇盐(碱)水在前。
3.应用
火灾现场存放有大量活泼金属(如Na)时,不能用水而需要用干燥的沙土来灭火。
三、钠与酸、盐的反应
1.钠与酸的反应
如果钠过量,钠把酸耗尽后,再与水反应。
(1)钠先与酸中的H+反应(不是与水先反应),离子方程式:2Na+2H+=2Na++H↑。
2
(2)如果钠过量,钠把酸消耗尽之后,再与水反应。
2.钠与盐溶液的反应
(1)钠与盐溶液反应时,首先与水反应生成NaOH(不是与盐先发生置换反应)。
(2)然后NaOH与盐发生复分解反应(若氢氧化钠不与盐反应,则只有钠与水的反应)。
例如:Na与Fe (SO ) 溶液的反应:2Na+2HO=2NaOH+H↑,6NaOH+Fe (SO )=2Fe(OH) ↓+
2 4 3 2 2 2 4 3 3
3NaSO ;Na与KNO 溶液的反应:2Na+2HO=2NaOH+H↑(仅此一步反应),若是饱和盐溶液,会有晶
2 4 3 2 2
体析出。
3.钠与熔融盐的反应
v
学科网(北京)股份有限公司4Na+TiCl ====Ti+4NaCl Na+KCl====K↑+NaCl
4
四、氧化钠和过氧化钠的性质
1.氧化钠的性质
氧化钠(Na O)是一种白色固体。属于 氧化物,能与水、酸、酸性氧化物等发生化学反应。
2
(1)氧化钠与水反应: 。
(2)氧化钠与盐酸反应: 。
(3)氧化钠与二氧化碳反应: 。
2.过氧化钠的性质
过氧化钠(Na O)是一种 色固体。NaO 中氧元素为-1价,既有 性也有 性。
2 2 2 2
(1)实验探究过氧化钠与水的反应
实验操作
实验现象 ①试管外壁发烫,带火星的木条 ;②用pH试纸检验,试纸
实验结论 NaO 与水反应 ,化学方程式为
2 2
(2)过氧化钠与二氧化碳反应的化学方程式: 。
思考与交流:NaO 使酚酞先变红后褪色的原因是什么?
2 2
3.过氧化钠的应用
(1)NaO 可在呼吸面具或潜水艇中作为 的来源。
2 2
(2)NaO 中氧元素的化合价为 价,具有 ,可作漂白剂。
2 2
【归纳总结】氧化钠与过氧化钠的比较
物质 氧化钠(Na O) 过氧化钠(Na O)
2 2 2
色、态
氧元素化合价
阴、阳离子个数比
是否为碱性氧化物
相同点 都能与水反应生成氢氧化钠,都能与CO 反应生成NaCO
2 2 3
化学
过氧化钠与水、二氧化碳反应有氧气产生,具有强氧化性,而NaO不具有强氧化
2
性质 不同点
性
五、过氧化钠与水、二氧化碳反应的定量关系
1.Na O 与HO、CO 反应的氧化还原关系
2 2 2 2
v
学科网(北京)股份有限公司2NaO+2HO===4NaOH+O↑
2 2 2 2
2NaO+2CO===2Na CO+O
2 2 2 2 3 2
(1)NaO 中氧的化合价为-1,在两个反应中NaO 的作用是既做氧化剂又做还原剂,从电子转移角度分
2 2 2 2
析,每生成一分子氧气转移2个电子。每消耗一个NaO 转移1个电子。
2 2
(2)从化学方程式的计量数分析可知,无论是CO、HO还是二者的混合物,与足量的NaO 反应时,参
2 2 2 2
与反应的CO 或HO与放出O 的分子个数之比均为2∶1。
2 2 2
2.Na O 与CO 、HO反应的质量关系
2 2 2 2
(1)2NaO+2CO===2Na CO+O Δm(2CO)
2 2 2 2 3 2
2×78 2×44 2×106 2×28
固体增加2个碳原子和2个氧原子,固体增加的质量相当于与CO 等分子数的CO的质量。
2
(2)2NaO+2HO===4NaOH+O↑ Δm(4H)
2 2 2 2
2×78 2×18 4×40 2×2
固体增加4个氢原子,固体增加的质量相当于与HO等分子数的H 的质量。
2 2
教材习题01 解题思路
将金属钠放入盛有下列溶液的小烧杯中,既有气
体产生,又有沉淀产生的是________(填序号)。
①MgSO 溶液
4
②NaHCO 溶液
3
③Na SO 溶液
2 4
④饱和澄清石灰水
⑤FeCl 溶液
3
教材习题02 解题思路
在鲜活水产品的长途运输中,必须考虑以下几
点:①水中需要保持适量的O;②及时去除鱼类
2
等排出的CO;③防止细菌的大量繁殖。现有两
2
种在水中能起供氧灭菌作用的物质:NaO 和
2 2
CaO,已知CaO 能缓慢与水反应。运输鲜活水产
2 2
品时应选择________放入水中,理由是
______________。
v
学科网(北京)股份有限公司核心考点一:钠的存在、物理性质及保存方法
【例1】下列有关钠的存在形式、保存及取用方法的描述正确的是( )
A.钠在自然界中主要以化合态的形式存在,少量以游离态的形式存在
B.钠需要密封保存在煤油或石蜡油中
C.实验室中可直接用药匙取用钠
D.实验室中取用后剩余的钠不能放回原试剂瓶中
核心考点二:钠与氧气的反应
【例2】等质量的两块钠,第一块在足量氧气中加热,第二块与足量氧气在常温下充分反应,则下列说法
正确的是( )
A.第一块钠失去的电子数多
B.两块钠失去的电子数一样多
C.第二块钠的生成物质量较大
D.两块钠的生成物质量一样大
核心考点三:钠与水的反应
【例3】某学生将一小块钠投入滴有酚酞溶液的水中,此实验能证明钠的性质包括下面4点中的( )
①钠的密度比水的小
②钠的熔点较低
③钠与水反应时放出热量
④钠与水反应后溶液呈碱性
A.①④ B.①②④
C.①③④ D.①②③④
核心考点四:钠与酸、碱、盐溶液的反应
【例4】把一小块金属钠放入不同溶液中,下列说法正确的是( )
A.饱和NaOH溶液:有氢气放出,恢复至室温后溶液浓度变大
B.稀CuSO 溶液:有氢气放出,有紫红色铜析出
4
C.MgCl 溶液:有氢气放出,有白色沉淀生成
2
D.滴有石蕊溶液的水:有氢气放出,溶液变为红色
v
学科网(北京)股份有限公司核心考点五:氧化钠和过氧化钠的性质
【例5】下列叙述正确的是( )
①Na O与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②Na O 中O元素的化合价为-2价
2 2
③Na O是淡黄色物质,NaO 是白色物质
2 2 2
④Na O 可作供氧剂,而NaO不可
2 2 2
⑤向NaO 与水反应后的溶液中滴加酚酞溶液,溶液先变红后褪色
2 2
A.都正确 B.④⑤
C.②③⑤ D.②③④⑤
核心考点六:过氧化钠的性质
【例6】NaO 是呼吸面具中常用的供氧剂,下列关于NaO 的叙述正确的是( )
2 2 2 2
A.NaO 中阴、阳离子的个数比为1∶1
2 2
B.NaO 分别与HO、CO 反应,产生相同质量的O 时,消耗HO和CO 分子的数量相等
2 2 2 2 2 2 2
C.在NaO 与CO 反应过程中,NaO 只做氧化剂
2 2 2 2 2
D.NaO 能漂白所有的有色物质
2 2
核心考点七:与过氧化钠有关的计算
【例7】将3.2 g H 和CO的混合气体(其密度为相同条件下氧气密度的),通入一盛有足量NaO 的密闭容
2 2 2
器中,再通入过量O,并用电火花点燃使其充分反应,最后容器中固体的质量增加了( )
2
A.3.2 g B.4.4 g
C.5.6 g D.6.4 g
核心考点八:过氧化钠性质探究
【例8】NaO 是中学化学常用的强氧化剂,除了能与CO 、HO反应外,还可与其他还原剂如H 、C发生
2 2 2 2 2
反应,某化学课外兴趣小组为探究NaO 与H 的反应情况,设计了如图所示装置进行有关实验。
2 2 2
(1)此装置中,怎样检查除启普发生器之外的装置的气密性?________________________。
(2)请完成该实验的有关操作步骤。
①检查装置气密性;
v
学科网(北京)股份有限公司②打开a、b,产生氢气,观察试管内物质的颜色变化;
③___________________________________________________________________________;
④加热过氧化钠,观察试管内物质的颜色变化;
⑤反应完全后,_______________________________________________________________;
⑥拆卸装置。
(3)该装置中,碱石灰的作用是__________________________________________________。
(4)实验过程中观察到(2)中步骤②无明显变化,步骤④NaO 熔化,黄色粉末立即变成白色,干燥管
2 2
内无水硫酸铜未变成蓝色。则NaO 与H 反应的化学方程式为___________________________________。
2 2 2
【基础练】
1.下列关于钠的叙述中,不正确的是
A.钠燃烧时发出黄色的火焰 B.钠具有很强的还原性
C.钠燃烧时生成氧化钠 D.钠原子的最外电子层上只有1个电子
2.下列关于氧化钠和过氧化钠的叙述正确的是
A.都是白色固体 B.都可在呼吸面具中作为氧气的来源
C.与水反应都能生成氢氧化钠 D.都属于碱性氧化物
3.钠在工业上有重要用途。下列有关钠的叙述不正确的是
A.有银白色金属光泽 B.在空气中很快生成
C.燃烧发出明亮的黄色火焰 D.将Na投入 溶液中可置换出Fe
4.下列关于钠与水反应的说法中,不正确的是
A.从元素化合价及氧化还原反应规律分析,反应中产生的无色气体只能是氢气
B.钠块熔化成小球,说明钠的熔点低且该反应放热
C.将酚酞溶液滴入反应后的溶液中,溶液变红,说明产物有碱性物质生成
D.钠与水反应的离子方程式:Na+HO=Na++OH-+H ↑
2 2
5.下列说法正确的是
A.利用焰色试验可区分NaCl与NaCO 固体
2 3
B.实验时,若取用的金属钠过多,应将其当废弃物处理
C.金属钠如果着火可以用湿抹布扑灭
D.既有单质参与又有单质生成的反应未必是氧化还原反应
6.在烧杯中加入一些水,滴入几滴酚酞溶液,搅拌均匀。然后把一块绿豆大小的钠放入水中,我们观察
到烧杯溶液变红,红色物质逐渐增多,最后溶液全部变红。下列解释正确的是
v
学科网(北京)股份有限公司A.钠离子扩散导致溶液变红 B.氢氧根离子扩散导致溶液变红
C.酚酞扩散导致溶液变红 D.钠与水反应生成的氢气导致溶液变红
7.下列离子方程式书写不正确的是
A.石灰石与稀盐酸反应:
B.过氧化钠与稀硫酸反应:
C.澄清石灰水与过量碳酸氢钠溶液反应:
D.钠与 溶液反应:
8.下列叙述正确的是
①Na O与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②Na O与CO 发生化合反应生成NaCO,NaO 与CO 发生置换反应生成O
2 2 2 3 2 2 2 2
③Na O是淡黄色物质,NaO 是白色物质
2 2 2
④Na O 可作供氧剂,而NaO不可
2 2 2
A.都正确 B.①③④ C.②③⑤ D.④
9.焰火“脚印”“笑脸”“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中焰色试验知
识相关。下列说法中正确的是
A.焰色试验是化学变化 B.用稀盐酸清洗做焰色试验的铂丝
C.焰色试验均应透过蓝色钴玻璃观察 D.利用焰色试验可区分NaCl与NaCO 固体
2 3
10.某实验小组通过下图所示实验,探究 与水的反应:
下列说法错误的是
A.②中大量气泡的主要成分是氧气
B.③中溶液变红,说明有碱性物质生成
C.④中现象可能是含有漂白性物质 造成的
D.⑤中 的作用是作催化剂
【提升练】
11.将一小块钠投入下列溶液时,既能产生气体又会出现白色沉淀的是
A.稀盐酸 B.Cu(NO ) 溶液 C.NaCl溶液 D.MgSO 溶液
3 2 4
12.某同学探究金属Na与CO 的反应,实验如下:
2
v
学科网(北京)股份有限公司编
实验Ⅰ 实验Ⅱ
号
操 将点燃的金属钠伸到盛有CO 将实验Ⅰ的集气瓶用水冲洗,过滤。取黑色滤渣灼烧;取滤液分
2
作 的集气瓶中 别滴加酚酞和氯化钡溶液
①火焰呈黄色
现 ①黑色滤渣可燃
②底部有黑色固体,瓶壁上附
象 ②滤液能使酚酞溶液变红,滴加氯化钡溶液有白色沉淀生成
有白色固体
下列说法不正确的是
A.生成的黑色固体中含有C
B.白色固体是NaO
2
C.实验Ⅱ中滤液呈碱性
D.金属Na着火不能用CO 灭火
2
13.观察是研究物质性质的一种基本方法。某同学将金属钠露置于空气中,观察到下列现象:银白色
变灰暗 变白色 出现液滴 变为白色晶体 变为白色粉末,根据钠及其化合物
的性质分析,下列说法正确的是
A.①发生了氧化还原反应 B.①是因为生成了过氧化钠
C.③是因为碳酸钠吸收空气中的水蒸气形成了溶液 D.④⑤只发生物理变化
14.为了探究钠的性质,某化学兴趣小组设计了如图所示装置进行实验,下列说法错误的是
A.密度:CuSO 溶液>Na>煤油
4
B.溶液中有红色固体生成
C.实验过程中,关闭弹簧夹,一段时间后,长颈漏斗中的液面上升
D.可观察到有气泡生成,钠在煤油和CuSO 溶液中上下跳动
4
15.下列有关NaO和NaO 的叙述中,正确的是
2 2 2
A.NaO比NaO 稳定
2 2 2
B.只用水来确定某NaO粉末中是否含有NaO
2 2 2
C.NaO、NaO 分别与CO 反应,产物相同
2 2 2 2
D.将足量的NaO 比NaO分别加到酚酞溶液中,最终溶液均为红色
2 2 2
16.过氧化钠有着独特的结构和性质,因而具有广泛的用途,如作为漂白剂,印染剂,空气中二氧化碳吸收
v
学科网(北京)股份有限公司剂,潜艇中供氧剂等。
(1)在下列溶液中分别加入一定量的过氧化钠固体,不会出现浑浊现象的是_______。
A.饱和 溶液 B. 稀溶液C. 稀溶液 D.饱和
(2)关于 和 的异同,下列说法错误的是_______。
A.常温常压下状态相同,颜色不同
B.包含的正负离子相同,但个数比不同
C.均可由Na和氧气反应得到,但反应条件不同
D.均可与水反应,但产物不同
(3)下列各组物质相互混合进行反应,最终既有气体又有沉淀生成的是______。
A.金属钠投入 溶液中 B. 投入 溶液中
C. 投入 溶液中 D. 投入到 溶液中
v
学科网(北京)股份有限公司