文档内容
1
滨城高中联盟 2024-2025 学年度上学期高一期中考试
化学试卷
考试时间:75分钟 试卷满分:100分
可能用到的相对原子质量:H-1、C-12、N-14、O-16、Na-23、Cl-35.5
一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项符合题目要求。)
1.化学与生产、生活密切相关,下列说法不正确的是
A. 、 可以用于自来水消毒 B. 在合成葡萄糖中发生了氧化反应
C.铁粉可用作食品保存的抗氧化剂 D.复方氢氧化铝可以用于做抗酸药
2.由一种阳离子与两种酸根阴离子组成的盐称为混盐, 是一种常见的混盐。下列说法不正确的是
A. 属于纯净物 B. 有较强的氧化性
C. 中两个氯原子化合价相同 D. 溶液中加入硫酸,可能有黄绿色气体产生
3.物质性质决定用途,下列两者对应关系不正确的是
A.石灰乳除去废气中二氧化硫,利用了 的碱性
B.氯化铁溶液腐蚀铜电路板,利用了 的氧化性
C.制作豆腐时添加石膏,利用了 的难溶性
D.制作水果罐头时加入维生素C,利用了维生素C的还原性
4.下列说法正确的是
A. 和稀盐酸的混合溶液中加入少量铁屑时,可能没有气泡冒出
B.用铂丝蘸取某溶液进行焰色试验,火焰呈黄色,该溶液为钠盐溶液
C.铁露置在空气中一段时间后就会生锈,铁锈的主要成分为四氧化三铁
D.由“金属钠与水反应生成氢氧化钠和氢气”可推出“铁与水反应生成氢氧化铁和氢气”
5.下列各组离子在指定条件下能够大量共存的是
A.在 的溶液中: 、 、 、
B.在 溶液中: 、 、 、
C.在澄清透明的溶液中; , 、 、
D.在强碱性溶液中: 、 、 、
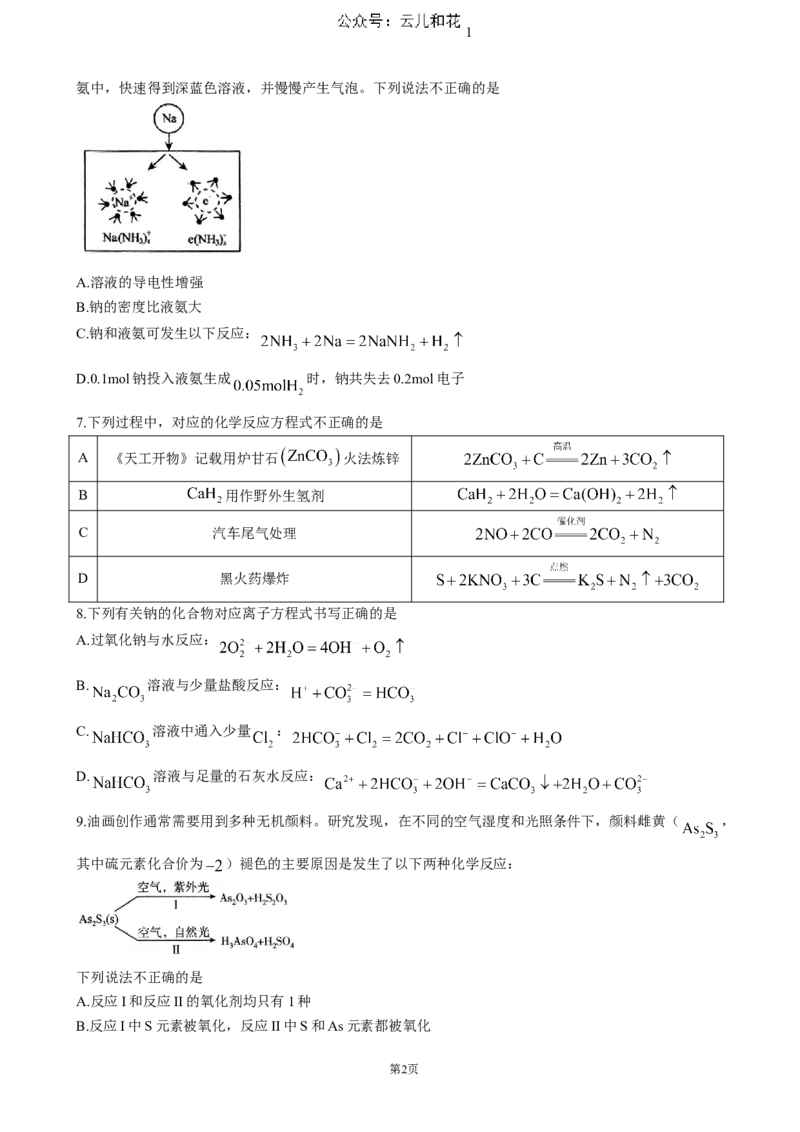
6.钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,下图为钠投入液氨中的溶剂化示意图,钠沉入液
第1页1
氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法不正确的是
A.溶液的导电性增强
B.钠的密度比液氨大
C.钠和液氨可发生以下反应:
D.0.1mol钠投入液氨生成 时,钠共失去0.2mol电子
7.下列过程中,对应的化学反应方程式不正确的是
A 《天工开物》记载用炉甘石 火法炼锌
B 用作野外生氢剂
C 汽车尾气处理
D 黑火药爆炸
8.下列有关钠的化合物对应离子方程式书写正确的是
A.过氧化钠与水反应:
B. 溶液与少量盐酸反应:
C. 溶液中通入少量 :
D. 溶液与足量的石灰水反应:
9.油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄( ,
其中硫元素化合价为 )褪色的主要原因是发生了以下两种化学反应:
下列说法不正确的是
A.反应I和反应II的氧化剂均只有1种
B.反应I中S元素被氧化,反应II中S和As元素都被氧化
第2页1
C.反应I和II中,参加反应的
D.反应I和II中,氧化 转移的电子数之比为6:7
10.超氧化钾 可用作潜水或宇航装置中 吸收剂和供氧剂,反应为
, 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的分子数为
B. 固体中含有离子的数目为
C. 溶液中含有氧原子的数目为
D.该反应中每转移1mol电子生成 的数目为
11.三种气体X、Y、Z的相对分子质量关系为 ,下列说法正确的是
A.相同质量的三种气体,物质的量最大的是Y
B.同温同压强下,气体密度最大的是X
C.一定条件下,若三种气体体积均为2.24L,则它们的物质的量一定均为0.1mol
D.同温下,体积相同的两容器分别充入2gY气体和1gZ气体,则其压强比为4:1
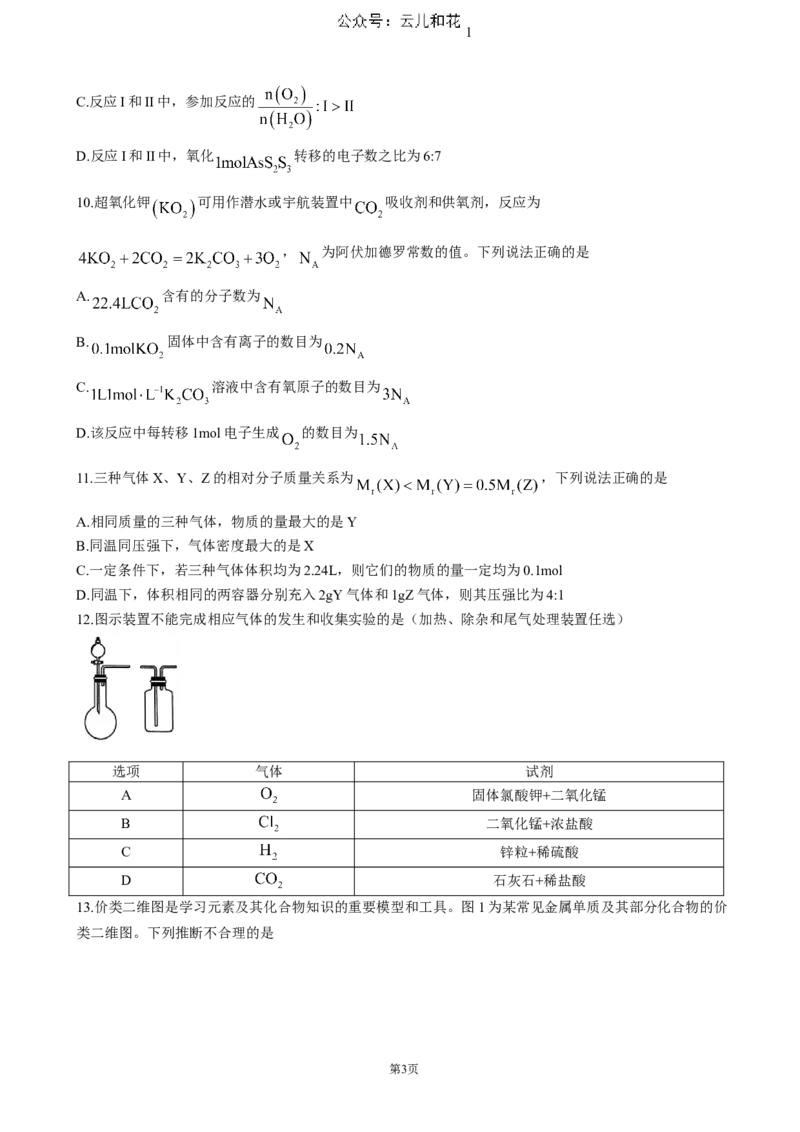
12.图示装置不能完成相应气体的发生和收集实验的是(加热、除杂和尾气处理装置任选)
选项 气体 试剂
A 固体氯酸钾+二氧化锰
B 二氧化锰+浓盐酸
C 锌粒+稀硫酸
D 石灰石+稀盐酸
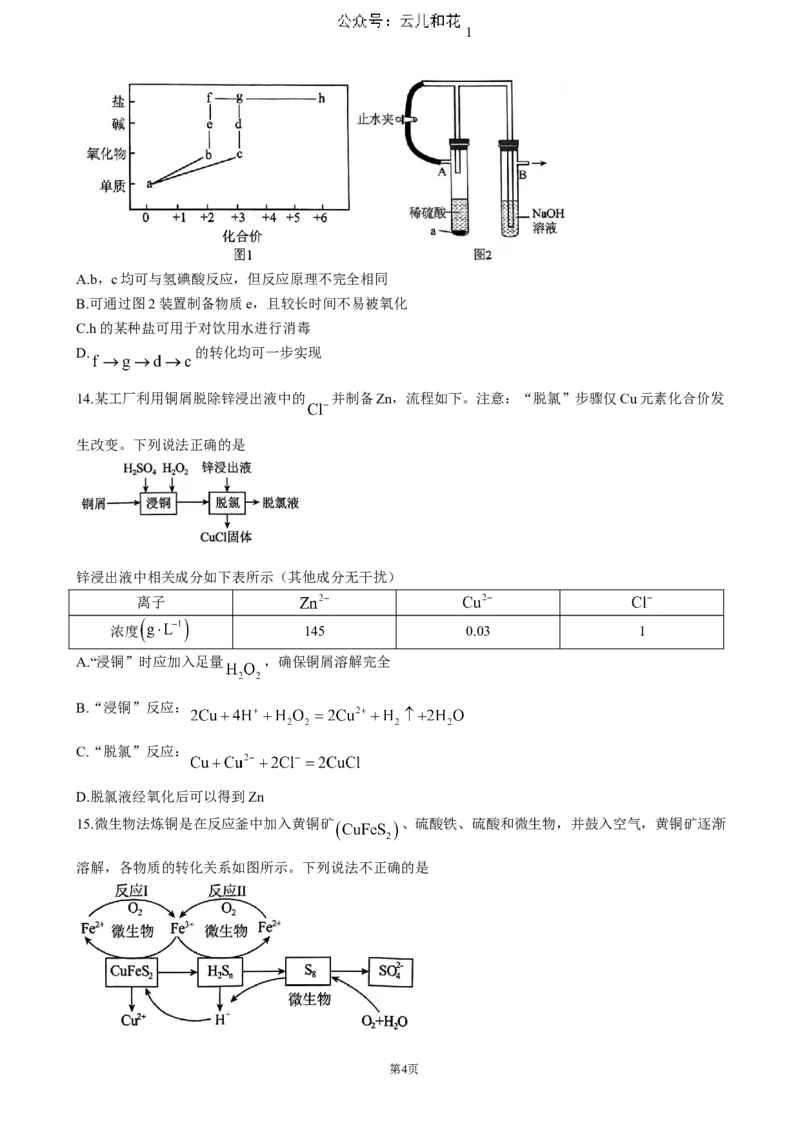
13.价类二维图是学习元素及其化合物知识的重要模型和工具。图1为某常见金属单质及其部分化合物的价
类二维图。下列推断不合理的是
第3页1
A.b,c均可与氢碘酸反应,但反应原理不完全相同
B.可通过图2装置制备物质e,且较长时间不易被氧化
C.h的某种盐可用于对饮用水进行消毒
D. 的转化均可一步实现
14.某工厂利用铜屑脱除锌浸出液中的 并制备Zn,流程如下。注意:“脱氯”步骤仅Cu元素化合价发
生改变。下列说法正确的是
锌浸出液中相关成分如下表所示(其他成分无干扰)
离子
浓度 145 0.03 1
A.“浸铜”时应加入足量 ,确保铜屑溶解完全
B.“浸铜”反应:
C.“脱氯”反应:
D.脱氯液经氧化后可以得到Zn
15.微生物法炼铜是在反应釜中加入黄铜矿 、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐
溶解,各物质的转化关系如图所示。下列说法不正确的是
第4页1
A.反应釜中保持高温不利于反应进行
B.反应I、II的离子方程式为
C.整个转化过程中,可以循环利用的物质有 和
D. 转化为 的过程中,每生成 ,消耗
二、非选择题(本小题共4小题,共55分。)
16.(15分)
I.分类法是研究物质性质的基本方法。将 、 、 、 、 按照一
定标准进行分类(如下图),相连的物质可以归为一类,相交部分以A、B、C、D为分类代码。
(1)相连的两种物质都是弱电解质的是________(填分类代码);请写出相连的两种物质的水溶液可以
反应且产生气体的离子方程式:________________________________________。
(2)已知: 溶液与NaOH溶液反应时最多生成两种盐,则 与足量的NaOH溶液反应的化学
方程式为________________________________________。
II.物质的量可以将宏观物质与微观粒子之间建立起联系。请运用相关知识回答以下问题:
(3)将一定量 和 混合,测得混合气体中碳元素与氮元素的质量之比为3:7,则该混合气体的密
度是同温同压下氢气密度的________倍。
(4)已知标准状况下 的密度为 ,则X原子最外层有________个电子。
(5) 与足量浓盐酸共热,收集到标准状况下氯气22.4L,则理论上起还原性作用的HCl的物质的量
为________mol。
(6)取 溶于水配成溶液,然后逐滴滴入质量分数为 ,密度为 的
盐酸直至没有气体放出,用去盐酸5.0mL。则生成标况下 气体的体积为________L;x的值为
________。
17.(12分)不同条件下, 与KI按照反应①②的化学计量比恰好反应,结果如下。
KI
反应序号 起始酸碱性 还原产物 氧化产物
物质的量 物质的量
① 酸性 0.001 n
② 中性 0.001 10n
第5页1
已知: 的氧化性随酸性减弱而减弱。请结合以上信息回答下列问题:
(1)反应①中, ________________, ________________。
(2)对比反应①和②, ________________。
(3)①的离子反应方程式为________________________________________________________________,
随反应进行,溶液的酸性________(填增强或减弱或不变)。
(4)②的离子反应方程式为________________________________________________________________,
随反应进行,溶液的碱性________(填增强或减弱或不变)。
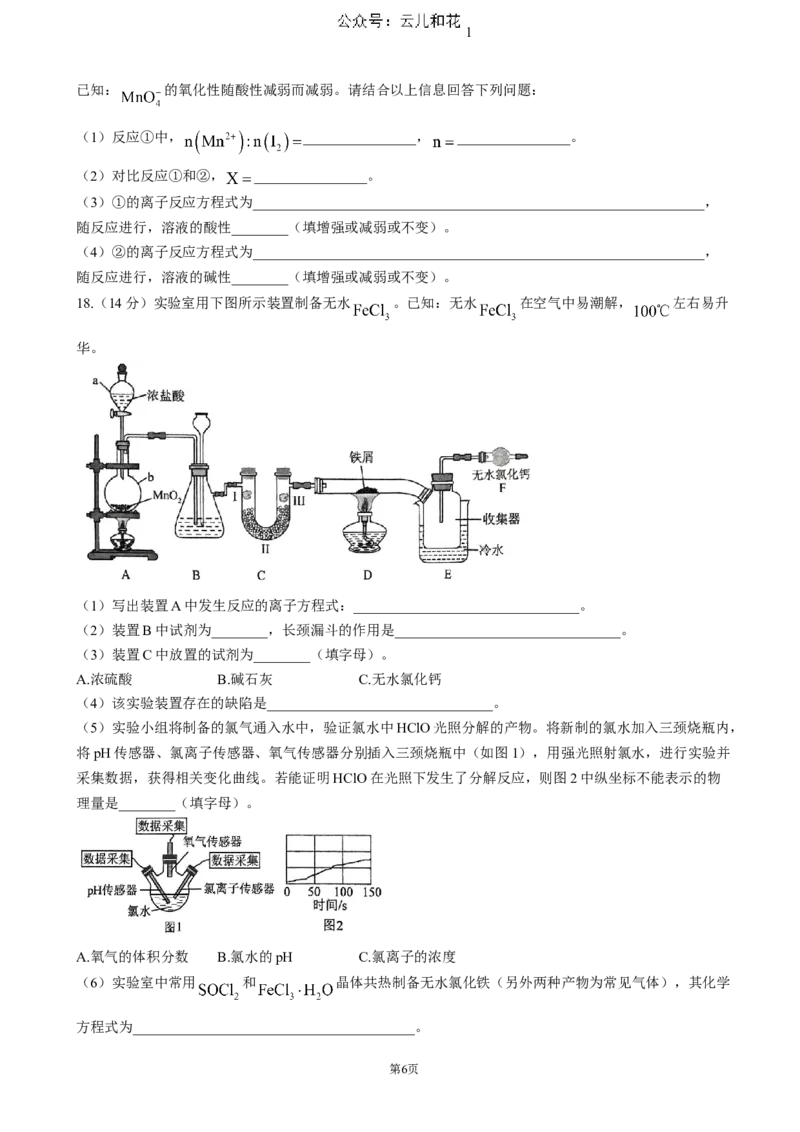
18.(14分)实验室用下图所示装置制备无水 。已知:无水 在空气中易潮解, 左右易升
华。
(1)写出装置A中发生反应的离子方程式:________________________________。
(2)装置B中试剂为________,长颈漏斗的作用是________________________________。
(3)装置C中放置的试剂为________(填字母)。
A.浓硫酸 B.碱石灰 C.无水氯化钙
(4)该实验装置存在的缺陷是________________________________。
(5)实验小组将制备的氯气通入水中,验证氯水中HClO光照分解的产物。将新制的氯水加入三颈烧瓶内,
将pH传感器、氯离子传感器、氧气传感器分别插入三颈烧瓶中(如图1),用强光照射氯水,进行实验并
采集数据,获得相关变化曲线。若能证明HClO在光照下发生了分解反应,则图2中纵坐标不能表示的物
理量是________(填字母)。
A.氧气的体积分数 B.氯水的pH C.氯离子的浓度
(6)实验室中常用 和 晶体共热制备无水氯化铁(另外两种产物为常见气体),其化学
方程式为________________________________________。
第6页1
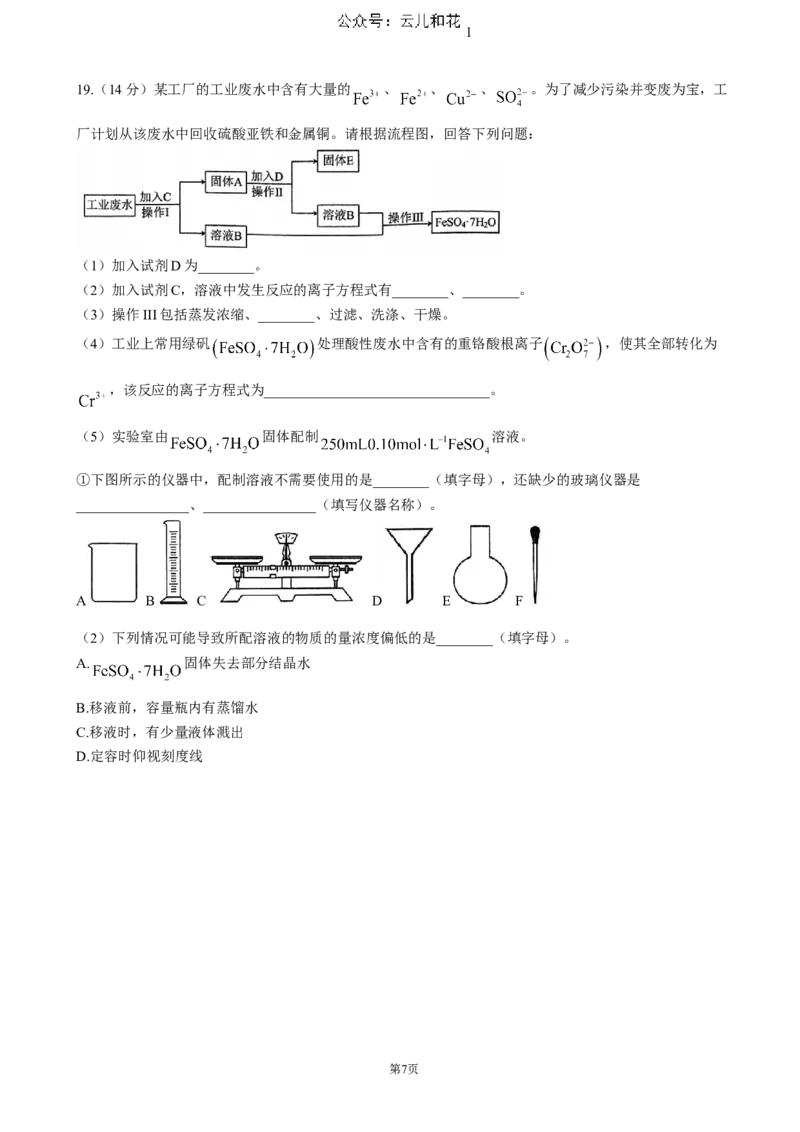
19.(14分)某工厂的工业废水中含有大量的 、 、 、 。为了减少污染并变废为宝,工
厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
(1)加入试剂D为________。
(2)加入试剂C,溶液中发生反应的离子方程式有________、________。
(3)操作III包括蒸发浓缩、________、过滤、洗涤、干燥。
(4)工业上常用绿矾 处理酸性废水中含有的重铬酸根离子 ,使其全部转化为
,该反应的离子方程式为________________________________。
(5)实验室由 固体配制 溶液。
①下图所示的仪器中,配制溶液不需要使用的是________(填字母),还缺少的玻璃仪器是
________________、________________(填写仪器名称)。
A B C D E F
(2)下列情况可能导致所配溶液的物质的量浓度偏低的是________(填字母)。
A. 固体失去部分结晶水
B.移液前,容量瓶内有蒸馏水
C.移液时,有少量液体溅出
D.定容时仰视刻度线
第7页1
滨城高中联盟 2024-2025 学年度上学期高一期中考试
化学答案
一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项符合题目要求。)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
B C C A C D A B D B D A B C D
二、非选择题(本小题共4小题,共55分。)
16.(共15分,最后一空1分,其余每空2分)
(1)AB(少选1分,错选、多选0分); 。
(2) 。
(3) 13 倍。
(4)X原子最外层有5 个电子。
(5)2mol。
(6)CO 气体的体积为0.672L;x的值为10。
2
17.(共12分,除特殊标注外,其余每空2分)
(1) 2:5, 0.0002。
(2) 3 。
(3) , 减弱( 1 分) 。
(4) , 增强( 1 分) 。
18.(共14分,每空2分)
(1) 。
(2)饱和氯化钠溶液,监测实验时装置是否发生堵塞(或防止堵塞)。
(3)装置C中放置的试剂为C。
(4)无尾气处理装置。
(5)纵坐标不能表示的物理量是 B (填字母)。
(6) 。
19.(共14分,除特殊标注外,其余每空2分)
(1)加入试剂D为 稀硫酸或 H SO 。
2 4
第8页1
(2) (1分)、 (1分)。
(3)蒸发浓缩、冷却结晶(或降温结晶)、过滤、洗涤、干燥。
(4) 。
(5)①DE(少选1分,错选、多选0分), 250mL 容量瓶 、玻璃棒(填写仪器名称,各1分)。
②CD(少选1分,错选、多选0分)。
第9页