文档内容
第一学期期中考试试卷
高一化学
可能用到的相对原子质量:H1 C12 N14 O16 Mg24 Cl35.5 S32 Cu64
一、选择题(每小题只有一个选项符合题意)
1. 古籍中记载的下列事实或现象的形成,未涉及氧化还原反应的是
A. 《本草纲目》:“野外之鬼磷,其火色青,其状如炬,俗称鬼火”
B. 《淮南万毕术》:“曾青得铁则化为铜”
C. 《梦溪笔谈》:“石穴中水所滴者皆为钟乳”
D. 《本草经疏》:“丹砂(HgS),味甘微寒而无毒……若经伏火……则毒等砒硇,服之必毙”
2. 下列关于物质分类正确的是
A. 混合物:水煤气、冰醋酸、冰水混合物
B. 电解质:氯化氢、硫酸钡、水
C. 正盐:小苏打、纯碱、氯化钠
D. 碱性氧化物:氧化钙、四氧化三铁、过氧化钠
3. 下列叙述正确的是
A. 盐酸溶液导电性比醋酸溶液导电性强,说明醋酸是弱酸
B. 在熔化状态下能导电的化合物一定属于电解质
C. 氯化钠溶液在通电的条件下发生电离
D. 氨水能导电,所以氨气是电解质
4. 下列有关胶体的说法正确的是
A. 其分散质粒子直径比氯化钠溶液中Na+的直径小
B. 能产生丁达尔效应
C. 其分散质粒子既能透过滤纸,也能透过半透膜
D. 将FeCl 饱和溶液直接煮沸至红褐色可得胶体
3
5. 下列各组离子混合,最终一定有白色沉淀生成的是
A. Cu2+、Na+、 、OH- B. Ca2+、H+、 、
C. 、Mg2+、 、 D. Na+、Ag+、Cl-、H+
6. 下列离子方程式书写正确的是
A. FeCl 溶液腐蚀印刷电路铜板:Cu+Fe3+=Cu2++Fe2+
3B. 醋酸溶解鸡蛋壳:2H++CaCO =Ca2++CO +H O
3 2 2
C. 在NaHSO 溶液中滴入Ba(OH) 溶液至溶液呈中性:Ba2++2OH+2H++ =BaSO +2H O
4 2 4 2
.
D 向NaHCO 溶液中加入NaOH: +OH=CO +H O
3 2 2
7. 下列对X+2Y=X2++2Y-的叙述中正确的是
A. Y被还原,X2+是还原产物 B. Y被还原,X发生氧化反应
C. X是还原剂,Y被氧化 D. X被氧化,X显氧化性
8. 在一定条件下PbO 与Cr3+反应,产物是 和Pb2+,则PbO 与Cr3+反应 的化学计量数之比为( )
2 2
A. 3:1 B. 3:2 C. 1:1 D. 3:4
9. 二氧化氯(ClO )是一种优良的消毒剂,可用氯酸钠和双氧水在酸性条件下制备,反应方程式为
2
NaClOHOHSO ClO NaSO HOO(未配平)。下列说法不正确的是
3 2 2 2 4 2 2 4 2 2
A. NaClO 做氧化剂,发生还原反应
3
B. 将该方程式配平后HO的化学计量数应为2
2
C. NaClO 与HO 的化学计量系数之比为2:1
3 2 2
D. 反应过程中每生成2.24LO 转移0.2mol电子
2
10. 已知Fe(OH) 为红褐色,下列关于钠的反应现象的叙述中,不正确的是
3
A. 切开钠,钠切面颜色变暗,久置空气中最后呈淡黄色
B. 把小块钠投入硫酸铁溶液中,钠浮在水面上、四处游动、产生红褐色沉淀
C. 把小块钠投入氯化铵溶液中,钠浮在水面上、四处游动、产生有刺激性气味的气体
D. 把燃着的钠伸入盛有氯气的集气瓶中,剧烈反应,产生大量白烟
11. 事实上,某些氧化物在一定条件下能与NaO 反应,且反应极有规律,如NaOSO =Na SO ;
2 2 2 2 2 2 4
2NaOSO (g)=Na SO O(g是指物质为气态)。据此判断下列反应方程式错误的是
2 2 3 2 4 2
.
A NaONO=2NaNO B. 2NaO2CO=2Na COO
2 2 2 4 3 2 2 2 2 3 2
.
C 2NaO2NO=4NaNO O D. 2NaO2MnO=4NaMnOO
2 2 2 3 2 2 2 2 2 7 4 2
12. 下列实验方案中,不能测定出NaCO 和NaHCO 的混合物NaCO 的质量分数的是( )
2 3 3 2 3
A. 取ag混合物充分加热,质量减少bg
B. 取ag混合物与足量NaOH溶液充分反应,得到bg溶液
C. 取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体
D. 取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg
13. 下列有关氯水的叙述正确的是
A. 氯气可使干燥的pH试纸先变红,后褪色B. 氯水放置数天后,溶液的酸性逐渐减弱
C. 新制 的氯水一定含有Cl、HO和HClO三种分子
2 2
D. 将氯气通入澄清石灰水中可制得漂白粉
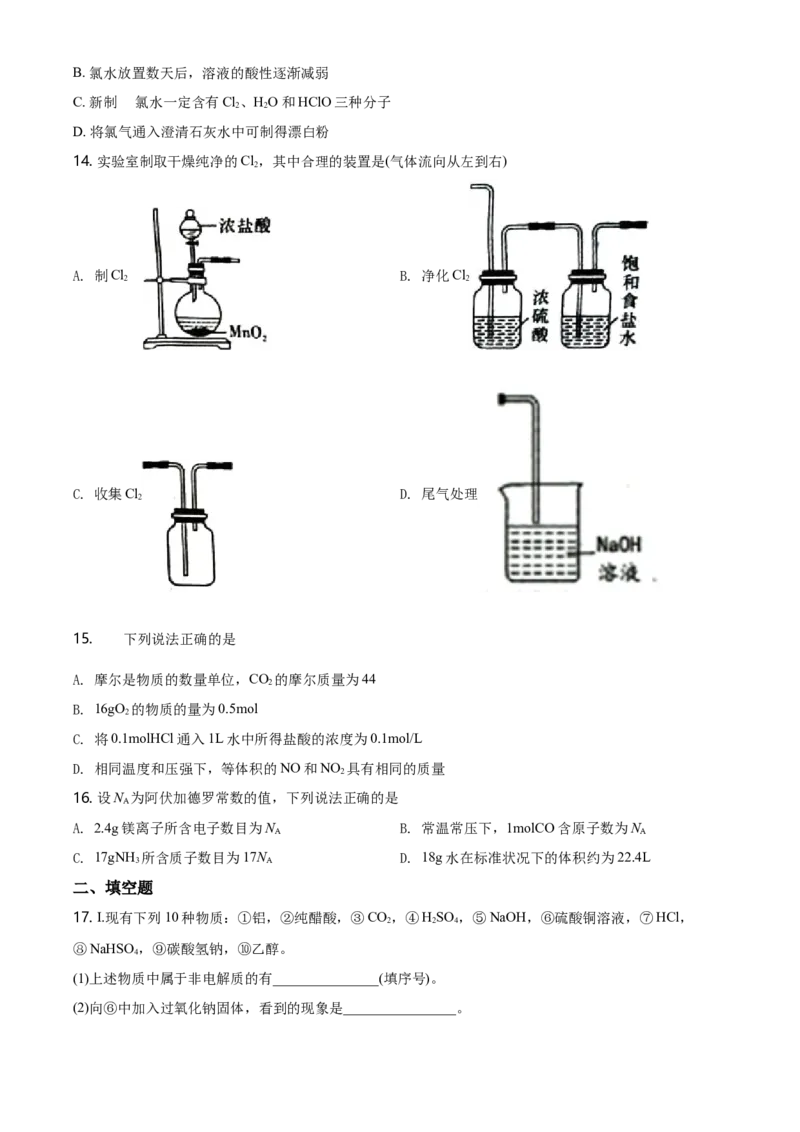
14. 实验室制取干燥纯净的Cl,其中合理的装置是(气体流向从左到右)
2
A. 制Cl B. 净化Cl
2 2
C. 收集Cl D. 尾气处理
2
15. 下列说法正确的是
A. 摩尔是物质的数量单位,CO 的摩尔质量为44
2
B. 16gO 的物质的量为0.5mol
2
C. 将0.1molHCl通入1L水中所得盐酸的浓度为0.1mol/L
D. 相同温度和压强下,等体积的NO和NO 具有相同的质量
2
16. 设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 2.4g镁离子所含电子数目为N B. 常温常压下,1molCO含原子数为N
A A
C. 17gNH 所含质子数目为17N D. 18g水在标准状况下的体积约为22.4L
3 A
二、填空题
17. Ⅰ.现有下列10种物质:①铝,②纯醋酸,③CO,④HSO ,⑤NaOH,⑥硫酸铜溶液,⑦HCl,
2 2 4
⑧NaHSO,⑨碳酸氢钠,⑩乙醇。
4
(1)上述物质中属于非电解质的有_______________(填序号)。
(2)向⑥中加入过氧化钠固体,看到的现象是________________。(3)⑧在水中的电离方程式为______________。
(4)②和⑤的溶液混合,反应的离子方程式为_____________。
(5)⑦的浓溶液与软锰矿反应制取氯气的离子方程式为______________。
Ⅱ.已知离子还原性BrFe2I,则氧化性Fe3+______I(填“>”“=”或“<”),有一混合溶液,其中只含有Fe2+、
2
Br-、I-,其中Br-、I-的个数比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是
_______。如果要使溶液中Br-、I-的个数比为3:1,通入氯气与溶液中剩余Fe2+的物质的量之比为_______。
三、框图推断题
18. A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
(1)若A的焰色反应为黄色,且A为化合物,回答下列问题:
①A的化学式为 ________________,A与HO反应的离子方程式为____________________。
2
②若X为具有强还原性的非金属单质,通常为黑色粉末,写出E的化学式______________。
③若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为______________(填
代号)。
a.NaCl溶液 b.BaCl 溶液 c.NaOH溶液 d.Ca(OH) 溶液
2 2
(2)若A为黄绿色气体,具有很强的氧化性,则:
①若C溶液显强酸性,则B的化学式为________________。
②X可能为_________________(填代号)。
a.NaHCO b.Na CO c.Na SO d.Al(OH)
3 2 3 2 4 3
③请写出A通入NaOH溶液的离子方程式______________。
四、实验题
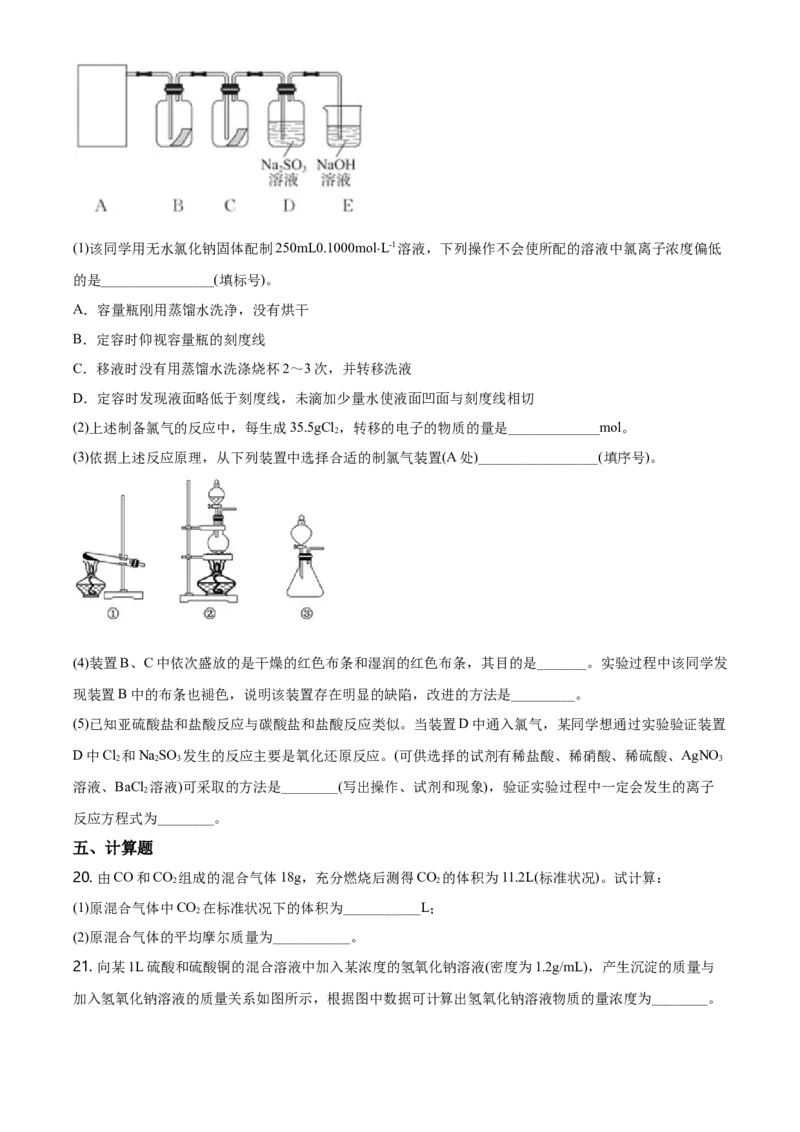
19. “84消毒液”是生活中常用的消毒剂,可与硫酸反应制取氯气,反应原理为NaClONaClHSO
2 4
NaSO ClHO,为探究氯气的性质,某同学利用此原理制氯气并设计了如图所示的实验装置。
2 4 2 2(1)该同学用无水氯化钠固体配制250mL0.1000molL-1溶液,下列操作不会使所配的溶液中氯离子浓度偏低
的是________________(填标号)。
A.容量瓶刚用蒸馏水洗净,没有烘干
B.定容时仰视容量瓶的刻度线
C.移液时没有用蒸馏水洗涤烧杯2~3次,并转移洗液
D.定容时发现液面略低于刻度线,未滴加少量水使液面凹面与刻度线相切
(2)上述制备氯气的反应中,每生成35.5gCl,转移的电子的物质的量是_____________mol。
2
(3)依据上述反应原理,从下列装置中选择合适的制氯气装置(A处)_________________(填序号)。
(4)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是_______。实验过程中该同学发
现装置B中的布条也褪色,说明该装置存在明显的缺陷,改进的方法是_________。
(5)已知亚硫酸盐和盐酸反应与碳酸盐和盐酸反应类似。当装置D中通入氯气,某同学想通过实验验证装置
D中Cl 和NaSO 发生的反应主要是氧化还原反应。(可供选择的试剂有稀盐酸、稀硝酸、稀硫酸、AgNO
2 2 3 3
溶液、BaCl 溶液)可采取的方法是________(写出操作、试剂和现象),验证实验过程中一定会发生的离子
2
反应方程式为________。
五、计算题
20. 由CO和CO 组成的混合气体18g,充分燃烧后测得CO 的体积为11.2L(标准状况)。试计算:
2 2
(1)原混合气体中CO 在标准状况下的体积为___________L;
2
(2)原混合气体的平均摩尔质量为___________。
21. 向某1L硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液(密度为1.2g/mL),产生沉淀的质量与
加入氢氧化钠溶液的质量关系如图所示,根据图中数据可计算出氢氧化钠溶液物质的量浓度为________。