文档内容
2024 年高一第二学期期末学业质量检测卷(2)
化 学
时长:75分钟 总分:100分
一、单选题(每小题3分,共60分)
1.垃圾分类并回收利用,可以节约自然资源,符合可持续发展的要求。与废弃矿泉水瓶对应的垃圾分类
标志是( )
A B C D
2.下列关于胶体和溶液的叙述正确的是( )
A. 溶液呈电中性,部分胶体带电荷,部分胶体不带电荷
B. 胶体与其他分散系的本质区别是能否产生丁达尔效应
C. 氢氧化铁胶体是一种红褐色 的液体
D. 胶体是具有一定稳定性的分散剂
3.钧瓷是中国古代五大名瓷之一,以其独特的釉料及烧制方法而闻名于世。下列钧瓷的制作工艺中,主
要发生了化学变化的是( )
A.掘泥 B.做坯 C.画坯 D.烧炉
的
4.下列金属在冷、浓 硝酸或硫酸中,能形成致密氧化膜的是( )
A.Mg B.Fe C.Cu D.Na
5.下列物质与水混合、振荡后静置,不出现分层现象的是
A.乙醇 B.苯 C.四氯化碳 D.乙酸乙酯
6.下列反应中,属于吸热反应的是
A.Al与稀硫酸的反应 B.Na与乙醇的反应
C.NaOH与硝酸的反应 D.Ba(OH) ·8H O与NH Cl的反应
2 2 4
学科网(北京)股份有限公司7.用光洁的铂丝蘸取无色溶液在无色灯焰上灼烧时观察到黄色火焰,下列叙述正确的是( )
A. 只含有Na+ B. 一定含Na+,也可含K+
C. 既含Na+又含有K+ D. 可能含Na+或K+中一种
8.下列化学用语不正确的是( )
A.羟基的电子式: B.甲烷的空间充填模型:
C.丁烷的球棍模型: D.乙醇的分子式:C HO
2 6
9.下列关于氨气性质的描述中,不正确的是( )
A.无色、有刺激性气味气体
B.极易溶于水
C.相同条件下,密度比空气的大
D.能与水反应生成碱性物质
10.下列反应中,属于取代反应的是
A.乙烯在空气中燃烧 B.甲烷与氯气混合光照发生反应
C.乙醇使酸性高锰酸钾溶液褪色 D.乙烯与溴的四氯化碳溶液反应
11.硫代硫酸钠溶液与稀硫酸反应的化学方程式为: NaSO + H SO = NaSO + SO + S↓+ HO,下
2 2 3 2 4 2 4 2 2
列各组实验中最先出现浑浊的是
NaSO 溶液 稀HSO HO
2 2 3 2 4 2
实验 反应温度/℃
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
A 25 5 0.1 10 0.1 5
B 25 5 0.2 5 0.2 10
C 35 5 0.1 10 0.1 5
D 35 5 0.2 5 0.2 10
12.设N 表示阿伏加德罗常数,下列叙述正确的是
A
A. 15g甲基( )中含有的电子数为9N
A
B. 标准状况下,2.24L辛烷中所含碳原子数为0.8N
A
C. 1.8g 与DO的混合物中含有的质子数和电子数均为N
2 A
D. —定条件下,密闭容器中2mol SO (g)与1mol O(g)充分反应,则容器中分子数为2N
2 2 A
学科网(北京)股份有限公司13.实验室制得的乙酸乙酯中常含有乙酸、乙醇和少量水,其精制过程如下:已知:乙醇能与CaCl 反应
2
生成CaCl •4C HOH,碳酸钠微溶于乙酸乙酯
2 2 5
①向粗制乙酸乙酯中加入饱和碳酸钠溶液,振荡
②静置分层后,取有机层,向其中加入饱和食盐水,振荡
③静置分层后,取有机层,向其中加入饱和氯化钙溶液,振荡
④静置分层后,取有机层,加入无水硫酸镁固体,进行干燥
下列说法不正确的是( )
A.制取乙酸乙酯的反应为:CHCOOH + C H18OH CHCO18OC H+ HO
3 2 5 3 2 5 2
B.步骤②~④有机层处于下层,涉及的实验操作为分液、过滤
C.步骤②目的是将碳酸钠从乙酸乙酯中萃取出来
D.步骤③目的是除去乙醇
14.下列实验结论与实验操作及现象不相符的一组是
选项 实验操作及现象 实验结论
向某酸雨样品中加入Ba(OH) 溶液,有白色沉
A 2 酸雨试样中一定含SO 2-
淀生成 4
B 向KI-淀粉溶液中滴入氯水,溶液变成蓝色 I-的还原性强于Cl-
将Ba(OH) ·8H O和NH Cl晶体在小烧杯中混 Ba(OH) ·8H O与NH Cl
C 2 2 4 2 2 4
合搅拌,用手触摸烧杯外壁感觉变凉 的反应是吸热反应
向某盐溶液中加入NaOH溶液,加热,用湿润
D 该盐溶液中含有NH +
的红色石蕊试纸放在试管口,试纸变蓝 4
15.一定条件下,在密闭容器中进行反应:3 SiCl (g) + 2 N(g) + 6 H(g) Si N(s) +
4 2 2 3 4
12HCl(g)。不能表示上述反应达到化学平衡状态的是
A.单位时间消耗2 mol N,同时生成6 mol H
2 2
B.c(HCl)保持不变
C.混合气体密度保持不变
D.c(N )∶c(H )∶c(HCl) = 1∶3∶6
2 2
16.黑火药爆炸时的反应为:S+2KNO+3C=K S+N↑+3CO↑,下列说法错误的是
3 2 2 2
A.每生成11.2 L的N,该反应转移电子物质的量为6 mol
2
B.被氧化的物质为:C
C.氧化产物:CO
2
D.该反应中氧化剂是:S、KNO
3
学科网(北京)股份有限公司17.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为 和 , 和 具有
相同的电子层结构。下列说法正确的是( )
A. 原子序数: B. 单质沸点:
C. 离子半径: D. 原子最外层电子数:
18.使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是( )
①用天平(使用游码)称量时,被称量物与砝码 的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤;
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线;
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A. ①②⑤ B. ①③⑤ C. ③④⑤ D. ②③⑤
19.三聚氰胺又名蛋白精[分子式: ,相对分子质量:126]是一种低毒性化工产品.婴幼儿大
量摄入可引起泌尿系统疾患。有关三聚氰胺的下列说法正确的是( )
A. 三聚氰胺含氮原子数目为 B. 三聚氰胺含氮量约为10%
C. 标准状况下 的三聚氰胺的体积为 D. 三聚氰胺的摩尔质量为126
20.下列关于化学反应与能量的说法中,不正确的是
A.镁条与盐酸的反应属于放热反应
B.碳与二氧化碳的反应属于放热反应
C.Ba(OH) ·8HO与NH Cl的反应属于吸热反应
2 2 4
D.化学变化中的能量变化主要是由化学键变化引起的
第II卷(非选择题 共40分)
二、填空题
21.(10分)有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有
相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质
在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出下列元素的名称:A_____,B_____,C_____,D_____。
(2)D元素位于周期表中____周期_____族。D2-的结构示意图是____。
(3)AB 是___(填“共价”或“离子”)化合物,C B 所含化学键的类型是___、___。写出AB 与C B 反应
2 2 2 2 2 2
的化学方程式:___________________。
学科网(北京)股份有限公司(4)用电子式表示化合物C D的形成过程:________。
2
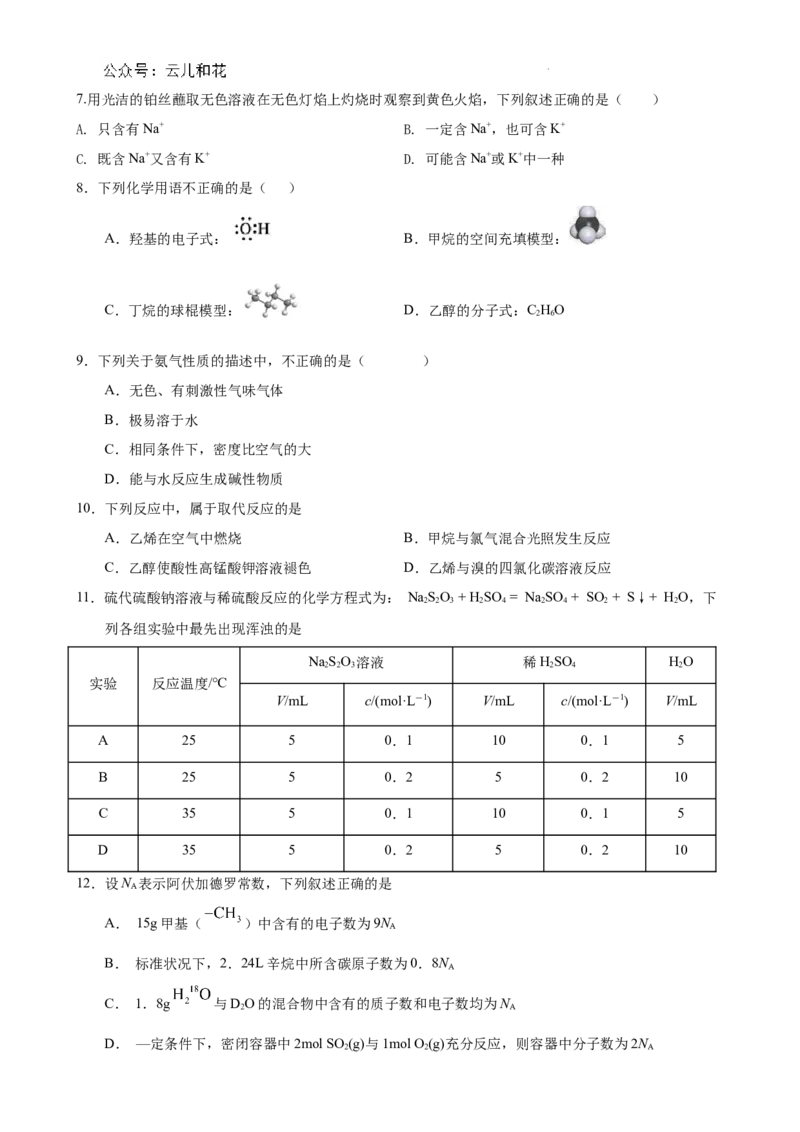
22.(10分)实验室里研究不同价态硫元素之间的转化可采用如下图所示装置进行:
(1)A中发生反应的化学方程式为________________。
(2)B中的现象是__________________。
(3)C中出现淡黄色沉淀,反应中NaS做 ____________(填“氧化剂”或“还原剂”)。
2
(4)D溴水褪色,该反应S元素的价态变化是由+4价变为________________价。
(5)某同学认为D中换成HO 溶液也可以实现上述硫元素的价态转化,并通过实验进一步证明了
2 2
他的观点。实验方案和现象为:取D中反应后的溶液于试管中,_________。
(6)E的作用是_____________,离子方程式为_________________________。
(7)上述实验体现SO 的性质有__________________。
2
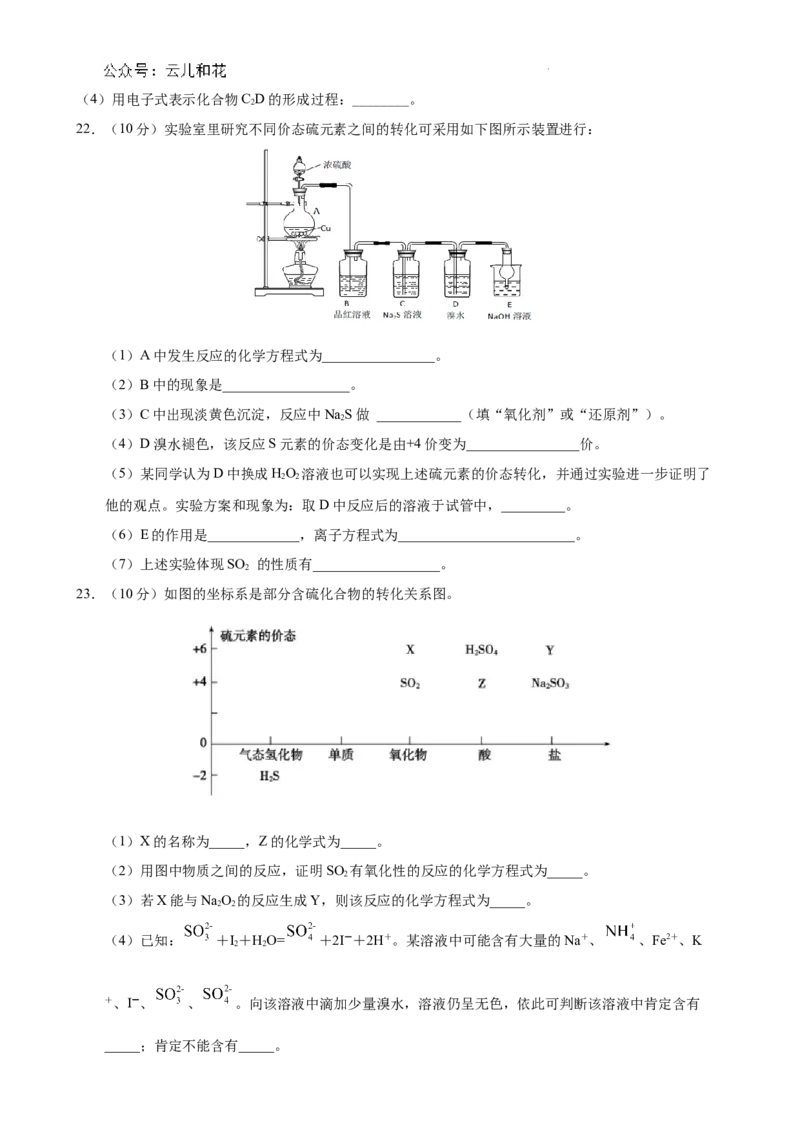
23.(10分)如图的坐标系是部分含硫化合物的转化关系图。
(1)X的名称为_____,Z的化学式为_____。
(2)用图中物质之间的反应,证明SO 有氧化性的反应的化学方程式为_____。
2
(3)若X能与NaO 的反应生成Y,则该反应的化学方程式为_____。
2 2
(4)已知: +I+HO= +2I-+2H+。某溶液中可能含有大量的Na+、 、Fe2+、K
2 2
+、I-、 、 。向该溶液中滴加少量溴水,溶液仍呈无色,依此可判断该溶液中肯定含有
_____;肯定不能含有_____。
学科网(北京)股份有限公司(5)向50 mL浓硫酸中加入铜片,加热,反应一段时间,共收集到2.24 L(标准状况)的SO ,将
2
反应后的混合物加水稀释,再加入足量锌粉放出15.68 L(标准状况)的H,则原浓硫酸的物质的量
2
浓度为_____,整个过程消耗锌粉的质量为_____。
24.(10分)近年来,乳酸成为研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过发酵法制
备。利用乳酸 为原料制成的高分子材料具有生物兼容性,而且在哺乳动物体内
或自然环境中都可以最终降解成为二氧化碳和水。乳酸还有许多其他用途。
(1)请写出乳酸分子中官能团的名称___、___。
(2)乳酸能与纯铁粉反应制备一种补铁药物--乳酸亚铁,反应如下,计算乳酸亚铁中铁的质量分
数为___。
(3)乳酸聚合成的纤维非常适合做手术缝合线,其原因是___。
(4)乳酸发生下列变化:
所用的试剂是a___,b___(写化学式)
(5)请写出乳酸与少量的NaCO 溶液反应的化学方程式___。
2 3
(6)乳酸乙酯( )是一种食用香料,常用于调制果香型、乳酸型食用和酒用精。乳酸
乙酯的同分异构体M有如下性质:0.1 mol M分别与足量的金属钠和碳酸氢钠反应,产生的气体在
相同状况下的体积相同,则M的结构最多有___(不考虑空间异构)种。
学科网(北京)股份有限公司