文档内容
武昌区 2024 届高三年级 5 月质量检测
化学
本试题卷共8页,共19题。满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Fe 56 Cu 64
一、选择题:本题共 15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 生产精细化学品已经成为当代化学工业结构调整的重点之一。下列对应关系不正确的是
A. 解热镇痛药-阿司匹林 B. 凝固剂-硫酸钙
C. 抗氧化剂-维生素C D. 营养强化剂-味精
2. 化学服务生产生活,下列关于物质用途说法错误的是
A. 二氧化硫不仅可用于杀菌消毒,还是一种食品添加剂
B. DDT具有较高和较宽广的杀虫活性;目前被广泛施用
C. 碳化硅陶瓷可用作耐高温结构材料、耐高温半导体材料
D. 叔丁基对苯二酚用作食用油的抗氧化剂,确保食品安全
3. 下列化学用语或图示表示正确的是
A. NH I的电子式: B. 反式聚异戊二烯的结构简式:
4
第1页/共9页
学科网(北京)股份有限公司C. 1-戊烯的球棍模型为 D. 基态溴原子的简化电子排布式:
4. 类比推理是化学中常用的思维方法,下列说法正确的是
A. NF 是极性分子,则BF 也是极性分子
3 3
B. HO 具有还原性,则NaO 也具有还原性
2 2 2 2
C. 氯化银能溶于浓氨水,则碘化银也能溶于浓氨水
D. 酸性KMnO 溶液能将甲苯氧化成苯甲酸,则也能将乙苯氧化成苯乙酸
4
5. 设N 为阿伏加德罗常数的值。下列叙述错误的是
A
A. 在电解精炼粗铜的过程中,当阴极质量增重32g时转移的电子数为
B. 标准状况下,11.2LSO 分子数目大于
3
C. 15g乙烯和20g丙烯的混合气体中含有C—H共价键的数目为
D. 4.6gNa与足量O 充分反应,反应中转移的电子数介于 和 之间
2
6. 不能正确描述其反应的方程式是
A. 工业制备高铁酸钠的一种方法:
B. 由石英与焦炭在高温的氮气流中制备氮化硅:
C. 在叶绿素中合成糖类化合物:
D. 牙膏中添加氟化物预防龋齿:
的
7. 物质结构决定物质性质,下列性质差异及对应 结构因素都正确的是
选
性质差异 结构因素
项
A. 酸性:CHCHOH>CH CHSH 共价键的极性
3 2 3 2
B. 热稳定性:CH>SiH 分子间作用力
4 4
C. 硬度:硅<锗 键长
D. 沸点:邻二甲苯>对二甲苯 分子 极的性
第2页/共9页
学科网(北京)股份有限公司A. A B. B C. C D. D
8. 下列实验方案不能达到实验目的的是
选
实验方案 实验目的
项
A 将乙醇与浓硫酸的混合物加热至170℃,并将产生的气体干燥后通
验证乙醇发生了消去反应
. 入少量溴的四氯化碳溶液中,观察溴的四氯化碳溶液颜色的变化
B 向 溶液中加入少许铁粉,静置一段时间,观察是否有
验证 具有氧化性
.
蓝色沉淀生成
C 比较 CHCOOH 溶液和 HCO
分别测定相同浓度的CHCOONH 溶液和NaHCO 溶液的pH 3 2 3
. 3 4 3 的酸性
验 证 结 合 H+ 的 能 力 :
D 向 溶液中滴加NaHCO 溶液,观察是否有白色沉
3
.
淀生成
A. A B. B C. C D. D
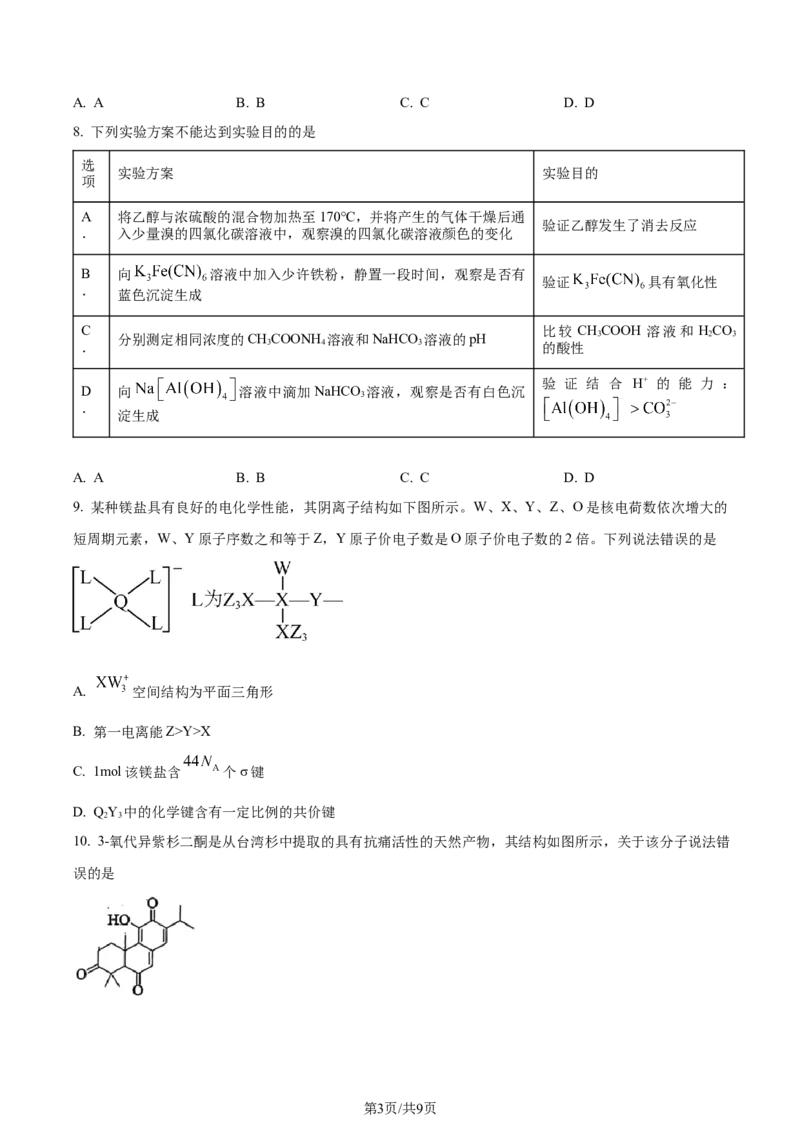
9. 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、O是核电荷数依次增大的
短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是O原子价电子数的2倍。下列说法错误的是
A. 空间结构为平面三角形
B. 第一电离能Z>Y>X
C. 1mol该镁盐含 个σ键
D. QY 中的化学键含有一定比例的共价键
2 3
10. 3-氧代异紫杉二酮是从台湾杉中提取的具有抗痛活性的天然产物,其结构如图所示,关于该分子说法错
误的是
第3页/共9页
学科网(北京)股份有限公司A. 可发生氧化、加成、取代、还原反应
B. 该分子具有手性
C. 核磁共振氢谱有9组吸收峰的
D. 1mol该物质与足量氢气加成后,最多可与4mol金属钠发生反应
11. 非金属的卤化物水解可以分为亲电水解和亲核水解,实例及部分机理示意如下:发生亲电水解的条件
是中心原子具有孤电子对,能接受HO的H+的进攻,如:
2
发生亲核水解条件是中心原子具有 和空的价层轨道,接受HO的孤电子对进攻,如:
2
下列说法错误的是
A. NCl 和SiCl 水解过程中中心原子的杂化方式不变
3 4
B. 推测CCl 比SiCl 难发生亲核水解
4 4
C. 推测NF 比NCl 难发生亲电水解:
3 3
D. 已知AsCl 的水解产物为HAsO 和HCl,推测其水解类型为亲核水解
3 3 3
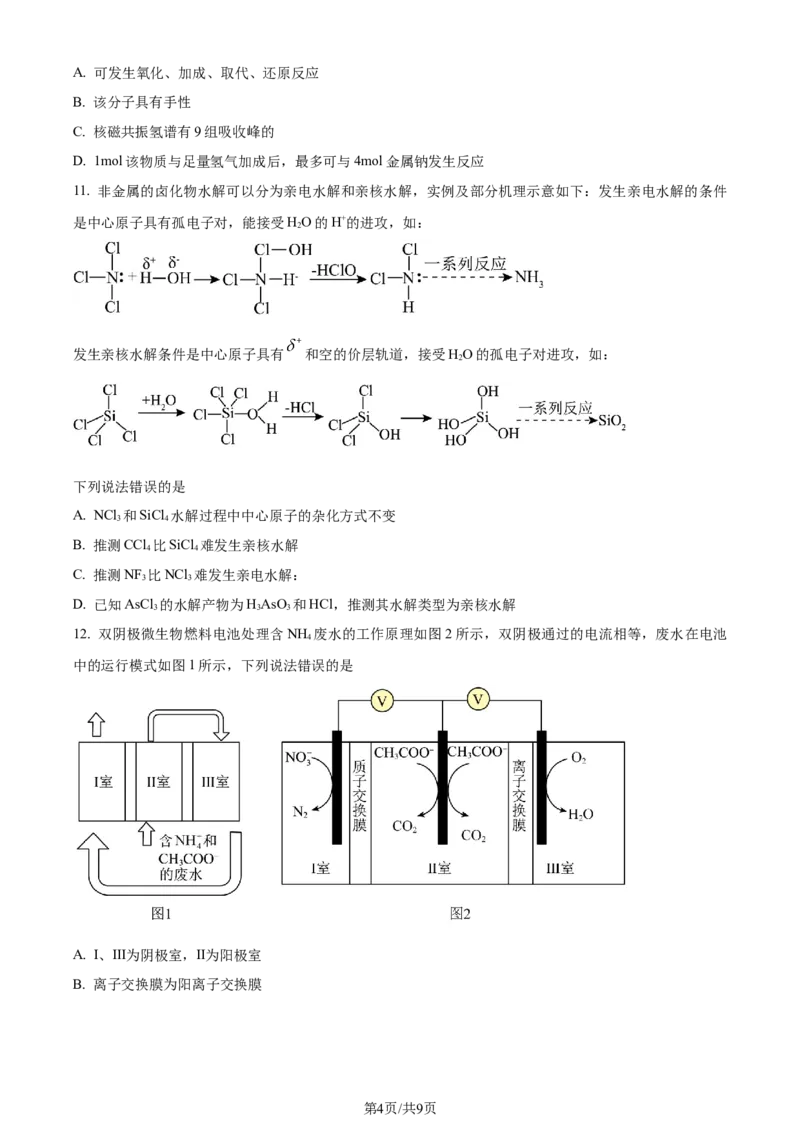
12. 双阴极微生物燃料电池处理含NH 废水的工作原理如图2所示,双阴极通过的电流相等,废水在电池
4
中的运行模式如图1所示,下列说法错误的是
A. I、Ⅲ为阴极室,Ⅱ为阳极室
B. 离子交换膜为阳离子交换膜
第4页/共9页
学科网(北京)股份有限公司C. Ⅲ室会发生反应
.
D 生成3.5gN ,理论上需要消耗10gO
2 2
13. 化合物Q是一种潜在热电材料,其晶胞结构如图甲所示,沿x、y、z轴方向的投影均如图乙所示。Q最
简式的式量为M,晶体密度为 。下列说法错误的是
r
A. Q的化学式为KSeBr
2 6
B. K+位于阴离子构成的四面体空隙内
C. Q固体颗粒的X射线衍射图谱有尖锐的衍射峰
D. 相邻K+之间的最短距离为
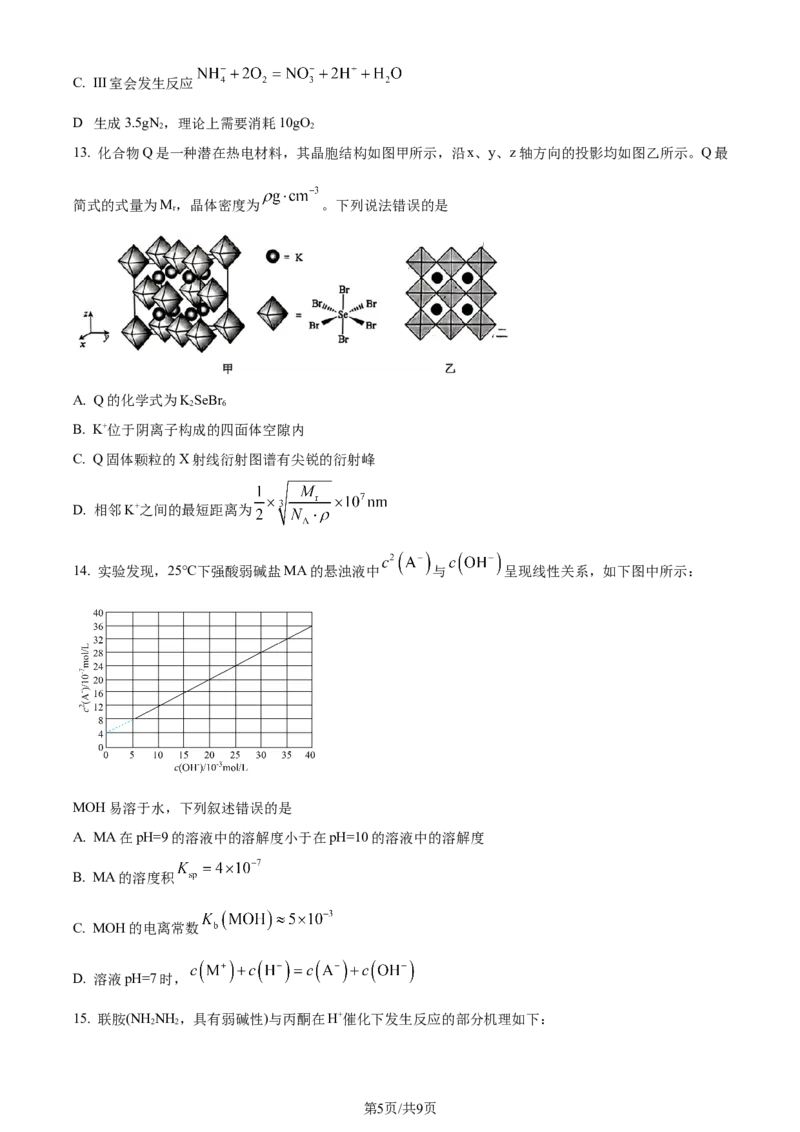
14. 实验发现,25℃下强酸弱碱盐MA的悬浊液中 与 呈现线性关系,如下图中所示:
MOH易溶于水,下列叙述错误的是
A. MA在pH=9的溶液中的溶解度小于在pH=10的溶液中的溶解度
B. MA的溶度积
C. MOH的电离常数
D. 溶液pH=7时,
15. 联胺(NH NH ,具有弱碱性)与丙酮在H+催化下发生反应的部分机理如下:
2 2
第5页/共9页
学科网(北京)股份有限公司下列说法错误的是
A. 反应②的活化能最大
B. 增大H+浓度一定可加快反应速率
C. 通过分子筛分离水可以增大丙酮的平衡转化率
D. 总反应为
二、非选择题:本题共4小题,共55分。
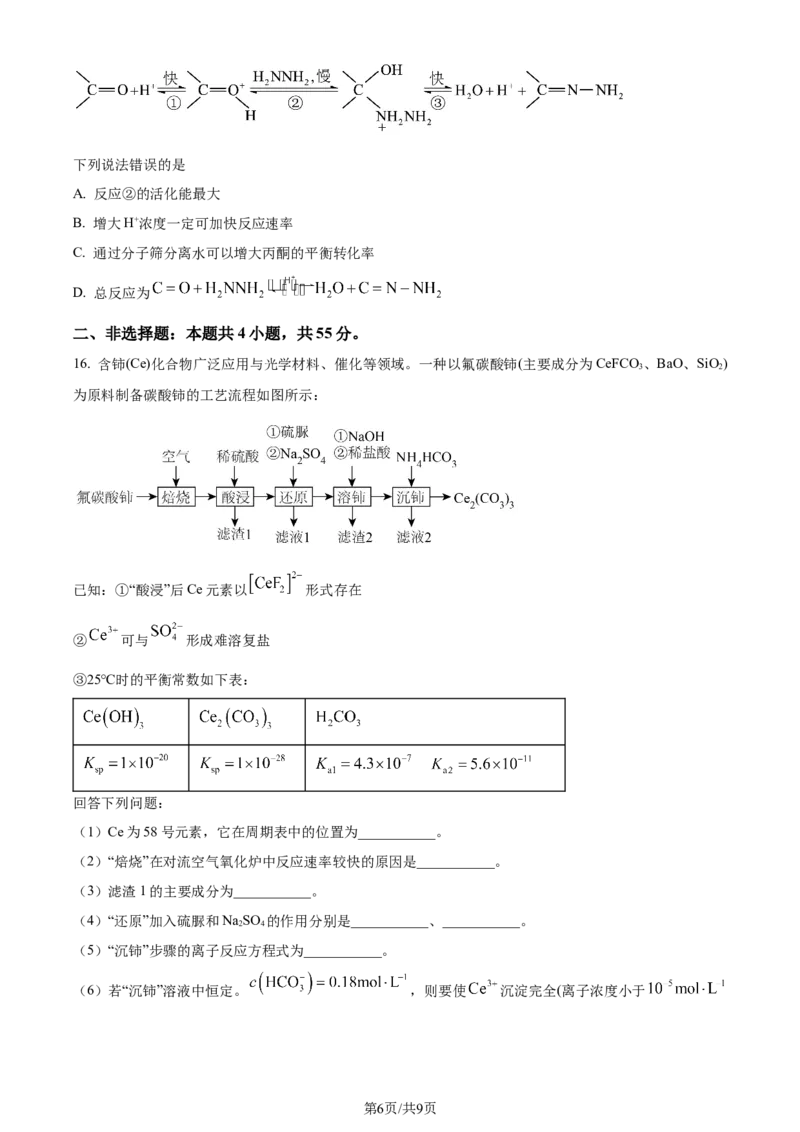
16. 含铈(Ce)化合物广泛应用与光学材料、催化等领域。一种以氟碳酸铈(主要成分为CeFCO、BaO、SiO)
3 2
为原料制备碳酸铈的工艺流程如图所示:
已知:①“酸浸”后Ce元素以 形式存在
② 可与 形成难溶复盐
③25℃时的平衡常数如下表:
回答下列问题:
(1)Ce为58号元素,它在周期表中的位置为___________。
(2)“焙烧”在对流空气氧化炉中反应速率较快的原因是___________。
(3)滤渣1的主要成分为___________。
(4)“还原”加入硫脲和NaSO 的作用分别是___________、___________。
2 4
(5)“沉铈”步骤的离子反应方程式为___________。
(6)若“沉铈”溶液中恒定。 ,则要使 沉淀完全(离子浓度小于
第6页/共9页
学科网(北京)股份有限公司),理论上pH不低于___________(保留一位小数)。
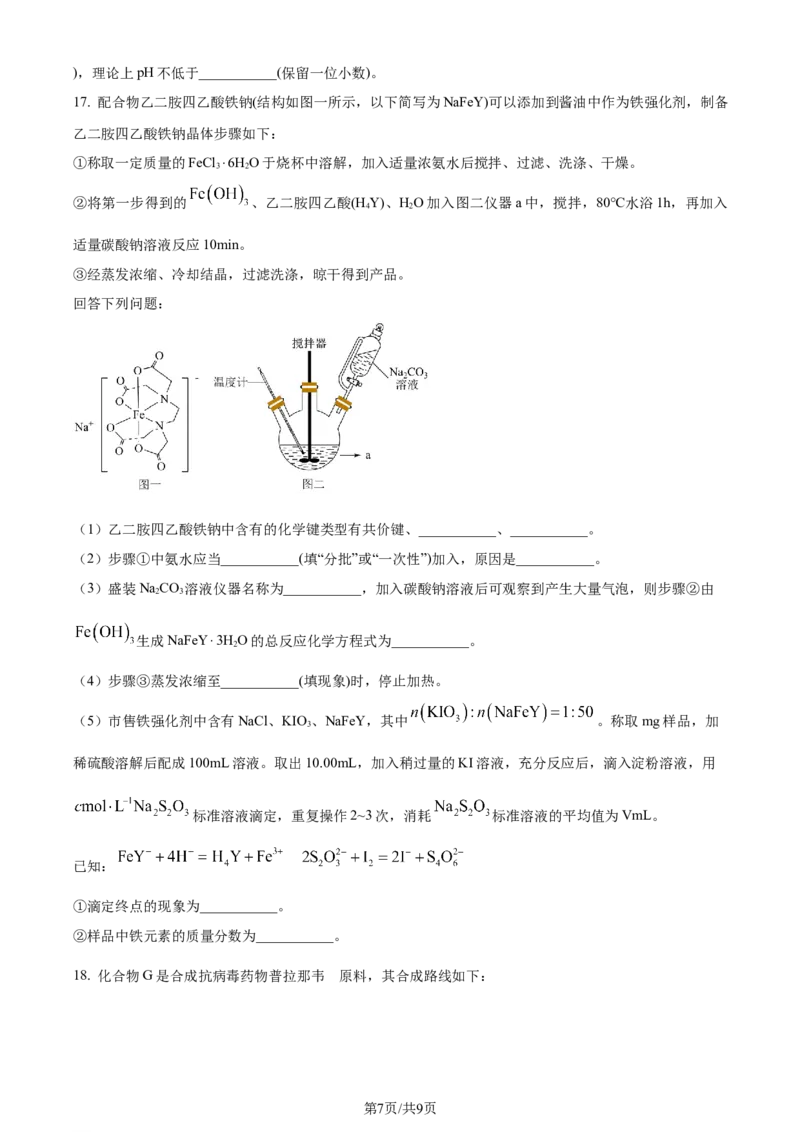
17. 配合物乙二胺四乙酸铁钠(结构如图一所示,以下简写为NaFeY)可以添加到酱油中作为铁强化剂,制备
乙二胺四乙酸铁钠晶体步骤如下:
①称取一定质量的FeCl ⋅6HO于烧杯中溶解,加入适量浓氨水后搅拌、过滤、洗涤、干燥。
3 2
②将第一步得到的 、乙二胺四乙酸(H Y)、HO加入图二仪器a中,搅拌,80℃水浴1h,再加入
4 2
适量碳酸钠溶液反应10min。
③经蒸发浓缩、冷却结晶,过滤洗涤,晾干得到产品。
回答下列问题:
(1)乙二胺四乙酸铁钠中含有的化学键类型有共价键、___________、___________。
(2)步骤①中氨水应当___________(填“分批”或“一次性”)加入,原因是___________。
(3)盛装NaCO 溶液仪器名称为___________,加入碳酸钠溶液后可观察到产生大量气泡,则步骤②由
2 3
生成NaFeY⋅3HO的总反应化学方程式为___________。
2
(4)步骤③蒸发浓缩至___________(填现象)时,停止加热。
(5)市售铁强化剂中含有NaCl、KIO 、NaFeY,其中 。称取mg样品,加
3
稀硫酸溶解后配成100mL溶液。取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用
标准溶液滴定,重复操作2~3次,消耗 标准溶液的平均值为VmL。
已知:
①滴定终点的现象为___________。
②样品中铁元素的质量分数为___________。
的
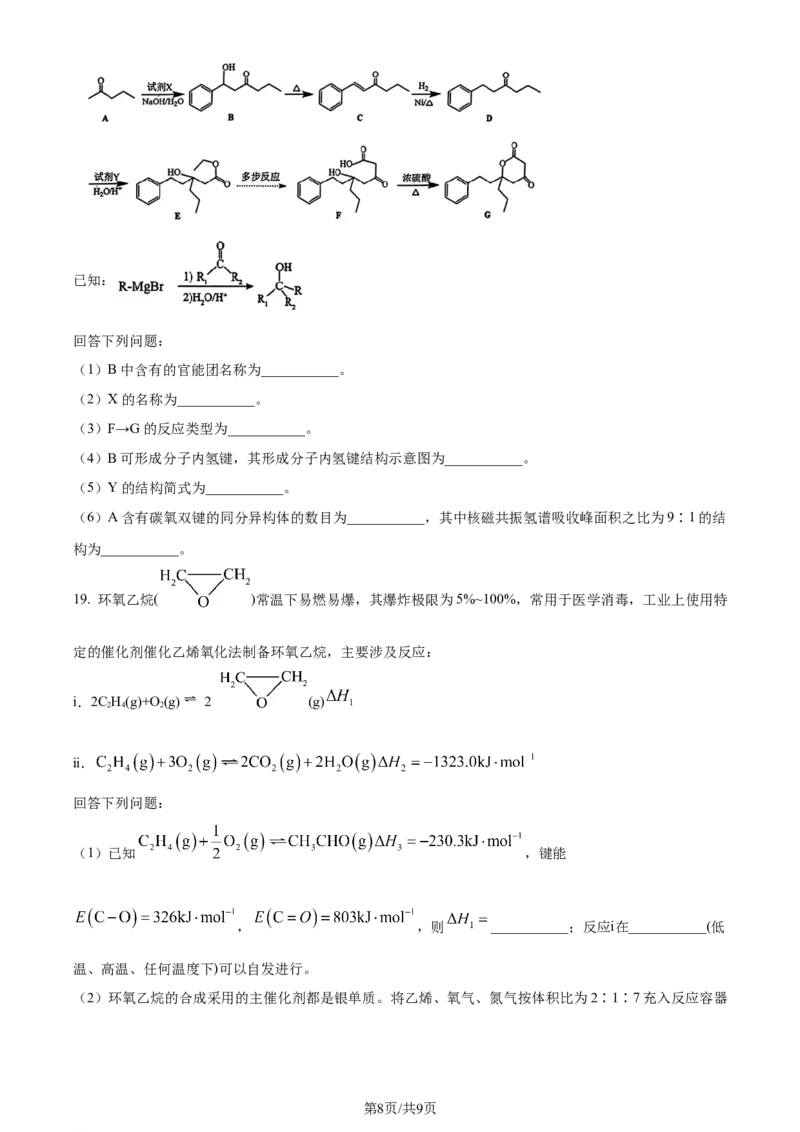
18. 化合物G是合成抗病毒药物普拉那韦 原料,其合成路线如下:
第7页/共9页
学科网(北京)股份有限公司已知:
回答下列问题:
(1)B中含有的官能团名称为___________。
(2)X的名称为___________。
(3)F→G的反应类型为___________。
(4)B可形成分子内氢键,其形成分子内氢键结构示意图为___________。
(5)Y的结构简式为___________。
(6)A含有碳氧双键的同分异构体的数目为___________,其中核磁共振氢谱吸收峰面积之比为9∶1的结
构为___________。
19. 环氧乙烷( )常温下易燃易爆,其爆炸极限为5%~100%,常用于医学消毒,工业上使用特
定的催化剂催化乙烯氧化法制备环氧乙烷,主要涉及反应:
ⅰ.2C H(g)+O(g) 2 (g)
2 4 2
ⅱ.
回答下列问题:
(1)已知 ,键能
, ,则 ___________;反应ⅰ在___________(低
温、高温、任何温度下)可以自发进行。
(2)环氧乙烷的合成采用的主催化剂都是银单质。将乙烯、氧气、氮气按体积比为2∶1∶7充入反应容器
第8页/共9页
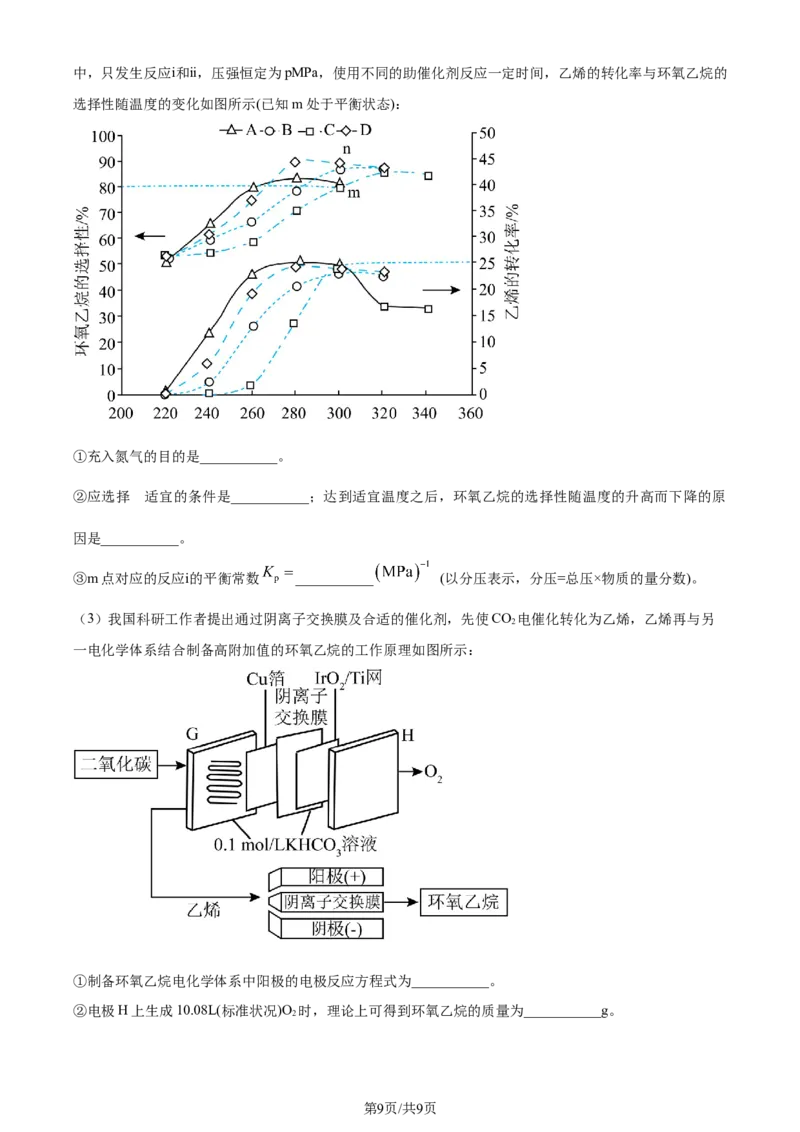
学科网(北京)股份有限公司中,只发生反应ⅰ和ⅱ,压强恒定为pMPa,使用不同的助催化剂反应一定时间,乙烯的转化率与环氧乙烷的
选择性随温度的变化如图所示(已知m处于平衡状态):
①充入氮气的目的是___________。
的
②应选择 适宜的条件是___________;达到适宜温度之后,环氧乙烷的选择性随温度的升高而下降的原
因是___________。
③m点对应的反应ⅰ的平衡常数 ___________ (以分压表示,分压=总压×物质的量分数)。
(3)我国科研工作者提出通过阴离子交换膜及合适的催化剂,先使CO 电催化转化为乙烯,乙烯再与另
2
一电化学体系结合制备高附加值的环氧乙烷的工作原理如图所示:
①制备环氧乙烷电化学体系中阳极的电极反应方程式为___________。
②电极H上生成10.08L(标准状况)O 时,理论上可得到环氧乙烷的质量为___________g。
2
第9页/共9页
学科网(北京)股份有限公司