文档内容
1
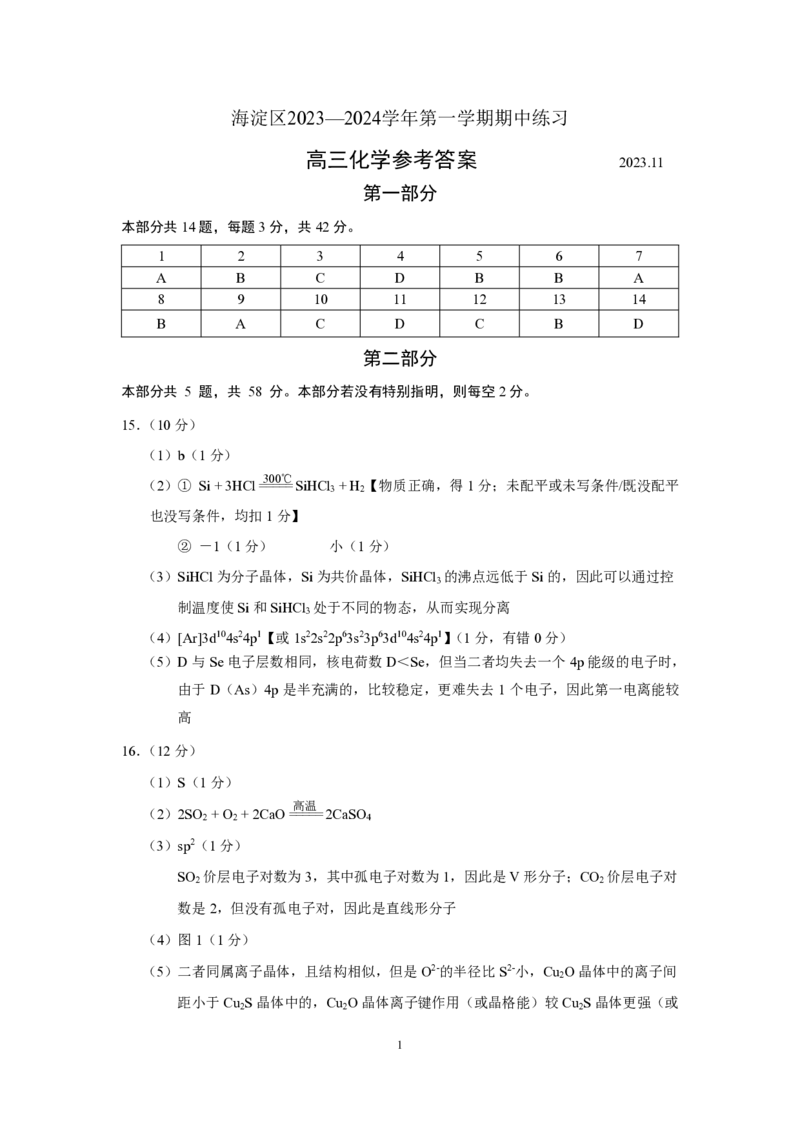
海淀区2023—2024学年第一学期期中练习
高三化学参考答案 2023.11
第一部分
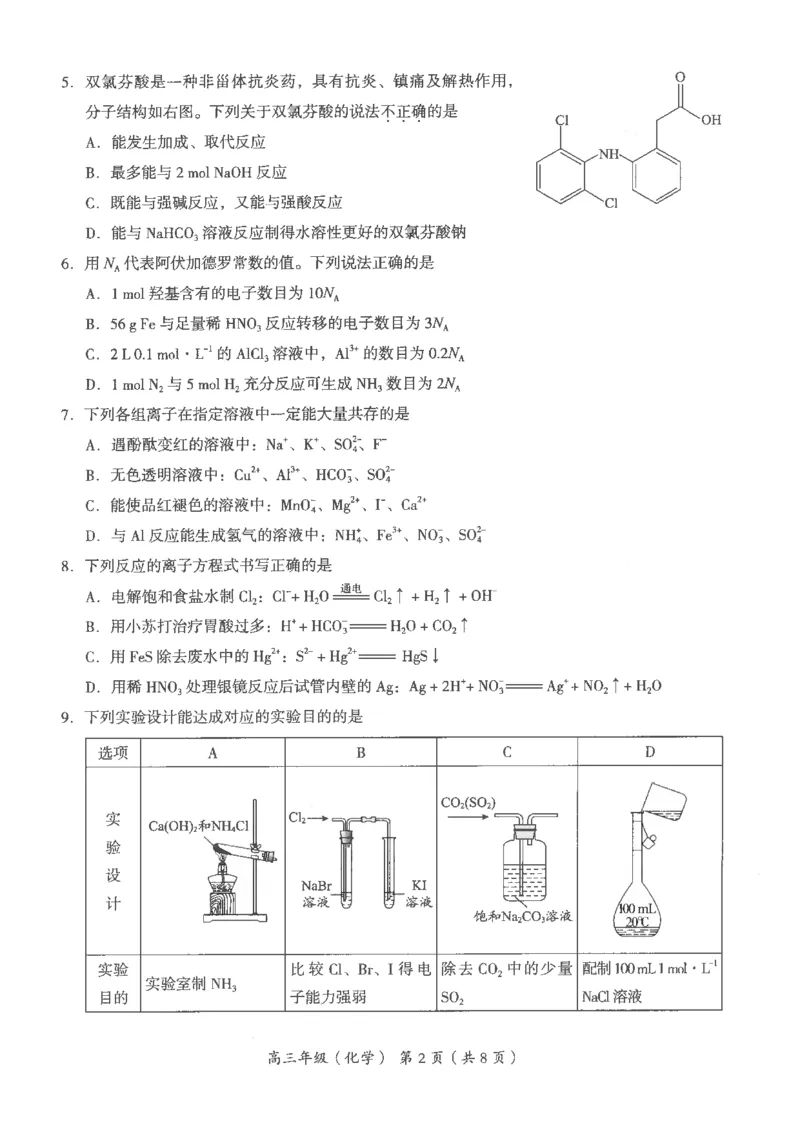
本部分共14 题,每题3 分,共42 分。
1
2
3
4
5
6
7
A
B
C
D
B
B
A
8
9
10
11
12
13
14
B
A
C
D
C
B
D
第二部分
本部分共 5 题,共 58 分。本部分若没有特别指明,则每空2 分。
15.(10 分)
(1)b(1 分)
(2)① Si + 3HCl ===== SiHCl3 + H2【物质正确,得1 分;未配平或未写条件/既没配平
也没写条件,均扣1 分】
② -1(1 分) 小(1 分)
(3)SiHCl 为分子晶体,Si 为共价晶体,SiHCl3 的沸点远低于Si 的,因此可以通过控
制温度使Si 和SiHCl3 处于不同的物态,从而实现分离
(4)[Ar]3d104s24p1【或1s22s22p63s23p63d104s24p1】(1 分,有错0 分)
(5)D 与Se 电子层数相同,核电荷数D<Se,但当二者均失去一个4p 能级的电子时,
由于D(As)4p 是半充满的,比较稳定,更难失去1 个电子,因此第一电离能较
高
16.(12 分)
(1)S(1 分)
(2)2SO2 + O2 + 2CaO ===== 2CaSO4
(3)sp2(1 分)
SO2 价层电子对数为3,其中孤电子对数为1,因此是V 形分子;CO2 价层电子对
数是2,但没有孤电子对,因此是直线形分子
(4)图1(1 分)
(5)二者同属离子晶体,且结构相似,但是O2-的半径比S2-小,Cu2O 晶体中的离子间
距小于Cu2S 晶体中的,Cu2O 晶体离子键作用(或晶格能)较Cu2S 晶体更强(或
300℃
高温
2
大),因此熔点更高(1 分)
(6)① 图4 中上底面中心的黑色原子(Fe)无法与下底面中心的白色原子(Cu)在平
移之后实现无隙并置 (1 分)
② 4(1 分)
③ √
368
4.3𝑁𝐴
3
×1010
17.(10 分)
(1)
(2)不变(1 分)
(3)丙烷直接脱氢反应为吸热反应,压强相同时,温度升高平衡正向移动,C3H6 体积
分数变大
(4)II(1 分)
(5)温度升高,丙烷氧化脱氢的反应速率加快
(6)降低(1 分)
温度升高,更有利于丙烷被氧化成其他产物的副反应发生(1 分)
18.(14 分)
(1)abc
(2)冷却结晶、过滤洗涤
(3)3[Fe(CN)6]4- + 4Fe3+ ===== Fe4[Fe(CN)6]3↓
(4)2KHCO3 ===== K2CO3 + CO2↑+ H2O
(5)6 ·OH + 2NH
+
4 ===== N2↑+ 6H2O + 2H+
(6)① 204 ② 13
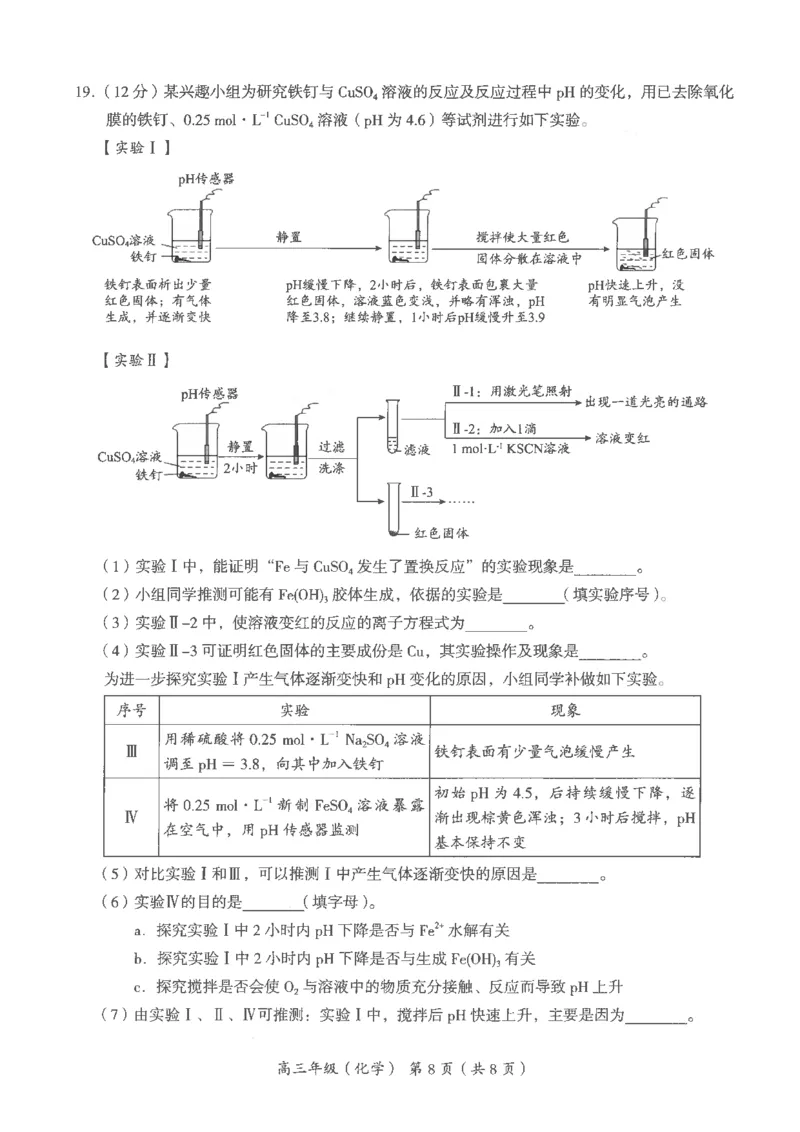
19.(12 分)
(1)析出红色固体,溶液蓝色变浅
(2)II-1(1 分)
(3)Fe3+ + 3SCN-
Fe(SCN)3(1 分)
(4)向红色固体中加入稀HNO3,红色固体溶解,溶液变蓝
(5)铁钉表面析出Cu 后,形成Fe-Cu 原电池
(6)abc
(7)搅拌后,Cu 与Fe3+发生反应:Cu + 2Fe3+ ===== 2Fe2+ + Cu2+,使Fe3+水解平衡逆
向移动
700℃