文档内容
2024~2025 学年度第一学期期中教学质量检测
高二化学试题
2024.11
本试卷分第I卷和第II卷,全卷满分100分,考试时间为90分钟。
注意事项:1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡(纸)指定位置上。
2.答第I卷选择题时,将每小题答案选出后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
3.第II卷题目的答案用黑色签字笔,将答案写在答题卡(纸)规定的位置上。写在试卷上无
效。可能用到的相对原子质量:H_1、 N_14、 O_16、 S_32
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.下列食品添加剂的使用中,与反应速率有关的是
A.炒菜时加味精 B.卤水点豆腐
C.水果罐头中加入维生素 D.食盐中加碘酸钾
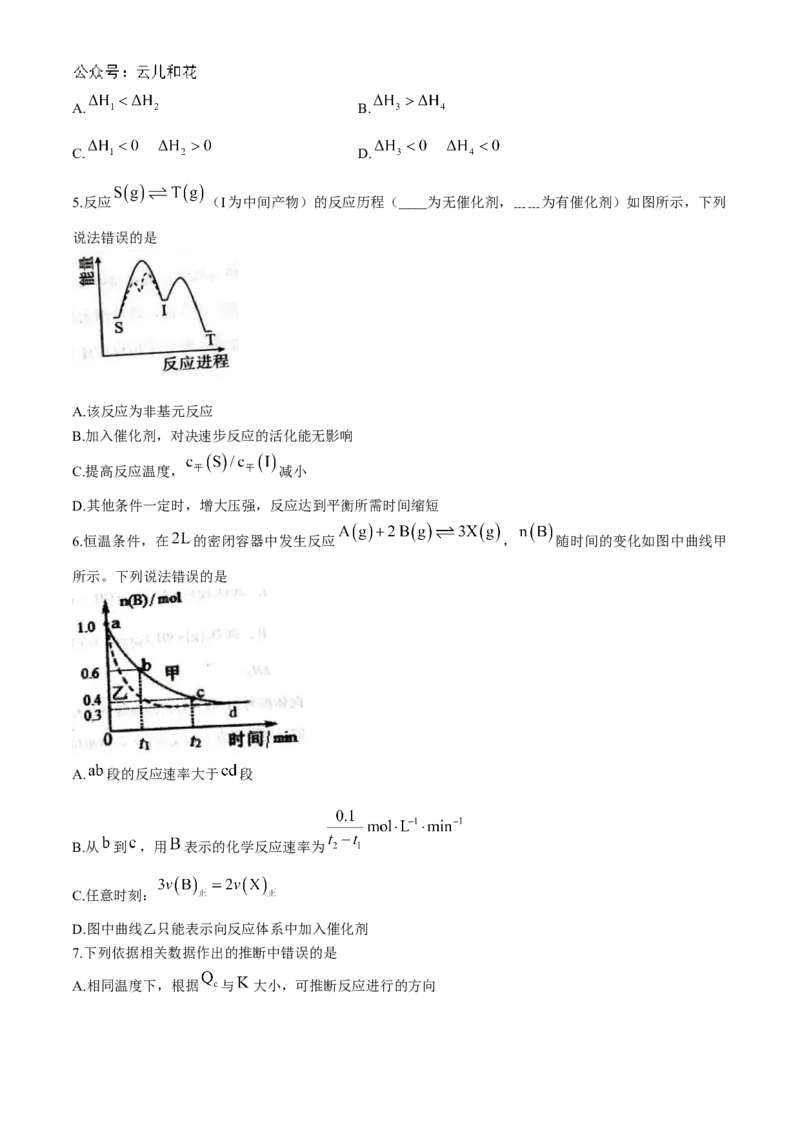
2.下列实验操作对应的装置正确的是
通过注射器活塞右移,验证 与
测量中和反应反应热 测定某溶液的 调控滴定速度
反应放热
A B C D
3.下列关于合成氨的说法正确的是
A.适当延长反应时间,可以提高合成氨气的平衡产率
B.升温会导致原料的平衡转化率降低
C.压强越大,合成氨的综合效益越好
D.铁触媒能减小该反应的焓变
4.关于下列 的判断正确的是A. B.
C. D.
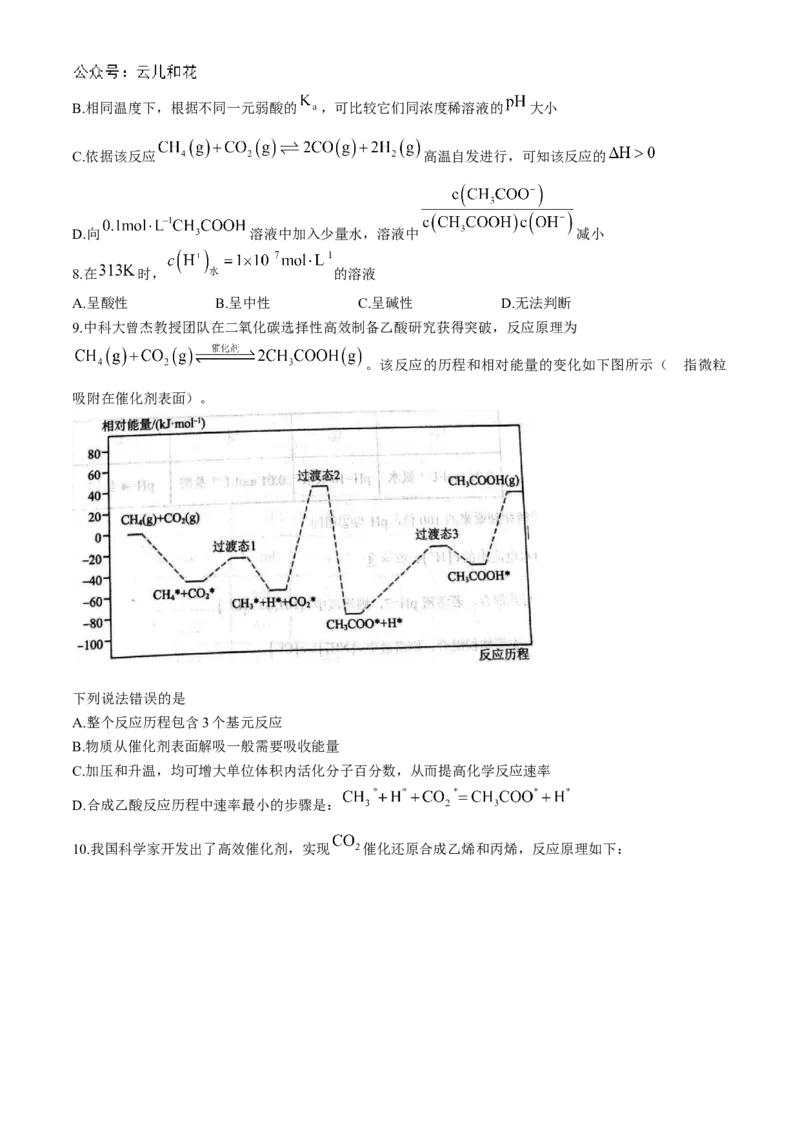
5.反应 (I为中间产物)的反应历程(__为无催化剂,﹍﹍为有催化剂)如图所示,下列
说法错误的是
A.该反应为非基元反应
B.加入催化剂,对决速步反应的活化能无影响
C.提高反应温度, 减小
D.其他条件一定时,增大压强,反应达到平衡所需时间缩短
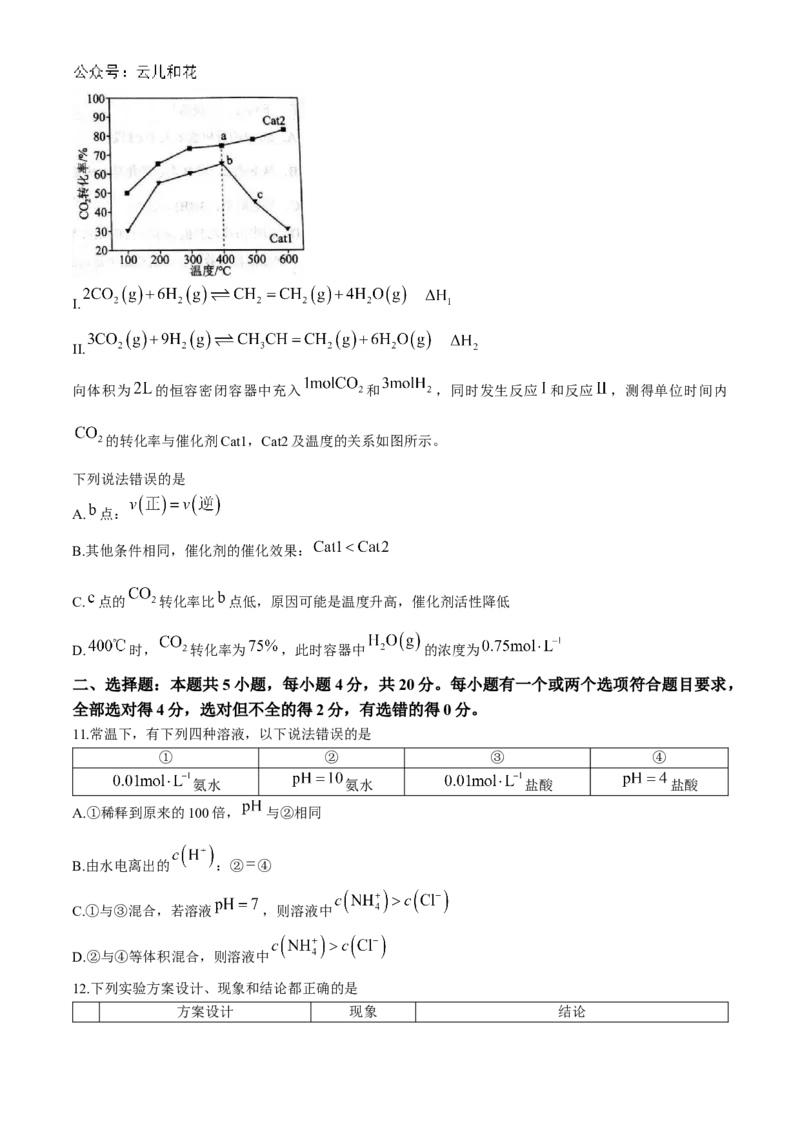
6.恒温条件,在 的密闭容器中发生反应 , 随时间的变化如图中曲线甲
所示。下列说法错误的是
A. 段的反应速率大于 段
B.从 到 ,用 表示的化学反应速率为
C.任意时刻:
D.图中曲线乙只能表示向反应体系中加入催化剂
7.下列依据相关数据作出的推断中错误的是
A.相同温度下,根据 与 大小,可推断反应进行的方向B.相同温度下,根据不同一元弱酸的 ,可比较它们同浓度稀溶液的 大小
C.依据该反应 高温自发进行,可知该反应的
D.向 溶液中加入少量水,溶液中 减小
8.在 时, 的溶液
A.呈酸性 B.呈中性 C.呈碱性 D.无法判断
9.中科大曾杰教授团队在二氧化碳选择性高效制备乙酸研究获得突破,反应原理为
。该反应的历程和相对能量的变化如下图所示( 指微粒
吸附在催化剂表面)。
下列说法错误的是
A.整个反应历程包含3个基元反应
B.物质从催化剂表面解吸一般需要吸收能量
C.加压和升温,均可增大单位体积内活化分子百分数,从而提高化学反应速率
D.合成乙酸反应历程中速率最小的步骤是:
10.我国科学家开发出了高效催化剂,实现 催化还原合成乙烯和丙烯,反应原理如下:I.
II.
向体积为 的恒容密闭容器中充入 和 ,同时发生反应 和反应 ,测得单位时间内
的转化率与催化剂Cat1,Cat2及温度的关系如图所示。
下列说法错误的是
A. 点:
B.其他条件相同,催化剂的催化效果:
C. 点的 转化率比 点低,原因可能是温度升高,催化剂活性降低
D. 时, 转化率为 ,此时容器中 的浓度为
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
11.常温下,有下列四种溶液,以下说法错误的是
① ② ③ ④
氨水 氨水 盐酸 盐酸
A.①稀释到原来的100倍, 与②相同
B.由水电离出的 :② ④
C.①与③混合,若溶液 ,则溶液中
D.②与④等体积混合,则溶液中
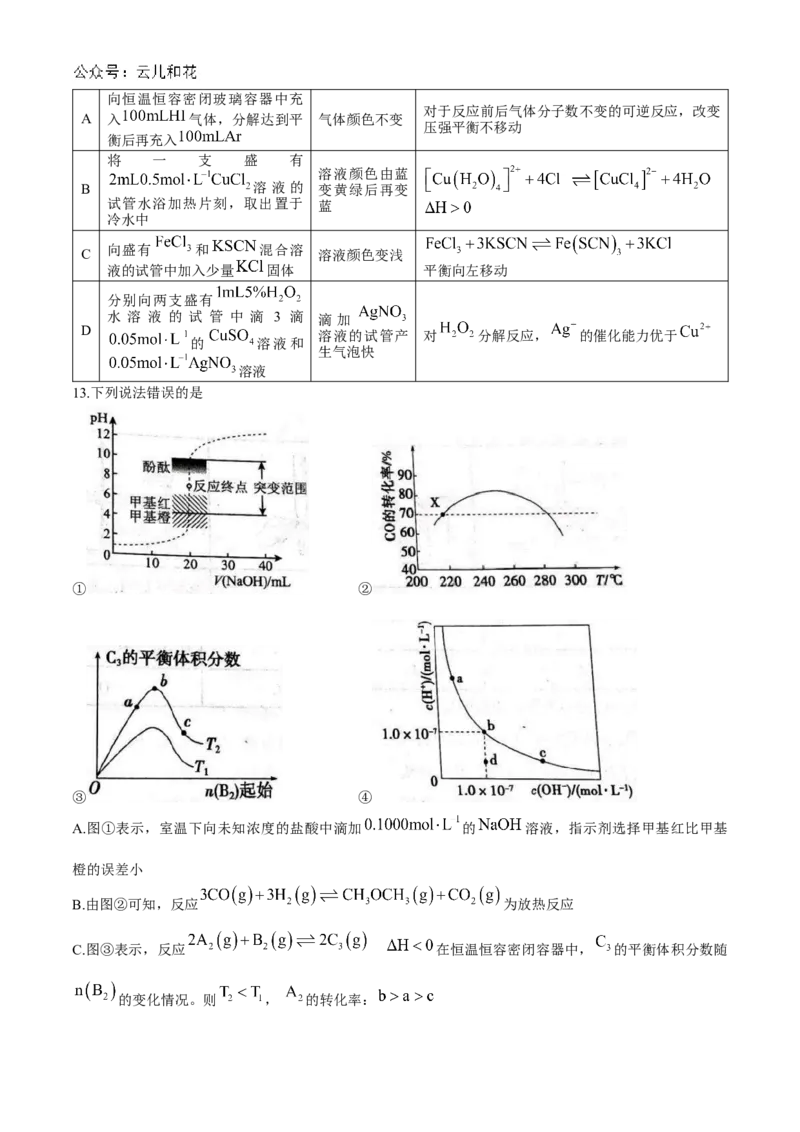
12.下列实验方案设计、现象和结论都正确的是
方案设计 现象 结论向恒温恒容密闭玻璃容器中充
对于反应前后气体分子数不变的可逆反应,改变
A 入 气体,分解达到平 气体颜色不变
压强平衡不移动
衡后再充入
将 一 支 盛 有
溶液颜色由蓝
B 溶 液 的 变黄绿后再变
试管水浴加热片刻,取出置于 蓝
冷水中
向盛有 和 混合溶
C 溶液颜色变浅
液的试管中加入少量 固体 平衡向左移动
分别向两支盛有
水 溶 液 的 试 管 中 滴 3 滴 滴 加
D
溶液的试管产 对 分解反应, 的催化能力优于
的 溶液和
生气泡快
溶液
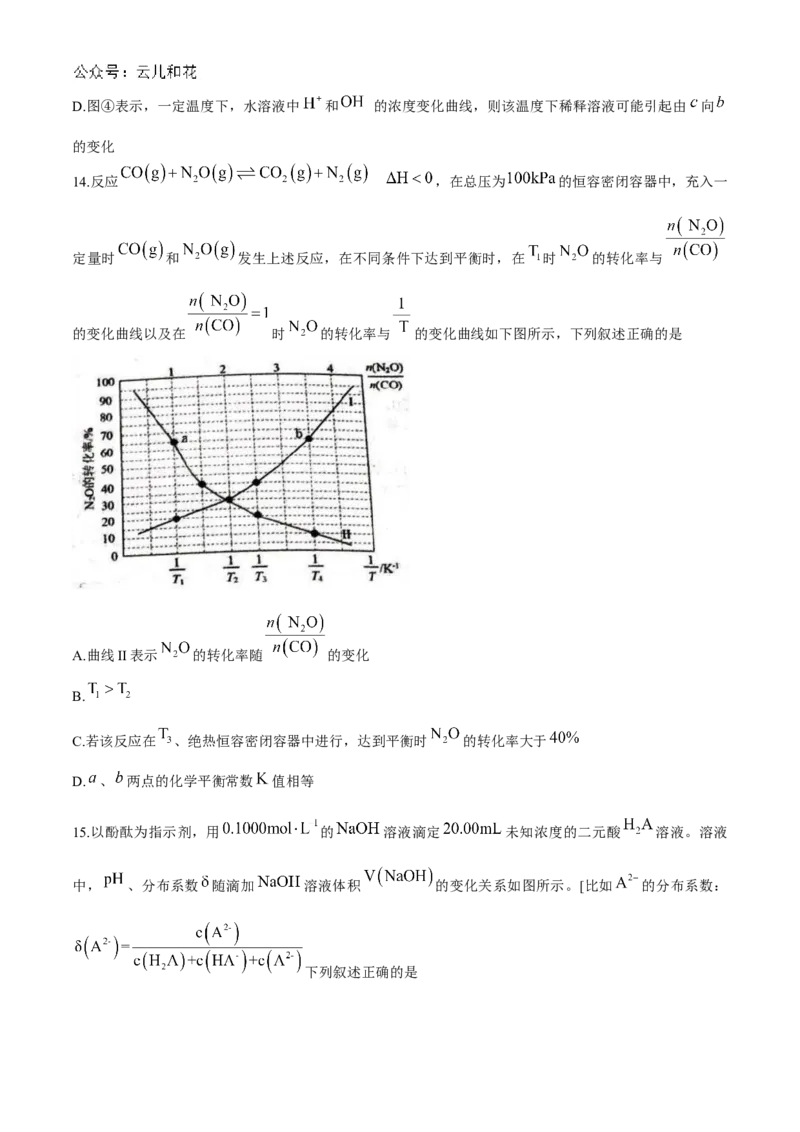
13.下列说法错误的是
① ②
③ ④
A.图①表示,室温下向未知浓度的盐酸中滴加 的 溶液,指示剂选择甲基红比甲基
橙的误差小
B.由图②可知,反应 为放热反应
C.图③表示,反应 在恒温恒容密闭容器中, 的平衡体积分数随
的变化情况。则 , 的转化率:D.图④表示,一定温度下,水溶液中 和 的浓度变化曲线,则该温度下稀释溶液可能引起由 向
的变化
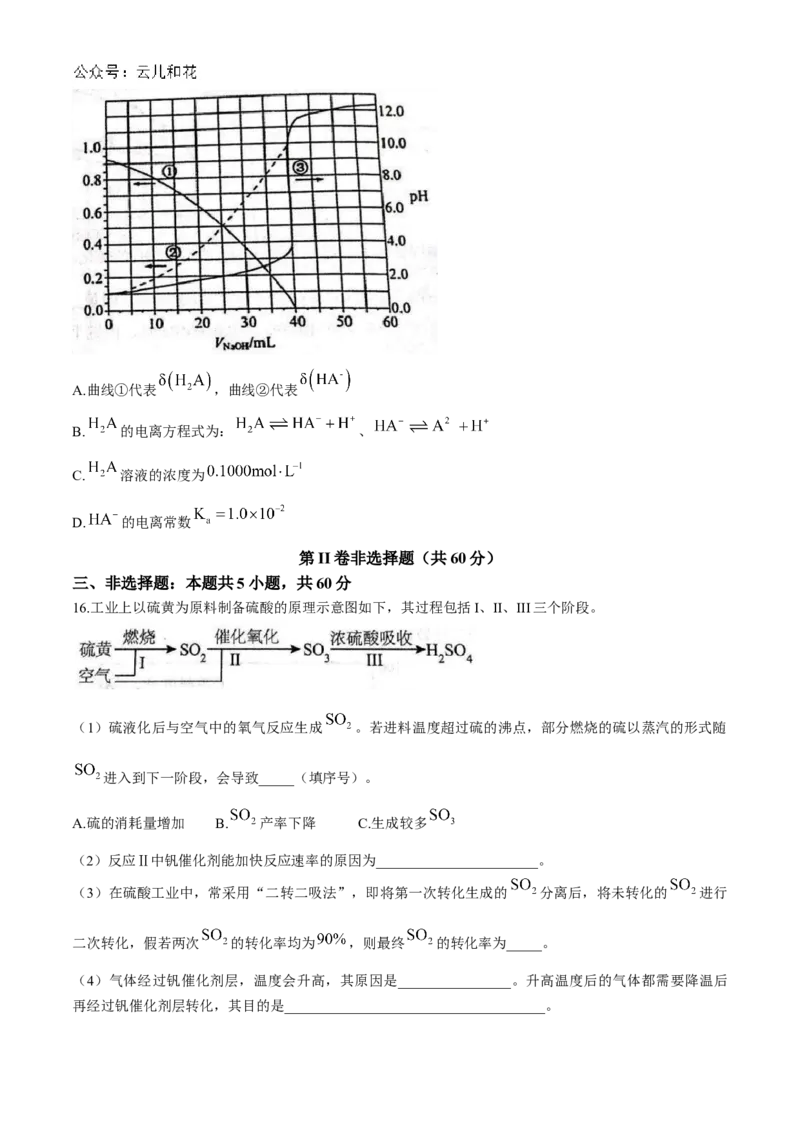
14.反应 ,在总压为 的恒容密闭容器中,充入一
定量时 和 发生上述反应,在不同条件下达到平衡时,在 时 的转化率与
的变化曲线以及在 时 的转化率与 的变化曲线如下图所示,下列叙述正确的是
A.曲线II表示 的转化率随 的变化
B.
C.若该反应在 、绝热恒容密闭容器中进行,达到平衡时 的转化率大于
D. 、 两点的化学平衡常数 值相等
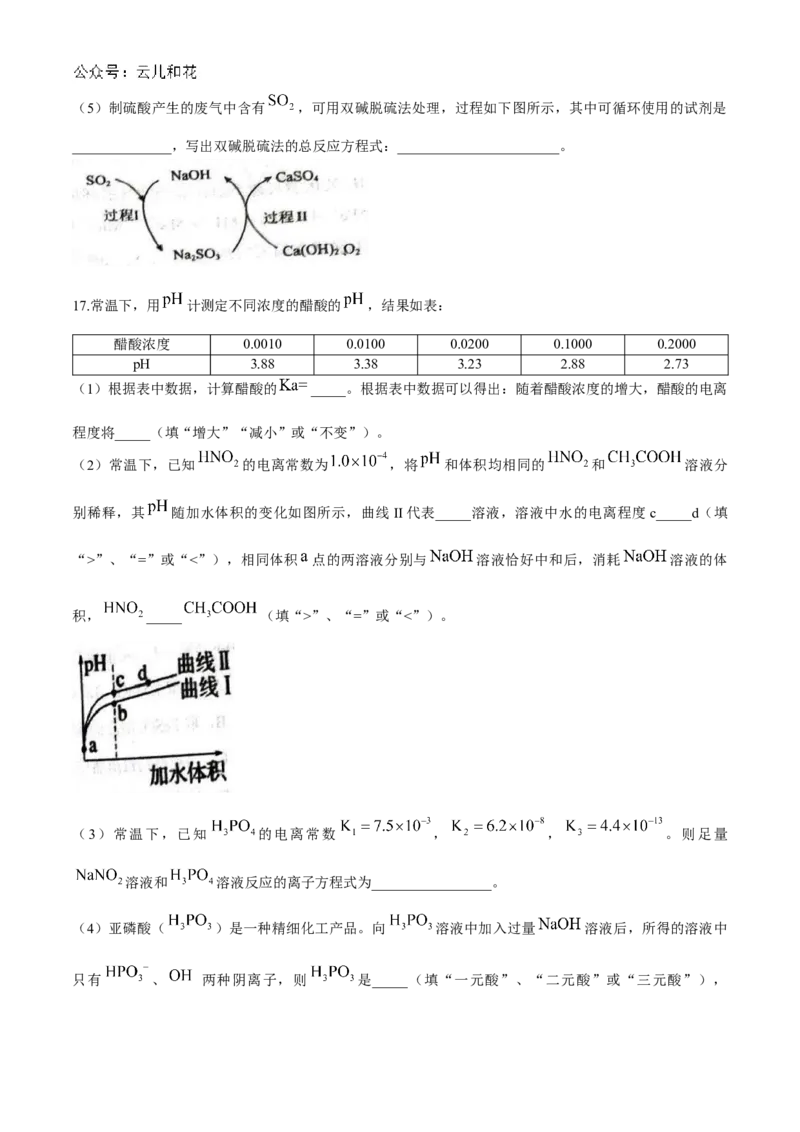
15.以酚酞为指示剂,用 的 溶液滴定 未知浓度的二元酸 溶液。溶液
中, 、分布系数 随滴加 溶液体积 的变化关系如图所示。[比如 的分布系数:
下列叙述正确的是A.曲线①代表 ,曲线②代表
B. 的电离方程式为: 、
C. 溶液的浓度为
D. 的电离常数
第II卷非选择题(共60分)
三、非选择题:本题共5小题,共60分
16.工业上以硫黄为原料制备硫酸的原理示意图如下,其过程包括I、II、III三个阶段。
(1)硫液化后与空气中的氧气反应生成 。若进料温度超过硫的沸点,部分燃烧的硫以蒸汽的形式随
进入到下一阶段,会导致_____(填序号)。
A.硫的消耗量增加 B. 产率下降 C.生成较多
(2)反应Ⅱ中钒催化剂能加快反应速率的原因为_______________________。
(3)在硫酸工业中,常采用“二转二吸法”,即将第一次转化生成的 分离后,将未转化的 进行
二次转化,假若两次 的转化率均为 ,则最终 的转化率为_____。
(4)气体经过钒催化剂层,温度会升高,其原因是________________。升高温度后的气体都需要降温后
再经过钒催化剂层转化,其目的是_____________________________________。(5)制硫酸产生的废气中含有 ,可用双碱脱硫法处理,过程如下图所示,其中可循环使用的试剂是
______________,写出双碱脱硫法的总反应方程式:_______________________。
17.常温下,用 计测定不同浓度的醋酸的 ,结果如表:
醋酸浓度 0.0010 0.0100 0.0200 0.1000 0.2000
pH 3.88 3.38 3.23 2.88 2.73
(1)根据表中数据,计算醋酸的 _____。根据表中数据可以得出:随着醋酸浓度的增大,醋酸的电离
程度将_____(填“增大”“减小”或“不变”)。
(2)常温下,已知 的电离常数为 ,将 和体积均相同的 和 溶液分
别稀释,其 随加水体积的变化如图所示,曲线 II代表_____溶液,溶液中水的电离程度c_____d(填
“>”、“=”或“<”),相同体积 点的两溶液分别与 溶液恰好中和后,消耗 溶液的体
积, _____ (填“>”、“=”或“<”)。
(3)常温下,已知 的电离常数 , , 。则足量
溶液和 溶液反应的离子方程式为_________________。
(4)亚磷酸( )是一种精细化工产品。向 溶液中加入过量 溶液后,所得的溶液中
只有 、 两种阴离子,则 是_____(填“一元酸”、“二元酸”或“三元酸”),电离的方程式为____________________________。
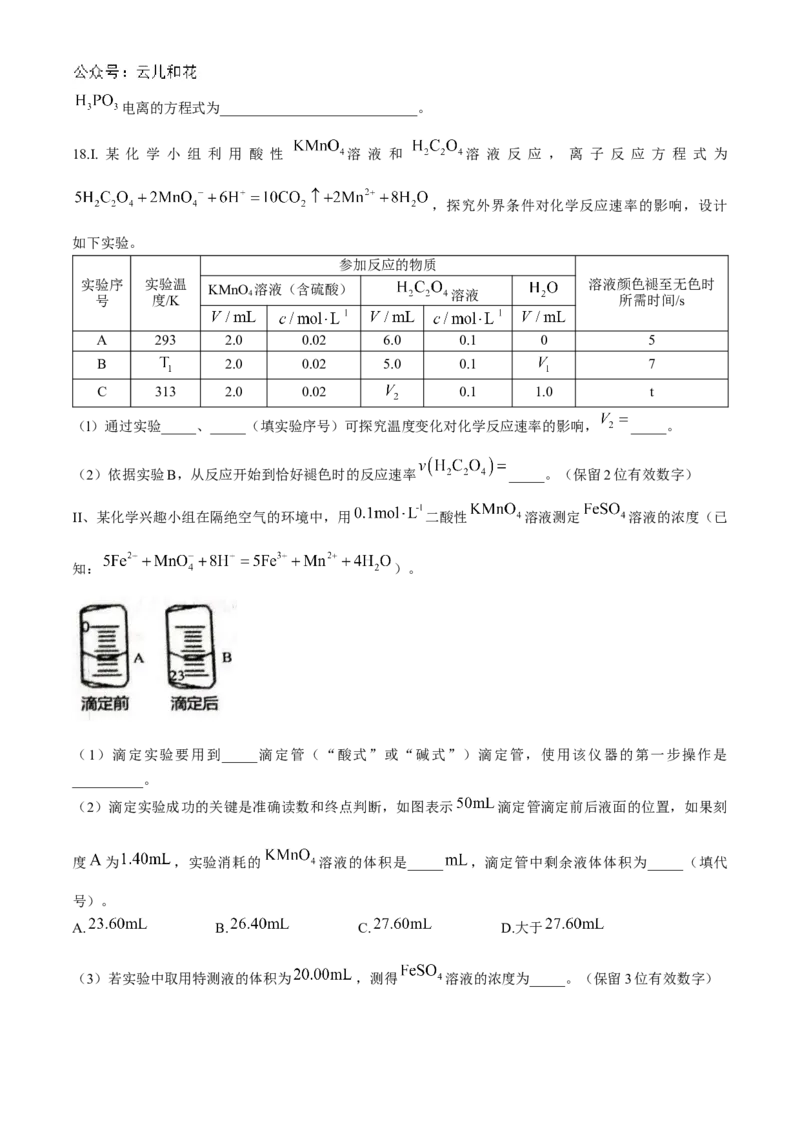
18.I. 某 化 学 小 组 利 用 酸 性 溶 液 和 溶 液 反 应 , 离 子 反 应 方 程 式 为
,探究外界条件对化学反应速率的影响,设计
如下实验。
参加反应的物质
实验序 实验温 溶液颜色褪至无色时
KMnO 溶液(含硫酸)
号 度/K 4 溶液 所需时间/s
A 293 2.0 0.02 6.0 0.1 0 5
B 2.0 0.02 5.0 0.1 7
C 313 2.0 0.02 0.1 1.0 t
(l)通过实验_____、_____(填实验序号)可探究温度变化对化学反应速率的影响, _____。
(2)依据实验B,从反应开始到恰好褪色时的反应速率 _____。(保留2位有效数字)
II、某化学兴趣小组在隔绝空气的环境中,用 二酸性 溶液测定 溶液的浓度(已
知: )。
(1)滴定实验要用到_____滴定管(“酸式”或“碱式”)滴定管,使用该仪器的第一步操作是
__________。
(2)滴定实验成功的关键是准确读数和终点判断,如图表示 滴定管滴定前后液面的位置,如果刻
度 为 ,实验消耗的 溶液的体积是_____ ,滴定管中剩余液体体积为_____(填代
号)。
A. B. C. D.大于
(3)若实验中取用特测液的体积为 ,测得 溶液的浓度为_____。(保留3位有效数字)(4)下列操作中,可能使 溶液的浓度偏低的是___________(填字母,下同)。
A.读取 溶液体积时,开始时俯视读数,滴定结束时仰视读数
B、取 溶液的滴定管,取液前滴定管尖嘴处无气泡,取液后尖嘴处出现气泡
C.当观察到锥形瓶中溶液颜色发生变化时,立即停止滴定并记下滴定管液面读数
D.滴定前向锥形瓶内加了少量蒸馏水
19.一定条件下,水煤气变换反应 的中间产物
是 。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
I. (快) II. (慢)
研究发现,在反应 、 中, 仅对反应 有催化加速作用;反应 速率远大于反应 ,近似认为反应
建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)反应 的活化能_____反应 的活化能(填“大于”、“小于”或“等于”)。
(2)反应 正反应速率方程为: , 为反应速率常数。 温度下, 电
离平衡常数为 ,当 平衡浓度为 时, 浓度为_____ ,此时反应I的反应
速率 _____ (用含 、 和 的代数式表示)。
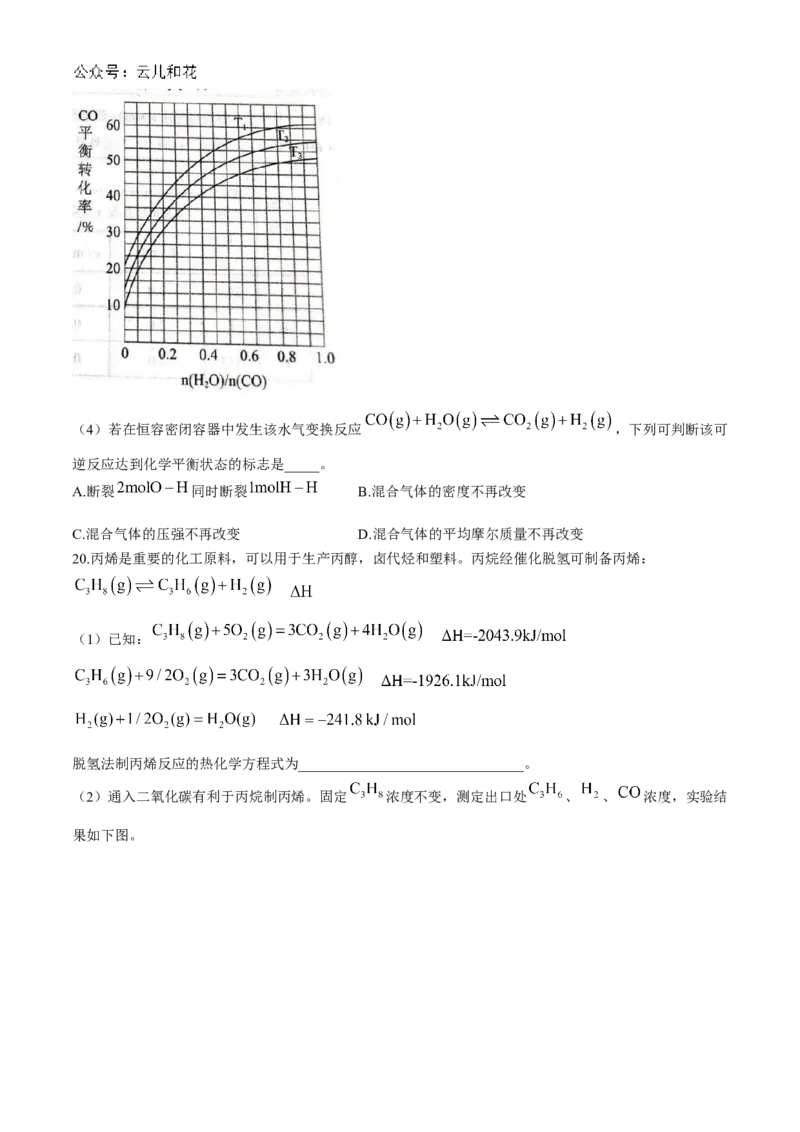
( 3 ) 对 于 水 气 变 换 反 应 ,
与 平衡转化率、温度的变化关系如下图所示,则图中温度由小到大的顺序是:
___________,判断依据是________________。(4)若在恒容密闭容器中发生该水气变换反应 ,下列可判断该可
逆反应达到化学平衡状态的标志是_____。
A.断裂 同时断裂 B.混合气体的密度不再改变
C.混合气体的压强不再改变 D.混合气体的平均摩尔质量不再改变
20.丙烯是重要的化工原料,可以用于生产丙醇,卤代烃和塑料。丙烷经催化脱氢可制备丙烯:
(1)已知:
脱氢法制丙烯反应的热化学方程式为________________________________。
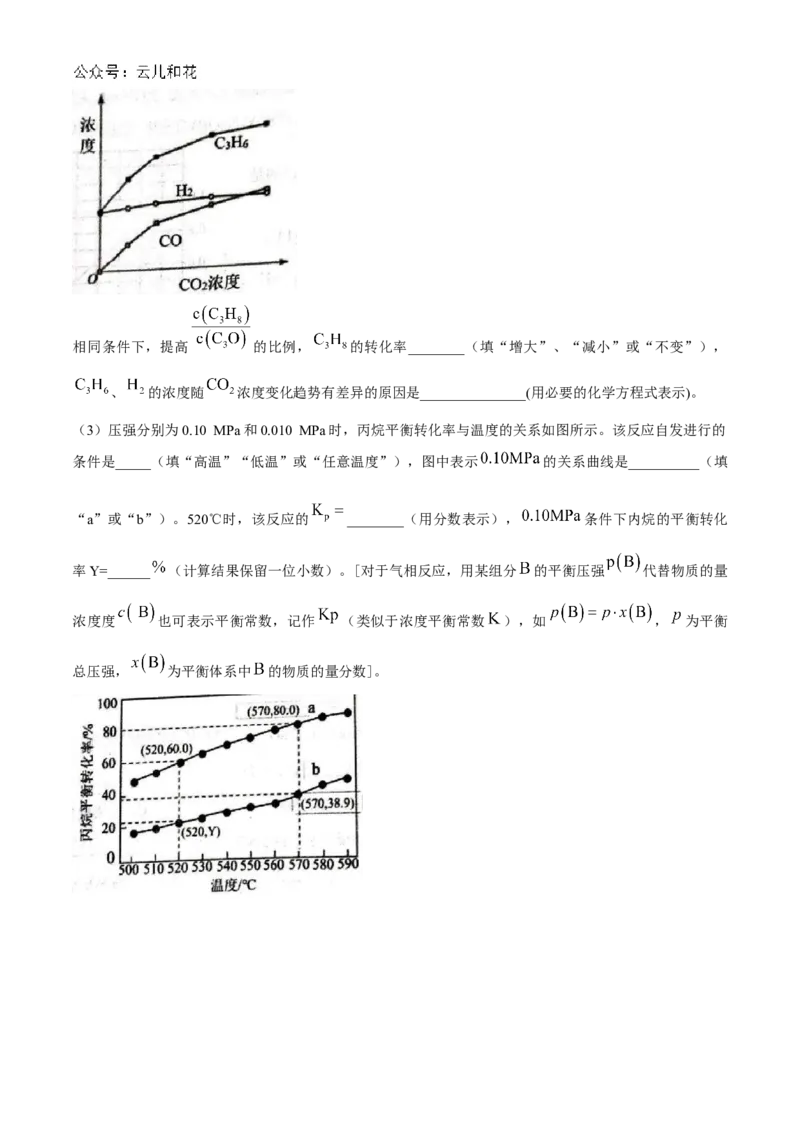
(2)通入二氧化碳有利于丙烷制丙烯。固定 浓度不变,测定出口处 、 、 浓度,实验结
果如下图。相同条件下,提高 的比例, 的转化率________(填“增大”、“减小”或“不变”),
、 的浓度随 浓度变化趋势有差异的原因是_______________(用必要的化学方程式表示)。
(3)压强分别为0.10 MPa和0.010 MPa时,丙烷平衡转化率与温度的关系如图所示。该反应自发进行的
条件是_____(填“高温”“低温”或“任意温度”),图中表示 的关系曲线是__________(填
“a”或“b”)。520℃时,该反应的 ________(用分数表示), 条件下内烷的平衡转化
率Y=______ (计算结果保留一位小数)。[对于气相反应,用某组分 的平衡压强 代替物质的量
浓度度 也可表示平衡常数,记作 (类似于浓度平衡常数 ),如 , 为平衡
总压强, 为平衡体系中 的物质的量分数]。2024~2025 学年度第一学期期中教学质量检测
高二化学答案
2024.1
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1-5 CABAB 6-10 DDDCA
二、选择题:本题共5小题,每小题4分,共20分口每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得。分。
11、AC 12、B 13、C 14、AB 15、CD
三、非选择题:本题共5小题,共60分
16.(10分)
(1)AB(2分)
(2)降低反应活化能(1分)
(3) (1分)
(4)反应放热(1分) 保持钒催化剂活性温度,保证反应速率,提高 转化率(2分)
(5) (1分)、 (2分)
17.(12分)
(1) (2分)减小(1分)
(2) (1分) (2分) (2分)
(3) (2分)
(4)一元酸(1分) (1分;“=”不扣分)
18(14分)
1.(1)BC(1分)5.0(1分)(2)0.0018 mol/(L·s)(2分)
II.(1)酸式(1分)检查滴定管是否漏水(1分)
(2) (2分) (2分)
(3) (2分)(4)C(2分)
19.(12分)
(1)小于(2分)
(2). (2分) (2分)(3)Ti