文档内容
大同市 2025 届高三年级第一次学情调研测试
化学
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡上相应的位置。
2.全部答案在答题卡上完成,答在本试题上无效。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用0.5mm黑色笔
迹签字笔写在答题卡上。
4.考试结束后,将本试题和答题卡一并交回。
5.本试卷共8页,满分100分,考试时间75分钟。
可能用到的相对原子质量:
一、选择题(本题共15个小题,每小题3分,共45分。每小题只有一个选项符合题目要
求。)
1.化学与生产、生活息息相关,下列叙述错误的是( )。
A.食盐可作调味剂,也可作食品防腐剂
B.日用铝制品表面覆盖的氧化膜,对内部金属起保护作用
C.二氧化硫是一种有毒气体,不能用作食品添加剂
D.化学品可以分为大宗化学品和精细化学品两大类
2.下列相关微粒的说法正确的是( )。
A.羟基的电子式: B.中子数为20的氯原子:
C. 的结构示意图: D. 的VSEPR模型为四面体型
3.布洛芬、对乙酰氨基酚为家中常备镇痛解热药物,下列说法正确的是( )。
布洛芬 对乙酰氨基酚
A.可以通过红外光谱来区分布洛芬和对乙酰氨基酚
B.对乙酰氨基酚分子的核磁共振氢谱图中最大质荷比为151
C.布洛芬和苯乙酸乙酯( )互为同系物
D.布洛芬分子中所有碳原子可能共面
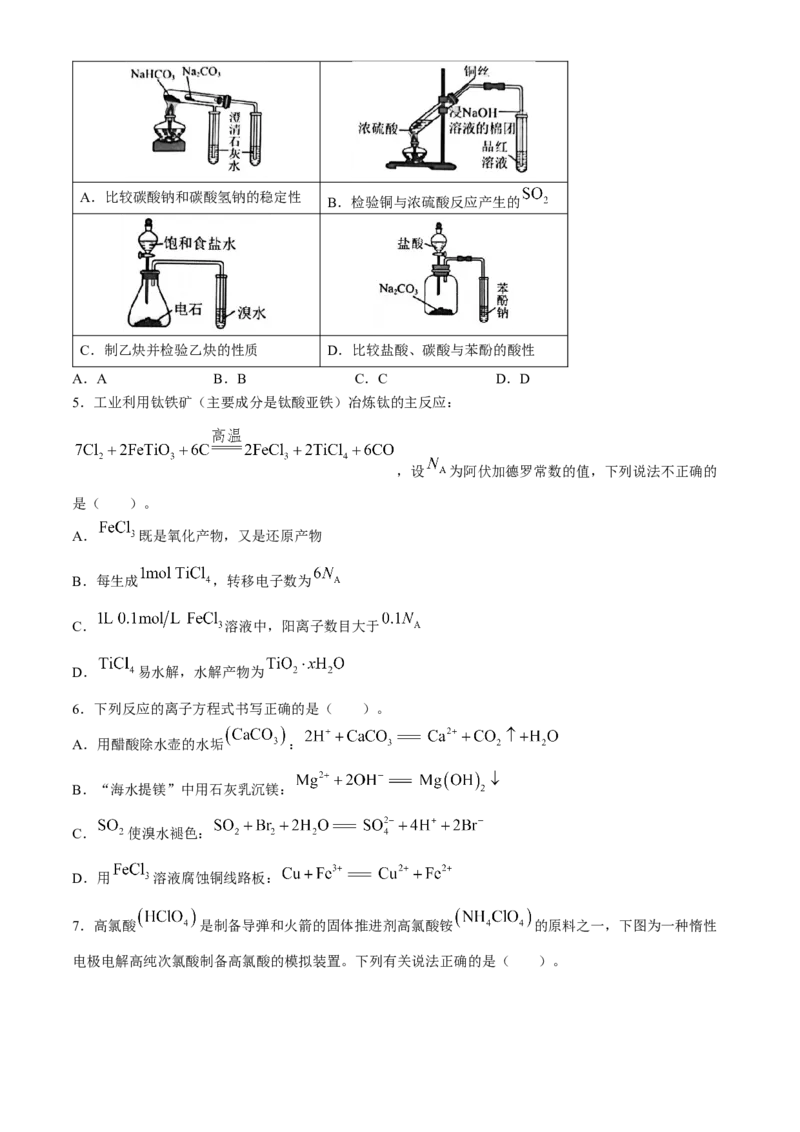
4.下列选用的仪器(部分夹持装置已略去)和药品能达到实验目的的是( )。
学科网(北京)股份有限公司A.比较碳酸钠和碳酸氢钠的稳定性
B.检验铜与浓硫酸反应产生的
C.制乙炔并检验乙炔的性质 D.比较盐酸、碳酸与苯酚的酸性
A.A B.B C.C D.D
5.工业利用钛铁矿(主要成分是钛酸亚铁)冶炼钛的主反应:
,设 为阿伏加德罗常数的值,下列说法不正确的
是( )。
A. 既是氧化产物,又是还原产物
B.每生成 ,转移电子数为
C. 溶液中,阳离子数目大于
D. 易水解,水解产物为
6.下列反应的离子方程式书写正确的是( )。
A.用醋酸除水壶的水垢 :
B.“海水提镁”中用石灰乳沉镁:
C. 使溴水褪色:
D.用 溶液腐蚀铜线路板:
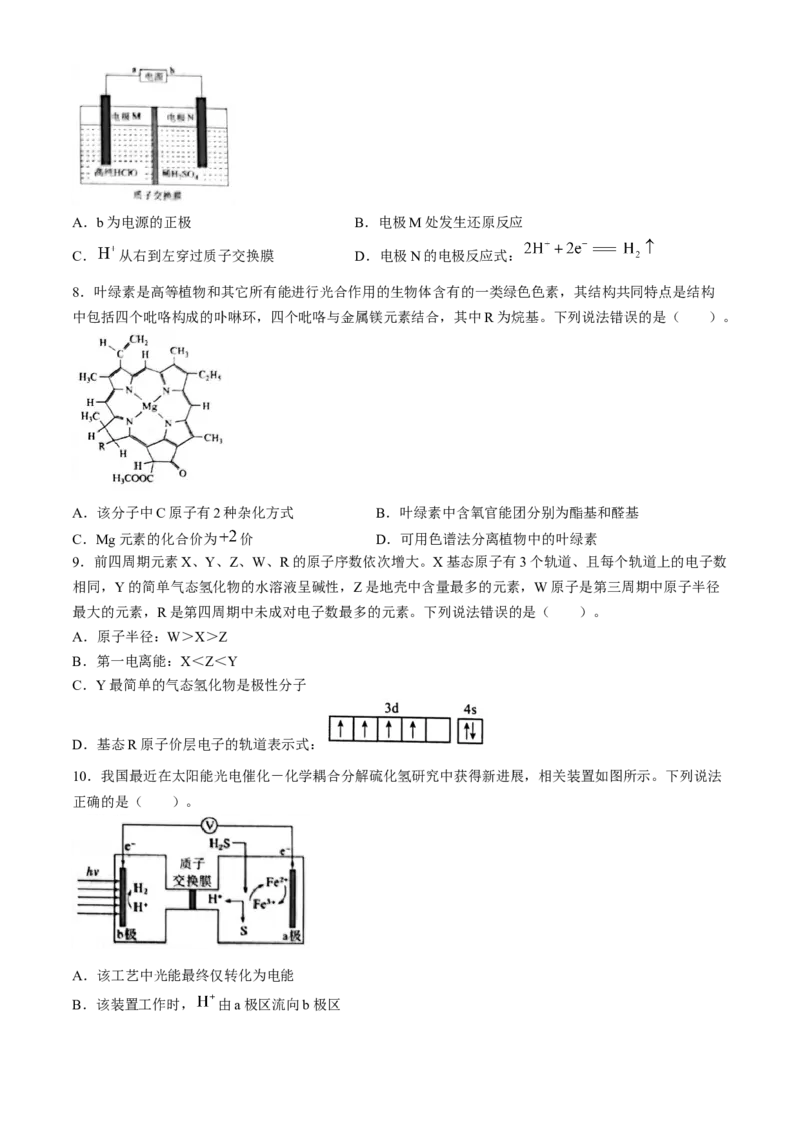
7.高氯酸 是制备导弹和火箭的固体推进剂高氯酸铵 的原料之一,下图为一种惰性
电极电解高纯次氯酸制备高氯酸的模拟装置。下列有关说法正确的是( )。
学科网(北京)股份有限公司A.b为电源的正极 B.电极M处发生还原反应
C. 从右到左穿过质子交换膜 D.电极N的电极反应式:
8.叶绿素是高等植物和其它所有能进行光合作用的生物体含有的一类绿色色素,其结构共同特点是结构
中包括四个吡咯构成的卟啉环,四个吡咯与金属镁元素结合,其中R为烷基。下列说法错误的是( )。
A.该分子中C原子有2种杂化方式 B.叶绿素中含氧官能团分别为酯基和醛基
C.Mg元素的化合价为 价 D.可用色谱法分离植物中的叶绿素
9.前四周期元素X、Y、Z、W、R的原子序数依次增大。X基态原子有3个轨道、且每个轨道上的电子数
相同,Y的简单气态氢化物的水溶液呈碱性,Z是地壳中含量最多的元素,W原子是第三周期中原子半径
最大的元素,R是第四周期中未成对电子数最多的元素。下列说法错误的是( )。
A.原子半径:W>X>Z
B.第一电离能:X<Z<Y
C.Y最简单的气态氢化物是极性分子
D.基态R原子价层电子的轨道表示式:
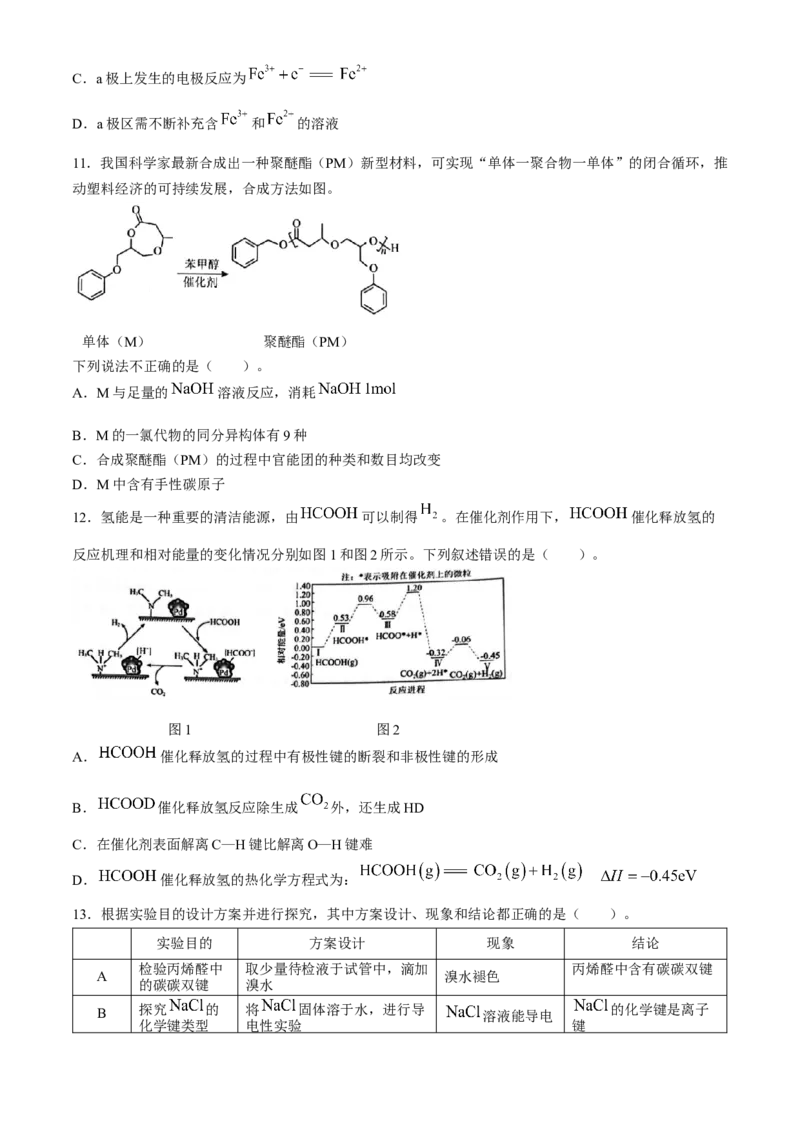
10.我国最近在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法
正确的是( )。
A.该工艺中光能最终仅转化为电能
B.该装置工作时, 由a极区流向b极区
学科网(北京)股份有限公司C.a极上发生的电极反应为
D.a极区需不断补充含 和 的溶液
11.我国科学家最新合成出一种聚醚酯(PM)新型材料,可实现“单体一聚合物一单体”的闭合循环,推
动塑料经济的可持续发展,合成方法如图。
单体(M) 聚醚酯(PM)
下列说法不正确的是( )。
A.M与足量的 溶液反应,消耗
B.M的一氯代物的同分异构体有9种
C.合成聚醚酯(PM)的过程中官能团的种类和数目均改变
D.M中含有手性碳原子
12.氢能是一种重要的清洁能源,由 可以制得 。在催化剂作用下, 催化释放氢的
反应机理和相对能量的变化情况分别如图1和图2所示。下列叙述错误的是( )。
图1 图2
A. 催化释放氢的过程中有极性键的断裂和非极性键的形成
B. 催化释放氢反应除生成 外,还生成HD
C.在催化剂表面解离C—H键比解离O—H键难
D. 催化释放氢的热化学方程式为:
13.根据实验目的设计方案并进行探究,其中方案设计、现象和结论都正确的是( )。
实验目的 方案设计 现象 结论
检验丙烯醛中 取少量待检液于试管中,滴加 丙烯醛中含有碳碳双键
A 溴水褪色
的碳碳双键 溴水
探究 的 将 固体溶于水,进行导 的化学键是离子
B 溶液能导电
化学键类型 电性实验 键
学科网(北京)股份有限公司先产生白色沉淀, 相同温度下,
向
然后沉淀变黑
溶液中加入
C
比较 大小
溶
液,再滴加 溶液
探究脱氧剂 取少量样品溶于盐酸,滴加
(主要成分是
溶液
D 无明显现象 脱氧剂没有变质
Fe粉)是否变
质
A.A B.B C.C D.D
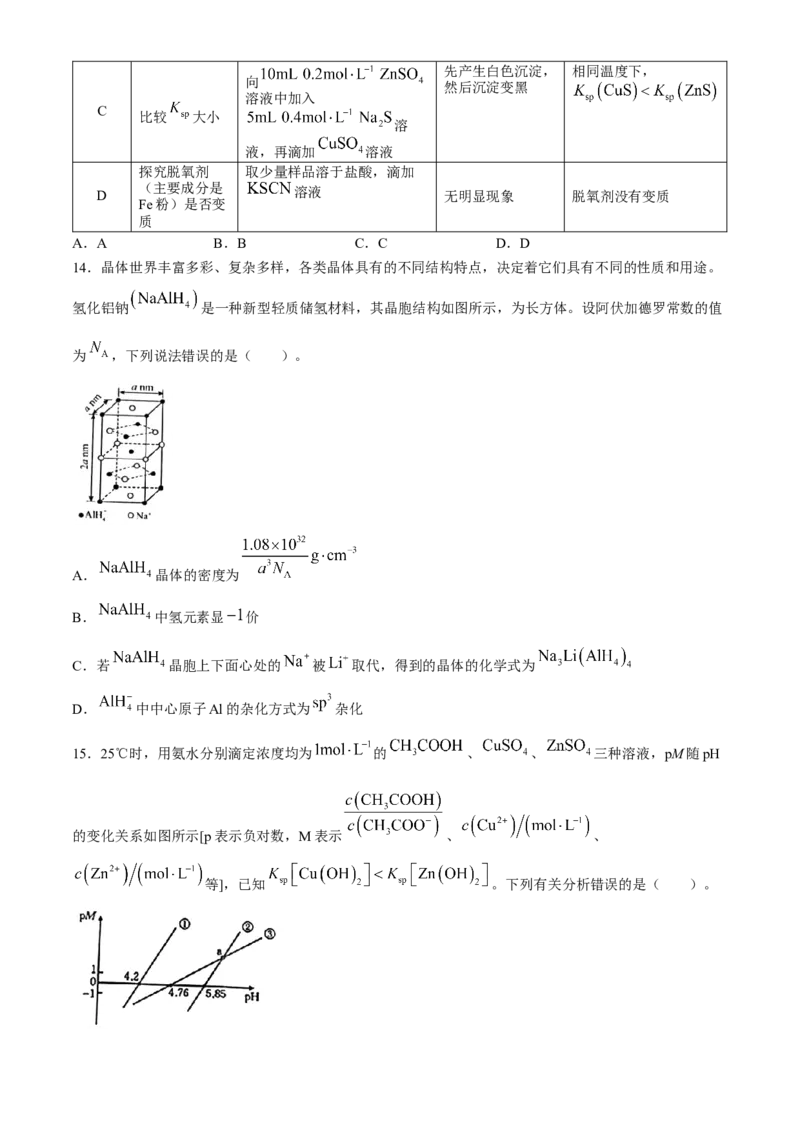
14.晶体世界丰富多彩、复杂多样,各类晶体具有的不同结构特点,决定着它们具有不同的性质和用途。
氢化铝钠 是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。设阿伏加德罗常数的值
为 ,下列说法错误的是( )。
A. 晶体的密度为
B. 中氢元素显 价
C.若 晶胞上下面心处的 被 取代,得到的晶体的化学式为
D. 中中心原子Al的杂化方式为 杂化
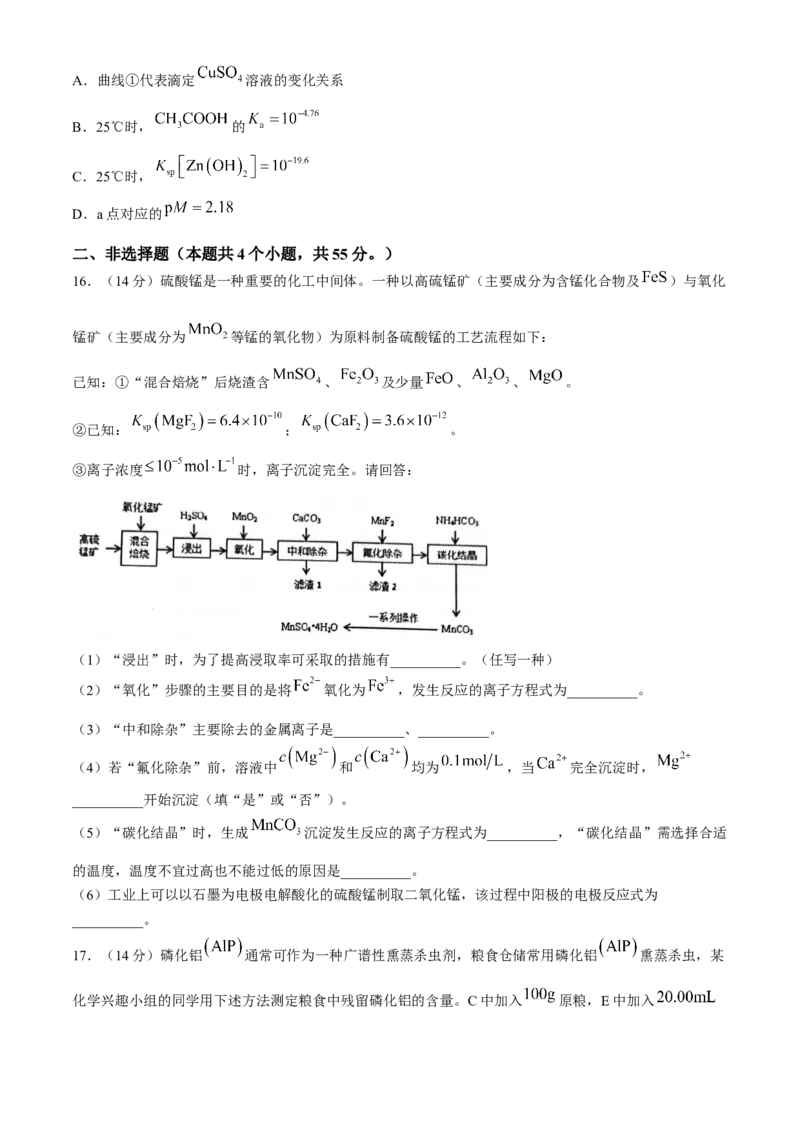
15.25℃时,用氨水分别滴定浓度均为 的 、 、 三种溶液,pM随pH
的变化关系如图所示[p表示负对数,M表示 、 、
等],已知 。下列有关分析错误的是( )。
学科网(北京)股份有限公司A.曲线①代表滴定 溶液的变化关系
B.25℃时, 的
C.25℃时,
D.a点对应的
二、非选择题(本题共4个小题,共55分。)
16.(14分)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰化合物及 )与氧化
锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程如下:
已知:①“混合焙烧”后烧渣含 、 及少量 、 、 。
②已知: ; 。
③离子浓度 时,离子沉淀完全。请回答:
(1)“浸出”时,为了提高浸取率可采取的措施有__________。(任写一种)
(2)“氧化”步骤的主要目的是将 氧化为 ,发生反应的离子方程式为__________。
(3)“中和除杂”主要除去的金属离子是__________、__________。
(4)若“氟化除杂”前,溶液中 和 均为 ,当 完全沉淀时,
__________开始沉淀(填“是”或“否”)。
(5)“碳化结晶”时,生成 沉淀发生反应的离子方程式为__________,“碳化结晶”需选择合适
的温度,温度不宜过高也不能过低的原因是__________。
(6)工业上可以以石墨为电极电解酸化的硫酸锰制取二氧化锰,该过程中阳极的电极反应式为
__________。
17.(14分)磷化铝 通常可作为一种广谱性熏蒸杀虫剂,粮食仓储常用磷化铝 熏蒸杀虫,某
化学兴趣小组的同学用下述方法测定粮食中残留磷化铝的含量。C中加入 原粮,E中加入
学科网(北京)股份有限公司一定浓度的 溶液( 酸化)。往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E
中过量的 溶液。
已知:① 吸水后会立即产生高毒性 气体(沸点 ℃,还原性强)。
②焦性没食子酸的碱性溶液具有还原性。
回答下列问题:
(1)仪器D中冷凝水从__________通入(填“a”或“b”)。
(2) 与水反应的化学方程式为__________。
(3)装置A中盛装 溶液的作用是除去空气中的还原性气体,装置B中盛有焦性没食子酸的碱性
溶液,其作用是__________。
(4)C中反应完全后继续通入空气的作用是 。
(5)装置E中 被氧化成磷酸, 的锰元素被还原为 ,则装置E中发生反应的还原剂和
氧化剂的物质的量之比为__________。
(6)收集装置E中的吸收液,加水稀释后用 标准溶液滴定剩余的 溶液,发生反应的离
子方程式为__________,若滴定过程中不慎将锥形瓶中部分液体外溅,则会导致测定出粮食中磷化铝的残
留量__________(填“偏高”或“偏低”)。
18.(13分)甲烷干重整(DRM)以温室气体 和 为原料在催化条件下生成合成气CO和 。
发生的反应有:
ⅰ.
ⅱ.
ⅲ.
ⅳ.
学科网(北京)股份有限公司(1) __________ ;__________(填“高温”或“低温”)有利于反应ⅳ自发进行。
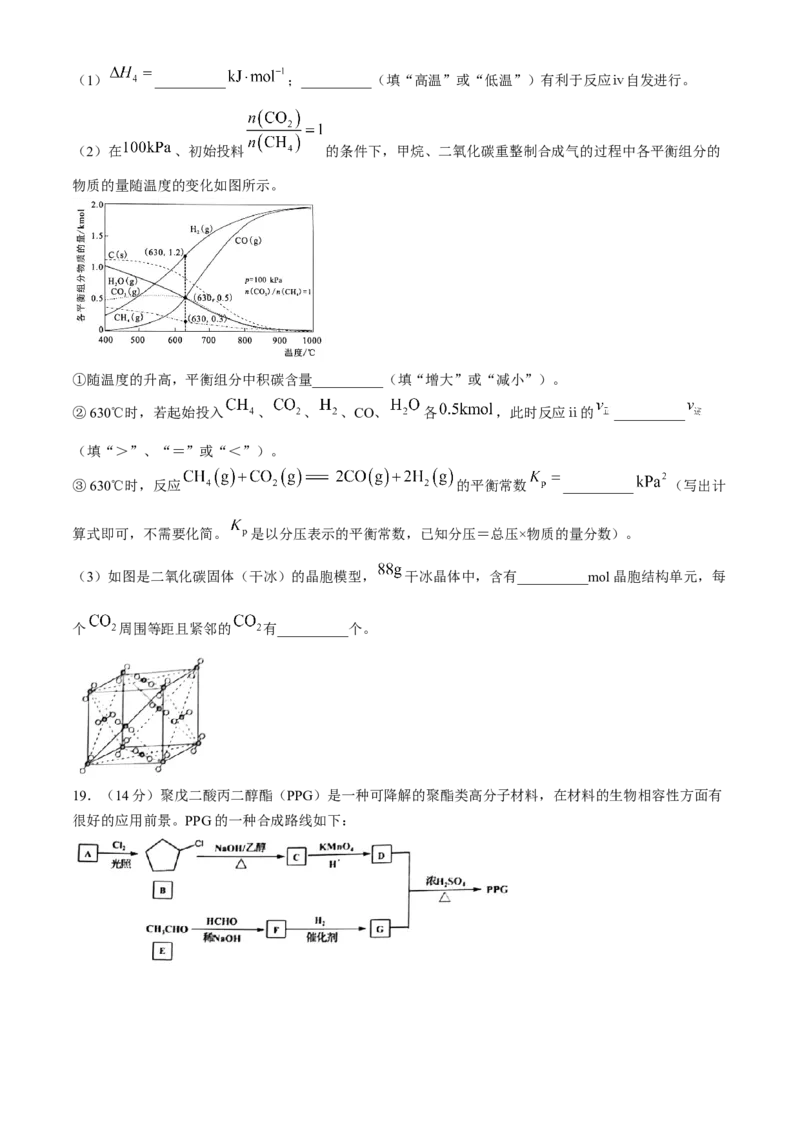
(2)在 、初始投料 的条件下,甲烷、二氧化碳重整制合成气的过程中各平衡组分的
物质的量随温度的变化如图所示。
①随温度的升高,平衡组分中积碳含量__________(填“增大”或“减小”)。
②630℃时,若起始投入 、 、 、CO、 各 ,此时反应ⅱ的 __________
(填“>”、“=”或“<”)。
③630℃时,反应 的平衡常数 __________ (写出计
算式即可,不需要化简。 是以分压表示的平衡常数,已知分压=总压×物质的量分数)。
(3)如图是二氧化碳固体(干冰)的晶胞模型, 干冰晶体中,含有__________mol晶胞结构单元,每
个 周围等距且紧邻的 有__________个。
19.(14分)聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有
很好的应用前景。PPG的一种合成路线如下:
学科网(北京)股份有限公司已知:
回答下列问题:
(1)由A生成B的化学方程式为__________。
(2)C的化学名称为__________。
(3)由B生成C的反应类型为__________。
(4)F的结构简式为__________。
(5)由D和G生成PPG的化学方程式为__________。
(6)写出能同时满足下列条件的D的同分异构体的结构简式__________。
①能与饱和 溶液反应产生气体
②既能发生银镜反应,又能发生水解反应
③核磁共振氢谱显示为3组峰,且峰面积比为
(7)若PPG平均相对分子质量为10000,则其平均聚合度约为__________(填标号)。
a.48 b.58 c.75 d.102
学科网(北京)股份有限公司