文档内容
D.每消耗1molO ,转移电子的数目约为4×6.02×1023
石嘴山市第一中学2024-2025学年高二年级9月月考 2
4.已知汽车尾气处理反应之一为: 。该反应的 、 。则上述
化学试题
反应在下列什么条件下易自发进行
A.高温 B.低温 C.任何温度下均不能D.任意温度下均能
一、单选题
5.下列关于反应能量的说法正确的是
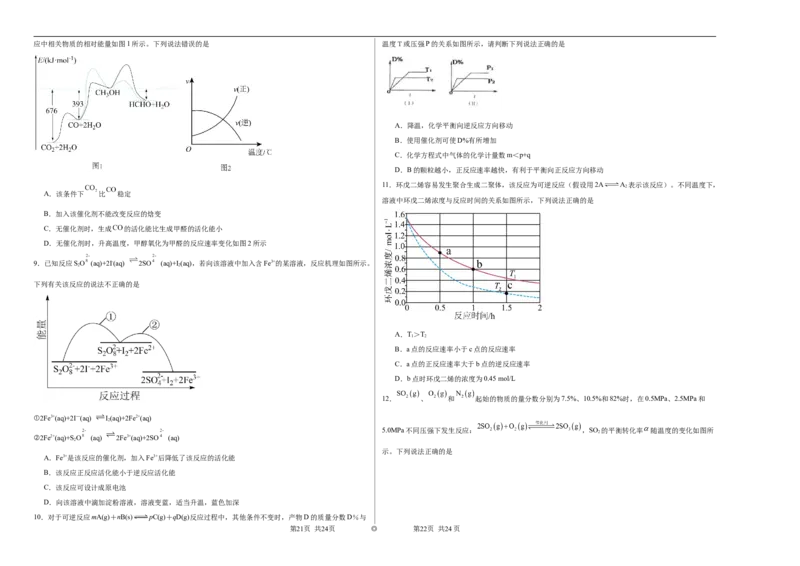
1.工业上,合成氨反应N 2 + 3H 2 2NH 3 的微观历程如图所示。用 、 、 A.已知C(石墨,s)=C(金刚石,s);△H>0 ,则金刚石比石墨稳定
B.相同条件下,如果1mol氢原子所具有的能量为E,1mol氢分子所具有的能量为E,则2E>E
1 2 1 2
C.101kPa时,2H(g)+O(g)=2HO(l);△H=-571.6kJ·mol-1,H 的燃烧热为571.6kJ·mol-1
2 2 2 2
分别表示N 2 、H 2 、NH 3 ,下列说法不正确的是 D.H+(aq)+OH-(aq)=H 2 O(l);△H=-57.3 kJ·mol-1,含1molNaOH的氢氧化钠溶液与含0.5molH 2 SO 4 的
浓硫酸混合后放出57.3kJ的热量
6.一定温度下,在某密闭容器中发生反应: ,若15s内 由0.1
降到0.07 ,则下列说法正确的是
A.减小反应体系的体积,化学反应速率不变
B.升高温度正反应速率增大,逆反应速率减小
C.0~15s内用I 表示的平均反应速率为v(I)=0.001mol·L-1·s-1
2 2
D. 由0.07 降到0.05 所需的反应时间小于10s
A.①→② 催化剂在吸附N、H 时,未形成新的化学键 7.白磷与氧可发生如下反应:P+5O =P O 。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—
2 2 4 2 4 10
B.②→③ 形成N原子和H原子是放热过程 1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
C.③→④形成了新的化学键
D.使用合适的催化剂,能提高合成氨反应的速率
2.下列有关工业生产的叙述正确的是
A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好
B.硫酸工业中,使用催化剂是为了提高SO 转化为SO 的转化率
2 3
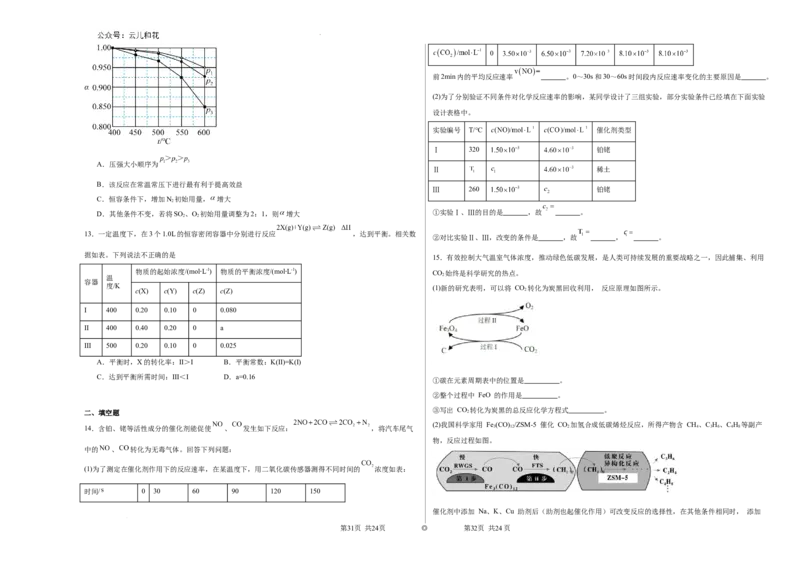
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
C.合成氨工业中,将NH 及时液化分离有利于氨的生产
3
A.(6a+5d-4c-12b)kJ·mol—1
D.硫酸工业中,SO 的催化氧化不采用高压,是因为压强对SO 转化率无影响
2 2
B.(4c+12b-6a-5d)kJ·mol—1
3.对于反应2NO(g)+O(g) 2NO (g) ΔH=-114.2kJ·mol-1,下列说法正确的是
2 2
C.(4c+12b-4a-5d)kJ·mol—1
A.该反应的ΔS>0 ⇌
D.(4a+5d-4c-12b)kJ·mol—1
B.使用高效催化剂能提高NO的平衡转化率
8.甲醇通过催化氧化制取甲醛时,在无催化剂(图中实线)和加入特定催化剂(图中虚线)时均会产生甲醛,反
C.增大压强,化学平衡正向移动,平衡常数K增大
第11页 共24页 ◎ 第12页 共24页
学科网(北京)股份有限公司应中相关物质的相对能量如图1所示。下列说法错误的是 温度T或压强P的关系如图所示,请判断下列说法正确的是
A.降温,化学平衡向逆反应方向移动
B.使用催化剂可使D%有所增加
C.化学方程式中气体的化学计量数m<p+q
D.B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动
11.环戊二烯容易发生聚合生成二聚体,该反应为可逆反应(假设用2A A 表示该反应)。不同温度下,
2
A.该条件下 比 稳定
溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是
B.加入该催化剂不能改变反应的焓变
C.无催化剂时,生成 的活化能比生成甲醛的活化能小
D.无催化剂时,升高温度,甲醇氧化为甲醛的反应速率变化如图2所示
9.已知反应SO (aq)+2I-(aq) 2SO (aq)+I (aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。
2 2
下列有关该反应的说法不正确的是
A.T>T
1 2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时环戊二烯的浓度为0.45 mol/L
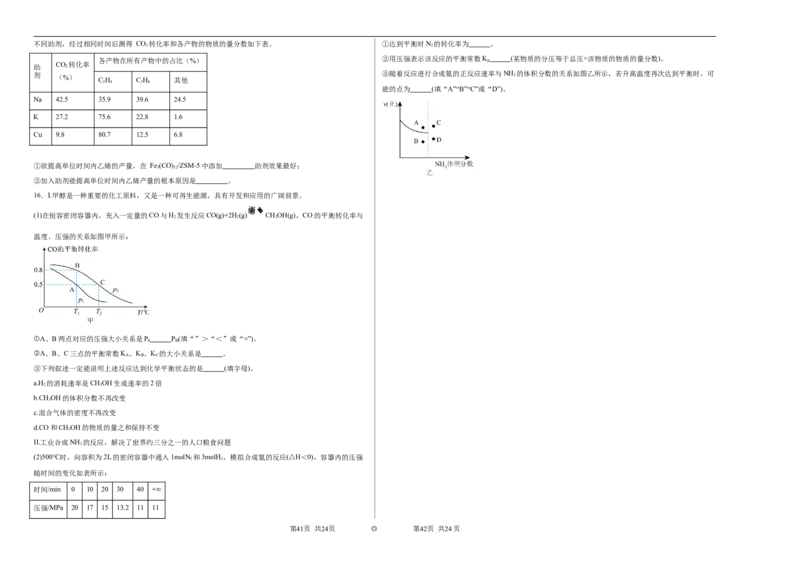
12. 、 和 起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和
①2Fe3+(aq)+2I—(aq) I(aq)+2Fe2+(aq)
2
5.0MPa不同压强下发生反应: ,SO 的平衡转化率 随温度的变化如图所
2
②2Fe2+(aq)+S O (aq) 2Fe3+(aq)+2SO (aq)
2
示。下列说法正确的是
A.Fe3+是该反应的催化剂,加入Fe3+后降低了该反应的活化能
B.该反应正反应活化能小于逆反应活化能
C.该反应可设计成原电池
D.向该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深
10.对于可逆反应mA(g)+nB(s) pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与
第21页 共24页 ◎ 第22页 共24页0
前2min内的平均反应速率 。0~30s和30~60s时间段内反应速率变化的主要原因是 。
(2)为了分别验证不同条件对化学反应速率的影响,某同学设计了三组实验,部分实验条件已经填在下面实验
设计表格中。
实验编号 T/℃ 催化剂类型
Ⅰ 320 铂铑
A.压强大小顺序为
Ⅱ 稀土
B.该反应在常温常压下进行最有利于提高效益
Ⅲ 260 铂铑
C.恒容条件下,增加N 初始用量, 增大
2
D.其他条件不变,若将SO 、O 初始用量调整为2:1,则 增大 ①实验Ⅰ、Ⅲ的目的是 ,故 。
2 2
13.一定温度下,在3个1.0L的恒容密闭容器中分别进行反应 ,达到平衡。相关数
②对比实验Ⅱ、Ⅲ,改变的条件是 ,故 , 。
据如表。下列说法不正确的是
15.有效控制大气温室气体浓度,推动绿色低碳发展,是人类可持续发展的重要战略之一,因此捕集、利用
物质的起始浓度/(molL-1) 物质的平衡浓度/(molL-1)
CO 始终是科学研究的热点。
温 2
容器
度/K ∙ ∙ (1)新的研究表明,可以将 CO 转化为炭黑回收利用, 反应原理如图所示。
c(X) c(Y) c(Z) c(Z) 2
I 400 0.20 0.10 0 0.080
II 400 0.40 0.20 0 a
III 500 0.20 0.10 0 0.025
A.平衡时,X的转化率:II>I B.平衡常数:K(Ⅱ)=K(Ⅰ)
C.达到平衡所需时间:III<I D.a=0.16
①碳在元素周期表中的位置是 。
②整个过程中 FeO 的作用是 。
③写出 CO 转化为炭黑的总反应化学方程式 。
二、填空题 2
(2)我国科学家用 Fe (CO) /ZSM-5 催化 CO 加氢合成低碳烯烃反应,所得产物含 CH、C H、C H 等副产
14.含铂、铑等活性成分的催化剂能促使 、 发生如下反应: ,将汽车尾气 3 12 2 4 3 6 4 8
物,反应过程如图。
中的 、 转化为无毒气体。回答下列问题:
(1)为了测定在催化剂作用下的反应速率,在某温度下,用二氧化碳传感器测得不同时间的 浓度如表:
时间/ 0 30 60 90 120 150
催化剂中添加 Na、K、Cu 助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时, 添加
第31页 共24页 ◎ 第32页 共24页
学科网(北京)股份有限公司不同助剂,经过相同时间后测得 CO 转化率和各产物的物质的量分数如下表。 ①达到平衡时N 的转化率为 。
2 2
②用压强表示该反应的平衡常数K (某物质的分压等于总压×该物质的物质的量分数)。
各产物在所有产物中的占比(%) p
CO 转化率
助 2
剂 (%) ③随着反应进行合成氨的正反应速率与NH 3 的体积分数的关系如图乙所示,若升高温度再次达到平衡时,可
C H C H 其他
2 4 3 6
能的点为 (填“A”“B”“C”或“D”)。
Na 42.5 35.9 39.6 24.5
K 27.2 75.6 22.8 1.6
Cu 9.8 80.7 12.5 6.8
①欲提高单位时间内乙烯的产量,在 Fe (CO) /ZSM-5中添加 助剂效果最好;
3 12
②加入助剂能提高单位时间内乙烯产量的根本原因是 。
16.I.甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在恒容密闭容器内,充入一定量的CO与H 发生反应CO(g)+2H(g) CHOH(g),CO的平衡转化率与
2 2 3
温度、压强的关系如图甲所示:
①A、B两点对应的压强大小关系是P P (填“”>“<”或“=”)。
A B
②A、B、C三点的平衡常数K 、K 、K 的大小关系是 。
A B C
③下列叙述一定能说明上述反应达到化学平衡状态的是 (填字母)。
a.H 的消耗速率是CHOH生成速率的2倍
2 3
b.CH OH的体积分数不再改变
3
c.混合气体的密度不再改变
d.CO和CHOH的物质的量之和保持不变
3
II.工业合成NH 的反应,解决了世界约三分之一的人口粮食问题
3
(2)500℃时,向容积为2L的密闭容器中通入1molN 和3molH ,模拟合成氨的反应(△H<0),容器内的压强
2 2
随时间的变化如表所示:
时间/min 0 10 20 30 40 +∞
压强/MPa 20 17 15 13.2 11 11
第41页 共24页 ◎ 第42页 共24页