文档内容
高二上学期 12 月考试
化学试题
全卷满分 100 分,考试时间 75 分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 P 31 S 32 Cl
35.5 Fe 56 Cu 64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1. 我国提出“碳达峰”与“碳中和”目标,大力发展清洁能源。下列能源的利用过程,主要涉
及化学能转化为电能的是( )
A. 氢氧燃料电池供电 B. 水力发电 C. 太阳能热水器供热 D. 核能发电
2. 下列化学用语或图示表达正确的是( )
A.Cl原子结构示意图:
B. 电子云图为
C. 的电子式为
D.基态 原子的价层电子轨道表示式为
3. 常温下,下列各组离子在有关限定条件下的溶液中一定能大量共存的是( )
A.加入Al能放出 的溶液中:Cl-、SiO2-、SO 2-、NH +
3 4 4
B.含有 的溶液:
C. 的溶液中:
D.水电离出的 溶液中:
4. 用N 表示阿伏加德罗常数的值,下列叙述正确的是( )
A
A. 溶液中 数的目为N
AB.100g 质量分数为46%的乙醇溶液中含有氧原子数为N
A
C.标准状况下,11.2L CO 所含分子数目为0.5N
2 A
D. pH=2的盐酸中,氢离子数目为0.01N
A
5. 下列关于热化学方程式的表述正确的是( )
A. 已知C(石墨,s)=C(金刚石,s) ,则石墨比金刚石稳定
B. 已知强酸与强碱反应的中和热为 ,则反应
的
C. 已知 ,则氢气的燃烧热为241.8
D. 已知CO(g)的燃烧热是283.0 ,则 的反应热
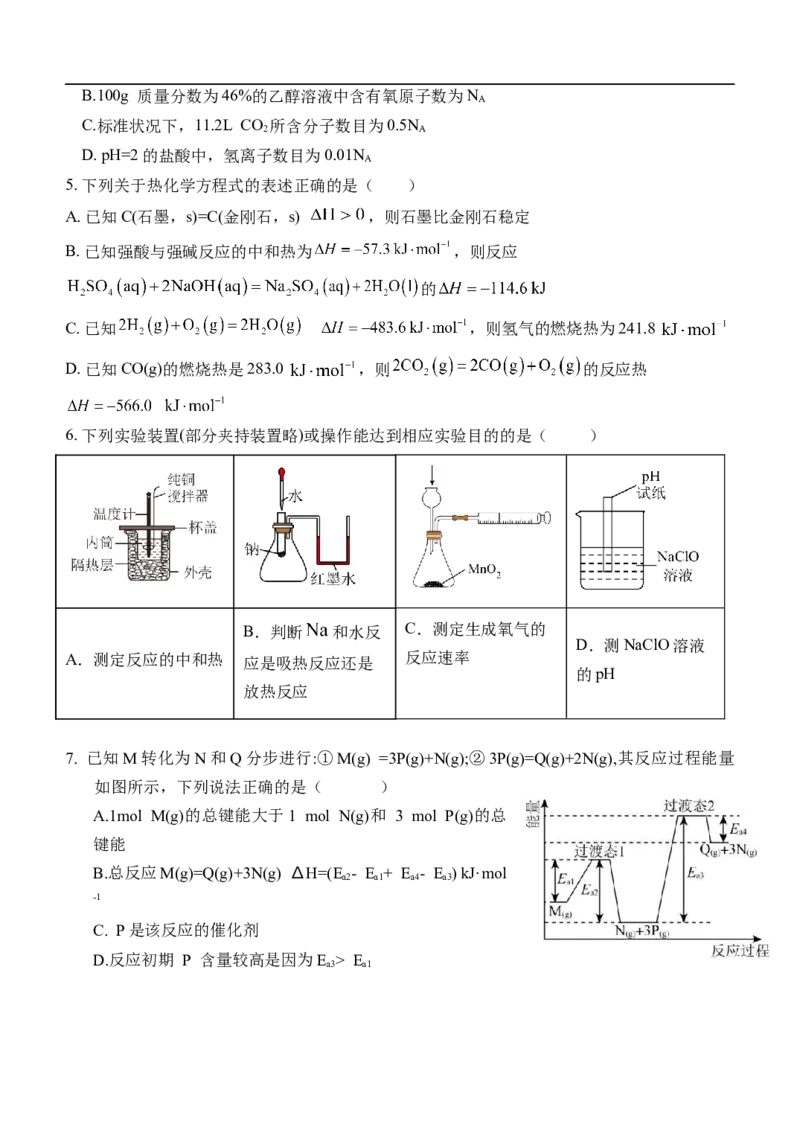
6. 下列实验装置(部分夹持装置略)或操作能达到相应实验目的的是( )
B.判断 和水反 C.测定生成氧气的
D.测NaClO溶液
A.测定反应的中和热 应是吸热反应还是 反应速率
的pH
放热反应
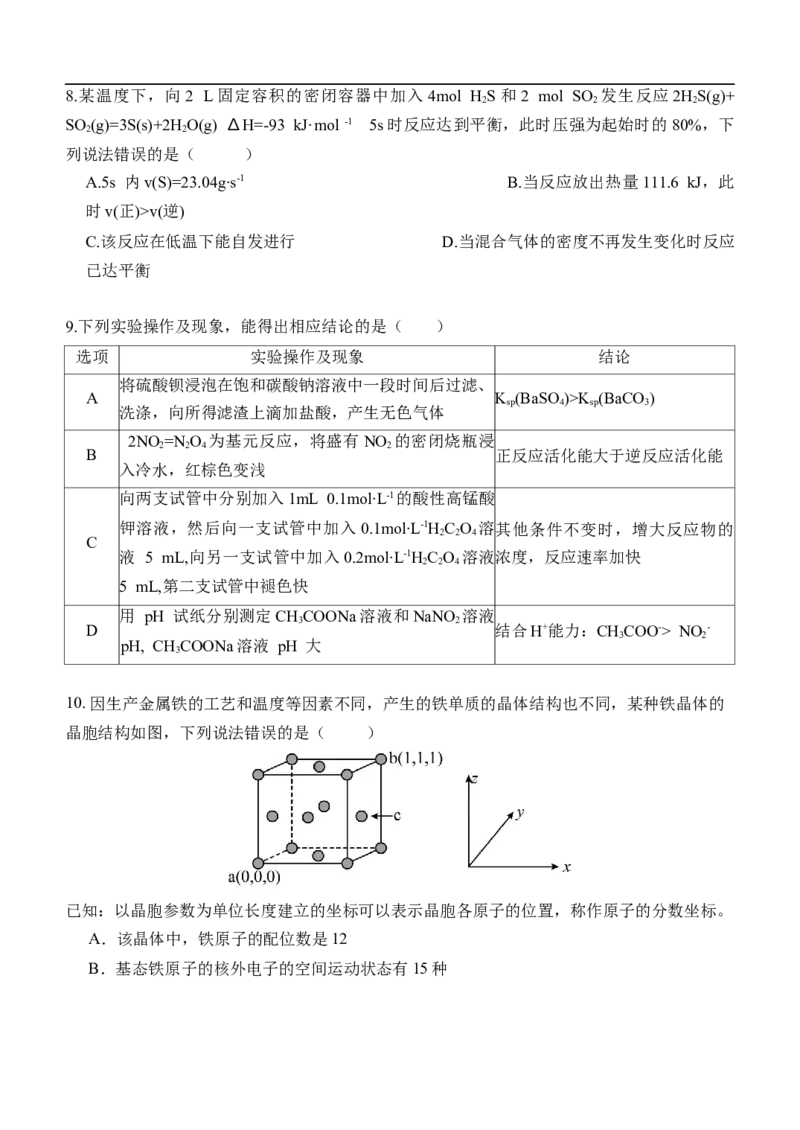
7. 已知M转化为N和Q分步进行:①M(g) =3P(g)+N(g);②3P(g)=Q(g)+2N(g),其反应过程能量
如图所示,下列说法正确的是( )
A.1mol M(g)的总键能大于1 mol N(g)和 3 mol P(g)的总
键能
B.总反应M(g)=Q(g)+3N(g) ∆H=(E - E + E - E ) kJ∙ mol
a2 a1 a4 a3
-1
C. P是该反应的催化剂
D.反应初期 P 含量较高是因为E > E
a3 a18.某温度下,向2 L固定容积的密闭容器中加入 4mol HS和2 mol SO 发生反应2HS(g)+
2 2 2
SO (g)=3S(s)+2H O(g) ∆H=-93 kJ∙ mol -1 5s时反应达到平衡,此时压强为起始时的80%,下
2 2
列说法错误的是( )
A.5s 内v(S)=23.04g∙s-1 B.当反应放出热量111.6 kJ,此
时v(正)>v(逆)
C.该反应在低温下能自发进行 D.当混合气体的密度不再发生变化时反应
已达平衡
9.下列实验操作及现象,能得出相应结论的是( )
选项 实验操作及现象 结论
将硫酸钡浸泡在饱和碳酸钠溶液中一段时间后过滤、
A K (BaSO)>K (BaCO)
sp 4 sp 3
洗涤,向所得滤渣上滴加盐酸,产生无色气体
2NO =N O 为基元反应,将盛有NO 的密闭烧瓶浸
2 2 4 2
B 正反应活化能大于逆反应活化能
入冷水,红棕色变浅
向两支试管中分别加入1mL 0.1mol∙L-1的酸性高锰酸
钾溶液,然后向一支试管中加入0.1mol∙L-1HC O 溶其他条件不变时,增大反应物的
2 2 4
C
液 5 mL,向另一支试管中加入0.2mol∙L-1HC O 溶液浓度,反应速率加快
2 2 4
5 mL,第二支试管中褪色快
用 pH 试纸分别测定CHCOONa溶液和NaNO 溶液
3 2
D 结合H+能力:CHCOO-> NO -
3 2
pH, CHCOONa溶液 pH 大
3
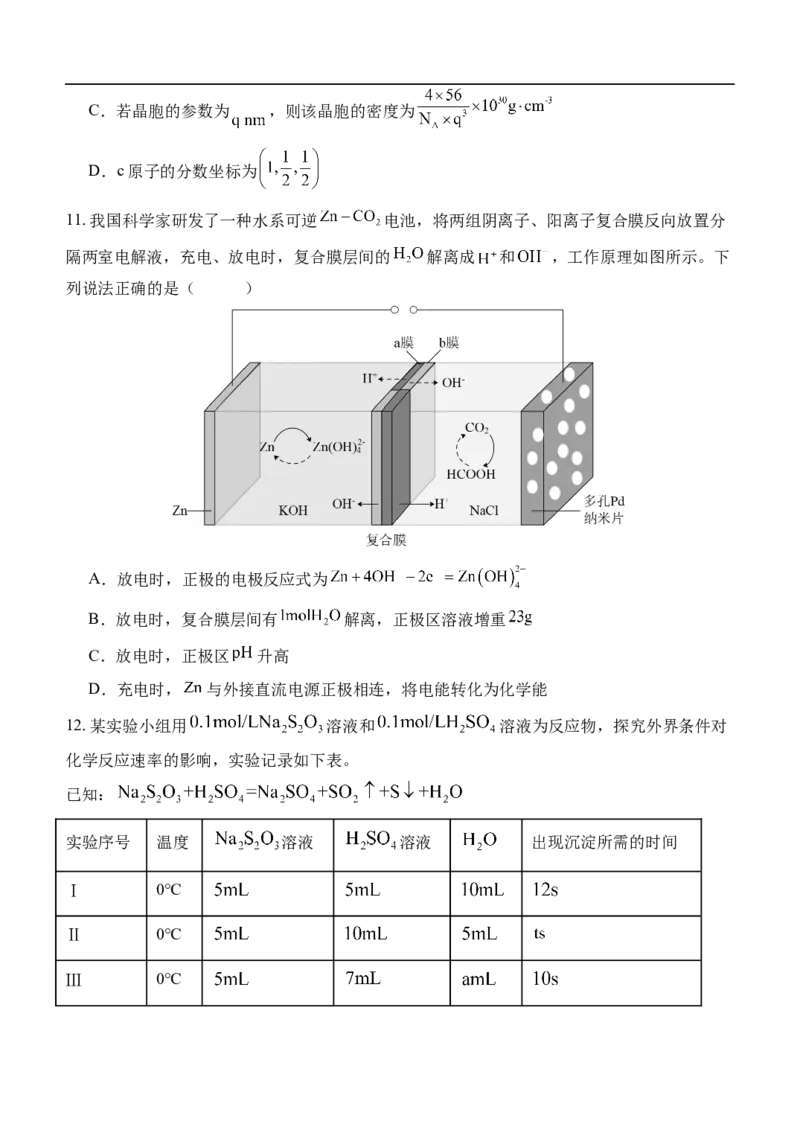
10. 因生产金属铁的工艺和温度等因素不同,产生的铁单质的晶体结构也不同,某种铁晶体的
晶胞结构如图,下列说法错误的是( )
已知:以晶胞参数为单位长度建立的坐标可以表示晶胞各原子的位置,称作原子的分数坐标。
A.该晶体中,铁原子的配位数是12
B.基态铁原子的核外电子的空间运动状态有15种C.若晶胞的参数为 ,则该晶胞的密度为
D.c原子的分数坐标为
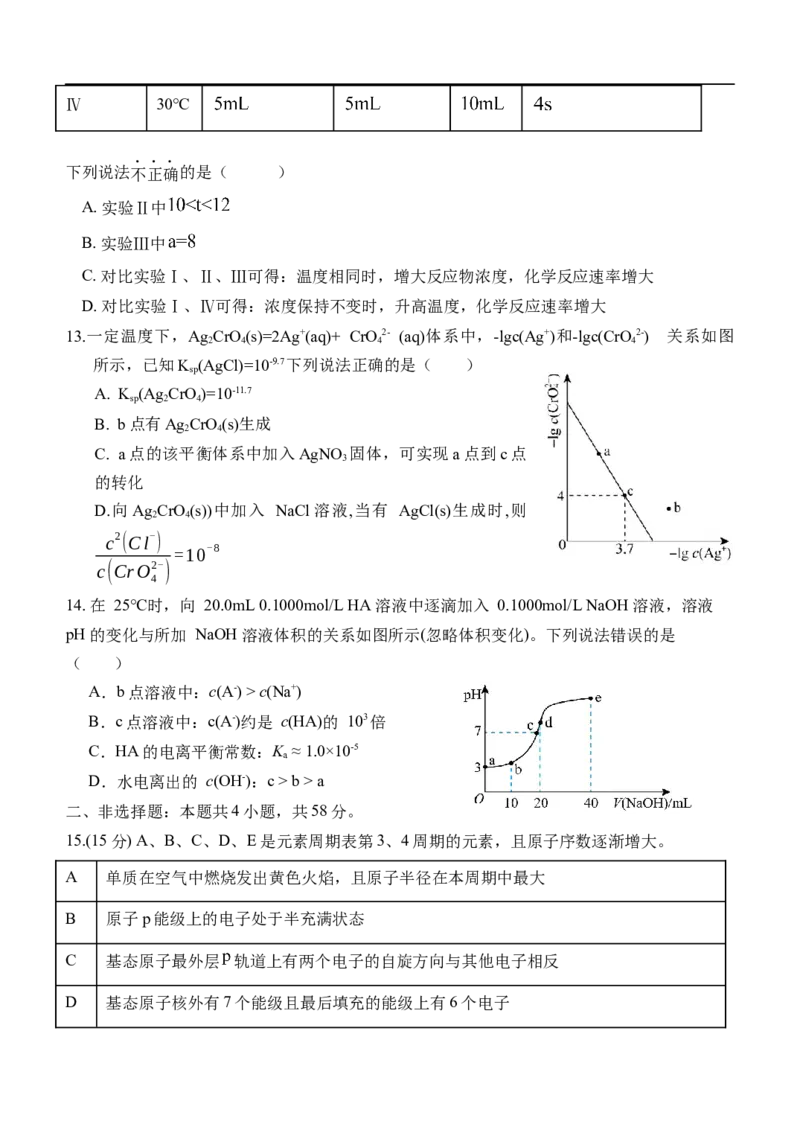
11. 我国科学家研发了一种水系可逆 电池,将两组阴离子、阳离子复合膜反向放置分
隔两室电解液,充电、放电时,复合膜层间的 解离成 和 ,工作原理如图所示。下
列说法正确的是( )
A.放电时,正极的电极反应式为
B.放电时,复合膜层间有 解离,正极区溶液增重
C.放电时,正极区 升高
D.充电时, 与外接直流电源正极相连,将电能转化为化学能
12. 某实验小组用 溶液和 溶液为反应物,探究外界条件对
化学反应速率的影响,实验记录如下表。
已知:
实验序号 温度 溶液 溶液 出现沉淀所需的时间
Ⅰ 0℃
Ⅱ 0℃
Ⅲ 0℃Ⅳ 30℃
下列说法不正确的是( )
A. 实验Ⅱ中
B. 实验Ⅲ中
C. 对比实验Ⅰ、Ⅱ、Ⅲ可得:温度相同时,增大反应物浓度,化学反应速率增大
D. 对比实验Ⅰ、Ⅳ可得:浓度保持不变时,升高温度,化学反应速率增大
13.一定温度下,Ag CrO(s)=2Ag+(aq)+ CrO2- (aq)体系中,-lgc(Ag+)和-lgc(CrO 2-) 关系如图
2 4 4 4
所示,已知K (AgCl)=10-9.7下列说法正确的是( )
sp
A. K (Ag CrO)=10-11.7
sp 2 4
B. b点有Ag CrO(s)生成
2 4
C. a点的该平衡体系中加入AgNO 固体,可实现a点到c点
3
的转化
D.向Ag CrO(s))中加入 NaCl溶液,当有 AgCl(s)生成时,则
2 4
c2(Cl-)
=10-8
c(CrO2-)
4
14. 在 25℃时,向 20.0mL 0.1000mol/L HA 溶液中逐滴加入 0.1000mol/L NaOH 溶液,溶液
pH 的变化与所加 NaOH 溶液体积的关系如图所示(忽略体积变化)。下列说法错误的是
( )
A.b点溶液中:c(A-) > c(Na+)
B.c点溶液中:c(A-)约是 c(HA)的 103倍
C.HA的电离平衡常数:Kₐ ≈ 1.0×10-5
D.水电离出的 c(OH-):c > b > a
二、非选择题:本题共4小题,共58分。
15.(15分) A、B、C、D、E是元素周期表第3、4周期的元素,且原子序数逐渐增大。
A 单质在空气中燃烧发出黄色火焰,且原子半径在本周期中最大
B 原子p能级上的电子处于半充满状态
C 基态原子最外层 轨道上有两个电子的自旋方向与其他电子相反
D 基态原子核外有7个能级且最后填充的能级上有6个电子E 基态原子核外有35种不同运动状态的电子
完成下列填空:
(1)A元素的焰色为黄色,这是由于A元素的核外电子由 (填“激发态”或“基
态”)跃迁到另一个状态时产生的光谱,该光谱属于 (填“发射”或“吸收”)光谱。
(2) C元素与E元素的电负性:C E(填“<”或“>”)。
(3)元素B的第一电离能 元素硫的第一电离能(填“<”或“>”)。
(4)元素D在元素周期表中的位置是 , 元素E位于元素周期
表的 区。
(5)基态E原子有 种能量不同的电子,共占有 个原子
轨道。
(6)基态 原子若其电子排布式表示为 违背了
。
16.(15分) 工业尾气HS对环境和人体健康会产生严重危害,回收HS是保护环境和资源利用
2 2
的有效措施。
I.已知:2HS(g) 2H(g)+S (g) ΔH=+169.8kJ/mol。
2 2 2
回答下列问题:
⇌
(1)上述反应中相关键能数据:
化学键
键能 a 329 436
反应能自发进行的条件是___________(“低温”或“高温”),a=_______。
(2)在恒温恒容密闭容器中,充入一定量HS气体发生上述反应,下列说法正确的是
2
______(填标号)。
A.HS的体积分数不再改变,说明该反应达到平衡
2
B.H 与S(g)物质的量浓度不再改变,说明该反应达到平衡
2 2
C.平衡时向容器中充入惰性气体,平衡正向移动
D.平衡时向容器中充入H 与S(g),再达平衡时, 不变
2 2
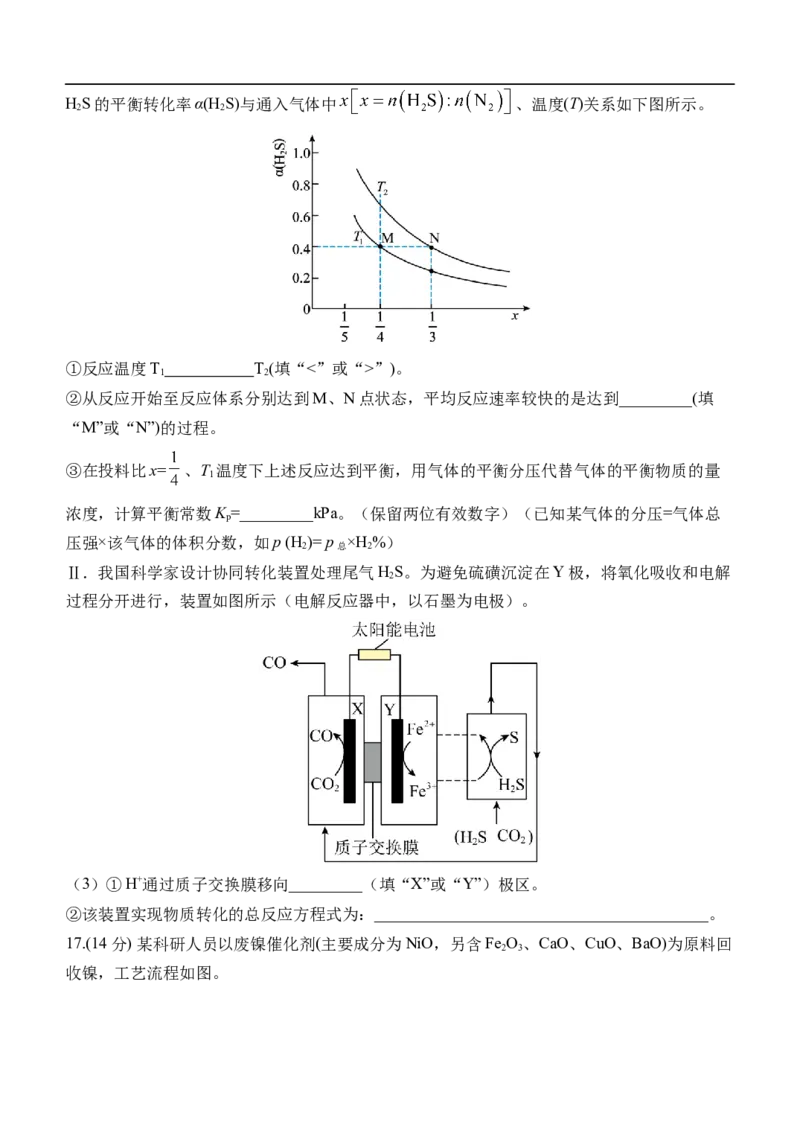
(3)保持压强恒定为100 kPa,向密闭容器中充入HS和N(N 不参与反应)发生上述反应,
2 2 2HS的平衡转化率α(H S)与通入气体中 、温度(T)关系如下图所示。
2 2
①反应温度T T(填“<”或“>”)。
1 2
②从反应开始至反应体系分别达到M、N点状态,平均反应速率较快的是达到_________(填
“M”或“N”)的过程。
③在投料比x= 、T 温度下上述反应达到平衡,用气体的平衡分压代替气体的平衡物质的量
1
浓度,计算平衡常数K =_________kPa。(保留两位有效数字)(已知某气体的分压=气体总
p
压强×该气体的体积分数,如p (H )= p ×H %)
2 总 2
Ⅱ.我国科学家设计协同转化装置处理尾气HS。为避免硫磺沉淀在Y极,将氧化吸收和电解
2
过程分开进行,装置如图所示(电解反应器中,以石墨为电极)。
(3)①H+通过质子交换膜移向_________(填“X”或“Y”)极区。
②该装置实现物质转化的总反应方程式为:_________________________________________。
17.(14分) 某科研人员以废镍催化剂(主要成分为NiO,另含Fe O、CaO、CuO、BaO)为原料回
2 3
收镍,工艺流程如图。已知:常温下,有关氢氧化物开始沉淀和沉淀完全的 如表。
氢氧化物
开始沉淀的 1.5 6.5 7.7
沉淀完全的 3.7 9.7 9.2
回答下列问题:
(1)为提高酸浸效率,可采取的措施是
。(写一条即可)
(2)浸出渣主要成分为 、 。(填化学式)
(3)“除铜”时, 将 氧化为S的反应离子方程式为
。
(4)“氧化”的目的是将溶液中氧 化为 ,温度需控制在 之间,该步骤温度不能
太高的原因是
。
(5)“调 ”时, 的控制范围为 。
(6)根据表中数据求算 的K = 。(沉淀完全时离子浓度
sp
≤1.0ⅹ10-5mol∙L-1)
(7) “除钙”后,若溶液中F-浓度为 ,则 。
[已知常温下, ]
18.(14分) 某化学学习小组探究测定草酸晶体中HC O 的质量分数。查阅资料得知,草酸易溶
2 2 4
于水,其水溶液可以用酸性KMnO 溶液进行滴定。
4
反应方程式为: 2MnO-+5HC O+6H+=2Mn2+(无色)+10CO↑+8HO。
4 2 2 4 2 2
该化学学习小组进行如下实验:
①称取1.000 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀硫酸。③用浓度为0.1000 mol·L-1的酸性KMnO 标准溶液进行滴定,达到终点时消耗10.00 mL。
4
④利用以上数据进行计算。
(1)滴定时,将酸性KMnO 标准液装在如右图中的 (填“A”或“B”)滴定管中。本实
4
验是否需要指示剂(若需要请写出指示剂名称若不需要请说明理由)
。
(2) 中量取25.00 mL待测液所用的仪器名称为
。
②
(3)本实验到达滴定终点的现象是
。
(4)通过上述数据,求得HC O 的质量分数为
2 2 4
。
(5)根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进
方法 。
(6)以下操作会导致HC O 的质量分数偏高的是___________(填字母)。
2 2 4
A.装待测液前,锥形瓶中有少量蒸馏水
B.滴定终点时仰视滴定管刻度
C.晃动锥形瓶时有部分草酸溶液洒出锥形瓶
D.滴定终点时滴定管尖嘴处有液滴悬挂
化学试题答案
一、单选题
二
1 2 3 4 5 6 7 8 9 10 11 12 13 14 非
A B C C A B D B C C B A D B 选
择
15.(1)激发态 发射 (2)>(3)>(4)第4周期VIII族 P(5)8 18(6)洪特规则
16. (1) 高温 274.2 (2). ABD
(3) ①. < ②. N ③1.7(4) ①. X ②.
17.(1)将含镍催化剂粉碎、适当升高温度、适当增大H SO 的浓度等
2 4
(2) CaSO 2H O(不写结晶水也对) BaSO
4 2 4
(3)2Fe3++H S=2Fe2++S +2H+
2∙
(4) 温度太高,H O 受热易分解
2 2 ↓
(5)3.7≤pH 7.7
(6) 1.0×10-35.9
<
(7)1.0×10-3
18. (1)A 高锰酸钾呈紫色被还原成二价锰离子为无色,所以不需要指示剂
(2)酸式滴定管
(3)滴入最后半滴酸性高锰酸钾标准液,溶液由无色变为浅红色,且半分钟内不恢复无色
(4)90.00%
(5)重复步骤②③增加2~3次平行实验
(6)BD