文档内容
2024 年春高二(下)期末联合检测试卷
化 学
化学测试卷共4页,满分100分。考试时间75分钟。
可能用到的相对原子质量:H-1 C-12 O-16 Ag-108
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 中国高铁在世界上是一张“金名片”,下列高铁使用材料属于有机高分子材料的是
A.列车车体——铝合金 B.光导纤维——二氧化硅
C.侧墙面板——碳纤维 D.车厢连接——聚四氟乙烯
2. 下列各组物质中,化学键类型相同,晶体类型也相同的是
A.金刚石和CO B.NaBr和HBr C.CH 和H O D.Cl 和KCl
2 4 2 2
3. 下列有关化学用语或图示表示错误的是
A.中子数为8的碳原子:14 C B.二氧化硫的VSEPR模型:
6
C.CO
2
的电子式:
O C O
D.基态氧原子的轨道表示式:
4. 下列有机物的命名正确的是
A.(CH ) CHCH=CH 3 甲基 1 丁烯 B.CH CH CHCl 二氯丙烷
3 2 2 3 2 2
C.(CH
3
)
3
CCOOH 2,3 二甲基丁酸 D.CH
3
CH(OH)CH
3
2 羟基丙烷
5. 合成高聚物 C H C F C F C F 的单体是
2 2 2 n
CF
3
A.CH
2
=CF CF=CF CF
3
B.CH
2
=CF
2
和CF
2
=CF CF
3
C.CH
2
=CF CF
3
和CF
2
=CF
2
D.CH
2
=CF CF
2
CF=CF
2
6. “无糖”饮料备受消费者喜爱,“无糖”指不含蔗糖,但常添加合成甜味剂。阿斯巴甜是合成甜味剂之一,
其结构如下图所示,下列有关阿斯巴甜分子的说法正确的是
A.所有原子可能共平面
O
B.含有4种官能团
HOOC CH CH C NH CH CH
2 2
C.含有3个手性碳原子
NH COOCH
2 3
D.碳原子均采用sp3杂化
7. 下列性质比较错误的是
A.基态原子第一电离能:C>B>Be B.熔点:SiO >NaCl>CCl
2 4
C.酸性:CF COOH>CCl COOH D.水中溶解度:CH OH>CH CH CH CH OH
3 3 3 3 2 2 2
8. 下列说法正确的是
A.共价键的成键原子只能是非金属原子 B.冰晶体中每个水分子周围有4个紧邻的水分子
C.HF比HCl稳定是因为HF间存在氢键 D.s s σ键与s p σ键的电子云形状的对称性不同
高二(下)期末联合检测试卷(化学)第1页 共7页
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}9. 强力粘胶剂“502”的主要成分为α 氰基丙烯酸乙酯,其结构如图所示。下列有关该分子的说法正确的是
A.分子式为C H O N
5 7 2
B.所有原子都满足8电子稳定结构 N O
O
C.分子中含有4个π键
D.分子中有2种不同化学环境的氢原子
10.白磷(P )在空气中易自燃,常保存在冷水中,熔点为44℃,其晶胞结构如图所示,下列说法错误的是
4
A.P 分子属于非极性分子
4
B.一个晶胞中含4个P 分子
4
代表白磷分子
C.晶体中相邻分子间存在范德华力
D.该晶体属于混合晶体
11.下列实验或操作能达到实验目的的是
饱和食盐水 气体
电石
酸性
溴水 KMnO
4
溶液
A.检验电石与水反 B.证明苯环使羟基活化 C.检验溴乙烷消去 D.分离饱和Na CO 溶液
2 3
应的产物乙炔 产物中的乙烯 和CH COOC H
3 2 5
12.花生、葡萄中蕴含丰富的白藜芦醇,经研究发现白藜芦醇具有抗癌和心血管保护作用,其结构如下图所示。
下列有关白藜芦醇的说法错误的是
HO
A.白藜芦醇存在顺反异构
B.光照下与氯气反应,苯环上可形成C-Cl键 OH
C.与足量NaOH溶液反应,O-H键均可断裂 HO
D.1mol白藜芦醇与浓溴水反应,最多消耗6mol Br
2
13.下列实验操作、现象及结论均正确的是
选项 实验操作 现象 结论
淀粉溶液中加入稀硫酸、加热,再加入
A 未出现银镜 淀粉未水解
银氨溶液,水浴加热
B 向丙烯醛(CH =CHCHO)中加入溴水,振荡 溴水褪色 丙烯醛与溴水发生了加成反应
2
油脂与足量NaOH溶液共热、搅拌,
C 无分层现象 油脂完全水解
取少量混合液滴入蒸馏水
D 将乙醇与酸性重铬酸钾溶液混合 橙色溶液变为绿色 乙醇具有氧化性
高二(下)期末联合检测试卷(化学)第2页 共7页
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}14.若苯的同系物侧链烷基中,直接与苯环连接的碳原子上没有 C-H,该物质一般不能被酸性高锰酸钾溶液
氧化成苯甲酸。分子式为 C H 的单烷基取代苯中可以被氧化成苯甲酸的同分异构体有(不含立体异构)
10 14
A.3种 B.4种 C.5种 D.6种
二、非选择题:本题共4个小题,共58分。
15.(14分)已知有A、B、C、D、E 5种有机物,其结构简式如下。
OH
H CH OH
Cl O HOOC COOH 2 n
A B C D E
(1)属于醚类物质的是 (填字母,下同),属于羧酸类物质的是 。
(2)A的名称是 ,A的一溴代物有 种(不考虑立体异构)。
(3)A与NaOH溶液发生反应的化学方程式为 。
(4)E可由苯酚和 (填物质名称)发生缩聚反应制得。
催化剂
(5)已知反应:R CH=CHR R CHO+R CHO,B发生类似反应可生成物质M。M的结构简式
1 2 1 2
为 ,M与新制Cu(OH) 悬浊液反应的化学方程式为 。
2
16.(15分)研究含氮化合物具有重要意义。
(1)硫酸镍(NiSO )溶于氨水形成[Ni(NH ) ]SO 蓝色溶液。
4 3 6 4
①Ni位于元素周期表 区(填“d”或“ds”),基态S原子的价层电子排布式为 。
②SO 2-的空间结构是 ,中心原子杂化轨道类型为 。
4
③1mol [Ni(NH ) ]2+中含σ键的数目为 mol。
3 6
(2)(NH ) SeBr(摩尔质量为M g/mol)可应用于太阳能电池,其晶体的晶胞结构如下图,其中阴离子位于
4 2 6
立方体的顶点和面心。
①H-N-H键角:NH+
4
NH
3
(填“大于” 代表NH+
4
Br
或“小于”),理由是 。
Br
Br
②已知晶胞边长为a cm,N
A
为阿伏加德罗常数 代表
B r
Se
Br
的值,则晶体密度ρ= g·cm-3。 Br
17.(14分)实验室以苯甲酸和乙醇为原料制备苯甲酸乙酯的装置如图1(部分装置省略)。
b
Ⅰ.合成苯甲酸乙酯粗产品:在仪器A中加入12.2g苯甲酸、稍过量乙醇、
B
10.0mL浓硫酸、适量环己烷(与乙醇、水可形成共沸物),控制一定温
a
度,加热一段时间后停止加热。
分水器
(1)仪器A名称是 ,冷凝水从 口进入(填“a”或“b”)。
A
(2)浓硫酸在该实验中的作用是 。
图1
(3)写出制取苯甲酸乙酯的化学方程式 。
高二(下)期末联合检测试卷(化学)第3页 共7页
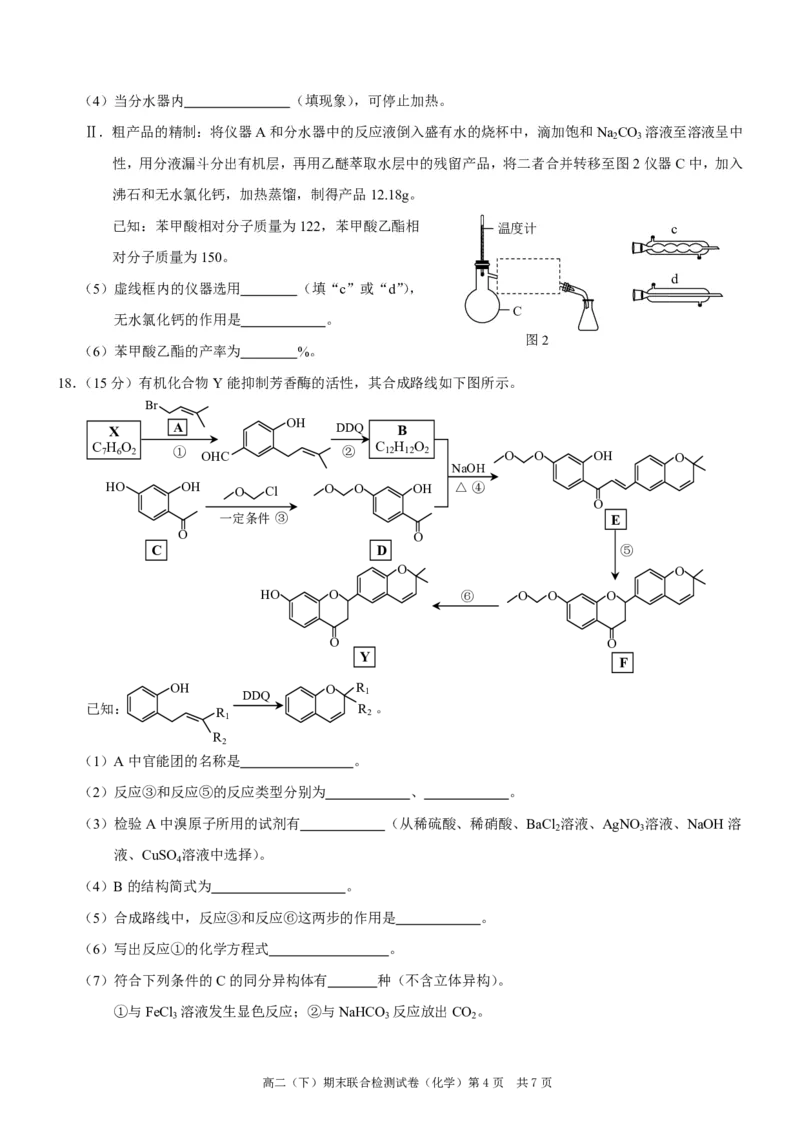
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}(4)当分水器内 (填现象),可停止加热。
Ⅱ.粗产品的精制:将仪器A和分水器中的反应液倒入盛有水的烧杯中,滴加饱和Na CO 溶液至溶液呈中
2 3
性,用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,将二者合并转移至图2仪器C中,加入
沸石和无水氯化钙,加热蒸馏,制得产品12.18g。
已知:苯甲酸相对分子质量为122,苯甲酸乙酯相 温度计 c
对分子质量为150。
d
(5)虚线框内的仪器选用 (填“c”或“d”),
C
无水氯化钙的作用是 。
图2
(6)苯甲酸乙酯的产率为 %。
18.(15分)有机化合物Y能抑制芳香酶的活性,其合成路线如下图所示。
Br
OH
X A DDQ B
C 7 H 6 O 2 ① OHC ② C 12 H 12 O 2 O O OH O
NaOH
HO OH O Cl O O OH △ ④
O
一定条件 ③ E
O O
C D ⑤
O O
HO O ⑥ O O O
O O
Y
F
OH DDQ O R 1
已知: R 1 R 2 。
R
2
(1)A中官能团的名称是 。
(2)反应③和反应⑤的反应类型分别为 、 。
(3)检验A中溴原子所用的试剂有 (从稀硫酸、稀硝酸、BaCl 溶液、AgNO 溶液、NaOH溶
2 3
液、CuSO 溶液中选择)。
4
(4)B的结构简式为 。
(5)合成路线中,反应③和反应⑥这两步的作用是 。
(6)写出反应①的化学方程式 。
(7)符合下列条件的C的同分异构体有 种(不含立体异构)。
①与FeCl 溶液发生显色反应;②与NaHCO 反应放出CO 。
3 3 2
高二(下)期末联合检测试卷(化学)第4页 共7页
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}高二化学答案
1~5 DCDAB 6~10 BABCD 11~14 DBCA
1.D。解析略。
2.C。解析:CH 和H O都是由共价键形成的分子晶体。
4 2
3.D。解析:基态氧原子的轨道表示式为
4.A。解析:B选项命名为1,1-二氯丙烷;C选项命名为2,2 二甲基丙酸;D选项命名为2-丙醇。
5.B。解析略。
6.B。解析:A选项,分子中含饱和碳原子,不可能所有原子共平面;B选项,含有羧基、氨基、酯基、酰胺
键等四种官能团;C选项,该分子中含有2个手性碳原子;D选项,碳原子有sp2、sp3杂化。
7.A。解析:A选项,基态原子第一电离能:C>Be>B。
8.B。解析:A选项,共价键的成键原子也可以是金属原子,如AlCl ;C选项,HF比HCl稳定是因为F的非
3
金属性比Cl强,非金属性强,其气态氢化物的稳定性强;D选项,s s σ键与s p σ键的电子云
形状的对称性相同,都是轴对称。
9.C。解析:A选项,分子式为C H O N;B选项,H原子不满足8电子;D选项,分子中有3种不同化学环
6 7 2
境的氢原子。
10.D。解析:该晶体属于分子晶体。
11.D。解析:A选项,电石与水反应会产生杂质H S,H S也会使溴水褪色;B选项,证明羟基使苯环活化;
2 2
C选项,溴乙烷发生消去反应时要加醇,挥发出来的醇也会使酸性高锰酸钾褪色。
12.B。解析:氯气取代苯环上的氢的条件是液氯和FeCl 作催化剂。
3
13.C。解析:A选项,操作有错误,加银氨溶液之前未加NaOH溶液中和酸;B选项,-CHO也能使溴水褪色,
发生的为氧化还原反应;D选项,结论错误,乙醇具有还原性。
14.A。解析:C H 除苯环外,还有1个-C H ,其同分异构体有-CH CH CH CH 、-CH(CH )CH CH 、
10 14 4 9 2 2 2 3 3 2 3
-CH CH(CH ) 、-C(CH ) ;当苯环上接-C(CH ) ,不能被氧化成苯甲酸。故只有3种。
2 3 2 3 3 3 3
15.(14分)
(1)C(1分) D(1分)
(2)一氯环戊烷(2分) 3(2分)
水
(3) C l + N a O H O H + N a C l (2分)
△
(4)甲醛(2分)
高二(下)期末联合检测试卷(化学)第5页 共7页
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}(5)OHCCH CHO(2分)
2
OHCCH CHO+4Cu(OH) +2NaOH △ NaOOCCH COONa+2Cu O↓+6H O (2分)
2 2 2 2 2
16.(15分)
(1)①d(2分) 3s23p4(2分)
②正四面体形(2分) sp3(2分)
③24(2分)
(2)①大于(1分)
NH+中心原子上无孤电子对,NH 的中心原子上有孤电子对,对成键电子对排斥作用更强(2分)。
4 3
4M
② (2分)
a3N
A
M
4
N 4M
解析:(2)②1个该晶胞中含有4个(NH ) SeBr ,晶体密度 A 。
4 2 6 a3 a3N
A
17.(14分)
(1)圆底烧瓶(2分) a(1分)
(2)作催化剂、吸水剂(2分)
浓硫酸
+CH
3
CH
2
OH +H
2
O
(3) △ (2分)
(4)油层高度不再发生变化(2分)
(5)d(1分) 吸收水分(2分)
(6)81.2(2分)
解析:(6)12.2g苯甲酸为0.1mol,理论可生成0.1mol苯甲酸乙酯,即15g。
苯甲酸乙酯的产率为 。
18.(15分)
(1)碳碳双键、碳溴键(2分)
(2)取代反应(1分)加成反应(1分)
(3)NaOH溶液、稀硝酸、AgNO 溶液(3分)
3
(4) (2分)
(5)保护C中酮羰基对位的羟基(2分)
OH OH
(6) + B r + H B r (2分)
OHC OHC
高二(下)期末联合检测试卷(化学)第6页 共7页
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}(7)13(2分)
【解析】(7)根据条件可知含有酚羟基和羧基。苯环上若有3个取代基:-OH、-COOH和-CH ,则不同的
3
结构有10种;若苯环上有2个取代基:-OH、-CH COOH,则有邻间对3种;一共13种结构。
2
高二(下)期末联合检测试卷(化学)第7页 共7页
{{##{{QQQQAABBbaYYKOAt5oggCg4okAIaJIAACACA5gLCQQUQVUY4CCkkoMQQkJkIAgCLWACgaMgAOQRCBCAuMAMwAKAAAJFQIAFIFAA=B}#A}A=}#}