文档内容
福州市八县(市)协作校2024-2025学年第一学期期中联考
高三 化学试卷
【完卷时间:75分钟;满分:100分】
可能用到的相对原子质量 O-16 Fe-56 Cu-64 Ni-59 Mn-55
一、选择题(本题共 10小题,每题4分,共40分。每小题只有一个选项符合题
意)
1. 能源、航天、信息等科技离不开新技术和新材料的发现和应用。下列有关说法正
确的是( )
.
A 量子通信材料如螺旋碳纳米管、石墨烯等纳米材料属于胶体
B. 航天核心舱搭载的柔性太阳能电池板的核心材料是晶体二氧化硅
C. 新一代运载火箭成功应用液氧、煤油发动机,煤油是石油分馏所得混合物
D. 福建舰舰身材料采用低碳合金钢,合金的强度一般低于成分金属
2.莽草酸结构简式如图,有关说法正确的是( )
A.分子中含有2种官能团
B.1mol莽草酸与Na反应最多生成4mol氢气
C.可与乙醇、乙酸反应,且反应类型相同
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
3.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使石蕊呈蓝色的溶液中: 、 、 、
B.使pH变红的溶液中: 、 、 、
C.与Al反应能放出 的溶液中: 、 、 、
D.0.1 mol·L-1酸性高锰酸钾溶液中:SO 2-、NH +、C O 2-、K+
4 4 2 4
4.下列指定反应的离子方程式书写正确的是( )
A. 溶液中加入足量 溶液:B.氢氧化钠溶液中加入过量碳酸氢钙溶液
C.铁粉与过量稀硝酸反应:Fe+NO +4H+=Fe3++NO↑+2H O
2
D.向次氯酸钠溶液通入少量二氧化碳:
5.探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案 现象 结论
溶液颜色由浅绿 的氧化能力比
A 往 溶液中加入 片
色变为无色 强
往 溶液中滴加 溶 溶液先变成血红 与 的反应
B
液,再加入少量 固体 色后无明显变化 不可逆
将食品脱氧剂样品和还原铁粉溶于 食品脱氧剂样品中
C 溶液呈浅绿色
盐酸,滴加 溶液 没有 价铁
向沸水中逐滴加5~6滴饱和 溶 溶液先变成红褐 此操作最终可制得
D
液,持续煮沸 色再析出沉淀 胶体
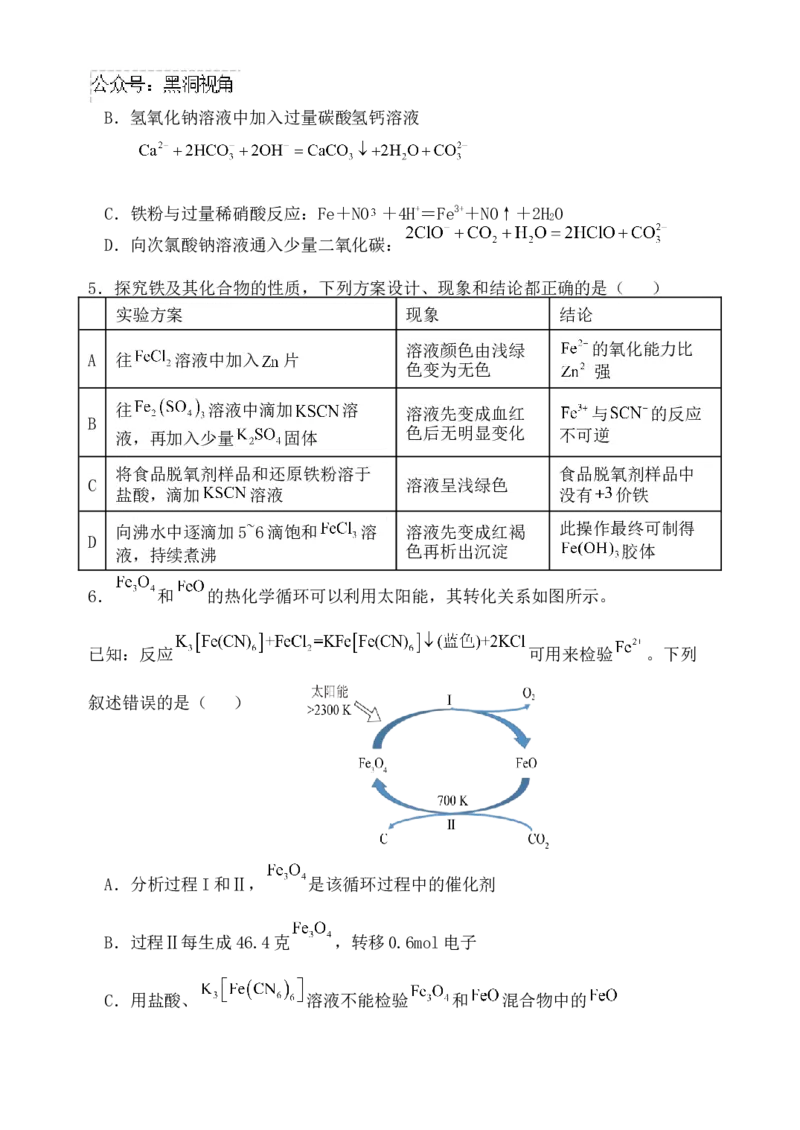
6. 和 的热化学循环可以利用太阳能,其转化关系如图所示。
已知:反应 可用来检验 。下列
叙述错误的是( )
A.分析过程I和Ⅱ, 是该循环过程中的催化剂
B.过程Ⅱ每生成46.4克 ,转移0.6mol电子
C.用盐酸、 溶液不能检验 和 混合物中的D.该循环过程利用了太阳能,而且降低了环境中 的含量
7.过二硫酸钾( )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
溶液制备,它在100℃下能发生分解反应:
(未配平),设 是阿伏加德罗常数的值,下
列说法正确的是( )
A. 中不存在非极性共价键
B.每生成 ,转移电子数2
C.标准状况下,11.2L 含有的原子数为2
D. 溶液的离子总数为0.1
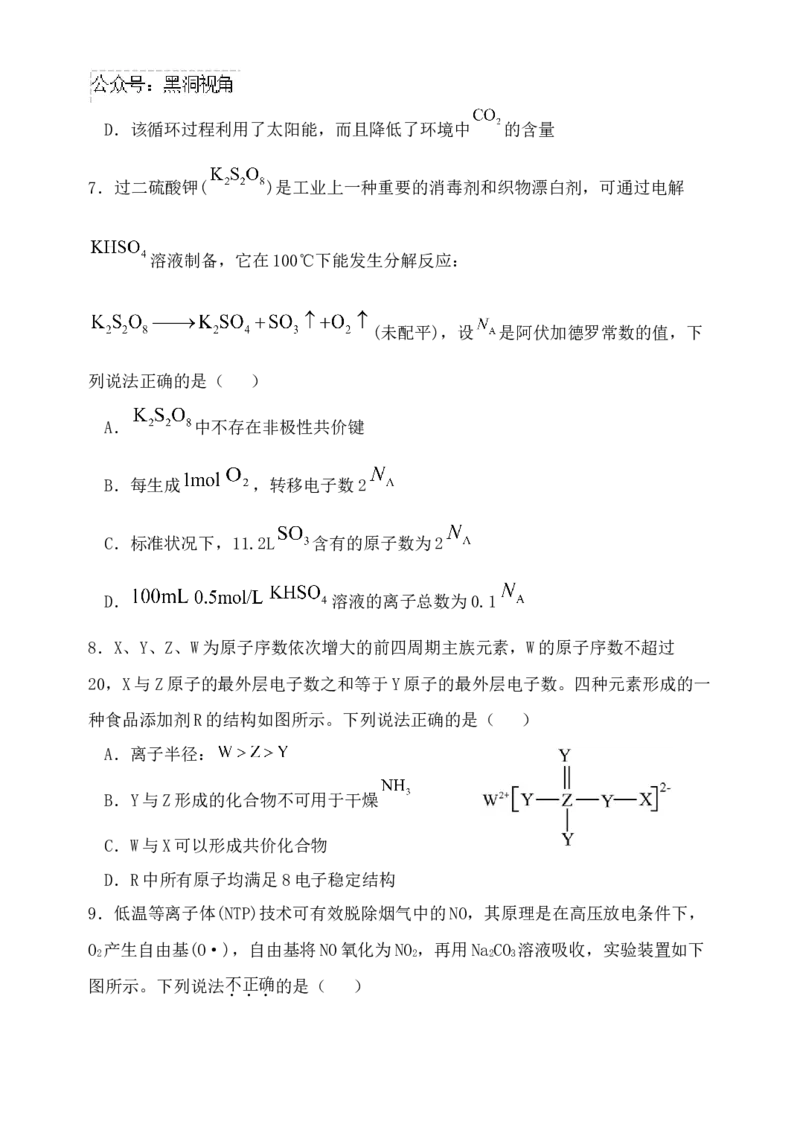
8.X、Y、Z、W为原子序数依次增大的前四周期主族元素,W的原子序数不超过
20,X与Z原子的最外层电子数之和等于Y原子的最外层电子数。四种元素形成的一
种食品添加剂R的结构如图所示。下列说法正确的是( )
A.离子半径:
B.Y与Z形成的化合物不可用于干燥
C.W与X可以形成共价化合物
D.R中所有原子均满足8电子稳定结构
9.低温等离子体(NTP)技术可有效脱除烟气中的NO,其原理是在高压放电条件下,
O 产生自由基(O·),自由基将NO氧化为NO ,再用Na CO 溶液吸收,实验装置如下
2 2 2 3
图所示。下列说法不正确的是( )A.氮元素只有被氧化的过程
B.高压电源的功率越大,NO的脱除效果不一定越好
C.尾气吸收采用气、液逆流的方式可提高NO 脱除率
2
D.单位时间内生成的自由基(O·)越多,越有利于NO的转化
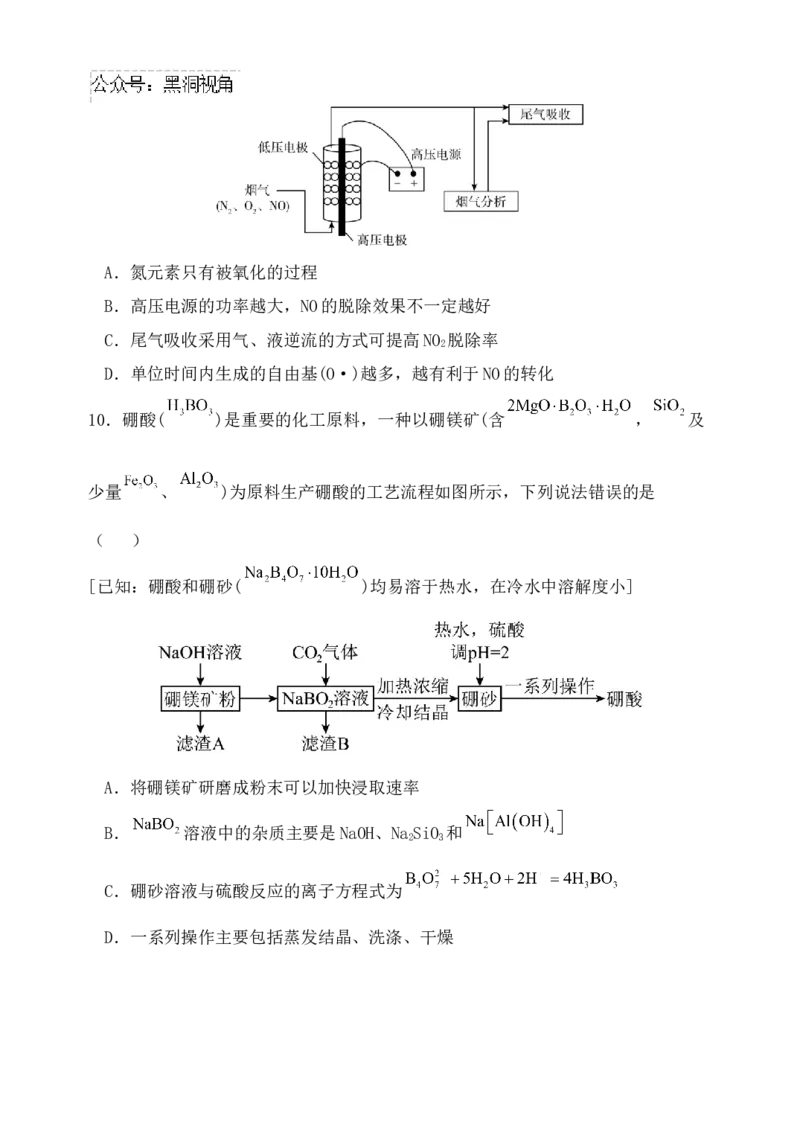
10.硼酸( )是重要的化工原料,一种以硼镁矿(含 , 及
少量 、 )为原料生产硼酸的工艺流程如图所示,下列说法错误的是
( )
[已知:硼酸和硼砂( )均易溶于热水,在冷水中溶解度小]
A.将硼镁矿研磨成粉末可以加快浸取速率
B. 溶液中的杂质主要是NaOH、Na SiO 和
2 3
C.硼砂溶液与硫酸反应的离子方程式为
D.一系列操作主要包括蒸发结晶、洗涤、干燥二、非选择题:(本题共4小题,共60分。)
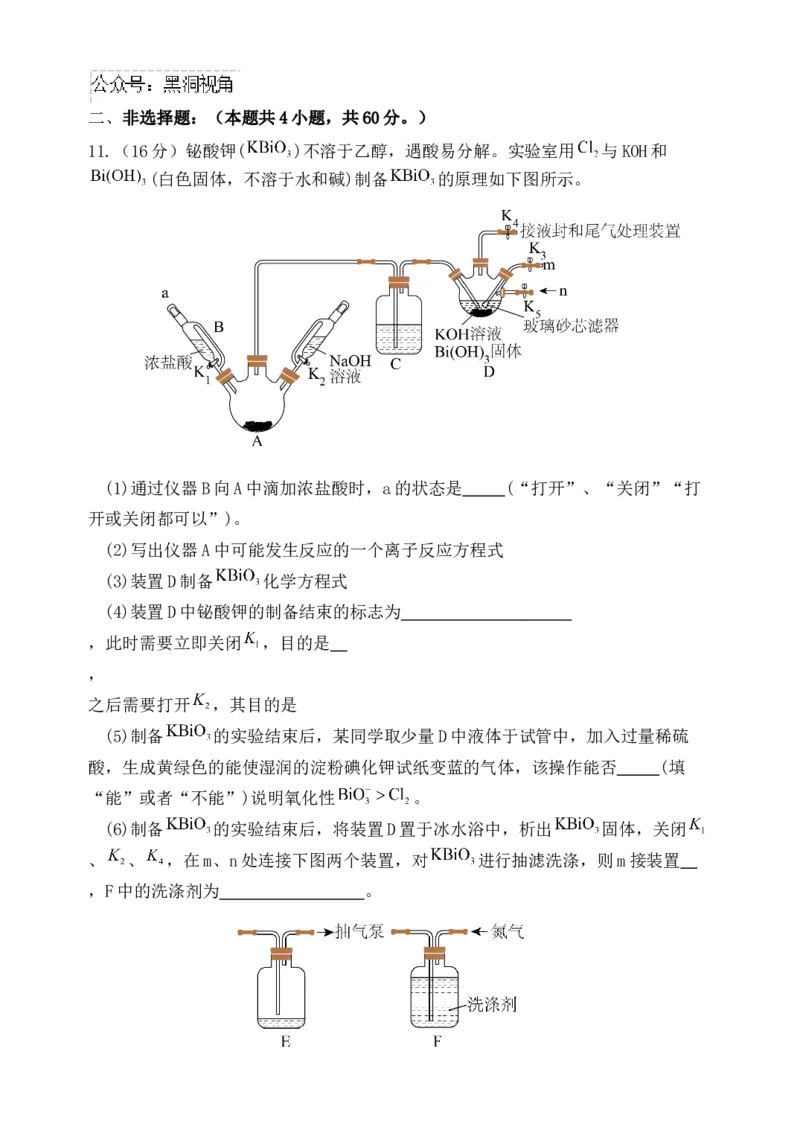
11.(16分)铋酸钾( )不溶于乙醇,遇酸易分解。实验室用 与KOH和
(白色固体,不溶于水和碱)制备 的原理如下图所示。
(1)通过仪器B向A中滴加浓盐酸时,a的状态是 (“打开”、“关闭”“打
开或关闭都可以”)。
(2)写出仪器A中可能发生反应的一个离子反应方程式
(3)装置D制备 化学方程式
(4)装置D中铋酸钾的制备结束的标志为
,此时需要立即关闭 ,目的是
,
之后需要打开 ,其目的是
(5)制备 的实验结束后,某同学取少量D中液体于试管中,加入过量稀硫
酸,生成黄绿色的能使湿润的淀粉碘化钾试纸变蓝的气体,该操作能否 (填
“能”或者“不能”)说明氧化性 。
(6)制备 的实验结束后,将装置D置于冰水浴中,析出 固体,关闭
、 、 ,在m、n处连接下图两个装置,对 进行抽滤洗涤,则m接装置
,F中的洗涤剂为 。12.(12分)溴化亚铜(CuBr)是一种白色结晶状粉末,微溶于水,不溶于乙醇,在
热水中或见光都会分解,在空气中逐渐变为浅绿色。实验室制备CuBr的实验步骤和
装置如下图。
回答下列问题:
(1)装仪器A名称为 装置A中的离子方程式为
(2)装置常采用60℃水浴加热,温度不宜过高的原因是
;
加料完成后,60℃水浴加热,以一定速率搅拌,能提高 吸收率的方法为
____________________________________。
(2)欲利用上述装置烧杯中的吸收液(经检测含有 、 )制取较纯净
的 晶体。补充完整制取 晶体的实验方案:向烧杯内的吸收液中,
向烧杯中通入 充分反应,再加入适量的 ,蒸发浓
缩至有大量晶体出现,在 ℃以上趁热过滤,用 洗涤2~3
次 ,置于真空干燥箱中干燥。
(已知:室温下从饱和 溶液中结晶出 ,34~100℃结晶出
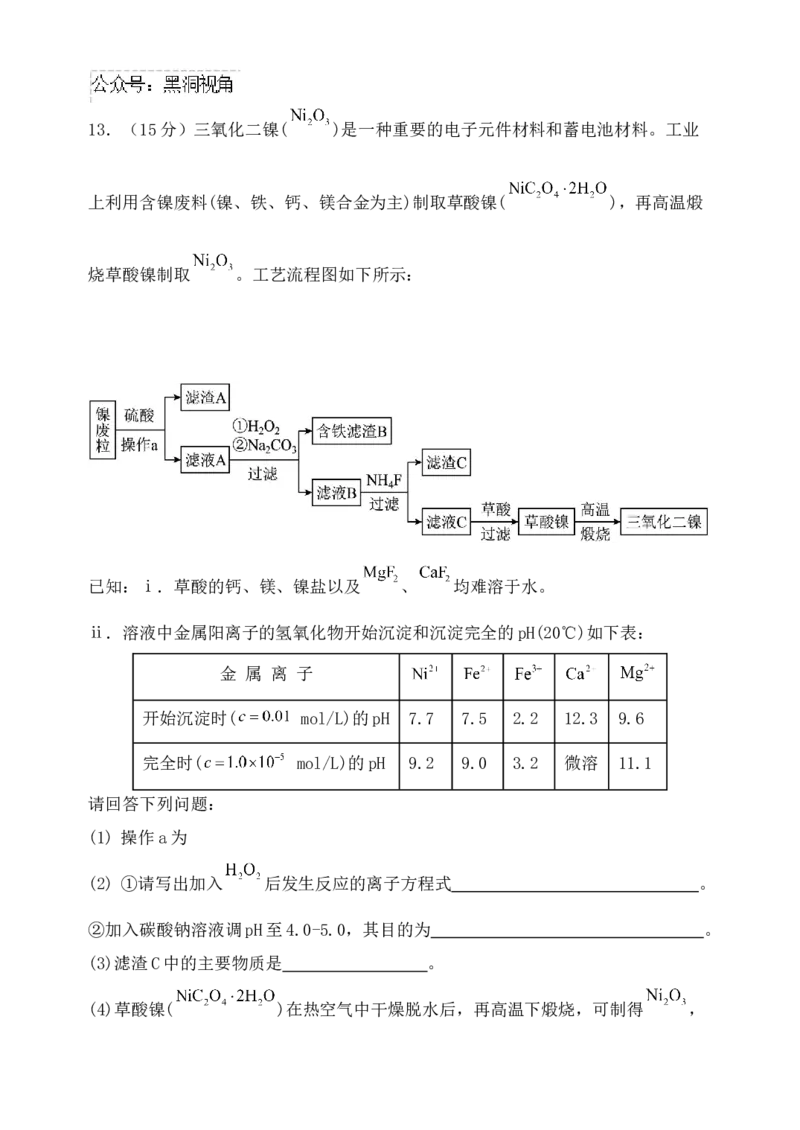
)13.(15分)三氧化二镍( )是一种重要的电子元件材料和蓄电池材料。工业
上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍( ),再高温煅
烧草酸镍制取 。工艺流程图如下所示:
已知:ⅰ.草酸的钙、镁、镍盐以及 、 均难溶于水。
ⅱ.溶液中金属阳离子的氢氧化物开始沉淀和沉淀完全的pH(20℃)如下表:
金 属 离 子
开始沉淀时( mol/L)的pH 7.7 7.5 2.2 12.3 9.6
完全时( mol/L)的pH 9.2 9.0 3.2 微溶 11.1
请回答下列问题:
(1) 操作a为
(2) ①请写出加入 后发生反应的离子方程式 。
②加入碳酸钠溶液调pH至4.0-5.0,其目的为 。
(3)滤渣C中的主要物质是 。
(4)草酸镍( )在热空气中干燥脱水后,再高温下煅烧,可制得 ,同时获得混合气体。 受热分解的化学方程式为 。
(5)若镍废料中镍含量为40%,用该方法处理1 t镍废料得到0.40 t (假设不
含杂质),则产率为 (保留2位小数)。
(6)工业上还可用电解法制取 。用NaOH溶液调 溶液的pH至7.5,加入适
量 后利用惰性电极电解。电解过程中产生的 有80%在弱碱性条件下生成
,再把二价镍氧化为三价镍。请写出 与 反应,生成 的离子
方程式为 。
14.(17分)Mn O 是一种重要的化工产品。以菱锰矿(主要成分为MnCO ,还含有少
2 3 3
量Fe O 、FeO、CoO、Al O )为原料制备Mn O 的工艺流程如图。
2 3 2 3 2 3
已知:①氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
②滤渣2为CoS。
(1) MnOOH中Mn的化合价为 价。酸浸池中氧化铁与硫酸反应的离子方程式
,加快酸浸速率的措施 (只写一种)。
(2)向“沉淀池I”中加入MnO 的作用是 ;
2
(3)“滤渣1”的主要成分是 (填化学式)。(4)MnSO 转化为MnOOH的离子方程式为 。
4
(5)MnSO 转化为MnOOH中“Ⅲ.实验操作”包含过滤、洗涤、干燥。检验MnOOH是
4
否洗涤干净,具体操作为 。
(6)菱锰矿中Mn的质量分数为50%,假设沉淀池I中加入MnO 的质量为菱锰矿质量
2
的87%,并且生产过程中Mn元素均完全转化,则100kg该菱锰矿可以制备Mn O 的质
2 3
量为 kg。(结果保留3位有效数字)福州市八县(市)协作校2024-2025学年第一学期期中联考
高三 化学试卷化学试卷评分细则
1.本答案及评分说明供阅卷评分时参考,考生若给出其他正确答案,可适当给分。
2.化学方程式(包括离子方程式)中的化学式、离子符号答错,不得分;化学式、离子
符号书答正确但未配平、“↑”“↓”未标、必须书答的反应条件未答(或答错)、
化学用语书答规范错误的,每个化学方程式累计扣1 分。
3.文字表达题写不完整得一半分数。
题号 1 2 3 4 5 6 7 8 9 10
答案 C C B C A B B B A D
11(16分)(1)关闭
(2) 或 或
(3)
(4)装置D中白色固体恰好消失 防止Cl 过量使溶液呈酸性,导致 分解
2
除去A装置中残留的Cl
2
(5)不能
(6) E 乙醇
12(12分)(1)三颈烧瓶,
(2) ①防止CuBr受热分解,防止 溶解度减小反应速率慢 缓慢通入
(3)过量 , NaOH溶液,34,乙醇
13(15分)(1) 过滤(2) 2Fe²⁺ + H₂O₂ + 2H⁺ = 2Fe³⁺ + 2H₂O 将铁转化为沉淀而除去
(3)CaF、MgF
2 2
(4)
(5)71.08%
(6)
14(17分)(1) +3 FeO+6H+═2Fe3++3HO
2 3 2
适当提高硫酸浓度或将菱锰矿粉碎或适当升高温度或搅拌
(2) 将Fe2+氧化为Fe3+,便于后续除杂
(3) Fe(OH)、Al(OH)
3 3
(4)
(5)取少量最后一次洗涤液于洁净试管中,向其中滴加 BaCl 溶液,若不出现白色沉淀,
2
说明 MnOOH 已洗涤干净,反之则未洗涤干净
(6)151