文档内容
秘密★启用前
铜梁一中高 2026 届高二上期十月月考
化学试题卷
注意事项:
1.考试时间:75分钟,满分:100分。
2.所有题目必须在答题卡上作答,在试题卷、草稿纸上答题无效。
3.需要填涂的地方,一律用2B铅笔涂满涂黑。需要书写的地方一律用0.5mm黑色签字笔。
4.答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置上。
5.考试结束后,将试题卷和答题卡一并交回。
6.可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 Na 23 Fe 56
第I卷(选择题,共42分)
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一个
选项符合题目要求。)
1. 化学与人类生产生活密切相关,下列说法不正确的是
A. 开发地热能、太阳能、风能等新能源,减少对矿物能源的依赖
B. 研发催化剂将CO 还原为甲醇有利于碳中和目标的实现
2
C. 使用干冰进行人工降雨,固态干冰升华为CO(g)是吸热反应
2
D. 升温,能增大单位体积活化分子百分数,所以反应速率增大
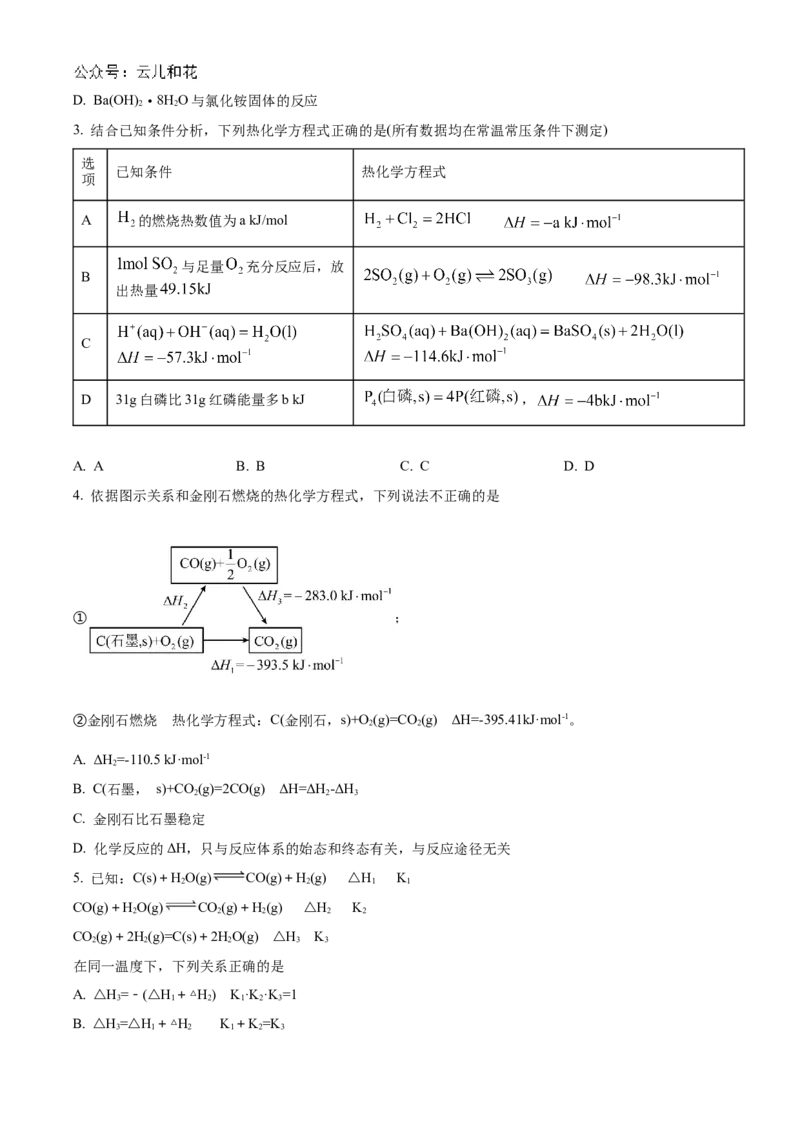
2. 如图是化学反应中物质变化和能量变化的示意图。若Ev(SO )
1 2 消耗 2 生成B. t 时刻之后,容器中混合气体的平均摩尔质量不变
2
C. OAB区域的面积代表了SO 浓度的减少量
2
D. t 时刻,反应达到限度,反应停止
3
13. 常温时,将10mL a mol/L Na AsO 、10mL a mol/L I 和10mL NaOH溶液混合,发生反应: (aq)
3 3 2
+I(aq)+2OH-(aq) (aq)+2I-(aq)+HO(l),溶液中 c(I-)与反应时间(t)的关系如图所示。下列不能
2 2
说明反应达到平衡状态的是
A. 溶液中OH-的浓度不再变化
B. v (I-)=2v ( )
正 逆
C. c( )=0.25b mol·L-1
D. 不再变化
14. 在某温度下,将含有H 和I 各0.1mol的混合气体充入容积为10L的密闭容器中,发生反应H(g)+I (g)
2 2 2 2
2HI(g) ΔH=-14.9kJ/ mol,充分反应并达到平衡后,测得c(H)=0.008mol/L,H 转化率为α(H ),反应
2 2 2
放热Q kJ。在上述温度下,再充入H 和I 各0.1mol,再次达到平衡后,c(H)=amol/L,下列说法正确的是
2 2 2
①该温度下上述反应的平衡常数K=0.25;②α (H )=20%;③Q=1.49;④a=0.008
, 2
.
A ①③ B. ①② C. ③④ D. ②③
第II卷(非选择题,共58分)
二、填空题
15. 研究化学反应中的能量变化和化学平衡有重要意义。回答下列问题:
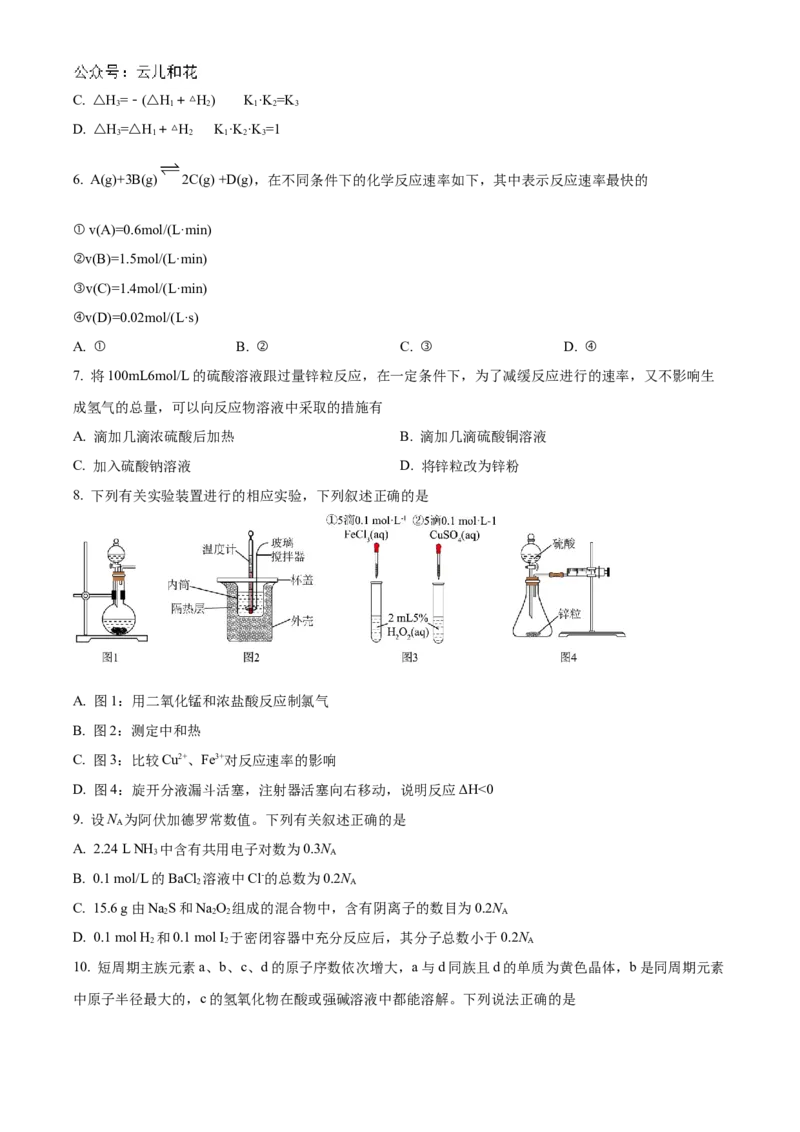
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:该反应的热化学方程式为___________。
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N 分子。N 分子结构如下图所示,
4 4
已知断裂1 mol N-N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,
N(g)=2N(g) ΔH=___________ kJ·mol-1。
4 2
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。298K时,已知:
①C(石墨,s)+O(g)=CO (g) ΔH=a kJ·mol-1
2 2 1
②2H(g)+O(g)=2HO(l) ΔH=b kJ·mol-1
2 2 2 2
③2C H(g)+5O(g)=4CO (g)+2HO(l) ΔH=c kJ·mol-1
2 2 2 2 2 3
则反应:2C(石墨,s)+H(g)=C H(g) 的焓变ΔH=___________ kJ·mol-1(用含a、b、c的式子表示)。
2 2 2
(4)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO (g) 的平衡常数K=0.25.
2
① t℃时,反应达到平衡时c(CO):c(CO)=___________;
2
② t℃时,若在1 L密闭容器中加入1.44 g FeO,并通入x mol CO,发生上述反应,达到平衡时FeO的转
化率为50%,则x=___________。
16. 某中学化学社团利用HC O 溶液和酸性KMnO 溶液反应来探究“条件对化学反应速率的影响”,实验时,
2 2 4 4
先分别量取下列溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应
的快慢。设计方案如下,其中t<t<t:
3 2 1
试管中所加试剂及用量(mL)
实
溶液褪至
验 温度
无色所需
编 0.6mol/LH C O 0.2mol/LKMnO 3mol/LHSO (℃)
2 2 4 4 2 4 HO 时间(min)
号 溶液 溶液 溶液 2
1 3.0 2.0 2.0 3.0 25 t
12 3.0 3.0 2.0 2.0 25 t
2
3 3.0 3.0 2.0 2.0 40 t
3
请回答:
(1)配制0.6mol/LH C O 溶液
2 2 4
①若实验中大约要使用480mLH C O 溶液,则需要称量HC O•2HO固体___________g。
2 2 4 2 2 4 2
②选择称量HC O•2HO固体所需要的仪器___________(填序号)。
2 2 4 2
名 量
托盘天平(带砝码) 小烧杯 坩埚钳 玻璃棒 药匙
称 筒
仪
器
序
a b c d e f
号
(2)已知反应后HC O 转化为CO 逸出,KMnO 转化为MnSO ,每消耗1molH C O 转移
2 2 4 2 4 4 2 2 4
___________mol电子。当观察到紫色刚好褪去,参加反应的HC O 和KMnO 的物质的量之比
2 2 4 4
n(H C O)∶n(KMnO)=___________。
2 2 4 4
(3)实验1测得KMnO 溶液的褪色时间为t=4 min,忽略混合前后溶液体积的变化,这段时间内平均反
4 1
应速率v(KMnO)=___________mol/(L·min)。
4
(4)根据表中的实验2和实验3数据,可以得到的结论是___________。
(5)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图a所示,但有同学查阅已有的实
验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应当如图b所示:
推测可能的原因是___________。
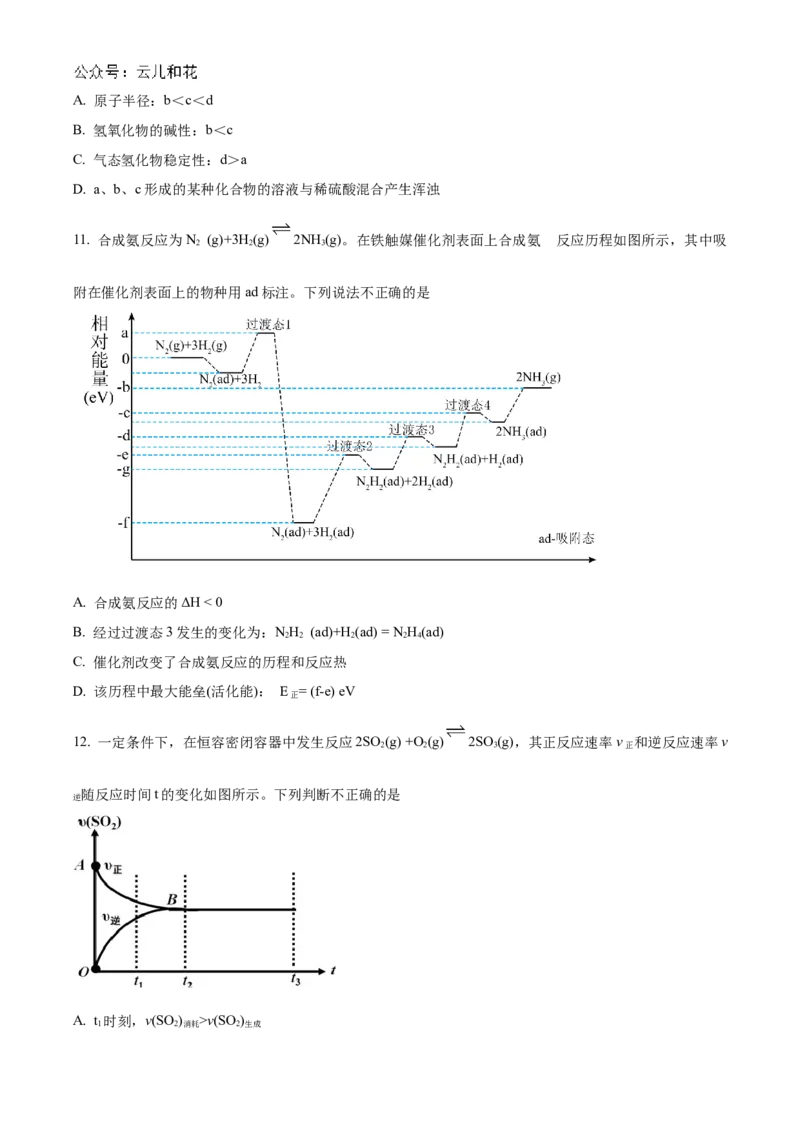
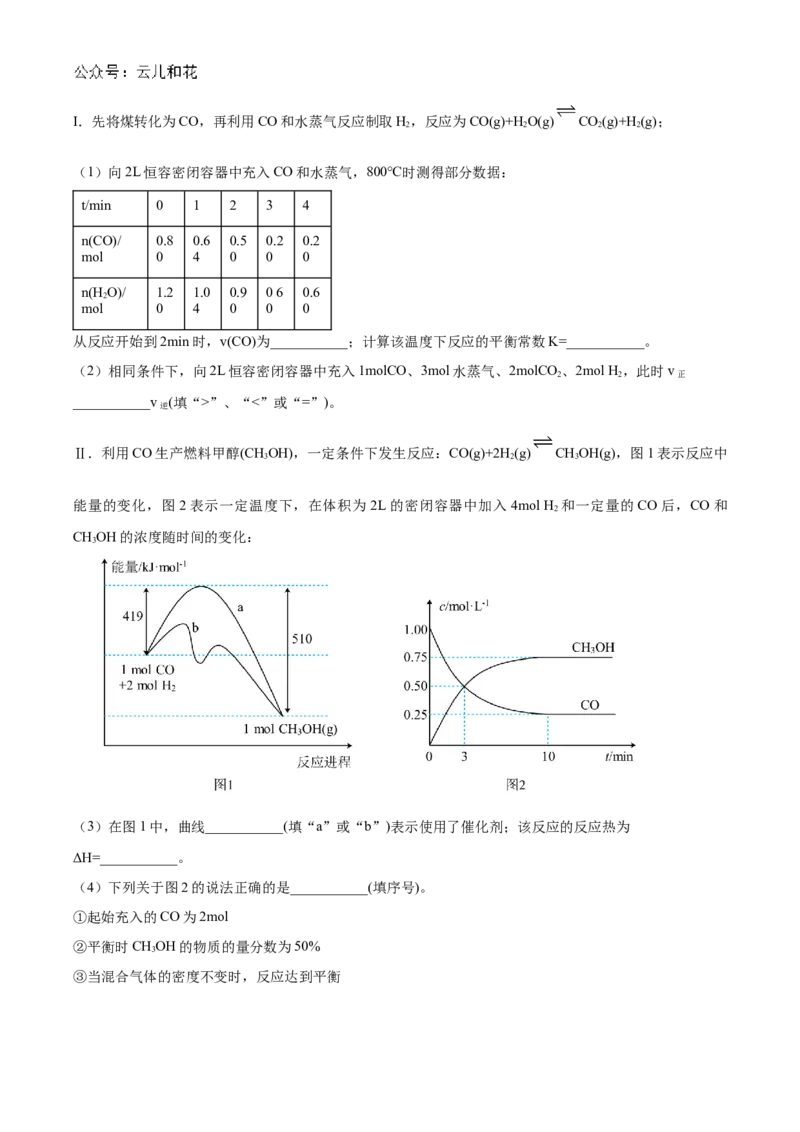
17. 我国煤炭资源丰富,通过煤的气化和液化。能使煤炭得以更广泛的应用。I.先将煤转化为CO,再利用CO和水蒸气反应制取H,反应为CO(g)+HO(g) CO(g)+H(g);
2 2 2 2
(1)向2L恒容密闭容器中充入CO和水蒸气,800℃时测得部分数据:
t/min 0 1 2 3 4
n(CO)/ 0.8 0.6 0.5 0.2 0.2
mol 0 4 0 0 0
.
n(H O)/ 1.2 1.0 0.9 06 0.6
2
mol 0 4 0 0 0
从反应开始到2min时,v(CO)为___________;计算该温度下反应的平衡常数K=___________。
(2)相同条件下,向2L恒容密闭容器中充入1molCO、3mol水蒸气、2molCO 、2mol H,此时v
2 2 正
___________v (填“>”、“<”或“=”)。
逆
Ⅱ.利用CO生产燃料甲醇(CHOH),一定条件下发生反应:CO(g)+2H(g) CHOH(g),图1表示反应中
3 2 3
能量的变化,图2表示一定温度下,在体积为2L的密闭容器中加入4mol H 和一定量的CO后,CO和
2
CHOH的浓度随时间的变化:
3
(3)在图1中,曲线___________(填“a”或“b”)表示使用了催化剂;该反应的反应热为
ΔH=___________。
(4)下列关于图2的说法正确的是___________(填序号)。
①起始充入的CO为2mol
②平衡时CHOH的物质的量分数为50%
3
③当混合气体的密度不变时,反应达到平衡④保持温度和容积不变,再充入2molCO和4mol H,再次达平衡时 会减小
2
(5)已知气体分压=气体总压×气体的物质的量分数,用平衡时气体分压代替平衡浓度可以计算出平衡常
数K,则上述温度下,当反应CO(g)+2H(g) CHOH(g)达到化学平衡时,气体总压为p,
p 2 3
K=___________(用含p的代数式表示)。
p
18. 利用黄铜矿(主要成分为CuFeS,含有SiO 等杂质)生产纯铜和绿矾(FeSO ·7H O),流程示意图如下。
2 2 4 2
(1)矿石在焙烧前需粉碎,其作用是___________。
(2)焙烧时,(NH )SO 发生热分解产生含NH 和SO 的高温气体,写出(NH )SO 发生热分解的化学方程
4 2 4 3 3 4 2 4
式___________。焙烧时SO 可以使矿石中的铜元素转化为CuSO 。
3 4
(3)从滤液C获得铜的方法在西汉《淮南万毕术》中就有描述“曾青得铁则化为铜”,写出反应的离子
方程式:___________。
(4)可以循环使用的物质是___________。(填化学式)
(5)操作X为蒸发浓缩至溶液表面出现晶膜,再___________,过滤,洗涤,干燥。