文档内容
D.1mol SiO 晶体中含有2N 个Si-O键(N 表示阿伏加德罗常数的值)
铁人中学 2023 级高二下学期开学考试 2 A A
4.只要善于观察和发现,化学之美随处可见。下列说法正确的是( )
A.舞台上干冰升华时,共价键断裂
化学试题
B.具有皇冠形状的S( )分子中S的杂化方式为sp2
8
时间:75分钟 满分:100分
C.晶莹剔透的水晶中也含有一定成分的离子键
D.气体单质中一定存在σ键,可能存在π键
可能用到的相对原子质量:H-1 C-12 N-14 O-16 O-19 Mg-24 Al-27 Ti-48 Cu-64
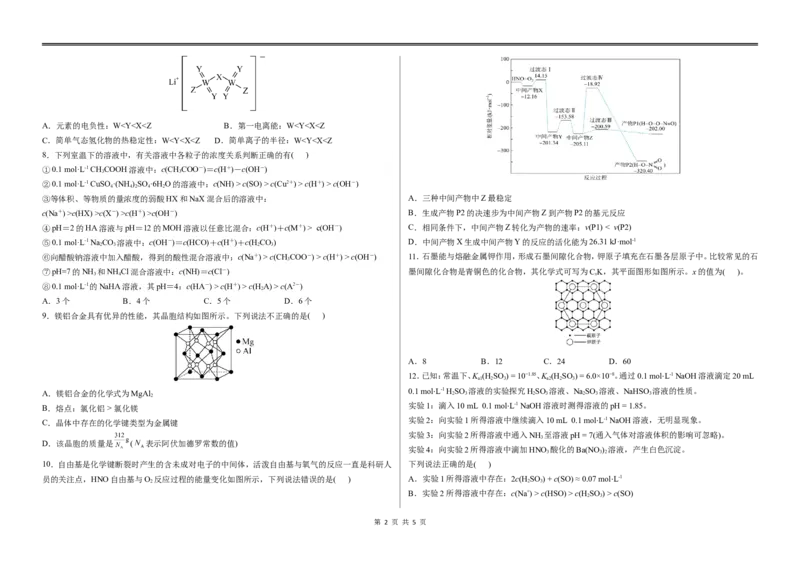
5.分子结构修饰是指不改变分子的主体骨架,保持分子的基本结构不变,仅改变分子结构中的某些
一、选择题(共15小题,每小题3分,共45分,每小题只有一个选项符合题意)
基团而得到新分子的过程,此法在药物设计与合成中有广泛的应用。如图为蔗糖分子修饰得到的三
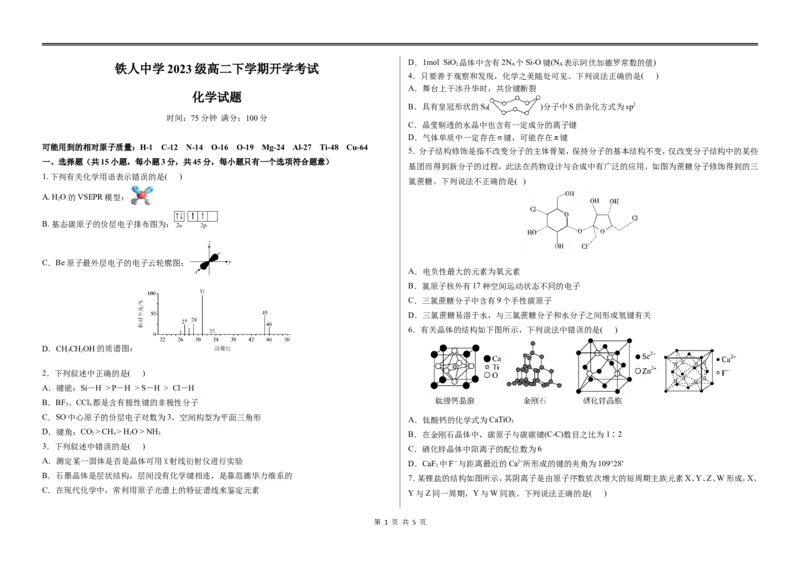
1. 下列有关化学用语表示错误的是( )
氯蔗糖。下列说法不正确的是( )
A. H O的VSEPR模型:
2
B. 基态碳原子的价层电子排布图为:
C.Be原子最外层电子的电子云轮廓图:
A.电负性最大的元素为氧元素
B.氯原子核外有17种空间运动状态不同的电子
C.三氯蔗糖分子中含有9个手性碳原子
D.三氯蔗糖易溶于水,与三氯蔗糖分子和水分子之间形成氢键有关
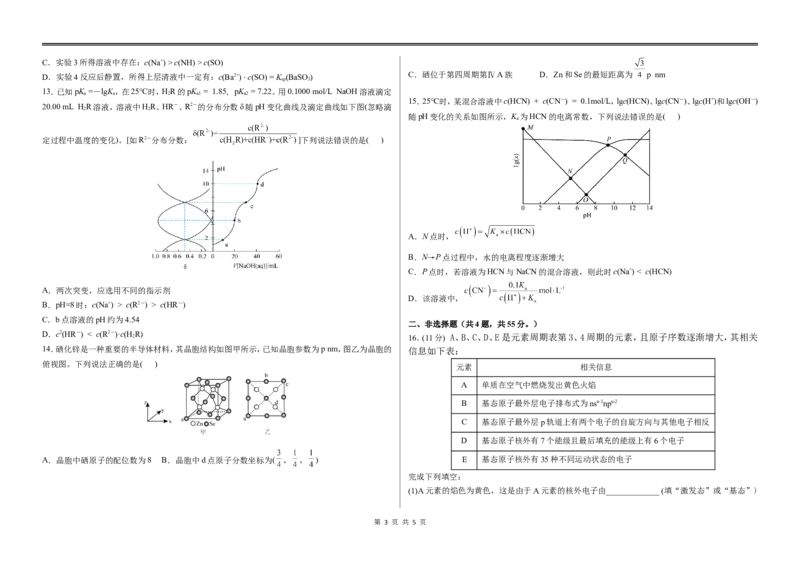
6.有关晶体的结构如下图所示,下列说法中错误的是( )
D.CHCHOH的质谱图:
3 2
2.下列叙述中正确的是( )
A.键能:Si-H > P-H > S-H > Cl-H
B.BF、CCl 都是含有极性键的非极性分子
3 4
C.SO中心原子的价层电子对数为3,空间构型为平面三角形
A.钛酸钙的化学式为CaTiO
3
D.键角:CO > CH > H O > NH
2 4 2 3 B.在金刚石晶体中,碳原子与碳碳键(C-C)数目之比为1∶2
3.下列叙述中错误的是( )
C.硒化锌晶体中阳离子的配位数为6
A.测定某一固体是否是晶体可用X射线衍射仪进行实验 D.CaF 中F-与距离最近的Ca2+所形成的键的夹角为109°28′
2
B.石墨晶体是层状结构,层间没有化学键相连,是靠范德华力维系的
7.某锂盐的结构如图所示,其阴离子是由原子序数依次增大的短周期主族元素X、Y、Z、W形成,X、
C.在现代化学中,常利用原子光谱上的特征谱线来鉴定元素
Y与Z同一周期,Y与W同族。下列说法正确的是( )
第 1 页 共 5 页A.元素的电负性:W c(SO) > c(Cu2+) > c(H+) > c(OH-)
4 4 2 4 2
③等体积、等物质的量浓度的弱酸HX和NaX混合后的溶液中: A.三种中间产物中Z最稳定
c(Na+) >c(HX) >c(X-) >c(H+) >c(OH-) B.生成产物P2的决速步为中间产物Z到产物P2的基元反应
④pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+) > c(OH-) C.相同条件下,中间产物Z转化为产物的速率:v(P1) < v(P2)
⑤0.1 mol·L-1 NaCO 溶液中:c(OH-)=c(HCO)+c(H+)+c(H CO) D.中间产物X生成中间产物Y的反应的活化能为26.31 kJ·mol-1
2 3 2 3
⑥向醋酸钠溶液中加入醋酸,得到的酸性混合溶液中:c(Na+) > c(CHCOO-) > c(H+) > c(OH-) 11.石墨能与熔融金属钾作用,形成石墨间隙化合物,钾原子填充在石墨各层原子中。比较常见的石
3
⑦pH=7的NH 和NH Cl混合溶液中:c(NH)=c(Cl-) 墨间隙化合物是青铜色的化合物,其化学式可写为CK,其平面图形如图所示。x的值为( )。
3 4 x
⑧0.1 mol·L-1的NaHA溶液,其pH=4:c(HA-) > c(H+) > c(H A) > c(A2-)
2
A.3个 B.4个 C.5个 D.6个
9.镁铝合金具有优异的性能,其晶胞结构如图所示。下列说法不正确的是( )
A.8 B.12 C.24 D.60
12.已知:常温下、K (H SO ) = 10−1.85、K (H SO ) = 6.0×10−8。通过0.1 molL-1 NaOH溶液滴定20 mL
a1 2 3 a2 2 3
A.镁铝合金的化学式为MgAl 2 0.1 molL-1 H 2 SO 3 溶液的实验探究H 2 SO 3 溶液、Na 2 SO 3 溶液、NaHSO 3 溶液 ⋅ 的性质。
B.熔点:氯化铝 > 氯化镁 实验1: ⋅ 滴入10 mL 0.1 molL-1 NaOH溶液时测得溶液的pH = 1.85。
C.晶体中存在的化学键类型为金属键 实验2:向实验1 所得溶液中 ⋅ 继续滴入10 mL 0.1 molL-1 NaOH溶液,无明显现象。
实验3:向实验2所得溶液中通入NH 至溶液pH = 7(通入气体对溶液体积的影响可忽略)。
3 ⋅
D.该晶胞的质量是 ( 表示阿伏加德罗常数的值)
实验4:向实验2所得溶液中滴加HNO 酸化的Ba(NO ) 溶液,产生白色沉淀。
3 3 2
10.自由基是化学键断裂时产生的含未成对电子的中间体,活泼自由基与氧气的反应一直是科研人 下列说法正确的是( )
员的关注点,HNO自由基与O 反应过程的能量变化如图所示,下列说法错误的是( ) A.实验1所得溶液中存在:2c(H SO ) + c(SO) ≈ 0.07 molL-1
2 2 3
B.实验2 所得溶液中存在:c(Na+) > c(HSO) > c(H SO ) > c(SO)
2 3 ⋅
第 2 页 共 5 页C.实验3所得溶液中存在:c(Na+) > c(NH) > c(SO)
D.实验4反应后静置,所得上层清液中一定有:c(Ba2+) c(SO) = K (BaSO) C.硒位于第四周期第ⅣA族 D.Zn和Se的最短距离为 p nm
sp 3
13.已知pK =-lgK,在25℃时,HR的pK = 1.85, pK = 7.22。用0.1000 mol/L NaOH溶液滴定
a a 2 a1 ⋅a2
15.25℃时,某混合溶液中c(HCN) + c(CN-) = 0.1mol/L,lgc(HCN)、lgc(CN-)、lgc(H+)和lgc(OH-)
20.00 mL HR溶液,溶液中HR、HR-、R2-的分布分数δ随pH变化曲线及滴定曲线如下图(忽略滴
2 2
随pH变化的关系如图所示,K 为HCN的电离常数,下列说法错误的是( )
a
定过程中温度的变化)。[如R2-分布分数: ]下列说法错误的是( )
A.N点时,
B.N→P点过程中,水的电离程度逐渐增大
C.P点时,若溶液为HCN与NaCN的混合溶液,则此时c(Na+)< c(HCN)
A.两次突变,应选用不同的指示剂
D.该溶液中,
B.pH=8时:c(Na+) > c(R2-) > c(HR-)
C.b点溶液的pH约为4.54
二、非选择题(共4题,共55分。)
D.c2(HR-) < c(R2-)·c(H 2 R) 16.(11分) A、B、C、D、E是元素周期表第3、4周期的元素,且原子序数逐渐增大,其相关
14.硒化锌是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞参数为p nm,图乙为晶胞的 信息如下表:
俯视图。下列说法正确的是( )
元素 相关信息
A 单质在空气中燃烧发出黄色火焰
B 基态原子最外层电子排布式为nsn-1npn-2
C 基态原子最外层p轨道上有两个电子的自旋方向与其他电子相反
D 基态原子核外有7个能级且最后填充的能级上有6个电子
A.晶胞中硒原子的配位数为8 B.晶胞中d点原子分数坐标为( , , ) E 基态原子核外有35种不同运动状态的电子
完成下列填空:
(1)A元素的焰色为黄色,这是由于A元素的核外电子由_____________ (填“激发态”或“基态”)
第 3 页 共 5 页跃迁到另一个状态时产生的光谱,该光谱属于_____________ (填“发射”或“吸收”)光谱。
(2)元素C在元素周期表中的位置是_____________,元素D位于元素周期表的________区。
(3)基态E原子有______种能量不同的电子,共占有_____________个原子轨道。
(4)A、B中第一电离能最大的是_____________ (填元素符号,下同),C、E中电负性较大的是
_____________。
已知:①金属离子生成氢氧化物沉淀所需的pH如图所示。
(5)与B元素成“对角线规则”关系的某短周期元素M的最高价氧化物对应水化物具有两性,写出
该两性化合物与A元素的最高价氧化物对应水化物反应的化学方程式:_____________,已知M元
素和C元素的电负性分别为1.5和3.0,则它们形成的化合物最可能是_____________ (填“离子”
或“共价”)化合物。
17.(16分) I.工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
2CO(g) + 6H(g) C HOH(g) + 3H O(g) ΔH < 0
2 2 2 5 2
(1)该反应的ΔS_____________ (填“>”、“<”或“=”)0;其正反应在_____________ (填“高温”、 ②25℃时,HF电离常数K=7.2×10-4, K (MgF)=7.4X10-11
a sp 2
“低温”或“任何温度”)下能自发进行。 (1)“酸浸”时,为提高浸出速率,可采取的措施有_____________ (写一条即可)。
(2)该反应的反应速率表达式为:v 正 = k 正 ·c2(CO 2 )·c6(H 2 ),v 逆 = k 逆 ·c(C 2 H 5 OH)·c3(H 2 O),其中k 正 、 (2)废渣 1 的主要成分是_____________ (填化学式)。“氧化”步骤中加入 H 2 O 2 的目的是
k 逆 为速率常数。则该反应的平衡常数K=_____________ (用含k 正 、k 逆 的代数式表示)。若其他条件不 _____________ (用离子方程式表示)。
变,降低温度,则下列推断合理的是_____________ (填标号)。 (3)25℃时,1 mol/L的NaF溶液中c(OH-)= _____________ (列出计算式即可) mol/L.
a.k 正 增大,k 逆 减小 b.k 正 减小,k 逆 增大 (4)已知沉淀前溶液中c(Mg2+)=1.85×10-3 mol/L,当除镁率达到99%时,溶液中c(F-)= _____mol/L.
c.k 减小的倍数大于k d.k 减小的倍数小于k 18. (14分)坦桑石是一种世界公认的新兴宝石,这种宝石于1967年首次在赤道雪山脚下的阿鲁沙地
正 逆 正 逆
H
(3)恒温时,向一密闭容器中充入2molCO 和6molH,发生上述反应, 2的平衡转化率( α )与压强的 区被发现。坦桑石的主要化学成分为Ca 2 Al 3 (SiO 4 ) 2 (OH),还可含有V、Cr、Mn等元素。
2 2
(1)下列状态的铝中,电离最外层的一个电子所需能量最大的是________(填序号)。
关系如图所示。
(2)烟酸铬是铬的一种化合物,其合成过程如下:
则此温度下,该反应的平衡常数K =___________ (气体的分压=气体总压强×气体的物质的量分数)。
p
II.某含镍(NiO)废料有FeO、Al O、 MgO、SiO 等杂质,用此提取NiSO 的工艺流程如图所示:
2 3 2 4
①Cr3+核外电子排布式为________。
第 4 页 共 5 页②H、C、N、O的电负性由大到小的顺序是________________。
③烟酸中碳、氮原子的杂化方式分别为________、________。
④分子中的大π键可用符号π表示,其中n表参与形成大π键的原子数,m表参与形成大π键的电子
数(如二氧化碳分子中的大π键可表示为 ),则烟酸中的大π键应表示为___________。
(3)SiCl 、SiF 都极易水解。SiCl 、SiF 都属于__________(填“极性”或“非极性”)分子,其熔点的
4 4 4 4
关系为SiCl ________(填“>”、“<”或“=”)SiF。
4 4
(4)氮化硼在一定条件下可以制得硼砂(Na B O·10H O),硼砂的阴离子化学式为B HO ,已知阴离
2 4 7 2 2 4
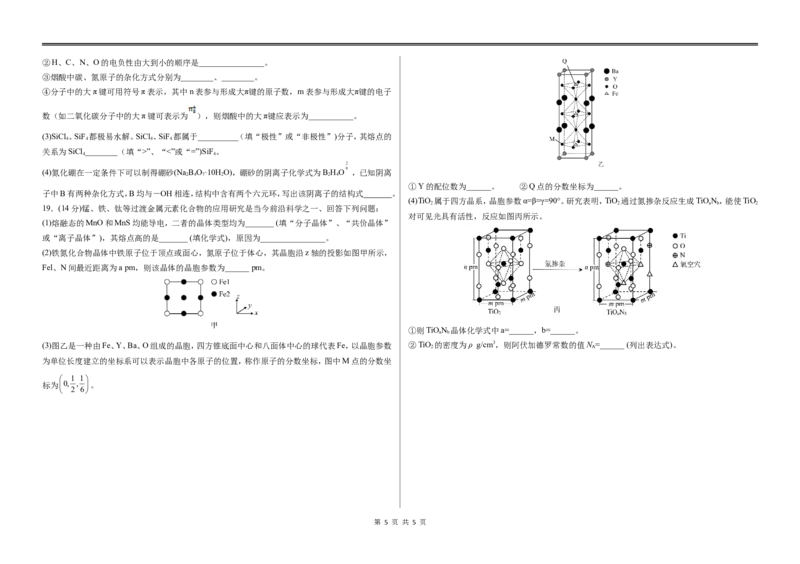
①Y的配位数为______。 ②Q点的分数坐标为______。
子中B有两种杂化方式,B均与-OH相连,结构中含有两个六元环,写出该阴离子的结构式 。
(4)TiO 属于四方晶系,晶胞参数α=β=γ=90°。研究表明,TiO 通过氮掺杂反应生成TiON,能使TiO
2 2 a b 2
19.(14分)锰、铁、钛等过渡金属元素化合物的应用研究是当今前沿科学之一、回答下列问题:
对可见光具有活性,反应如图丙所示。
(1)熔融态的MnO和MnS均能导电,二者的晶体类型均为_______ (填“分子晶体”、“共价晶体”
或“离子晶体”),其熔点高的是_______ (填化学式),原因为________________。
(2)铁氮化合物晶体中铁原子位于顶点或面心,氮原子位于体心,其晶胞沿z轴的投影如图甲所示,
Fel、N间最近距离为apm,则该晶体的晶胞参数为______ pm。
①则TiON 晶体化学式中a=______,b=______。
a b
(3)图乙是一种由Fe、Y、Ba、O组成的晶胞,四方锥底面中心和八面体中心的球代表Fe,以晶胞参数 ②TiO 的密度为ρ g/cm3,则阿伏加德罗常数的值N =______ (列出表达式)。
2 A
为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,图中M点的分数坐
1 1
标为0, , 。
2 6
第 5 页 共 5 页