文档内容
济宁市实验中学 2024-2025 学年高二下学期 3 月月
考化学试卷
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1、下列化学用语或图示正确的是
A. 溶液中的水合离子:
B. 的价层电子对互斥 模型:
C. 中的 键为 键
D.固体 中的链状结构:
2、下列说法不正确的是
A.纯碱和烧碱熔化时克服的化学键类型相同
B.加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
C.石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
D. 溶于水和干冰升华都只有分子间作用力改变
3、金属晶体中金属原子有三种常见的堆积方式,a、b、c分别代表这三种晶胞的结构,晶胞
a、b、c内金属原子个数比为( )
A.11∶8∶4 B.3∶2∶1
C.9∶8∶4 D.21∶14∶9
4、根据物质的组成和分类,下列晶体分类中正确的一组是选项 离子晶体 共价晶体 分子晶体 金属晶体
A. NH Cl Ar C H O 生铁
4 6 12 6
B. AlCl 石墨 S Hg
3
C. CHCOONa SiO C Fe
3 2 60
D. Ba(OH) 玛瑙 普通玻璃 Cu
2
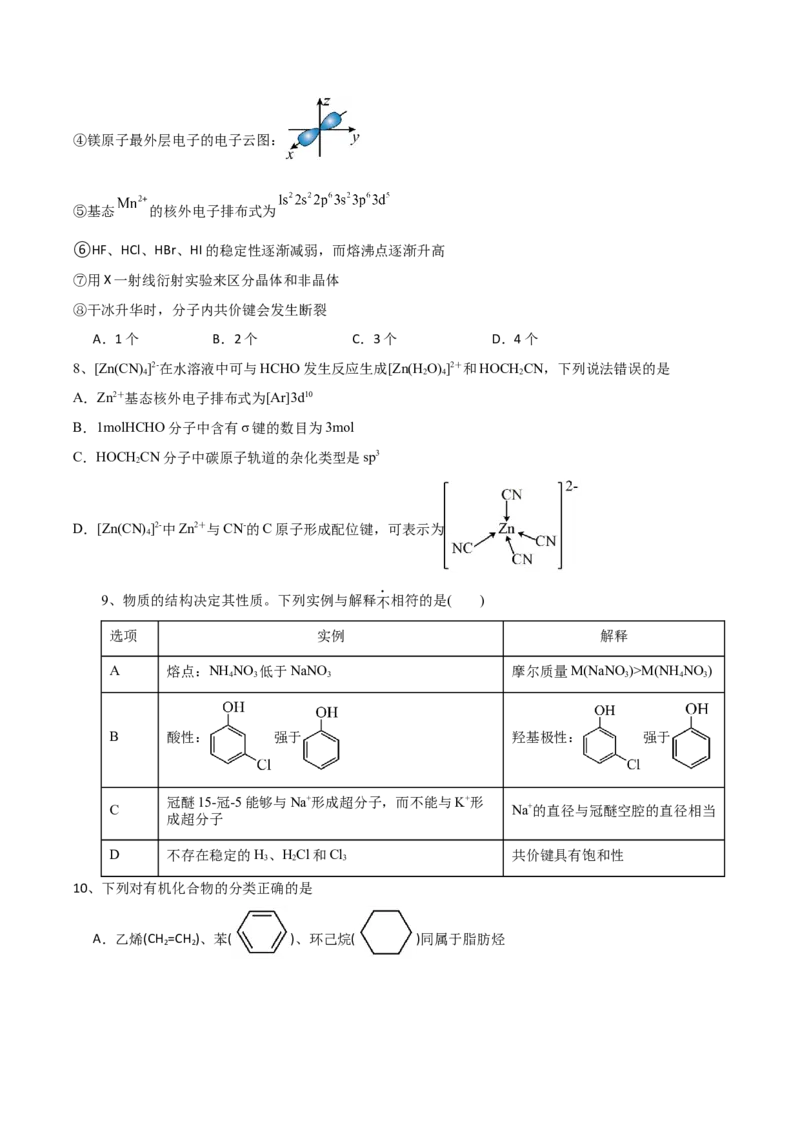
5、有关某些晶体的结构如图所示,下列说法不正确的是
在NaCl晶体中,距
铜晶体为面心立方最密堆 在6g二氧化硅晶体中, 该气态团簇分子的分子
Na+最近的Cl-形成正八
积,铜原子的配位数为4 硅氧键个数为0.4N 式为EF 或FE
面体 A 4 4 4 4
A B C D
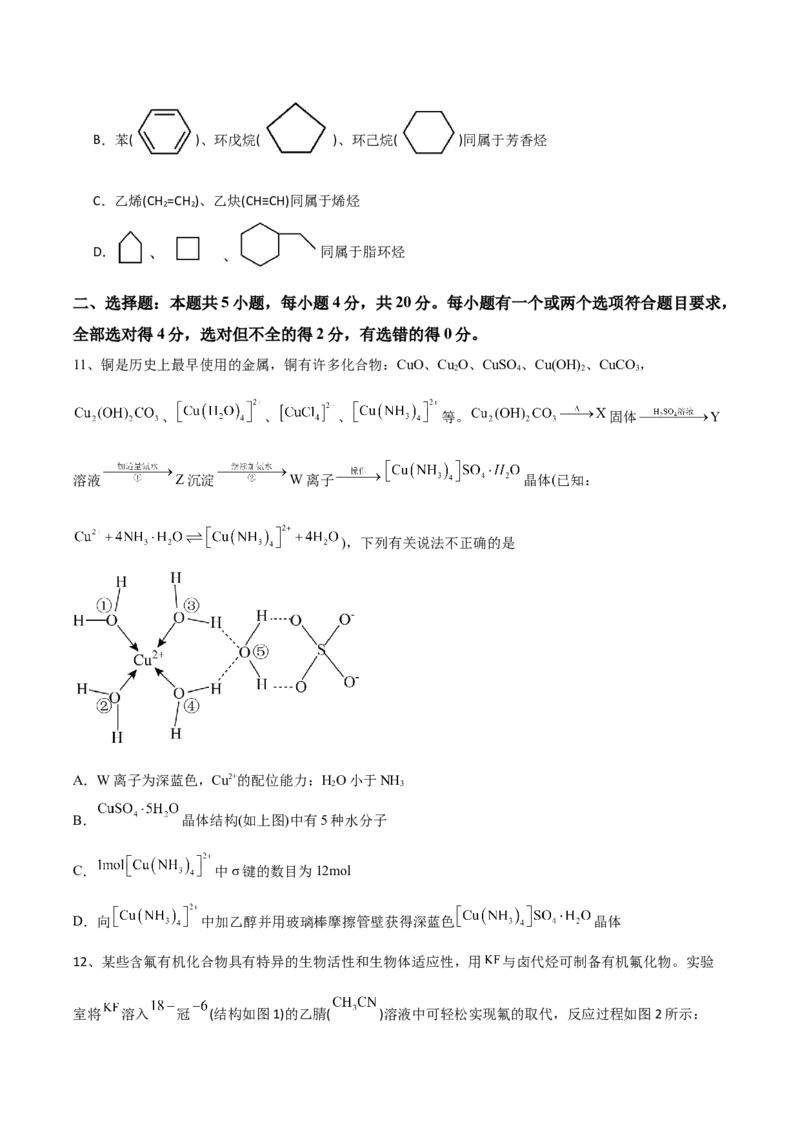
6、铁有δ、γ、α三种同素异形体,其晶胞结构如图所示,下列判断正确的是
A.δ、γ、α铁晶体中存在金属阳离子和阴离子
B. 晶胞中所含有的铁原子数为9
C.δ、α两种晶胞中铁原子周围等距离且最近的铁原子个数之比为3∶1
D.若 晶胞棱长为acm, 晶胞棱长为bcm,则两种晶体的密度比为
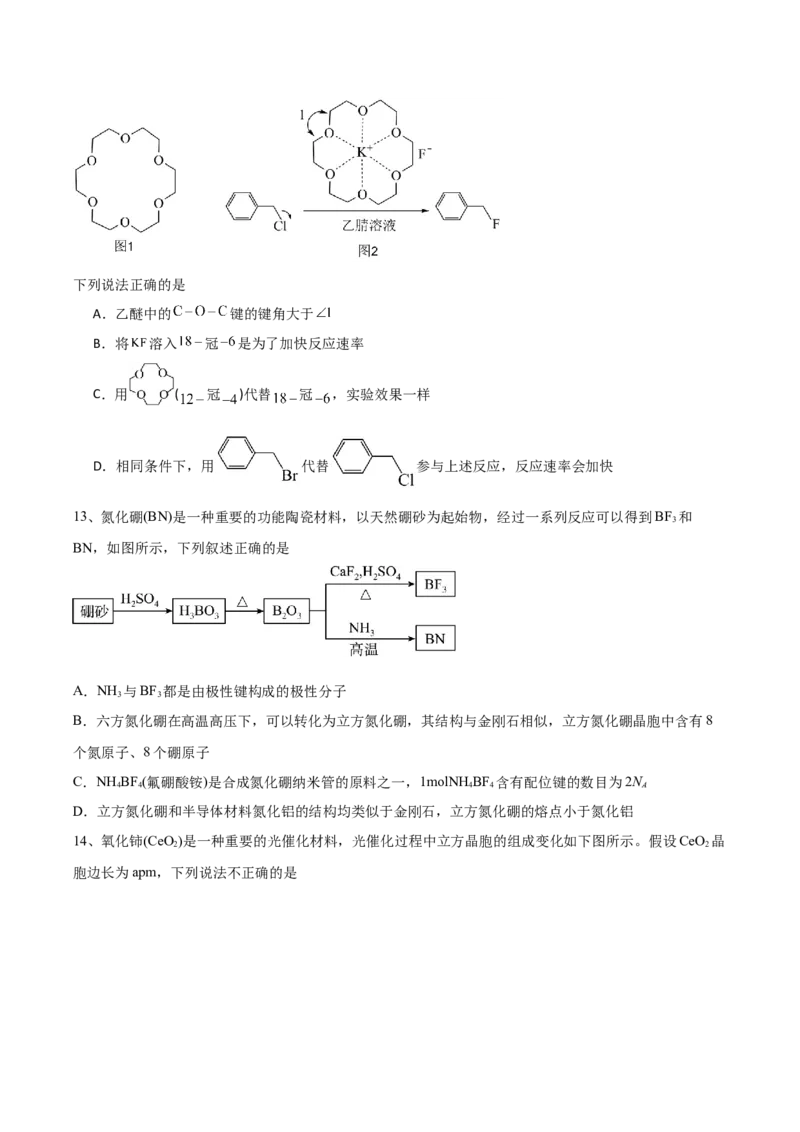
7、下列叙述中正确的个数有
①基态氧原子的电子排布图:
②处于最低能量状态原子叫基态原子, 过程中形成的是发射光谱
③所有元素中,氟的第一电离能最大④镁原子最外层电子的电子云图:
⑤基态 的核外电子排布式为
⑥HF、HCl、HBr、HI的稳定性逐渐减弱,而熔沸点逐渐升高
⑦用X一射线衍射实验来区分晶体和非晶体
⑧干冰升华时,分子内共价键会发生断裂
A.1个 B.2个 C.3个 D.4个
8、[Zn(CN) ]2-在水溶液中可与HCHO发生反应生成[Zn(HO) ]2+和HOCH CN,下列说法错误的是
4 2 4 2
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1molHCHO分子中含有σ键的数目为3mol
C.HOCH CN分子中碳原子轨道的杂化类型是sp3
2
D.[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,可表示为
4
9、物质的结构决定其性质。下列实例与解释不相符的是( )
选项 实例 解释
A 熔点:NH NO 低于NaNO 摩尔质量M(NaNO)>M(NH NO )
4 3 3 3 4 3
B 酸性: 强于 羟基极性: 强于
冠醚15-冠-5能够与Na+形成超分子,而不能与K+形
C Na+的直径与冠醚空腔的直径相当
成超分子
D 不存在稳定的H、HCl和Cl 共价键具有饱和性
3 2 3
10、下列对有机化合物的分类正确的是
A.乙烯(CH =CH )、苯( )、环己烷( )同属于脂肪烃
2 2B.苯( )、环戊烷( )、环己烷( )同属于芳香烃
C.乙烯(CH =CH )、乙炔(CH≡CH)同属于烯烃
2 2
D. 同属于脂环烃
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
11、铜是历史上最早使用的金属,铜有许多化合物:CuO、Cu O、CuSO 、Cu(OH) 、CuCO,
2 4 2 3
、 、 、 等。 固体 Y
溶液 Z沉淀 W离子 晶体(已知:
),下列有关说法不正确的是
A.W离子为深蓝色,Cu2+的配位能力:HO小于NH
2 3
B. 晶体结构(如上图)中有5种水分子
C. 中σ键的数目为12mol
D.向 中加乙醇并用玻璃棒摩擦管壁获得深蓝色 晶体
12、某些含氟有机化合物具有特异的生物活性和生物体适应性,用 与卤代烃可制备有机氟化物。实验
室将 溶入 冠 (结构如图1)的乙腈( )溶液中可轻松实现氟的取代,反应过程如图2所示:下列说法正确的是
A.乙醚中的 键的键角大于
B.将 溶入 冠 是为了加快反应速率
C.用 ( 冠 )代替 冠 ,实验效果一样
D.相同条件下,用 代替 参与上述反应,反应速率会加快
13、氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF 和
3
BN,如图所示,下列叙述正确的是
A.NH 与BF 都是由极性键构成的极性分子
3 3
B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化硼晶胞中含有8
个氮原子、8个硼原子
C.NH BF(氟硼酸铵)是合成氮化硼纳米管的原料之一,1molNH BF 含有配位键的数目为2N
4 4 4 4 A
D.立方氮化硼和半导体材料氮化铝的结构均类似于金刚石,立方氮化硼的熔点小于氮化铝
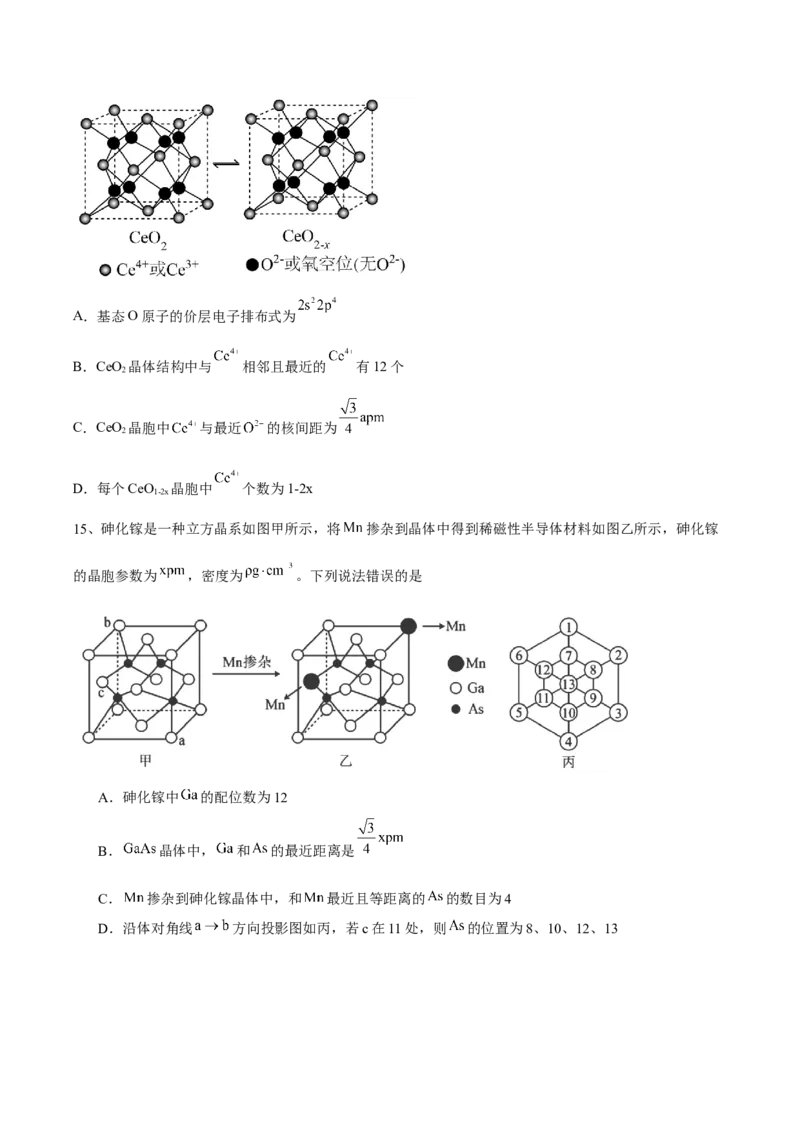
14、氧化铈(CeO)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如下图所示。假设CeO 晶
2 2
胞边长为apm,下列说法不正确的是A.基态O原子的价层电子排布式为
B.CeO 晶体结构中与 相邻且最近的 有12个
2
C.CeO 晶胞中 与最近 的核间距为
2
D.每个CeO 晶胞中 个数为1-2x
1-2x
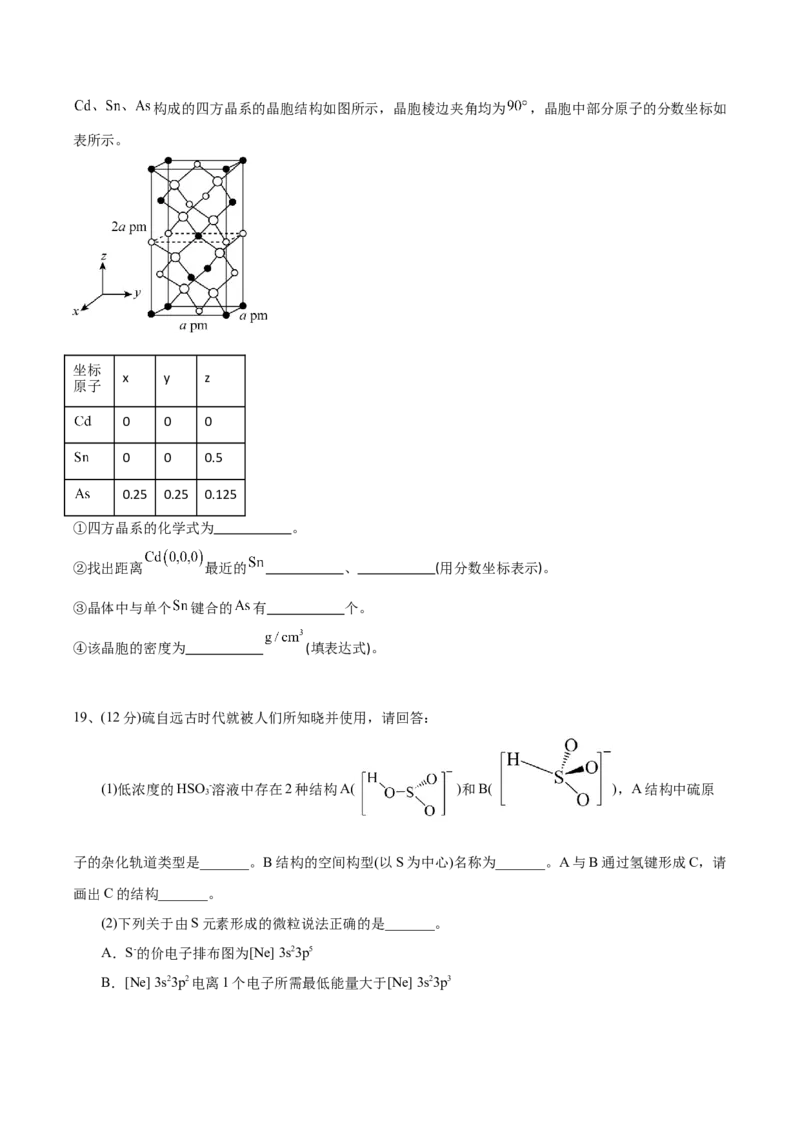
15、砷化镓是一种立方晶系如图甲所示,将 掺杂到晶体中得到稀磁性半导体材料如图乙所示,砷化镓
的晶胞参数为 ,密度为 。下列说法错误的是
A.砷化镓中 的配位数为12
B. 晶体中, 和 的最近距离是
C. 掺杂到砷化镓晶体中,和 最近且等距离的 的数目为4
D.沿体对角线 方向投影图如丙,若c在11处,则 的位置为8、10、12、13三、非选择题:本题共5小题,共60分
16、(12分)
(1)现有下列5种有机化合物:
A. B.
C. D. E.
其中:
①可以看作醇类的是 (填字母,下同)。
②可以看作酚类的是 。
③可以看作羧酸类的是 。
④可以看作酯类的是 。
(2)某有机化合物的键线式为 ,含有的官能团名称为 ,它属于 (填“芳
香族化合物”或“脂环化合物”)。
17、(12分)过氧乙酸又名过醋酸(C HO),是重要化工原料。也是一种绿色生态杀菌剂,其制法为
2 4 3
CHCOOH+H O=CH COOOH+H O。
3 2 2 3 2
(1)某同学写出了碳原子的4种不同状态的电子排布图,表示基态碳原子的是 。
A. B.
C. D.
其中能量最低的是 (填标号),电子由状态C到状态B所得到的光谱为光谱(填“原子发射”或“原子吸收”)。
(2)过氧乙酸分子中C原子的杂化方式有 。
(3)乙酸比乙醇易电离出H+的原因 。
(4)造纸中,用NaBH 与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化
4
铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如表所示:
硼氢化物 NaBH Al(BH)
4 4 3
熔点/℃ 400 -64.5
解释表中两种物质熔点差异的原因 。
②硼氢化钠晶胞结构如图所示,该晶体中Na+的配位数为 。已知:硼氢化钠晶体的密度
为ρg·cm-3,N 代表阿伏加德罗常数的值,则a= nm(用含ρ、N 的最简式子表示)
A A
18、完成下列问题。
(1)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观
结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为________。
(2)在硼酸盐中,阴离子有链状、环状等多种结构形式。如图是一种链状结构的多硼酸根,则多硼酸根的离
子符号为________。
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。由构成的四方晶系的晶胞结构如图所示,晶胞棱边夹角均为 ,晶胞中部分原子的分数坐标如
表所示。
坐标
x y z
原子
0 0 0
0 0 0.5
0.25 0.25 0.125
①四方晶系的化学式为 。
②找出距离 最近的 、 (用分数坐标表示)。
③晶体中与单个 键合的 有 个。
④该晶胞的密度为 (填表达式)。
19、(12分)硫自远古时代就被人们所知晓并使用,请回答:
(1)低浓度的HSO -溶液中存在2种结构A( )和B( ),A结构中硫原
3
子的杂化轨道类型是_______。B结构的空间构型(以S为中心)名称为_______。A与B通过氢键形成C,请
画出C的结构_______。
(2)下列关于由S元素形成的微粒说法正确的是_______。
A.S-的价电子排布图为[Ne] 3s23p5
B.[Ne] 3s23p2电离1个电子所需最低能量大于[Ne] 3s23p3C. 的氧化性强于
D.[Ne] 3s13p44s1的发射光谱不止1条谱线
(3)CuS的晶胞如图所示,该图中缺失了部分硫原子,请在如图上用白球或黑球将缺失的原子补齐
_______,该晶胞内含有Cu原子为_______个,其中配位4个硫原子的Cu原子有_______个。
20.(12分)配合物在工农业生产中有广泛应用。
(1)铁的一种配合物的化学式为 ,配体Htrz为三氮唑( )。
①基态Fe2+与Fe3+中未成对的电子数之比为 。
②阴离子ClO -的键角 ClO -的键角(填“等于”“大于”或“小于”)。
4 3
③配体三氮唑( )中配位原子是 ,碳原子的杂化方式为 。
④三氮唑沸点为260℃,与其结构类似的环戊二烯沸点为42.5℃,三氮唑沸点明显偏高的原因是
。
(2)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。 属
于正交晶系(长方体形)。晶胞参数为 。如图为沿z轴投影的晶胞中所有氯原子的分布
图和原子分数坐标。①据此推断该晶胞中氯原子数目为 。 的摩尔质量为 ,晶胞密度为 ,
则阿伏加德罗常数的值 为 (列出计算表达式,后同)。
②图中A、B两原子的核间距为 。