文档内容
2024-2025 学年高二化学上学期期中模拟卷
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.选出小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选
涂其他答案标号。写在本试卷上无效。
3.回答时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第1~3章(沪科版2020)。
5.难度系数:0.60。
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 N14 O16 Na23 Mg24 Al27 S32 Cl35.5
一、中和热的测定(22 分)
1.按要求回答问题。
Ⅰ.中和热的测定:
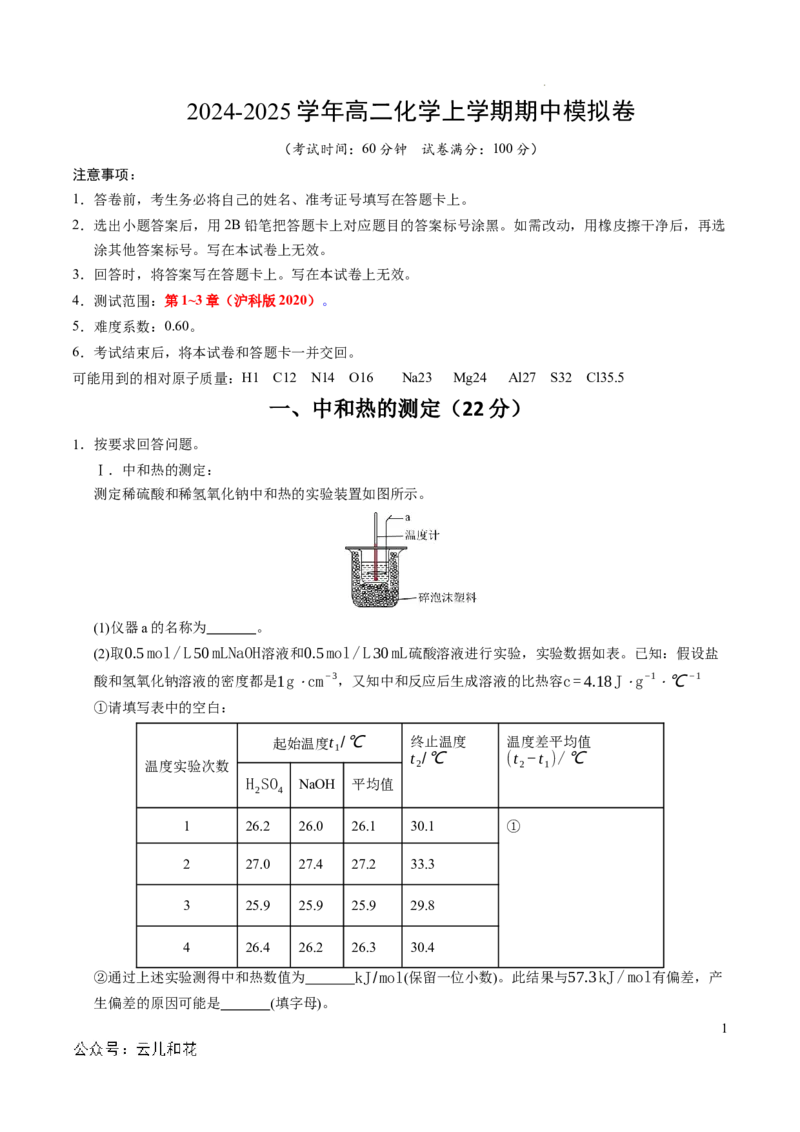
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(1)仪器a的名称为 。
(2)取0.5mol/L50mLNaOH溶液和0.5mol/L30mL硫酸溶液进行实验,实验数据如表。已知:假设盐
酸和氢氧化钠溶液的密度都是1g⋅cm−3,又知中和反应后生成溶液的比热容c=4.18J⋅g−1 ⋅℃−1
①请填写表中的空白:
起始温度t /℃ 终止温度 温度差平均值
1
t /℃ (t −t )/℃
温度实验次数 2 2 1
H SO NaOH 平均值
2 4
1 26.2 26.0 26.1 30.1 ①
2 27.0 27.4 27.2 33.3
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
②通过上述实验测得中和热数值为 kJ/mol(保留一位小数)。此结果与57.3kJ/mol有偏差,产
生偏差的原因可能是 (填字母)。
1
学科网(北京)股份有限公司a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时,俯视容量瓶刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时,倒出溶液后用少量水洗涤量筒,将洗涤液再倒入装置中
③下列有关反应热说法错误的是 。
A.中和热测定的装置中,填充碎泡沫、内外烧杯口齐平的目的都是减少热量损失
B.已知:H+ (aq)+OH− (aq)=H O(l) ΔH=−57.3kJ⋅mol−1,则NaOH稀溶液与稀醋酸生成
2
1mol水时,反应热数值偏小
C.已知:H (g)+I (g)⇌2HI(g) ΔH=−akJ⋅mol−1,则1mol I (g)和1mol H (g)充分反应,
2 2 2 2
放出的热量小于a kJ
D.25℃时,甲烷摩尔燃烧焓的热化学方程式可表示为:CH (g)+2O (g)=CO (g)+2H O(g)
4 2 2 2
ΔH=−890.31kJ⋅mol−1
Ⅱ.某探究性学习实验小组做了如下实验:利用HC O 溶液和酸性KMnO 溶液之间的反应来探究外界
2 2 4 4
条件改变对化学反应速率的影响。
实验温 KMnO 溶液(硫酸酸 溶液颜色褪至无色时
4 HC O 溶液 HO
度/K 化) 2 2 4 2 所需时间/s
实验
序号
V/mL c/mol⋅L−1 V/mL c/mol⋅L−1 V/mL
A 293 2 0.02 5 0.1 3 t
1
B T 2 0.02 3 0.1 V 8
1 1
C 313 2 0.02 V 2 0.1 5 t 2
(3)通过实验A、B,可探究 的改变对反应速度的影响,其中V = ,T = ;通过
1 1
实验 可探究出温度变化对化学反应速度的影响。
(4)对照实验A和B,时间t 的范围为:t 8(填“<”“>”或“=”);利用实验B中数据计算,用
1 1
KMnO 的浓度变化表示的反应速率为υ(H C O )= mol⋅L−1 ⋅s−1。
4 2 2 4
二、有害烟道气的治理(19 分)
2.烟道气中含氧NO、NO 、SO 等多种有害气体,合理治理烟道气具有重要意义。
2 2
(1)烟道气中的氮氧化物与悬浮在大气中海盐粒子相互作用时,涉及如下反应:
2NO (g)+NaCl(s)⇌ NaNO (s)+ClNO(g) ΔH
2 3 1
2NO(g)+Cl (g)⇌2ClNO(g) ΔH
2 2
2
学科网(北京)股份有限公司则反应:4NO (g)+2NaCl(s)⇌2NaNO (s)+2NO(g)+Cl (g) ΔH = (用含ΔH 、ΔH 的
2 3 2 3 1 2
式子表示)。
(2)利用CO可将NO转化为无害的N ,其反应为:2NO(g)+2CO(g)⇌ N (g)+2CO (g)。在容积均为2L
2 2 2
的甲、乙两个恒温(反应温度分别为300℃、T℃)恒容密闭容器中,分别加入物质的量之比为1:1的
NO和CO,测得各容器中n(CO)(单位:mol)随反应时间t的变化情况如下表所示:
t/min 0 40 80 120 160
甲(300℃) 2.00 1.50 1.10 0.80 0.80
乙(T℃) 2.00 1.45 1.00 1.00 1.00
①该反应的△H 0(填“>”或“<”)。
②甲容器达平衡时,体系的压强与反应开始时体系的压强之比为 。
③乙容器反应达到平衡后,若容器内各物质的物质的量均增加1倍,则平衡 (填“正向”、“逆
向”或“不”)移动。
(3)对烟道气中的SO 进行回收再利用具有较高的社会价值和经济价值。
2
其反应为:2CO(g)+SO (g)⇌ S(s)+2CO (g)
2 2
①写出该反应平衡常数表达式 。
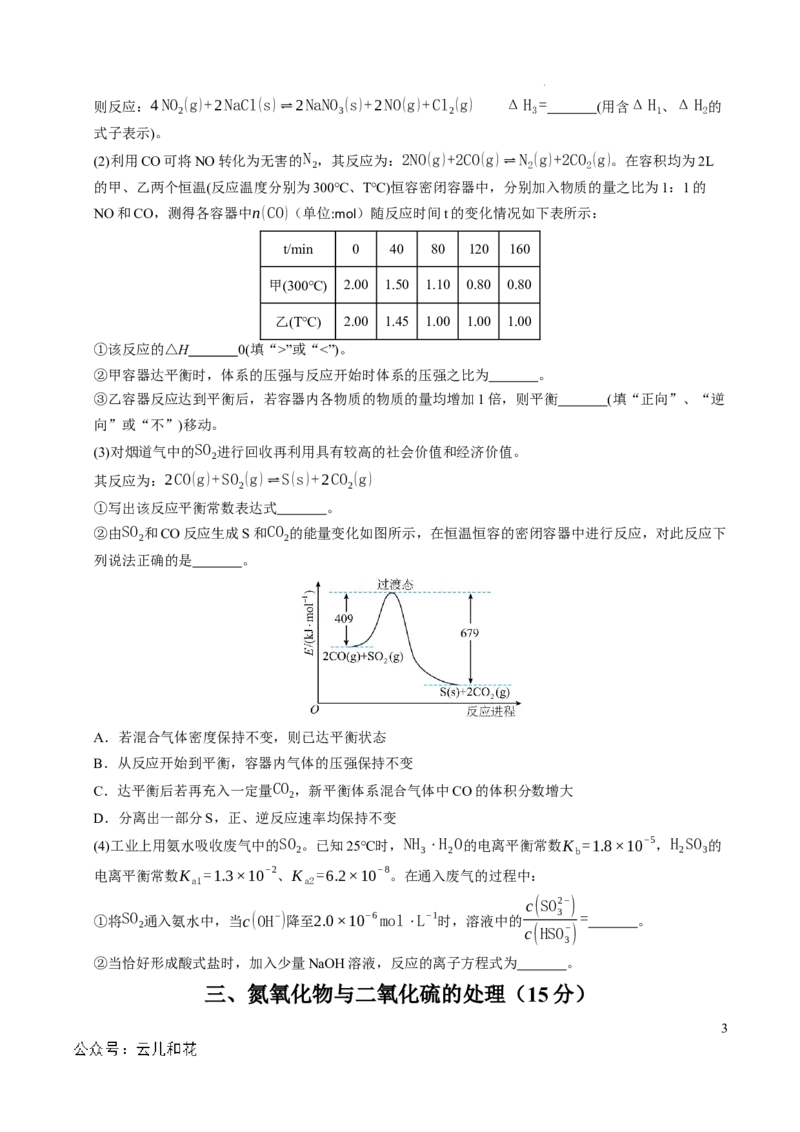
②由SO 和CO反应生成S和CO 的能量变化如图所示,在恒温恒容的密闭容器中进行反应,对此反应下
2 2
列说法正确的是 。
A.若混合气体密度保持不变,则已达平衡状态
B.从反应开始到平衡,容器内气体的压强保持不变
C.达平衡后若再充入一定量CO ,新平衡体系混合气体中CO的体积分数增大
2
D.分离出一部分S,正、逆反应速率均保持不变
(4)工业上用氨水吸收废气中的SO 。已知25℃时,NH ⋅H O的电离平衡常数K =1.8×10−5,H SO 的
2 3 2 b 2 3
电离平衡常数K =1.3×10−2、K =6.2×10−8。在通入废气的过程中:
a1 a2
c(SO2−)
①将SO 通入氨水中,当c(OH−)降至2.0×10−6mol⋅L−1时,溶液中的 3 = 。
2 c(HSO−)
3
②当恰好形成酸式盐时,加入少量NaOH溶液,反应的离子方程式为 。
三、氮氧化物与二氧化硫的处理(15 分)
3
学科网(北京)股份有限公司3.研究处理NO 、SO ,对环境保护有着重要的意义。回答下列问题:
x 2
(1)已知:2SO
2
(g)+O
2
(g)⇌2SO
3
(g) ΔH
1
=−196.6kJ⋅mol−1
2NO(g)+O
2
(g)⇌2NO
2
(g) ΔH
2
=−113.0kJ⋅mol−1
则反应NO
2
(g)+SO
2
(g)⇌SO
3
(g)+NO(g)的ΔH= kJ⋅mol−1。
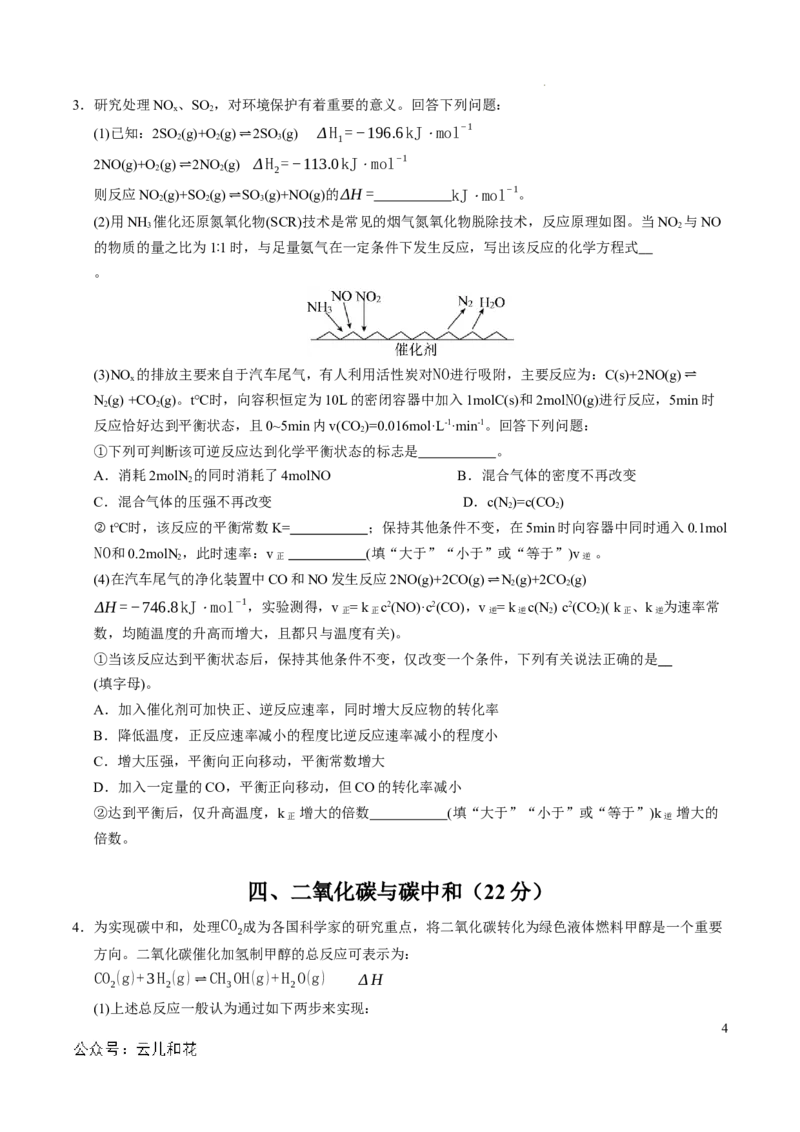
(2)用NH 催化还原氮氧化物(SCR)技术是常见的烟气氮氧化物脱除技术,反应原理如图。当NO 与NO
3 2
的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应,写出该反应的化学方程式
。
(3)NO
x
的排放主要来自于汽车尾气,有人利用活性炭对NO进行吸附,主要反应为:C(s)+2NO(g)⇌
N(g)+CO (g)。t℃时,向容积恒定为10L的密闭容器中加入1molC(s)和2molNO(g)进行反应,5min时
2 2
反应恰好达到平衡状态,且0~5min内v(CO)=0.016mol·L-1·min-1。回答下列问题:
2
①下列可判断该可逆反应达到化学平衡状态的标志是 。
A.消耗2molN 的同时消耗了4molNO B.混合气体的密度不再改变
2
C.混合气体的压强不再改变 D.c(N)=c(CO )
2 2
② t℃时,该反应的平衡常数K= ;保持其他条件不变,在5min时向容器中同时通入0.1mol
NO和0.2molN,此时速率:v (填“大于”“小于”或“等于”)v 。
2 正 逆
(4)在汽车尾气的净化装置中CO和NO发生反应2NO(g)+2CO(g)⇌N
2
(g)+2CO
2
(g)
ΔH=−746.8kJ⋅mol−1,实验测得,v = k c2(NO)·c2(CO),v = k c(N)c2(CO)( k 、k 为速率常
正 正 逆 逆 2 2 正 逆
数,均随温度的升高而增大,且都只与温度有关)。
①当该反应达到平衡状态后,保持其他条件不变,仅改变一个条件,下列有关说法正确的是
(填字母)。
A.加入催化剂可加快正、逆反应速率,同时增大反应物的转化率
B.降低温度,正反应速率减小的程度比逆反应速率减小的程度小
C.增大压强,平衡向正向移动,平衡常数增大
D.加入一定量的CO,平衡正向移动,但CO的转化率减小
②达到平衡后,仅升高温度,k 增大的倍数 (填“大于”“小于”或“等于”)k 增大的
正 逆
倍数。
四、二氧化碳与碳中和(22 分)
4.为实现碳中和,处理CO 成为各国科学家的研究重点,将二氧化碳转化为绿色液体燃料甲醇是一个重要
2
方向。二氧化碳催化加氢制甲醇的总反应可表示为:
CO (g)+3H (g)⇌ CH OH(g)+H O(g) ΔH
2 2 3 2
(1)上述总反应一般认为通过如下两步来实现:
4
学科网(北京)股份有限公司i.CO (g)+H (g)⇌ CO(g)+H O(g) ΔH =+41kJ/mol
2 2 2 1
ii.CO(g)+2H (g)⇌ CH OH(g) ΔH =−90kJ/mol
2 3 2
根据盖斯定律,总反应的ΔH= kJ/mol,总反应能在 (填“高温”或“低温”)下自
发进行。
(2)在一恒温、体积为2L的恒容密闭容器中,充入1 molCO (g)和4 mol H (g)发生反应CO (g)+3H (g)
2 2 2 2
⇌
CH OH(g)+H O(g),初始压强为8MPa,10min时测得体系的压强为6.4MPa且不再随时间变化。
3 2
①0~10min内,v(CO )= mol⋅L−1 ⋅min−1。
2
②该温度下的压强平衡常数K = MPa−2 [用平衡分压代替平衡浓度计算,分压=(总压×物质
a
的量分数)]。
n(H )
(3)二氧化碳催化加氢制甲醇的总反应在起始物 2 =3时,在不同条件下达到平衡,设体系中甲醇的
n(CO )
2
物质的量分数为x(CH OH),在t=250℃下的x(CH OH)~p,在p=5×105Pa下的x(CH OH)~t如图所
3 3 3
示。
①图中对应等温过程的曲线是 (填“a”或“b”),判断的理由是 。
②当x(CH OH)=0.10时,CO 的平衡转化率= (填分数),反应条件可能为 或
3 2
。
(4)研究发现,CO 加氢还可制备甲酸(HCOOH),反应为CO (g)+H (g)⇌ HCOOH(g) ΔH<0。在一
2 2 2
容积固定的密闭容器中进行反应,实验测得:v =k c(CO )⋅c(H ),v =k c(HCOOH),k ,k
正 正 2 2 逆 逆 正 逆
为速率常数。温度为T ℃时,该反应的平衡常数K=2,温度为T ℃时,k =1.9k ,则T ℃时平衡
1 2 正 逆 2
压强 (填“>”“<”或“=”)T ℃时平衡压强。
1
(5)CO 加氢制备CH 的一种催化机理如图,下列说法中正确的是 (填字母标号)。
2 4
5
学科网(北京)股份有限公司A.催化过程使用的催化剂为La O 和La O CO
2 3 2 2 3
B.La O CO 可以释放出CO *(活化分子)
2 2 3 2
C.H 经过Ni活性中心裂解产生活化态H*的过程为放热过程
2
D.CO 加氢制备CH 的过程需要La O 和Ni共同完成
2 4 2 3
五、常见酸性物质的电离平衡(22 分)
5.T℃下,下列物质的电离平衡常数如表。按要求回答下列问题(均T℃下)。
化学式 CH COOH H CO HF H O
3 2 3 2
K 或 1.6×10−5 K =4.4×10−7 7.2×10−4 9.9×10−15
a a1
K K =4.7×10−11
w a2
(1)取1mL0.1mol/L醋酸于试管中,向其中加入2滴0.1mol/LHCl溶液。CH COOH的电离平衡将
3
(填“正向移动”“逆向移动”或“不移动”); K(CH COOH) 1.6×10−5(填“>”“<”或“=”)。
3
(2)向1mL0.10mol/LCH COOH溶液中滴入1mL0.10mol/LNaOH溶液,充分反应,至T℃,测得反应
3
后溶液的pH=9。
①此时溶液中由水电离出来的c(OH−)= mol/L。
②此时溶液中各离子的浓度由大到小的顺序是 。
(3)醋酸初始c(CH COOH)=0.010mol/L,则达电离平衡时溶液中c(H+)= mol/L。
3
(4)CH COO−、CO2−、F−、OH-结合H+的能力由强到弱的顺序是 。
3 3
(5)已知①HF(aq)+OH− (aq)=F− (aq)+H O(l) ΔH=−67.7kJ/mol
2
②H+ (aq)+OH− (aq)=H O(l) ΔH=−57.3kJ/mol
2
写出HF的电离过程的热化学方程式: 。
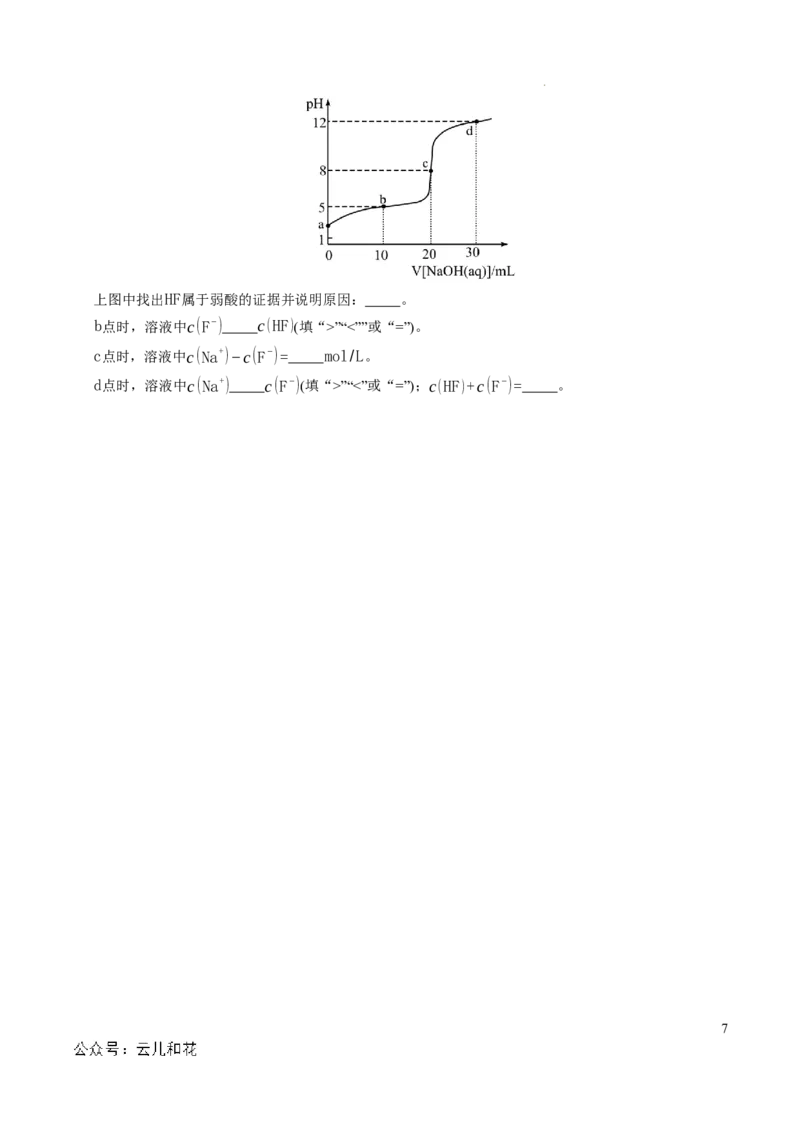
(6)T℃下,在20mL0.1mol/LHF溶液中加入V mL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线
如下图所示。
6
学科网(北京)股份有限公司上图中找出HF属于弱酸的证据并说明原因: 。
b点时,溶液中c(F−) c(HF)(填“>”“<””或“=”)。
c点时,溶液中c(Na+)−c(F−)= mol/L。
d点时,溶液中c(Na+) c(F−)(填“>”“<”或“=”);c(HF)+c(F−)= 。
7
学科网(北京)股份有限公司