文档内容
2024-2025 学年高二化学上学期第一次月考卷
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.选出选择题每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.测试范围:1-2章(沪科版2020选择性必修1)。
4.难度系数:0.60
5.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Na 11 C 12 N 14 O 16 S 32
一、氢气与一氧化碳合成甲醇(15分)
1.综合利用CO、CO对实现“零排放”有重要意义。H 和CO合成甲醇反应为:
2 2
催化剂
CO(g)+2H (g)
⇌
CH OH(g) 。回答下列问题:
2 3
Δ
(1)决定化学反应速率的主要因素是_______。
A.温度和压强 B.反应物浓度 C.反应物自身的性质D.催化剂
(2)以下四种情况反应速率最快的是_______。
A. B.
V(CO)=0.2mol·L-1·s-1 V(H )=0.4mol·L-1·s-1
2
C. D.
V(CH OH)=5mol·L-1·min-1 V(CH OH)=0.25mol·L-1·s-1
3 3
(3)若要加快CHOH的生成速率并提高CO的转化率,可采取的措施是_______。
3
A.增大CO浓度 B.不断移出CHOH C.减小压强 D.增大H 浓度
3 2
(4)下图为CO的转化率与温度、压强的相关实验数据:
5.05×105Pa 1.01×106Pa 3.03×106Pa
230℃ 0.7961 0.8972 0.8974
330℃ 0.6675 0.7767 0.7770
430℃ 0.5520 0.6897 0.6906
根据表中信息回答下列问题:
1
学科网(北京)股份有限公司①合成甲醇最合适的温度和压强分别是 、 ,理由是 。
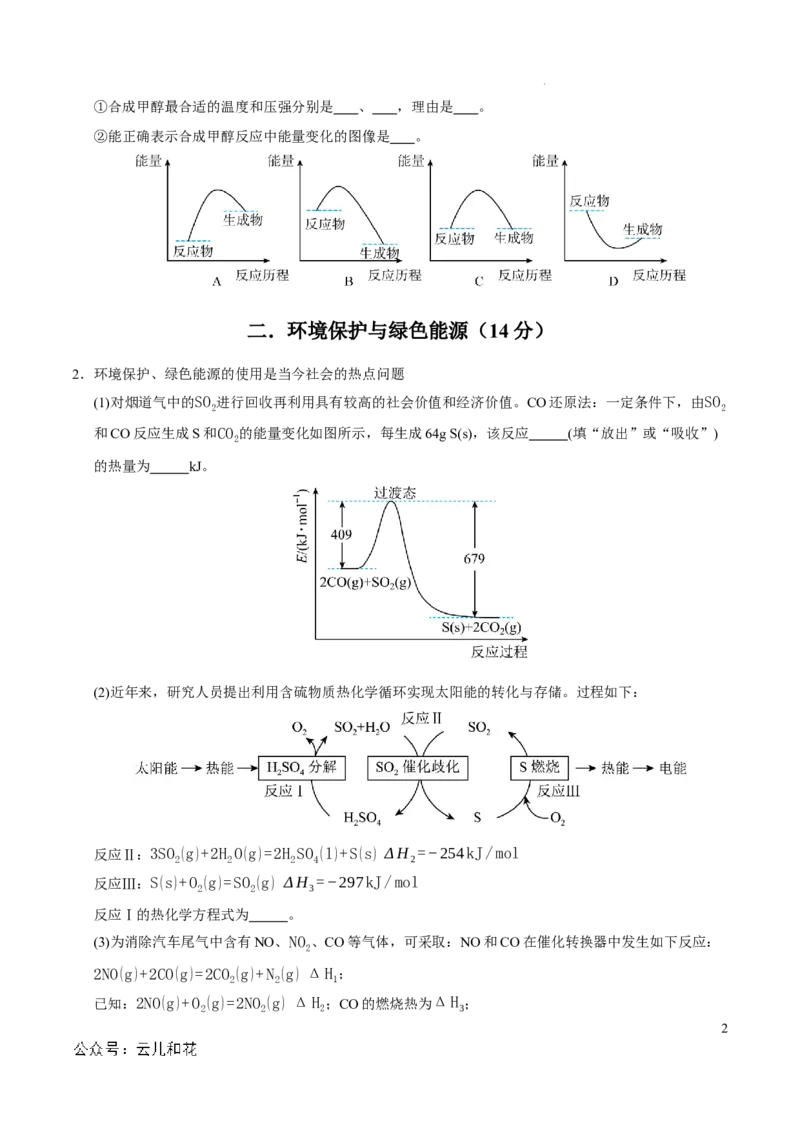
②能正确表示合成甲醇反应中能量变化的图像是 。
二.环境保护与绿色能源(14分)
2.环境保护、绿色能源的使用是当今社会的热点问题
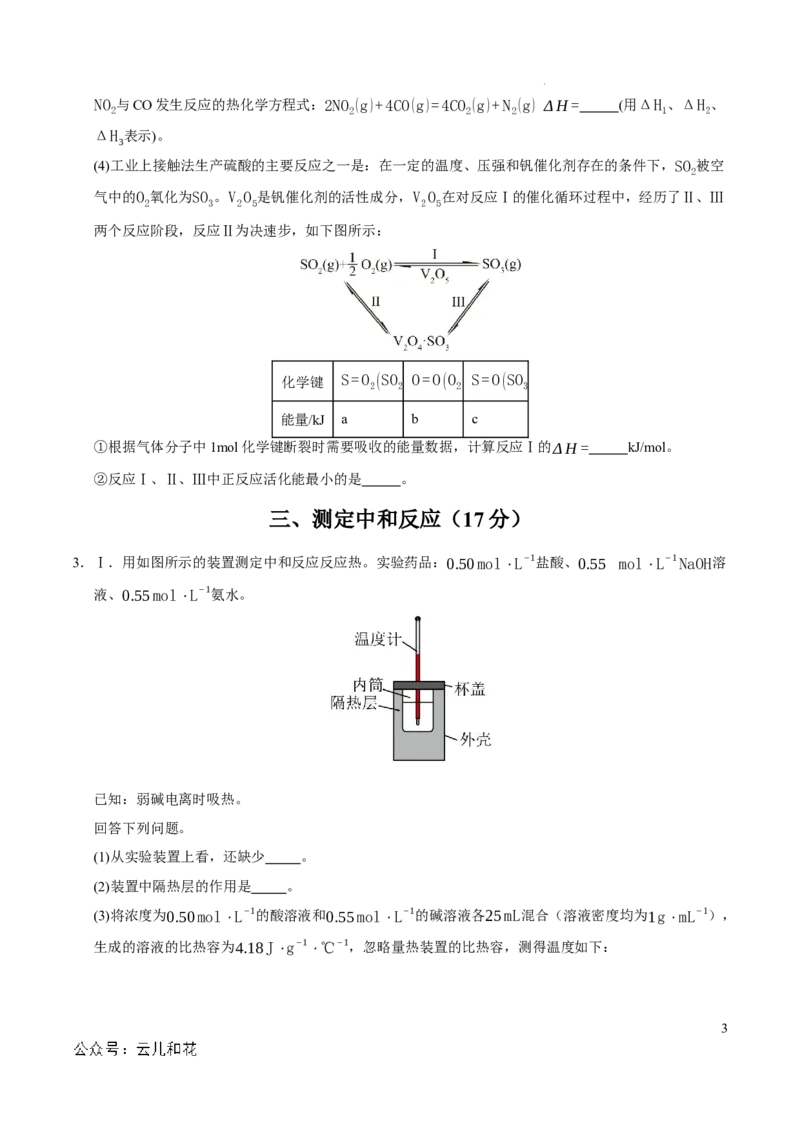
(1)对烟道气中的SO 进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由SO
2 2
和CO反应生成S和CO 的能量变化如图所示,每生成64g S(s),该反应 (填“放出”或“吸收”)
2
的热量为 kJ。
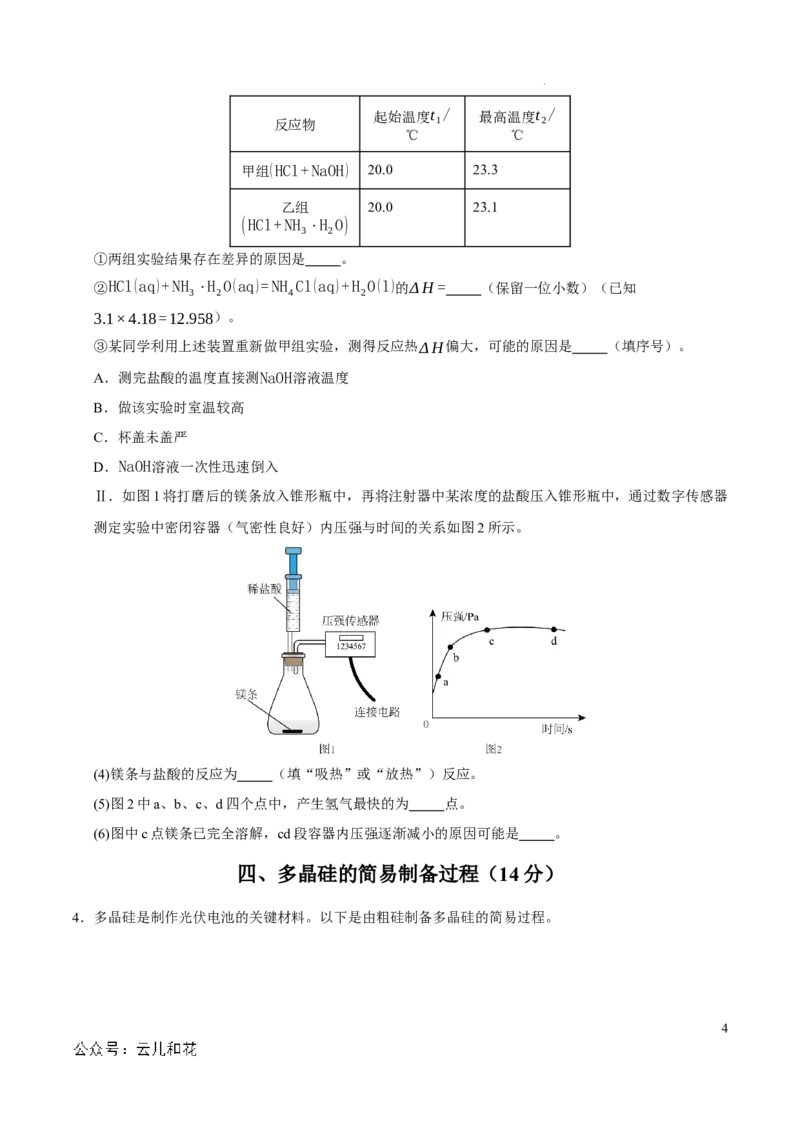
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
反应Ⅱ:3SO (g)+2H O(g)=2H SO (l)+S(s) ΔH =−254kJ/mol
2 2 2 4 2
反应Ⅲ:S(s)+O (g)=SO (g) ΔH =−297kJ/mol
2 2 3
反应Ⅰ的热化学方程式为 。
(3)为消除汽车尾气中含有NO、NO 、CO等气体,可采取:NO和CO在催化转换器中发生如下反应:
2
2NO(g)+2CO(g)=2CO (g)+N (g) ΔH ;
2 2 1
已知:2NO(g)+O (g)=2NO (g) ΔH ;CO的燃烧热为ΔH ;
2 2 2 3
2
学科网(北京)股份有限公司NO 与CO发生反应的热化学方程式:2NO (g)+4CO(g)=4CO (g)+N (g) ΔH= (用ΔH 、ΔH 、
2 2 2 2 1 2
ΔH 表示)。
3
(4)工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下,SO 被空
2
气中的O 氧化为SO 。V O 是钒催化剂的活性成分,V O 在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ
2 3 2 5 2 5
两个反应阶段,反应Ⅱ为决速步,如下图所示:
化学键 S=O (SO )O=O(O ) S=O(SO )
2 2 2 3
能量/kJ a b c
①根据气体分子中1mol化学键断裂时需要吸收的能量数据,计算反应Ⅰ的ΔH= kJ/mol。
②反应Ⅰ、Ⅱ、Ⅲ中正反应活化能最小的是 。
三、测定中和反应(17 分)
3.Ⅰ.用如图所示的装置测定中和反应反应热。实验药品:0.50mol⋅L−1盐酸、0.55 mol⋅L−1NaOH溶
液、0.55mol⋅L−1氨水。
已知:弱碱电离时吸热。
回答下列问题。
(1)从实验装置上看,还缺少 。
(2)装置中隔热层的作用是 。
(3)将浓度为0.50mol⋅L−1的酸溶液和0.55mol⋅L−1的碱溶液各25mL混合(溶液密度均为1g⋅mL−1),
生成的溶液的比热容为4.18J⋅g−1 ⋅℃−1,忽略量热装置的比热容,测得温度如下:
3
学科网(北京)股份有限公司起始温度t / 最高温度t /
反应物 1 2
℃ ℃
甲组(HCl+NaOH) 20.0 23.3
乙组 20.0 23.1
(HCl+NH ⋅H O)
3 2
①两组实验结果存在差异的原因是 。
②HCl(aq)+NH ⋅H O(aq)=NH Cl(aq)+H O(l)的ΔH= (保留一位小数)(已知
3 2 4 2
3.1×4.18=12.958)。
③某同学利用上述装置重新做甲组实验,测得反应热ΔH偏大,可能的原因是 (填序号)。
A.测完盐酸的温度直接测NaOH溶液温度
B.做该实验时室温较高
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
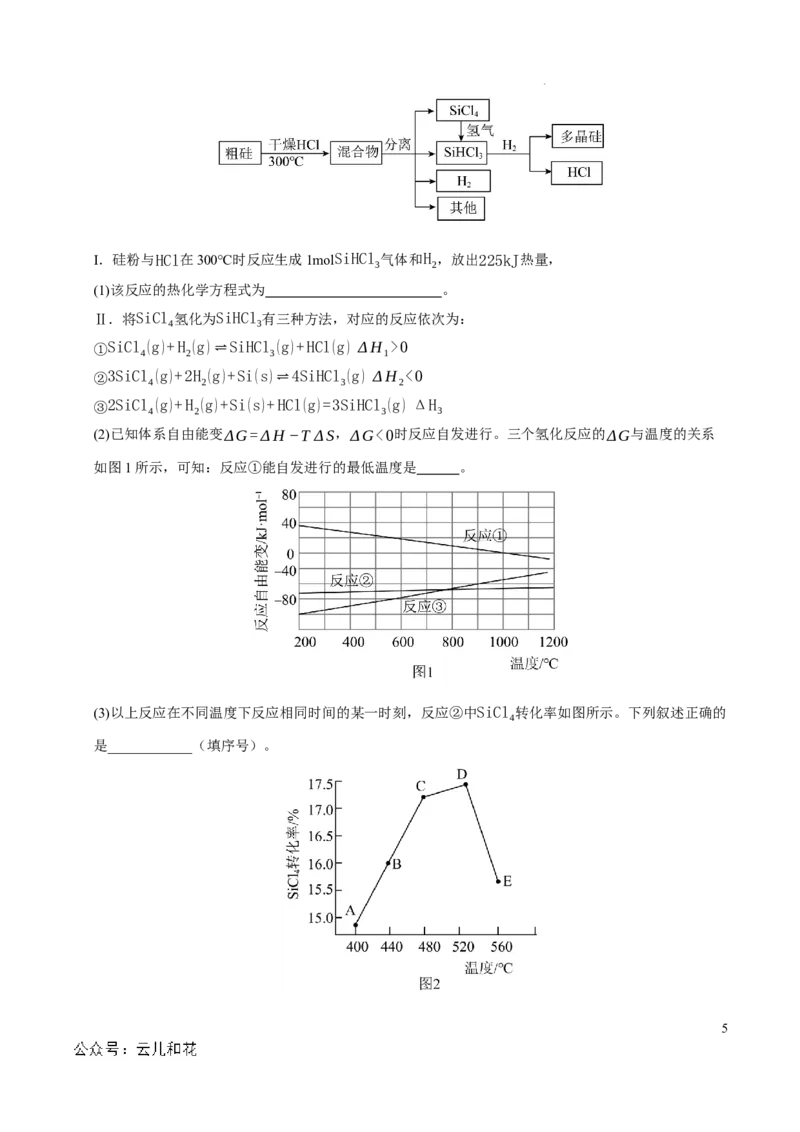
Ⅱ.如图1将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器
测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。
(4)镁条与盐酸的反应为 (填“吸热”或“放热”)反应。
(5)图2中a、b、c、d四个点中,产生氢气最快的为 点。
(6)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是 。
四、多晶硅的简易制备过程(14分)
4.多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
4
学科网(北京)股份有限公司I.硅粉与HCl在300℃时反应生成1molSiHCl 气体和H ,放出225kJ热量,
3 2
(1)该反应的热化学方程式为 。
Ⅱ.将SiCl 氢化为SiHCl 有三种方法,对应的反应依次为:
4 3
①SiCl (g)+H (g)⇌ SiHCl (g)+HCl(g) ΔH >0
4 2 3 1
②3SiCl (g)+2H (g)+Si(s)⇌ 4SiHCl (g) ΔH <0
4 2 3 2
③2SiCl (g)+H (g)+Si(s)+HCl(g)=3SiHCl (g) ΔH
4 2 3 3
(2)已知体系自由能变ΔG=ΔH−T ΔS,ΔG<0时反应自发进行。三个氢化反应的ΔG与温度的关系
如图1所示,可知:反应①能自发进行的最低温度是 。
(3)以上反应在不同温度下反应相同时间的某一时刻,反应②中SiCl 转化率如图所示。下列叙述正确的
4
是____________(填序号)。
5
学科网(北京)股份有限公司A.B点:v >v B.v正:A点>E点 C.反应适宜温度:480-520℃
正 逆
(4)反应③的ΔH = (用ΔH ,ΔH 表示)。温度升高,反应③的平衡常数K (填“增大”、
3 1 2
“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除SiCl 、SiHCl 和Si外,还有 (填分子式)。
4 3
五.化学反应与能量变化(16分)
5.化学反应中均伴随着能量的变化,回答下列问题:
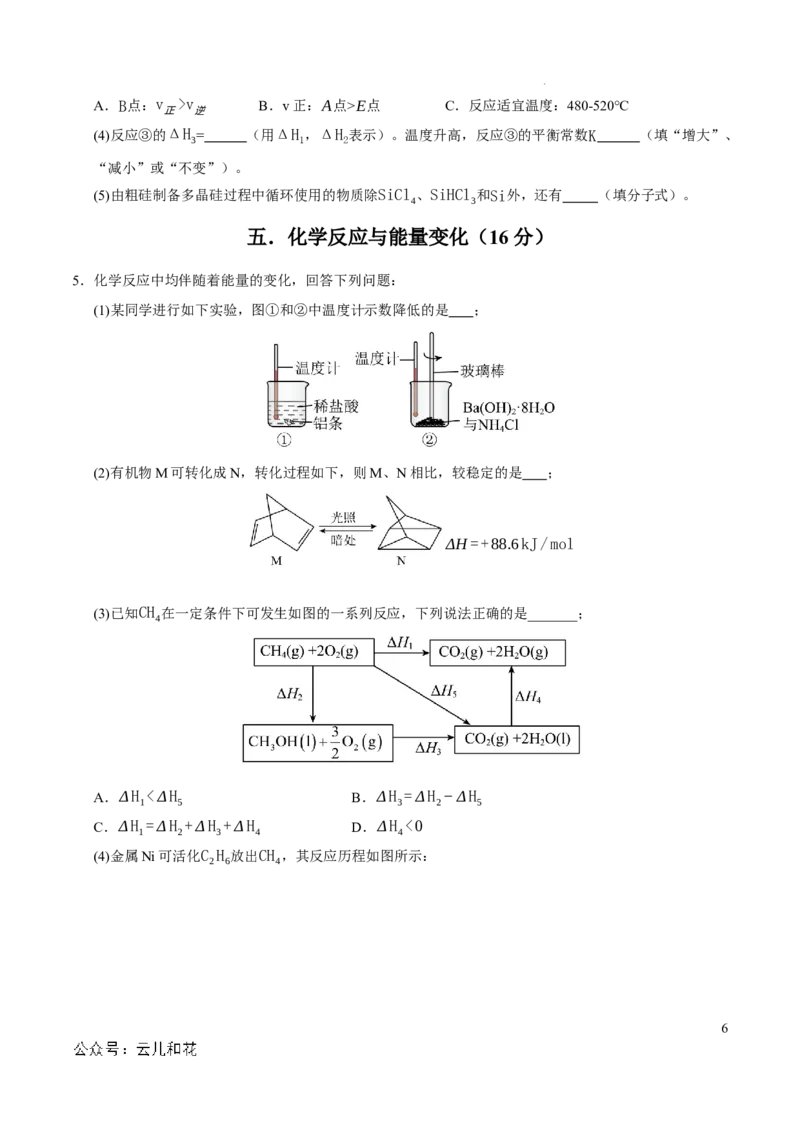
(1)某同学进行如下实验,图①和②中温度计示数降低的是 ;
(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是 ;
ΔH=+88.6kJ/mol
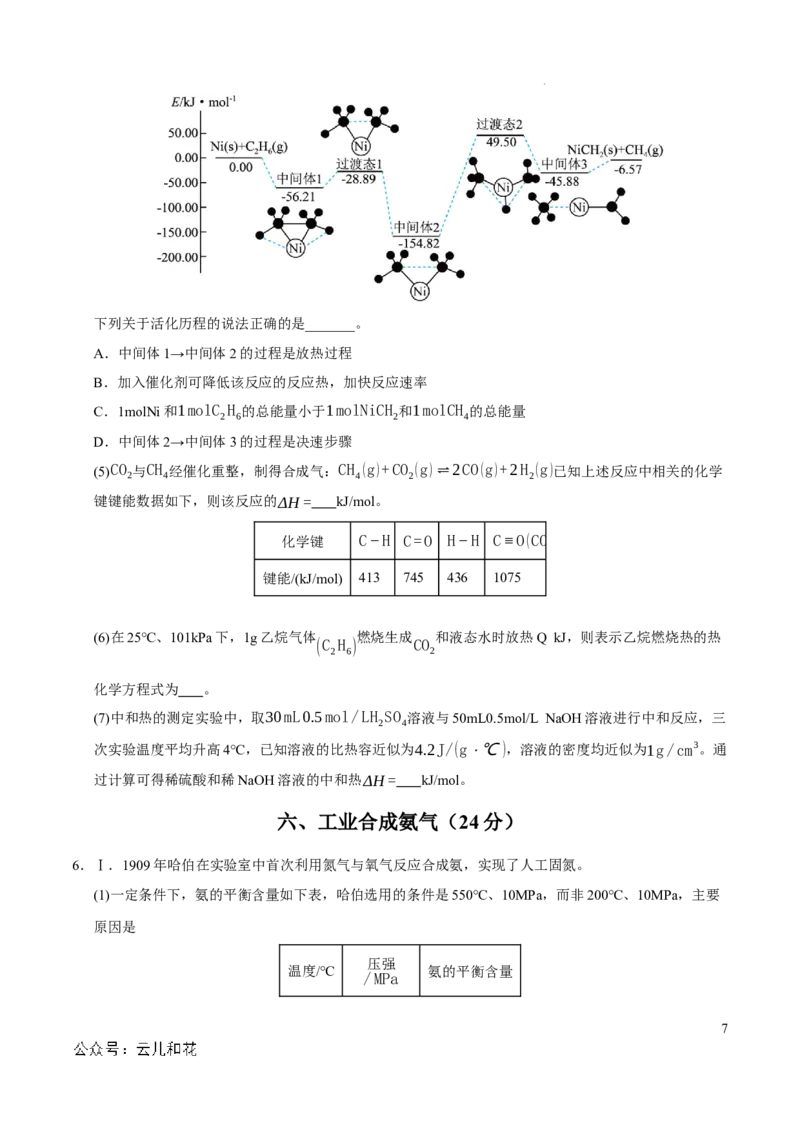
(3)已知CH 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
4
A.ΔH <ΔH B.ΔH =ΔH −ΔH
1 5 3 2 5
C.ΔH =ΔH +ΔH +ΔH D.ΔH <0
1 2 3 4 4
(4)金属Ni可活化C H 放出CH ,其反应历程如图所示:
2 6 4
6
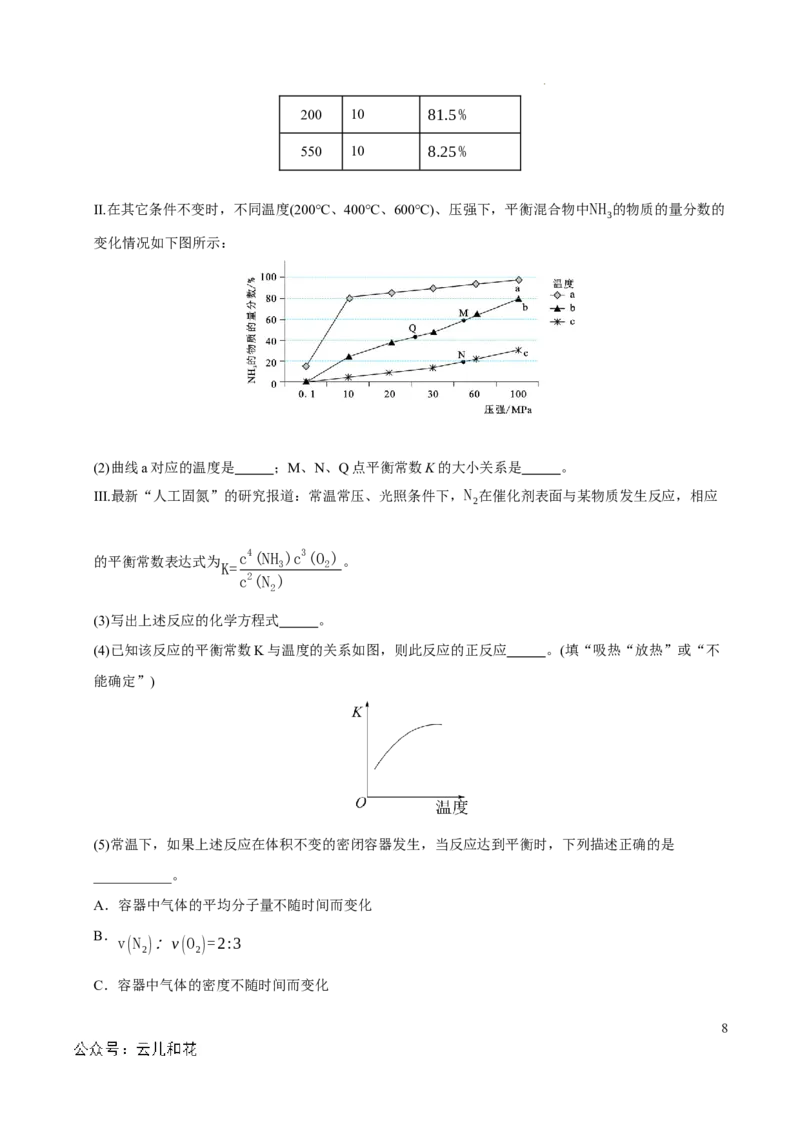
学科网(北京)股份有限公司下列关于活化历程的说法正确的是_______。
A.中间体1→中间体2的过程是放热过程
B.加入催化剂可降低该反应的反应热,加快反应速率
C.1molNi和1molC H 的总能量小于1molNiCH 和1molCH 的总能量
2 6 2 4
D.中间体2→中间体3的过程是决速步骤
(5)CO 与CH 经催化重整,制得合成气:CH (g)+CO (g)⇌2CO(g)+2H (g)已知上述反应中相关的化学
2 4 4 2 2
键键能数据如下,则该反应的ΔH= kJ/mol。
化学键 C−H C=O H−H C≡O(CO)
键能/(kJ/mol) 413 745 436 1075
(6)在25℃、101kPa下,1g乙烷气体 燃烧生成 和液态水时放热Q kJ,则表示乙烷燃烧热的热
(C H ) CO
2 6 2
化学方程式为 。
(7)中和热的测定实验中,取30mL0.5mol/LH SO 溶液与50mL0.5mol/L NaOH溶液进行中和反应,三
2 4
次实验温度平均升高4℃,已知溶液的比热容近似为4.2J/(g⋅℃),溶液的密度均近似为1g/cm3。通
过计算可得稀硫酸和稀NaOH溶液的中和热ΔH= kJ/mol。
六、工业合成氨气(24分)
6.Ⅰ.1909年哈伯在实验室中首次利用氮气与氧气反应合成氨,实现了人工固氮。
(1)一定条件下,氨的平衡含量如下表,哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,主要
原因是
压强
温度/℃ 氨的平衡含量
/MPa
7
学科网(北京)股份有限公司200 10 81.5%
550 10 8.25%
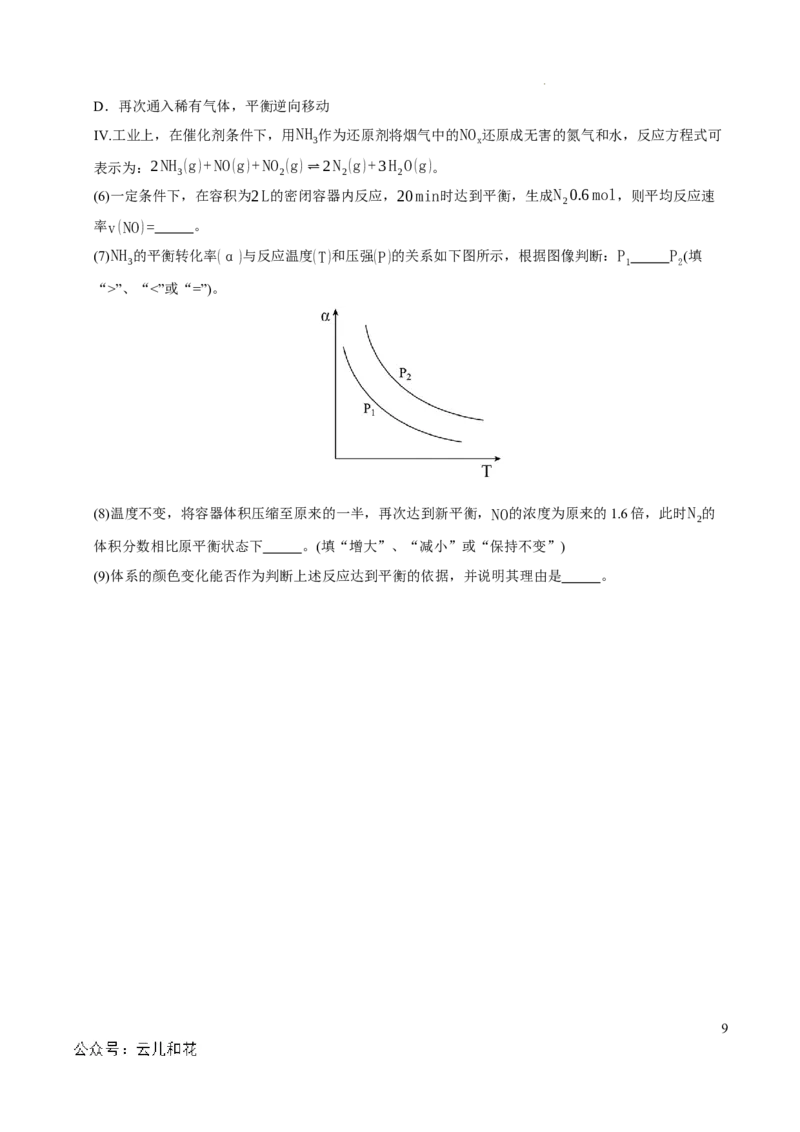
Ⅱ.在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中NH 的物质的量分数的
3
变化情况如下图所示:
(2)曲线a对应的温度是 ;M、N、Q点平衡常数K的大小关系是 。
Ⅲ.最新“人工固氮”的研究报道:常温常压、光照条件下,N 在催化剂表面与某物质发生反应,相应
2
c4(NH )c3(O )
的平衡常数表达式为 。
K= 3 2
c2(N )
2
(3)写出上述反应的化学方程式 。
(4)已知该反应的平衡常数K与温度的关系如图,则此反应的正反应 。(填“吸热“放热”或“不
能确定”)
(5)常温下,如果上述反应在体积不变的密闭容器发生,当反应达到平衡时,下列描述正确的是
___________。
A.容器中气体的平均分子量不随时间而变化
B.
v(N ):v(O )=2:3
2 2
C.容器中气体的密度不随时间而变化
8
学科网(北京)股份有限公司D.再次通入稀有气体,平衡逆向移动
Ⅳ.工业上,在催化剂条件下,用NH 作为还原剂将烟气中的NO 还原成无害的氮气和水,反应方程式可
3 x
表示为:2NH (g)+NO(g)+NO (g)⇌2N (g)+3H O(g)。
3 2 2 2
(6)一定条件下,在容积为2L的密闭容器内反应,20min时达到平衡,生成N 0.6mol,则平均反应速
2
率v(NO)= 。
(7)NH 的平衡转化率(α)与反应温度(T)和压强(P)的关系如下图所示,根据图像判断:P P (填
3 1 2
“>”、“<”或“=”)。
(8)温度不变,将容器体积压缩至原来的一半,再次达到新平衡,NO的浓度为原来的1.6倍,此时N 的
2
体积分数相比原平衡状态下 。(填“增大”、“减小”或“保持不变”)
(9)体系的颜色变化能否作为判断上述反应达到平衡的依据,并说明其理由是 。
9
学科网(北京)股份有限公司