文档内容
届高三 月大联考化学
2024 4
参考答案、提示及评分细则
【答案】
1. C
【解析】非电解质是化合物 而蛋白质是混合物 错误 合金的硬度高于成分金属单质 错
, ,A ; ,B
误 燃煤中加入的 与二氧化碳反应生成碳酸钙 而碳酸钙在高温时又分解生成二氧化
; CaO ,
碳 故不能减少二氧化碳的排放 错误
, ,D .
【答案】
2. C
【解析】电子式表示 的形成过程 错误 为正四
MgCl2 : ,A ;CCl4
面体结构 原子位于四面体的中心 但 原子半径小于 其空间填充模型不是
,C , C Cl, ,B
错误 质子数为 中子数为 的 质量数为 表示为 错误
138
; 58、 80 Ce 58+80=138, 58Ce,D .
【答案】
3. B
【解析】关闭 打开 橡胶导管的存在使烧瓶液面上方与漏斗液面上方压强保持一致 不存
a, b, ,
在压强差 故此操作不能检验该装置气密性 错误 溶液具有强氧化性 能够腐蚀
, ,A ;K2Cr2O7 ,
橡胶管 应该盛放在酸式滴定管中 错误 制取 胶体 向煮沸的蒸馏水中滴加几滴
, ,C ; Fe(OH)3 :
饱和氯化铁溶液 继续加热至液体呈红褐色 错误
, ,D .
【答案】
4. C
【解析】 完全燃烧生成的 为极性分子 为非极性分子 错误 分子 的熔点
C16S8 SO2 ,CO2 ,A ; C16S8
由范德华力的大小决定 错误 由分子结构可知 一个分子中 键和 键的数目比为
,B ; , σ π 4∶1,
正确 分子中没有能形成氢键的原子 故二者之间的作用力是范德华力 错误
C ;C16S8 , ,D .
【答案】
5. B
【解析】铵根离子 亚铁离子水解使得溶液显酸性 酸性溶液使紫色石蕊试液变红色 正确
、 , ,A ;
少量摩尔盐 与过量的 溶液反应的离子方程式为
+
[(NH4)2Fe(SO4)26H2O] NaOH 2NH4 +
错误 价的铁被 氧化为 价
2+ - -
Fe +4OH 2NH3H2O+Fe(OH)2↓,B ;+2 MnO4 +3 ,
被还原为 反应的离子方程式为
- 2+ 2+ - + 3+ 2+
MnO4 Mn , 5Fe +MnO4 +8H 5Fe +Mn +
正确 用来鉴别 生成蓝色沉淀 反应的离子方程式为
2+ + 2+
4H2O,C ;K3[Fe(CN)6] Fe , K +Fe
正确
3-
+[Fe(CN)6] KFe[Fe(CN)6]↓,D .
【答案】
6. D
【解析】根据结构图所示 均为原子序数依次增大的前四周期元素 原子的价
,X、Y、Z、W、M ,M
电子数为 可推断出 只形成单键且原子序数最小 为 元素 形成 个共价键
10, ,X ,X H ,Y 4 ,Y
高三化学试题参考答案 第 页 共 页
【 1 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}为 元素 形成 个共价键 且与 形成氢键 为 元素 则 为氮 氮形成一个单键与
C ,W 2 , X ,W O , Z ,
一个双键 氮原子中含有孤电子对 则 与 形成配位键 原子的价电子数为 为
, , Z M ;M 10,M Ni
元素 由分析可知 分子中存在碳氢等共价键 且氮镍之间存在配位键 正确 同周期元素
. , , ,A ;
基态原子第一电离能从左到右呈现增大的趋势 但 的电子排布是半充满 第一电离能比
, N , O
高 故第二周期中基态原子第一电离能比 高的有 这 种元素 正确 的
, O N、F、Ne 3 ,B ;Y、Z、W
简单氢化物分别为 中心原子的杂化类型相同 孤电子对数分别是 则
CH4、NH3、H2O, , 0、1、2,
键角 正确 根据结构图可知
2+
CH4(H-C-H)>NH3(H-N-H)>H2O(H-O-H),C ; M
的配体数为 错误
2,D .
【答案】
7. A
【解析】麦芽糖中含有醛基 可以发生银镜反应 不能用该实验判断麦芽糖是否发生水解 错
, , ,A
误 将 液体和 固体分别暴露在潮湿空气中 只有前者会冒 白烟 说明
; TiCl4 FeCl3 , “ ”, TiCl4+
x x 产生大量 说明水解程度 正
(+2)H2OTiO2 H2O↓+4HCl, HCl, :TiCl4>FeCl3,B
确 发生沉淀的转化 则 的溶度积比 的小 正确 石蜡油是液态烷烃混
; , Cu(OH)2 Mg(OH)2 ,C ;
合物 受热分解的产物中含有烷烃和烯烃 故 正确
, , D .
【答案】
8. C
【解析】对比邻氨甲酰苯甲酸和邻苯二甲酰亚胺结构可知反应 是取代反应 故 错误 邻氨
② , A ;
甲酰苯甲酸分子含酰胺基 和羧基 这两种官能团 故 错误 邻苯二甲
(-CONH2) (-COOH) , B ;
酰亚胺水解生成邻苯二甲酸 邻苯二甲酰亚胺与足量 溶液反应最多可消耗
,1mol NaOH 2
正确 邻苯二甲酰亚胺分子中所有原子共平面 原子 轨道的孤电子对参与
molNaOH,C ; ,N P
形成大 键 其杂化类型为 杂化 故 错误
2
π , sp , D .
【答案】
9. C
【解析】焙烧时 杂质元素转化为氧化物 由题可知 加入稀盐酸后的滤液经过
Fe、S、As、Sb、Pb , ,
处理得到 和 所以烟尘 烟气中的主要杂质元素是 故 正确 酸浸时
Fe Pb, 、 S、As、Sb, A ; ,PbO
生成 离子方程式为 浸出过程中添加氯
2- + - 2-
[PbCl4] , PbO+2H +4Cl [PbCl4] +H2O,
化钠 可促使氯化铅转化成铅的氯络阴离子 提高其浸出效果 故 正确 与熔融
, , , B ;PbS NaOH
熔融
反应的化学方程式为 元素化合价只有
3PbS+6NaOH3Pb+2Na2S+Na2SO3+3H2O,S
部分升高 故 错误 电解精炼时 与电源的正极相连的是粗锡 故 正确
, C ; , , D .
【答案】
10. C
【解析】充电时 电极为阴极 发生还原反应 其电极反应式为
2- -
,Zn , , [Zn(OH)4] +2e Zn
故 错误 充电时 阳极由于有副反应 电路中每通过 电子 产生的
-
+4OH , A ; , , 1mol ,
小于 故 错误 年我国科学家通过铂负载的氢氧化镍正极 解决了传
NiOOH 1mol, B ;2023 ,
统镍锌电池的短板 所以放电时 铂的作用为氧还原催化剂 故 正确 放电时 阴离子向负
, , , C ; ,
极迁移 故 移向 电极 故 错误
-
, OH Zn , D .
高三化学试题参考答案 第 页 共 页
【 2 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}【答案】
11. A
【解析】根据萤石晶胞结构 浅色 离子分布在晶胞的顶点和面心上 则 个晶胞中浅色
, X , 1 X
离子共有 1 1 个 深色 离子分布在晶胞内部 则 个晶胞中共有 个深色
8× +6× =4 , Y , 1 8 Y
8 2
离子 因此该晶胞的化学式应为 结合萤石的化学式可知 为 故 错误 离子
2+
, XY2, ,X Ca , A ;X
的配位离子为 离子 将晶胞进行平移操作 即可找到与其配位的 离子有 个 故 正
Y , , Y 8 , B
确 根据图中所示坐标系 点坐标为 1 1 1 点坐标为 3 3 1 若将 点 离
; ,m ( , , ),n ( , , ), m Y
4 4 4 4 4 4
子平移至原点 晶胞中各点坐标均由xyz 变为 x 1y 1z 1 因此 点坐标变
, (,,) ( - ,- ,- ); n
4 4 4
为 1 1 即晶胞xy 面的面心 故 正确 该晶体的摩尔体积为 1 -36a3
( , ,0), , C ; ×10
2 2 4
N 3 -1 故 正确
Am mol , D .
【答案】
12. D
【解析】 原子在周期表中位于第五周期 族 价层电子排布式为 正确 反应
10 1
47Ag IB , 4d5s,A ;
液中存在物料守恒式c + c - c 2- c c 3-
(Na )=2[(HSO3)+ (SO3 )+ (H2SO3)+2 [Ag(SO3)2] ],
故c + c - c 2- c 成立 正确 由图可知 的范围在
(Na )>2[(HSO3)+ (SO3 )+ (H2SO3)] ,B ; ,pH 8
时 离子浓度大 利于形成更多的 从而利于 分银 反应的进行
2- 3-
~9 SO3 , [Ag(SO3)2] , “ ” ,C
正确 由图可知 为 时c - c 2- 所以亚硫酸的K -7.30 可计算反
; ,pH 7.30 (HSO3)= (SO3 ), a2=10 ,
应 - 3- + - 的平衡常数K K 2
AgCl+2HSO3[Ag(SO3)2] +2H +Cl =Ksp(AgCl)×( a2)
K -10 -7.30 2 8.68 -15.92 平衡常数太小 反应正向进行程
× 1=1.8×10 ×(10 )×1.0×10 =1.8×10 , ,
度小 故不可以用 溶液代替 溶液来 分银 错误
, NaHSO3 Na2SO3 “ ”,D .
【答案】
13. B
【解析】根据题目信息 容器在恒压条件下充入了与反应无关的水蒸气作为稀释气 相对
,Ⅱ , I
容器而言是在更低的压强下发生反应 根据 H
, C3H8(g)C3H6(g)+H2(g) Δ =
可知 该反应正方向为气体体积增大的吸热反应 升高温度 平衡正向移
-1
+124kJmol , , ,
动 丙烷减少 丙烯增多 减小压强 平衡正向移动 所以 线对应 容器中的 和
, , ; , , a、c I C3H8(g)
图中 线对应 容器中的 和 错误 假设丙烷初始量为
C3H6(g), d、b Ⅱ C3H8(g) C3H6(g),A ;
1mol
C3H8(g)C3H6(g)+H2(g)
起始
(mol) 1 0 0
转化 x x x
(mol)
平衡 x x x
(mol) 1-
高三化学试题参考答案 第 页 共 页
【 3 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}x
A点丙烷含量为 则1- x 1 反应后总的物质的量为4
50%, x×100%=50%, = mol, mol,
1+ 3 3
( )( )
1 1
×0.1MPa ×0.1MPa
则 点对应的该反应平衡常数K 4 4 正确
A p= ( ) =0.0125MPa,B ;
2
×0.1MPa
4
B点代表 容器中 物质的量的变化 因为不能获知 容器中水蒸气加入的量 所
Ⅱ C3H6(g) , Ⅱ ,
以不能计算出丙烷的平衡转化率 错误 容器相当于在更小的压强下发生该反应 根据
,C ;Ⅱ ,
方程式正方向为气体体积增大的方向 所以减压条件下平衡正移 相同温度下丙烷转化率
, ,
比 容器更大 错误
I ,D .
【答案】
14. C
【解析】 原子含氮配体为 所以分子式为 正确 中 结合 个
-
Pt , C8H6N4,A ;c Pt 1 HSO4 、1
个 和一个中性分子配体 根据化合价代数和为零可知 其化合价为 价 中 结合
-
CH3 , , +2 ,d Pt
个 一个 和一个中性分子配体 根据化合价代数和为零 其化合价为 价
- -
3 HSO4 、 CH3 , , +4 ,
可知 正确 物质是该反应的催化剂 在反应过程中量保持不变 所以不会影响 物质
B ;b , , a、b
催化剂
之间的平衡 错误 根据题中信息可知该反应的总反应为
,C ; CH4+SO3+H2SO4 →
正确
CH3OSO3H+H2O+SO2,D .
【答案】 加入一定量的乙醇 分 答 加入稍过量的氨水 再加入一定量的乙醇 也给分
15. (1) (2 , “ , ” )
沿玻璃棒向过滤器中加入乙醇至浸没沉淀 静置 乙醇自然流尽后 重复 次即可 分
, , , 2~3 (2 )
安全管 或平衡气压 避免 中压强过大 分
(2) ( , b )(2 )
酸式滴定管 或移液管 分 回答了规格且正确也给分 液封 防止氨气逸出 分
(3) ( )(1 , ) , (1 )
确保氨完全蒸出 分
(4) (2 )
分 写 不得分
(5)99.1(2 , 99.1% )
分 少选得 分 有错不给分
(6)AC(2 , 1 , )
【解析】 结晶水合物通常可以通过 蒸发浓缩 冷却结晶 从溶液中分离提纯 但由于存在
(1) “ 、 ” ,
加热会促进分解 结合信息 在乙
2+ 2+
[Cu(NH3)4] Cu +4NH3, , [Cu(NH3)4]SO4H2O
醇中难溶 通过改变溶剂的极性 可以使其析出 应选择乙醇 或乙醇 水 作洗涤剂 玻
, , ; ( - ) .(2)
璃管 与大气相通 能平衡气压 避免 中压强过大 作安全管 量取 不能用
a , , b , .(3) 30.00mL
量筒 要选择精度更高的滴定管 或移液管 中保留少量水 的目的是液封 防止氨气逸
, ( );“d ” ,
出 步骤 进行较长时间蒸馏的目的是确保氨完全蒸出 使测定结果更准确 减少误差
.(4) V , , .
样品的纯度测定原理为 通过返滴法进行测定 用 标准液滴定得到过量的盐酸的
(5) : , NaOH
物质的量 结合盐酸总量得到与 反应的n 结合关系式
→ NH3 (HCl)→ 4HCl~4NH3~
高三化学试题参考答案 第 页 共 页
【 4 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}可得到 的质量 进而计算出样品纯度
[Cu(NH3)4]SO4H2O, [Cu(NH3)4]SO4H2O , .
c V c V 1
[(HCl)(HCl)- (NaOH)(NaOH)]× ×246
w 4 代入数据 w
= ×100%, , =99.1%.
0.2210
c( )V( ) c( )V( ) 1
[ HCl HCl- NaOH NaOH ]× ×246
纯度计算公式w 4 滴
(6) = ×100%.A.
0.2210
定终点俯视读数 V 偏低 w偏高 碱式滴定管未润洗 V 偏高 w偏
→ (NaOH) → ;B. → (NaOH) →
低 量取 溶液的仪器未润洗 V 偏低 w偏高 中溶液未
;C. 0.5000mol/LHCl → (NaOH) → ;D.d
与 中溶液合并 V 偏高 w偏低
g → (NaOH) → .
【答案】 分 少选给 分 错选不给分
16. (1)BD(2 , 1 , )
H H H H 分
(2)Δ 1+Δ 2+1/2Δ 3-1/2Δ 4(2 )
分 没写不扣分 副反应的 H 温度升高利于副反应更多
(3)10%ZrO2/In2O3(1 ,10% ) Δ >0,
地正向进行 副反应的选择性提高 主反应选择性降低 导致单位时间内甲醇生成速率下降
, , , ;
催化剂在温度高于 失去活性 导致速率下降 分 答对 个原因给 分
330℃ , (2 , 1 1 )
分 0.0024×0.0024 分
(4)0.012(2 )
3
(2 )
0.0076×0.0128
薄膜材料 分 分
- +
(5)Cu2O/CuO (1 ) CO2+6e +6H CH3OH+H2O(2 )
【解析】 甲醛常温下为气体 错误 甲醇分子中碳原子采取 杂化 是四面体结构 甲醛
3
(1) ,A ; sp , ,
分子中的碳采取 杂化 是平面三角形结构 所以甲醇分子的 键角小于甲醛分子的
2
sp , , ∠OCH
键角 正确 过氧化氢分子中两个氢原子如在半展开的书的两面上 非直线形分
∠OCH ,B ; ,
子 错误 反应的化学方程式为 S
,C ;② CH3OH(g)+O2(g)=HCHO(g)+H2O2(l) Δ <0,
根据自由能判据 G H T S 只有 H 时 G 反应正向自发进行 正确
Δ =Δ - Δ , Δ 2<0 Δ <0, ,D .
根据图及盖斯定律 总反应 是 1
(2) , 2H2(g)+CO2(g)H2O(g)+HCHO(g) ①+②+ ③
2
1 得到的 则反应热 H H H H
- ④ , Δ 1+Δ 2+1/2Δ 3-1/2Δ 4.
2
据图1所示 其他条件相同时使用 作催化剂 甲醇的生成速率最大 所
(3) , 10%ZrO2/In2O3 , ,
以选择 作催化剂 根据题中信息 甲醇生成速率在温度高于 时下降
10%ZrO2/In2O3 . , 330℃ ,
可分析得到的原因可能有两个 一是副反应的 H 温度升高利于副反应更多的正向进
: Δ >0,
行 副反应的选择性提高 主反应选择性降低 导致单位时间内甲醇生成速率下降 二是催化
, , , ;
剂在温度高于 失去活性 导致速率下降
330℃ , .
反应 为 初始投入 为 则为
(4) ① 3H2(g)+CO2(g)H2O(g)+CH3OH(g), CO2 1mol,H2
初始物质的量共 起始时容器内气体的总压强为 若 时反应到达
2mol, 3mol, 3.0kPa, 10min c
点 点 的物质的量为xx 则反应生成的 物质的量也为
,c H2O(g) , =0.24mol, CH3OH
高三化学试题参考答案 第 页 共 页
【 5 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}0.24mol
v 2L 平衡时各物质的物质的量分别为
0.24mol,(CH3OH)= =0.012mol/(Lmin);
10min
n H n n
( 2)=2mol-0.24mol×3=1.28mol,(CO2)=1moL-0.24mol=0.76mol, (H2O)=
n 则分压分别为p p p
(CH3OH)=0.24mol, (H2)=1.28kPa, (CO2)=0.76kPa, (H2O)=
p p
(CH3OH) (H2O)
pθ × pθ
p 代 入 Kθ 得 Kθ 的 计 算 式 为
(CH3OH)= 0.24kPa, = p (CO2) é ê ê p (H2) ù ú ú 3
pθ ×ë pθ û
0.0024×0.0024
.
3
0.0076×0.0128
根据图中信息可知 薄膜材料的电极上发生的反应为
- +
(5) ,Cu2O/CuO CO2+6e +6H
则此电极为阴极
CH3OH+H2O, .
【答案】 分
+ 2+ 3+
17. (1)SiO2、CaSO4(1 ) 2CuFeS2+10H +5H2O22Cu +2Fe +4S+10H2O
分
(2 )
加热使滤液中过量的 分解 防止与后续加入的 反应 造成药品浪费
(2) H2O2 , (NH4)2SO3 ,
分
(2 )
分 少选给 分 错选不给分
(3)BD(2 , 1 , )
或者
2- - 2+ + 2- 2- - 2+
(4)SO3 +2Cl +2Cu +H2O2CuCl↓+2H +SO4 SO3 +6Cl +2Cu +
分 任意写一个都给 分
2- + 2-
H2O2[CuCl3] +2H +SO4 (2 , 2 )
当n n 时 + - 随 - 量的增多
(5) (NH4Cl):(CuSO4)<3∶2 ,CuCl(s)Cu (aq)+Cl (aq), Cl ,
使 沉淀溶解平衡逆向移动 有利于 沉淀的生成n n
CuCl , CuCl ;(NH4Cl)∶ (CuSO4)>3∶2
时 过多的 的会与 形成可溶的 分
- 2- - 2-
,CuCl+2Cl [CuCl3] , Cl CuCl [CuCl3] (2 )
y3 z3
分子晶体 分 射线衍射 分 16π( + ) 分
(6) (1 ) X (1 ) x3 ×100%(2 )
3
【解析】 不与硫酸反应 与硫酸反应生成的 是微溶物
(1)SiO2 ,CaO CaSO4 ;
把 改为 会引入新杂质 错误 流程中有 生成 可以做氮肥 正
(3) CuO ZnO ,A ; (NH4)2SO4 , ,B
确 容易分解 温度不宜太高 错误
;H2O2 , ,C ;
分子晶体熔沸点比较低 熔融状态不能导电 通过分析 射线衍射谱图可以得到晶胞等
(6) , ; X
结构信息 例如键长 键角等 晶胞原子的空间占有率
, , ; :
4 y3 -7 3 4z3 -7 3 16 y3 z3 -21
4× π ×(10 )+4× π ×(10 ) π( + )×(10 ) y3 z3
3 3 3 16π( + )
x3 -7 3 = x3 -7 3 = x3 ×100%
×(10 ) ×(10 ) 3
【答案】 苯甲醛 分 消去反应 分 分
18. (1) (1 ) (2) (1 ) (2 )
高三化学试题参考答案 第 页 共 页
【 6 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}分
(3)2(1 )
分
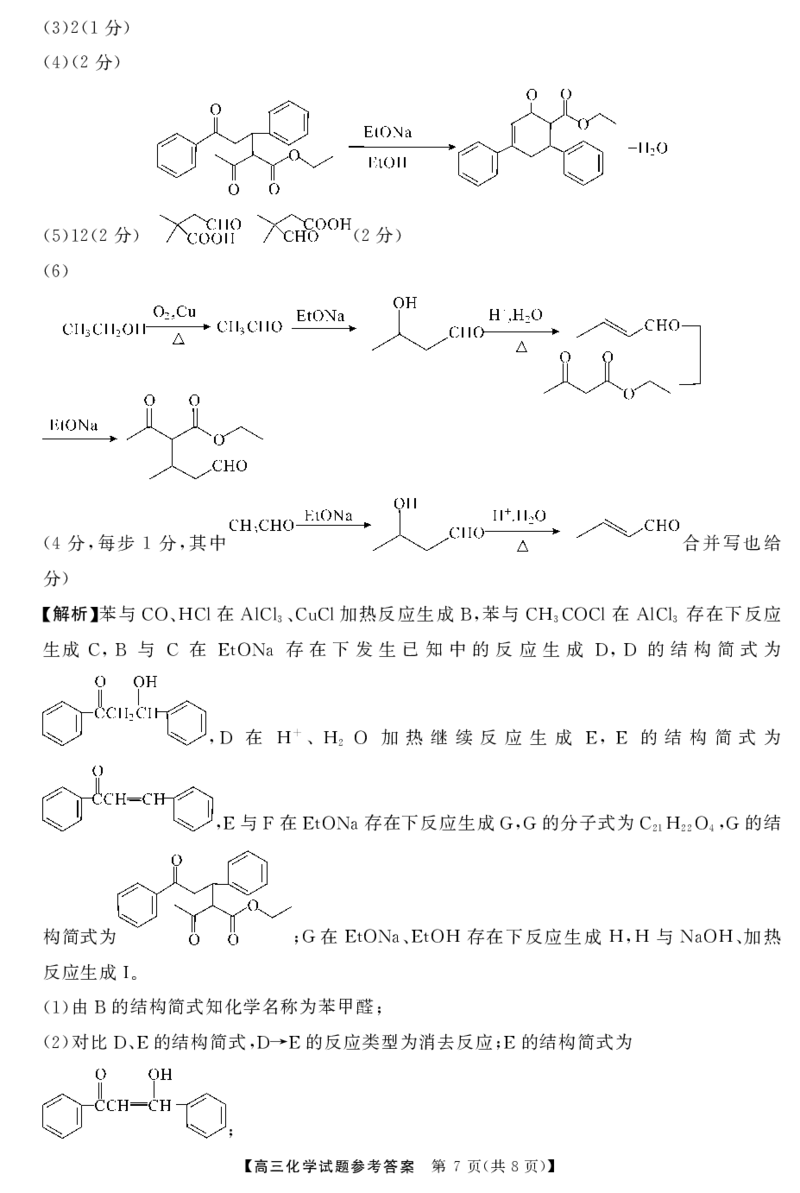
(4)(2 )
分 分
(5)12(2 ) (2 )
(6)
分 每步 分 其中 合并写也给
(4 , 1 ,
分
)
【解析】苯与 在 加热反应生成 苯与 在 存在下反应
CO、HCl AlCl3、CuCl B, CH3COCl AlCl3
生成 与 在 存 在 下 发 生 已 知 中 的 反 应 生 成 的 结 构 简 式 为
C,B C EtONa D,D
在 加 热 继 续 反 应 生 成 的 结 构 简 式 为
+
,D H 、H2 O E,E
与 在 存在下反应生成 的分子式为 的结
,E F EtONa G,G C21H22O4,G
构简式为 在 存在下反应生成 与 加热
;G EtONa、EtOH H,H NaOH、
反应生成
I.
由 的结构简式知化学名称为苯甲醛
(1) B ;
对比 的结构简式 的反应类型为消去反应 的结构简式为
(2) D、E ,D→E ;E
;
高三化学试题参考答案 第 页 共 页
【 7 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}分子中有 个手性碳原子 标注的碳原子
(3)H 2 , (∗ );
根 据 分 析 的 方 程 式 为
(4) ,E+F→G + →
对比 结构简式 根据已知 的反应过程为分子中与酮羰
, G、H , ①,G→H
基相连的 先与另一酮羰基加成形成六元环 再消去脱水得到 的反应方程式
-CH3 , H,G→H
为
;
根据条件分析 含有的官能团为 和 链状结构的碳链异构有 种
(5) , -COOH -CHO, 2 :
和 由定一移一的方法 定 移 分析官能团位置异构
, ( -COOH -CHO) ,
种 种 种 种
(4 )、 (4 )、 (3 )、 (1 ),
共 种 核磁共振氢谱共有 组峰 且峰面积之比为 的同分异构体应满足 个
12 ; 4 , 6∶2∶1∶1 :2
连接同一 原子上 个 故结构简式为 和
-CH3 C ,1 -CH2-, ;
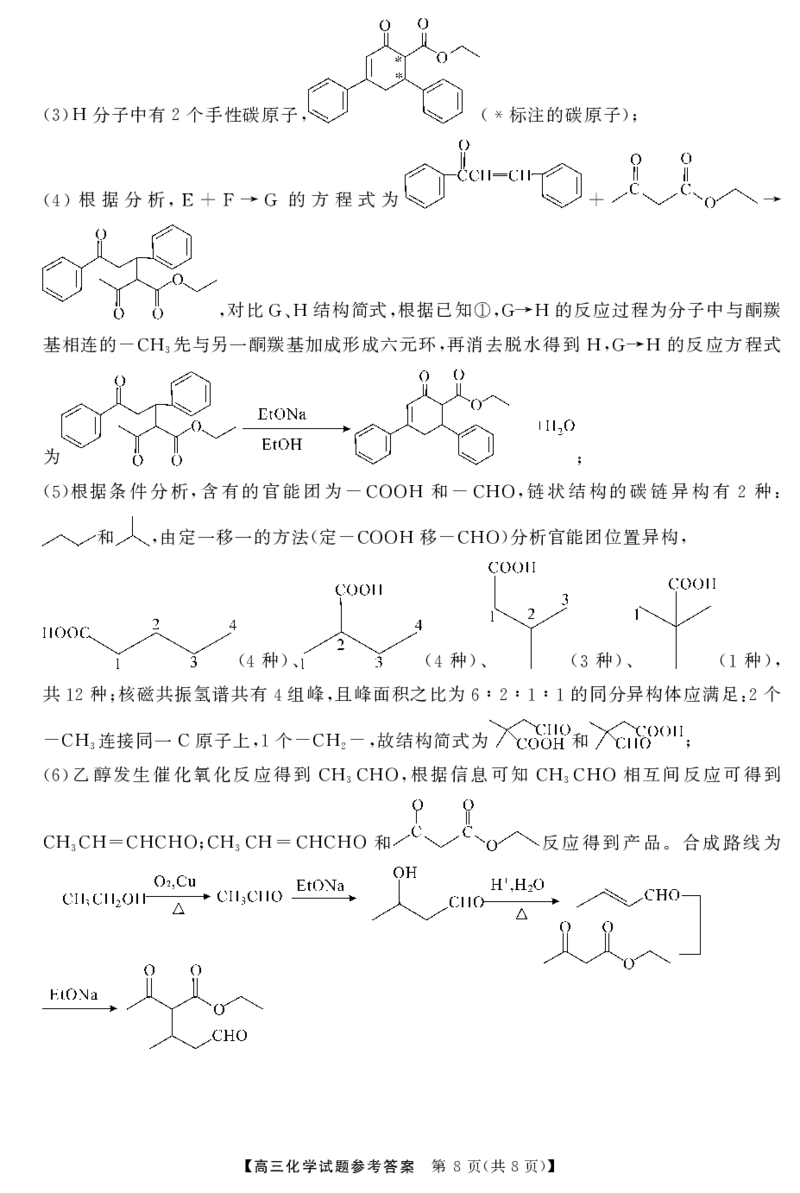
乙醇发生催化氧化反应得到 根据信息可知 相互间反应可得到
(6) CH3CHO, CH3CHO
和 反应得到产品 合成路线为
CH3CH=CHCHO;CH3CH=CHCHO .
高三化学试题参考答案 第 页 共 页
【 8 ( 8 )】
{#{QQABDQiAogCIAIIAABhCQQkQCAOQkAECCAoOgFAMoAABCQFABAA=}#}