文档内容
高三 化学答案
1.D
合金材料属于金属材料,D正确。
2.A
硝酸根sp2杂化,夹角120o,由于没有孤电子对,属于正三角形等性杂化,VSEPR模型与
空间结构一致。A正确。
H O分子之间氢键O-H...O的键角成一直线,夹角为180o;B错误。
2
NH 分子含有极性共价键,O 含有非极性共价键;C错误。
3 2
OH-的电子式的总电子数超过了8e-,D错误。
3.C
亚硫酸钠与硝酸发生氧化还原反应,生成NO,A错误。
分液漏斗盛装为液体物质,不能盛装氯化铵固体;同时,反应需要加热,该装置无加热装
置,B错误。
高锰酸钾固体与浓盐酸,常温下制取氯气,C正确。
碳酸钙与硫酸反应会迅速停止,实验室一般用盐酸与碳酸钙反应,D错误。
4.A
2.8g(0.1mol)氮气完全反应,Mg失去0.2mol电子,氮气中0.1molN失去0.2mol电子,
共失去0.4mol电子。即该反应中转移的电子数为0.4N ;A正确。
A
22.4LNO不一定为1mol,共价键数也无法计算,B错误。
1mol 含有的中子数包含镁、氧中的中子数,C选项中只计算了镁中的中子数;C错
误。
1molTiO 中含有的离子数包括以下判断过程:第一,是否为离子化合物?第二,如果为离
2
子化合物也应为3N ;D错误。
A
5.C
氯气会氧化亚硫酸氢根,HClO与SO 也不会共存;A错误。
2
NO 与NaOH溶液反应生成硝酸根与亚硝酸根,B错误。
2
醋酸与氨都是弱电解质,离子方程式正确;C正确。
碳酸钙不溶于水,不能拆开,D错误。
6.D
金雀花碱分子式为C H N O,A错误。
11 14 2
金雀花碱没有芳香性,六元环中含有酰胺、二烯双键,也不符合4n+2规则,B错误。
金雀花碱双键碳为sp2,其他碳为sp3,C错误。
碱与酸反应生成铵盐,D正确。
7.B
C
2(H+)=K
aC
(CH
3
NO
2
) ,则 (10-6.1)2=K a×0.01 K
a
=10-10.2 ;A正确。
滴入碱,消耗CH =NOOH得到CH =NOO+,平衡向正方向移动,B错误。
2 2
二硝基甲烷,由于强吸电子基硝基增多,吸电子效应更强,酸性增强,C正确。
1
{#{QQABSQIAogCAQJJAARgCAQFSCAEQkAECCCoOwAAAIAABSQFABAA=}#}硝基具有氧化性,甲基具有还原性,硝基甲烷可以作炸药,D正确。
8.B
主族 Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ Ⅶ
未成对电子 0 1 2 3 2 1
依据2Y=2Q=Z+M,Y=Q=2,Y为C,Q为S,则Z为N,M为F。
离子液体为C H -NH + 、SF -离子组成的。
2 5 3 5
9.B
Zn/ZnSO /MnO 锌离子电池,负极为Zn、正极为MnO ,还可以称为锌电池。锌离子电
4 2 2
池——溶液中以锌离子为导体,放电时进入正极,形成不溶于水的ZnMn O ,充电时,进
2 4
入锌电极,成为锌原子。A、C、D错误。
难溶于水的物质均存在溶解平衡,当锰变成低价离子时溶解性增大,加入MnSO 可以抑制
4
正极材料溶解,保持正极稳定,B正确。
10.A
M在左右、前后的竖直面各有4个面,每个面心有一个M;平面有4个面,面心有一个M,
共12个M。A错误。
H与顶角、3个邻位面心,形成正四面体,配位数为4;顶角M周围有8个小立方体(晶
胞的1/8),其中只有4个邻位H,配位数也为4;B、C正确。
晶胞含有4个H,8×1/8+6×1/2=4,共4个M,D正确。
11.C
M点,假设生成物H PO -、HPO 2-各占50%,H PO - HPO 2-+H+
2 4 4 2 4 4
10-7.2=c(H+)c(HPO 2-)/c(H PO -)
4 2 4
c(H+)=10-7.2,而M点pH=4.5,与计算不符。A错误。
M点pH=4.5时,滴定终点产物为NaH PO 。
2 4
假设磷酸物质的量浓度为X,
18.0mL×1mol/L=50.0mL·X,计算得:X=0.36mol/L,所以C正确。
结合N点体积量36.00,恰好是M点的2倍,其滴定终点产物为Na HPO ,
2 4
所以B也是错误的。
pH=7,是 NaH PO 转变为Na HPO 过程,c(Na+)>c(H PO -)+c(HPO 2-)+c(PO 3-),故
2 4 2 4 2 4 4 4
D错误。
12.A
②③铜化合价变化了,④碳化合价变化了,A正确。
⑤②③过程提供了OH,OH氧化EDTA,B错误。
CuEDTA中铜配位数为6,C错误。
CuEDTA配合物非常稳定,原因有二:配位数多;多个五元环位阻大;D错误。
13.D
曲线B前60min迅速生成,后逐渐减少;曲线C表示乙酸的生成量基本在60min后,几乎
没有受到甲醇减少的影响,由此可以判断:前期,甲醇迅速生成乙酸和中间物,后期由甲
醇转化为乙酸的量越来越少,但是乙酸生成速率没有影响,证明中间产物转化为乙酸。中
2
{#{QQABSQIAogCAQJJAARgCAQFSCAEQkAECCCoOwAAAIAABSQFABAA=}#}间产物能转化为乙酸,说明中间产物含有乙酸的部分结构——乙酸酯。从反应物和比例判
断,中间产物为乙酸甲酯,不能为乙酸乙酯。
14.C
实验中浓度变化得到方形点曲线(常温),因为高浓度硫酸会使铁钝化;温度变化得到三
角形点曲线(没有硫酸),温度升高到一定程度(即后期),会发生相关反应。
方形点曲线,30%硫酸放出氢气(不会大量发生吸氧腐蚀),腐蚀速率最大,大于30%后
腐蚀速率开始减慢。
三角形点曲线,70℃以前氧化膜稳定,不会腐蚀;温度进一步升高,氧化膜被破坏了,腐
蚀速率迅速加快。由于没有加入硫酸,不可能有二氧化硫生成。
15.(14分)
(1)SO (1分) 直线形(1分) (1分)
2
(2)MoO +CO 2-==MoO 2-+CO ↑ (2分)
3 3 4 2
(3)①60~80 ℃(2分)
②水蒸发量增大,Na MoO 析出,钼浸出率降低(2分)
2 4
【得分点“水大量蒸发”“Na MoO 析出”】
2 4
(4)氧化低价钼(1分) 沉淀铜、锌元素(2分)
【按点给分,意思相近可以给分,答“净化作用”、“除杂”“提高什么”等等均不给分】
(5)4MoO 2-+2NH ++6H+==(NH ) Mo O ·2H O↓+H O (2分)
4 4 4 2 4 13 2 2
16.(14分)
(1)①3ZrO (s)+13Al(l)==2Al O (s)+3Al Zr(l) △H =-(3b-a)kJ/mol (2分)
2 2 3 3 3
② 去除水分,防止与金属单质反应 (2分)【得分点“去除水”、“防止与金属反应”】
③ 铝熔化吸热(1分) 总反应放热【反应放热】(1分)
大于(2分)
④ (2分)【若不是最后计算结果但是正确,给1分】
2
25
解析 2:Al——80%,则Zr——20%
Al Zr ~ Zr ~ 3Al
3
1 1 3
20% 20% 60%
则Al为80%-60%=20%
V
m =V ,n =
总 总
M
V
n(Al)= ·20% c(Al)= ·20%
M M
V
n(Al Zr)= ·20% c(Al Zr)= ·20%
3 3
M M
3
{#{QQABSQIAogCAQJJAARgCAQFSCAEQkAECCCoOwAAAIAABSQFABAA=}#}
·20%
1 25M2
M
K=
3 2 1 1 2
·20% · ·
M M2 5 5
(2)①sp3d2 (1分)
②AB(2分)【有错扣分】 < (1分)【填“小于”不扣分】
17.(15分)
(1)①玻璃棒、胶头滴管和漏斗(3分)【有错扣分】
②氢氧化锌被氨水溶解生成锌氨配离子而流失(2分)
③铵根离子或NH + 硫酸根离子或SO 2- (2分)【见对给分】
4 4
(2)Zn(OH) +2H N-CH -COOH==Zn(H N-CH -COO) +2H O (2分)
2 2 2 2 2 2 2
(3)蒸发浓缩 冷却结晶(2分)【见对给分】
(4)90.1%(2分)【答“90.14%”,不扣分】
(5)纯度高(1分) 步骤多(1分)【意思相近合理,即可给分】
18.(15分)
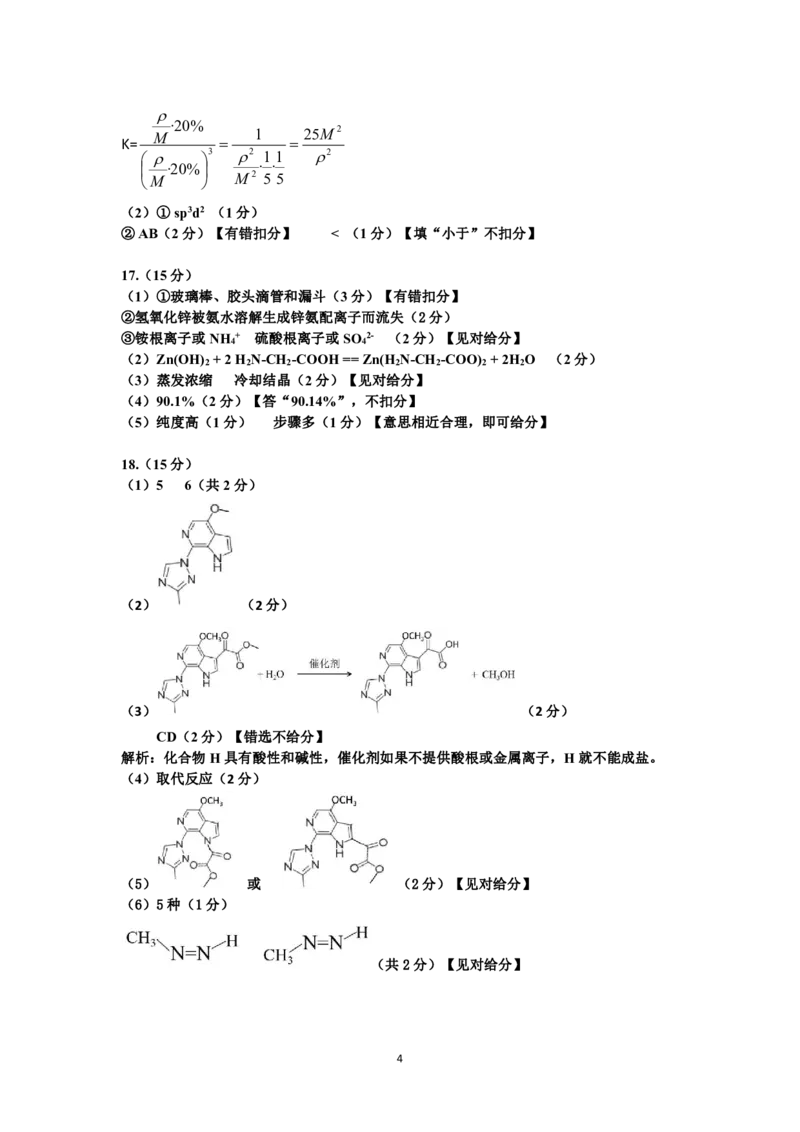
(1)5 6(共2分)
(2) (2分)
(3) (2分)
CD(2分)【错选不给分】
解析:化合物H具有酸性和碱性,催化剂如果不提供酸根或金属离子,H就不能成盐。
(4)取代反应(2分)
(5) 或 (2分)【见对给分】
(6)5种(1分)
(共2分)【见对给分】
4
{#{QQABSQIAogCAQJJAARgCAQFSCAEQkAECCCoOwAAAIAABSQFABAA=}#}