文档内容
广西贵港市2015年中考化学试卷
一、我会选择(每小题3分,共42分)
1.生活中处处有化学,在实际生活中下列物质的用途与其物理性质有关的是( )
A.稀有气体用作焊接保护气 B.铜用作导线
C.氮气用作食品防腐剂 D.氧气用作医疗急救
2.下列说法中不正确的是( )
A.化学使世界变得更加绚丽多彩
B.地球上的金属资源大多以化合物的形式存在
C.二氧化碳是形成酸雨的主要气体
D.生活中通过煮沸可以降低水的硬度
3.我国已禁止在公共场所吸烟,因为香烟燃烧会产生有毒物质,影响吸烟者和被吸烟者的健康,被动吸“二
手烟”是因为( )
A.分子在不断运动 B.分子体积很小
C.分子质量很小 D.分子间有间隔
4.(3分)(2015•贵港)下列物质在空气中燃烧,能产生淡蓝色火焰的是( )
A.硫 B.一氧化碳 C.红磷 D.木炭
5.(3分)(2015•贵港)下列是我市2015年基本实验操作考试中的部分操作,其中错误的是( )
A. B.
点燃酒精灯 检查装置的气密性
C. D.
在玻璃管上套上胶皮管
倾倒液体
6.(3分)(2015•贵港)下列物品所使用的主要材料属于有机合成材料的是( )
A.陶瓷茶杯 B.塑料凉鞋 C.纯棉T恤 D.不锈钢饭盒
7.(3分)(2015•贵港)下列关于四种粒子的结构示意图的说法中不正确的是( )
A.①④的化学性质相似
B.①③属于同种元素
C.②表示的元素在化合物中通常显+2价
D.④属于离子,离子符号为S﹣2
8.(3分)(2015•贵港)今年5月12日是我国第七个“防灾减灾日”.下列做法不合理的是( )
A.扑灭森林火灾,可将大火蔓延路线前的一片树木砍掉,形成隔离带
B.室内电器着火,先切断电源,再用灭火器灭火
C.把燃气热水器安装在浴室内
D.油库、面粉加工厂、纺织厂等场所要严禁烟火
19.(3分)(2015•贵港)2015年世界环境日中国的主题是“践行绿色生活”,下列不符合这一主题的是(
)
A.衣:废旧衣服回收在利用
B.食:利用地沟油制售食用油
C.住:清洁乡村,美丽贵港
D.行:能走不骑,能骑不开,少开多乘公交车
10.(3分)(2015•贵港)已知某种氮的氧化物中氮、氧元素的质量之比为7:12,则该氧化物中氮元素的化合
价为( )
A.+2 B.+3 C.+4 D.+5
11.(3分)(2015•贵港)硝酸钾在不同的溶解度数据如表,下列说法错误的是( )
温度/℃ 0 20 40 60 80 100
溶解度/g 13.3 31.6 63.9 110 169 246
A.硝酸钾的溶解度受温度影响变化较大
B.60℃时,饱和硝酸钾溶液中溶质与溶液质量之比为11:21
C.20℃时,10g水中加入5g硝酸钾充分溶解后再加入5g水,前后溶质的质量分数不变
D.将溶质质量分数为28%的硝酸钾溶液从60℃降温至20℃,没有晶体析出
12.(3分)(2015•贵港)某化合物是由氢、氧及另一种元素组成,下列对该化合物判断正确的是( )
A.可能是盐 B.可能是氧化物 C.一定是碱 D.不可能是酸
13.(3分)(2015•贵港)下列有关物质鉴别方案中,正确的是( )
A.NaCO、NaCl、KOH三种溶液,只用酸碱指示剂即可鉴别
2 3
B.MgCl、NaOH、HCl、NaSO 四种溶液,不加任何试剂即可鉴别
2 2 4
C.(NH)CO、Ca(OH)、BaCl、HCl四种溶液,不加任何试剂即可鉴别
4 2 3 2 2
D.FeO、CuO、C、Fe只用一种试剂无法鉴别
2 3
14.(3分)(2015•贵港)已知在相同的温度和压强下,任何气体的体积与分子数成正比,N 中可能混有HCl、
2
CO、CO、H 四种气体中的一种或几种,把气体依次通过饱和碳酸氢钠溶液、足量氢氧化钠溶液、灼热的氧化
2 2
铜,气体体积变化依次为:不变、变小、变小.则下列判断正确的是( )
A.一定混有HCl B.一定混有CO C.一定混有CO D.一定混有H
2 2
二、我会填空(每空1分,共16分)
15.(4分)(2015•贵港)请用数字和化学符号填空:
(1)2个磷原子 ;
(2)硝酸根离子 ;
(3)人体中含量最多的金属元素 ;
(4)氦气 .
16.(5分)(2015•贵港)“东方之星”号客轮于2015年6月1日发生翻沉事故.6月3日为了方便用生命探
测仪进行搜救,在舱底用氧炔焰对空气舱位置进行切割.
(1)氧炔焰是乙炔(CH)气体和氧气反应产生的高温火焰.乙炔气体属于 (填“有机物”或
2 2
“无机物”).
(2)切割的舱底属于 (填“金属”或“合成”)材料.
(3)由于沉船燃料没有抽掉,切割可能导致起火,现场准备了灭火设施,可燃物燃烧的条件是 、
.
(4)二氧化碳能灭火是因为 .
A.不能燃烧,也不支持燃烧 B.能与水反应 C.密度比空气大 D.不能供给呼吸.
217.(7分)(2015•贵港)化学就在我们身边.请用相关的化学知识回答下列问题:
(1)牛奶中富含的营养素是 .
(2)人体摄入不足会引起多种疾病,补锌可通过服用葡萄糖酸锌(C H O Zn)口服液,则葡萄糖酸锌是由
12 22 14
种元素组成,其中属于微量元素的是 (填名称).
(3)化石燃料是不可再生能源,可利用和开发的新能源有 (填一种即可).
(4)“绿色化学”的特点之一是在化工生产中尽可能实现“零排放”.用CO 和H 反应,只生成一种产物并
2 2
且能实现“零排放”,该反应的基本类型为 反应,反应生成物是下列中的 (填字
母序号).
A.CHO B.CHO C.CHO D.CHO
2 4 2 4 2 2 2 3 6
(5)人呼吸产生的CO 若不能及时排出,滞留在血液中会使血液的pH (填“不变”、“变大”
2
或“变小”).
三、我要回答(每空2分,共12分)
18.(4分)(2015•贵港)在反应前后有化合价的反应是氧化还原反应.已知:Cu+2FeCl═2FeCl+CuCl,则铁
3 2 2
与氯化铁溶液反应的化学方程式为 ,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,充分
反应后过滤,滤纸上不可能出现的是 (填字母序号).
A.有铜无铁 B.有铁无铜 C.铁铜都有 D.铁铜都无.
19.(8分)(2015•贵港)已知A﹣I均为初中化学常见的物质,它们相互间的关系如图所示.该图体现了化合
物F四种不同的化学性质,其中B溶液呈蓝色,I是无色无味的气体,B、C分别与A反应均有不溶于稀硝酸
的同种白色沉淀产生,E与F反应生成另一种不溶于稀硝酸的白色沉淀,C与E反应产生氨味气体.(“﹣”
表示两物质间能反应,“→”表示物质间的转化关系.)
(1)A、I的化学式分别为 、 .
(2)E与F反应的化学方程式为 .
(3)B与G反应的化学方程式为 .
四、我会实验(除20题第(1)小题每空1分外,其余每空2分,共22分)
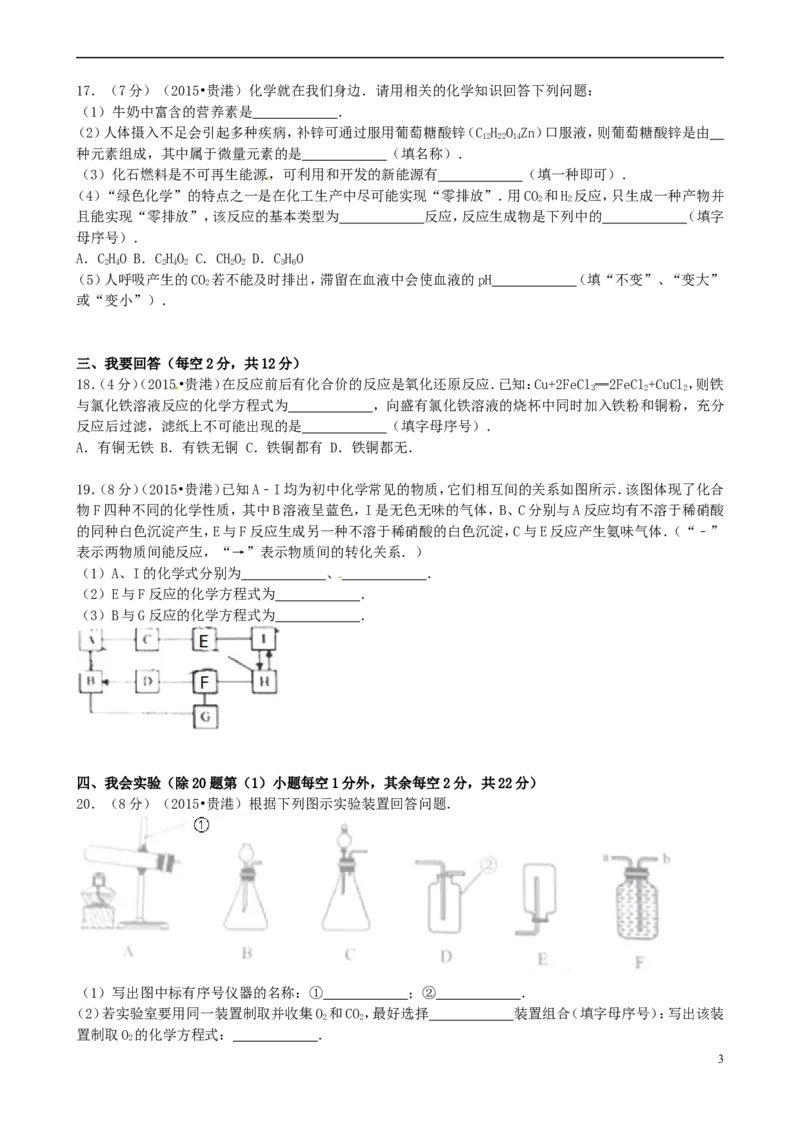
20.(8分)(2015•贵港)根据下列图示实验装置回答问题.
(1)写出图中标有序号仪器的名称:① ;② .
(2)若实验室要用同一装置制取并收集O 和CO,最好选择 装置组合(填字母序号):写出该装
2 2
置制取O 的化学方程式: .
2
3(3)若用F装置收集氢气,则气体应从 (填“a”或“b”)端进入.
21.(14分)(2015•贵港)某兴趣小组先往甲、乙试管中各加入2mL 10%的CuSO 溶液,再往甲试管中加入
4
5mL、乙试管中滴入2滴10%的NaOH溶液,观察到甲试管中有蓝色沉淀生成,乙试管中有浅绿色沉淀生成.
【实验讨论】得到的蓝色沉淀一定是氢氧化铜,写出反应的化学方程式: ,那么浅绿色沉淀是
什么呢?
【查阅资料】
(1)NaOH溶液和CuSO 溶液反应可生成碱式硫酸铜,它是浅绿色固体,受热会分解.
4
(2)碱式硫酸铜有多种可能的组成,如Cu(OH)SO、Cu(OH)SO 或Cu(OH)SO,它们的相对分子质量分别
2 2 4 3 4 4 4 6 4
为:258、356、454.
(3)SO 气体能使酸性高锰酸钾溶液褪色.
2
【实验探究】该小组对碱式铜产生了兴趣,想探究碱式硫酸铜受热分解的产物.
【实验设计】取少量碱式硫酸铜加入试管中并按以下流程进行实验:
实验结束后,试管中残留有黑色固体,滴入稀硫酸黑色固体溶解,溶液呈蓝色:证明黑色固体是CuO;B中无
水CuSO 变蓝色,证明有水生成;C中 ,证明生成SO;D中气体能使带火星木条复燃,证明生成
4 2
O.
2
【实验反思】(1)当NaOH溶液和CuSO 溶液反应时,只要控制CuSO 溶液的量一定,NaOH溶液
4 4
(填“过量”或“不足”)时就能生成浅绿色沉淀,此实验利用的科学方法是 (填“控制变量
法”或“对比观察法”).
(2)碱式硫酸铜可表示为:aCu(OH)•bCuSO,则Cu(OH)SO 还可表示为: .
2 4 4 6 4
【拓展延伸】(1)当反应物的量不同,产物可能不同,试另举一个例子: .
(2)为了确定所得浅绿色沉淀的组成,再进行后续实验,取8.9g碱式硫酸铜放入试管中加热,充分反应后生
成了0.9g水,通过计算确定所得浅绿色沉淀的化学式为 .
五、我会计算(共8分)
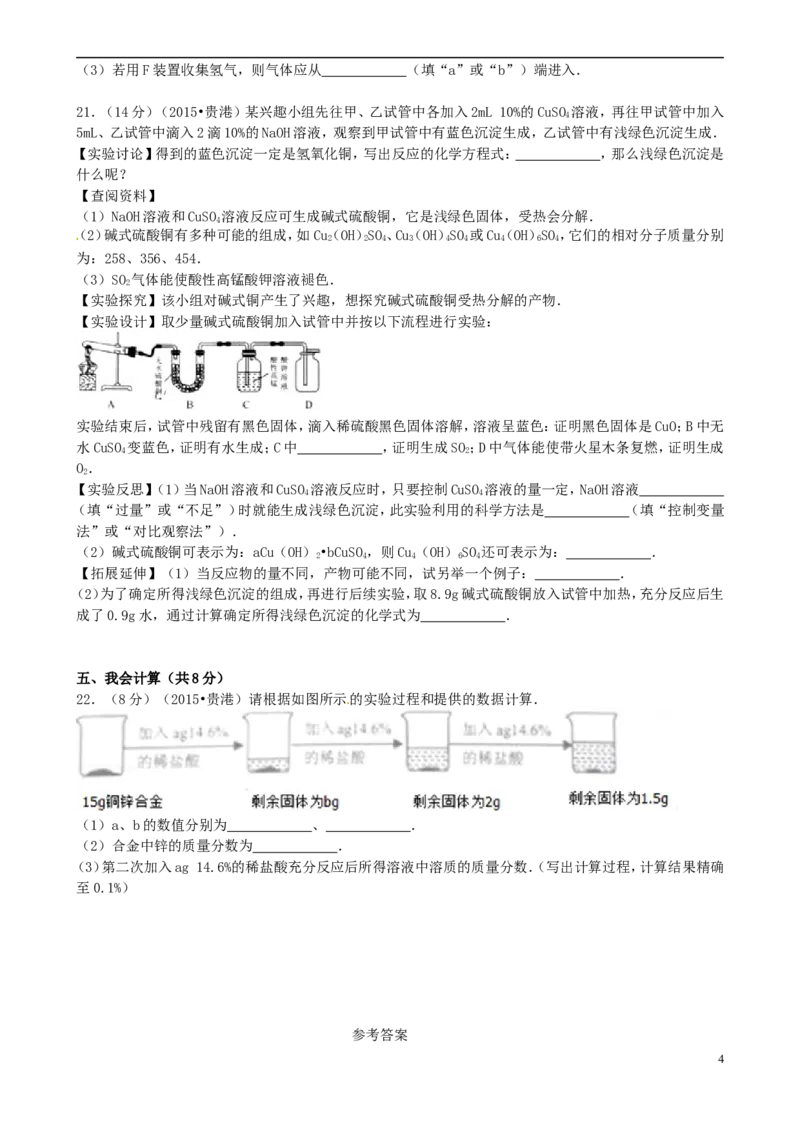
22.(8分)(2015•贵港)请根据如图所示的实验过程和提供的数据计算.
(1)a、b的数值分别为 、 .
(2)合金中锌的质量分数为 .
(3)第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数.(写出计算过程,计算结果精确
至0.1%)
参考答案
41-10、BCAAC BDCBB 11-14、DACD
15、(1)2P;(2)NO﹣;(3)Ca;(4)He.
3
16、(1)有机物 (2)金属
(3)与氧气或空气接触 温度必须达到燃烧所需的最低温度即着火点
(4)AC
17、蛋白质;
四;锌;
太阳能(答案合理即可);
化合;C
变小
18、Fe+2FeCl=3FeCl,B
3 2
19、(1)AgNO,CO;
3 2
(2)HSO+Ba(OH)=BaSO↓+2HO;
2 4 2 4 2
(3)CuCl+Fe=FeCl+Cu.
2 2
20、铁架台 集气瓶;
CD 2HO 2HO+O↑;
2 2 2 2
a
21、2NaOH+CuSO═NaSO+Cu(OH)↓
4 2 4 2
酸性高锰酸钾溶液褪色
控制变量法
3Cu(OH)•CuSO
2 4
Cu(OH) SO.
3 4 4
22、解:(1)由题意可知,第一次和第二次加入稀盐酸后锌有剩余,稀盐酸完全反应,即2ag14.6%的稀盐酸消
耗锌粒15g﹣2g=13g;故b=15g﹣ =8.5g;
Zn+2HCl═ZnCl+H↑,
2 2
65 73
6.5g ag×14.6%
a=50
(2)合金中锌的质量分数为 ×100%=90%;
(3)设,第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量为x,生成氢气质量为y,
Zn+2HCl═ZnCl+H↑
2 2
65 136 2
15g﹣2g x y
x=27.2g
y=0.4g
第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数:
×100%=24.2%.
答案:(1)50;8.5;
5(2)90%;
(3)第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数为24.2%.
6