文档内容
河南省2018年中考化学真题试题
注意事项:
1.本试卷共四页,四个大题,25个小题,满分50分,考试时间50分钟。
2.本试卷上不要答题,请按答题卡上注意事项的要求直接把答案填写在答题卡上。答在试卷
上的答案无效。
相对原子质量H:1 C:12 N:14 O:16 Mg:24 Al:27 S:32 Cl:35.5 Ca:40 Cu:64
Zn:65 Ag:108
一、选择题(本题包括14小题,每小题1分,共14分,每小题只有一个选项符合题意)
1.生活中的下列变化,属于物理变化的是
A.蜡熔化 B.铁生锈 C.米酿酒 D.纸燃烧
2.开封小笼包是地方特色美食,其主要食材瘦肉中富含的营养素为
A. 糖类 B. 油脂 C. 维生素 D. 蛋白质
3.“建设美丽中国”是新时代的目标。下列说法不利于减少环境污染的是
A. 回收各种废弃塑料 B. 开发和利用新能源
C. 工业废水任意排放 D. 积极植树、造林、种草
4.下列物质在氧气里燃烧,生成物为白色固体的是
A. 硫 B. 镁条 C. 铁丝 D. 木炭
5.下列各组元素中,元素符号的第一个字母不相同的一组是
A.锰、钛 B. 氩、金 C. 铅、铂 D. 氦、汞
6.下列有关水的说法正确的是
A.冰水共存物属于混合物 B.水是由氢元素和氧元素组成的化合物
C. 将硬水过滤可得到软水 D.凡是有水生成的反应一定是中和反应
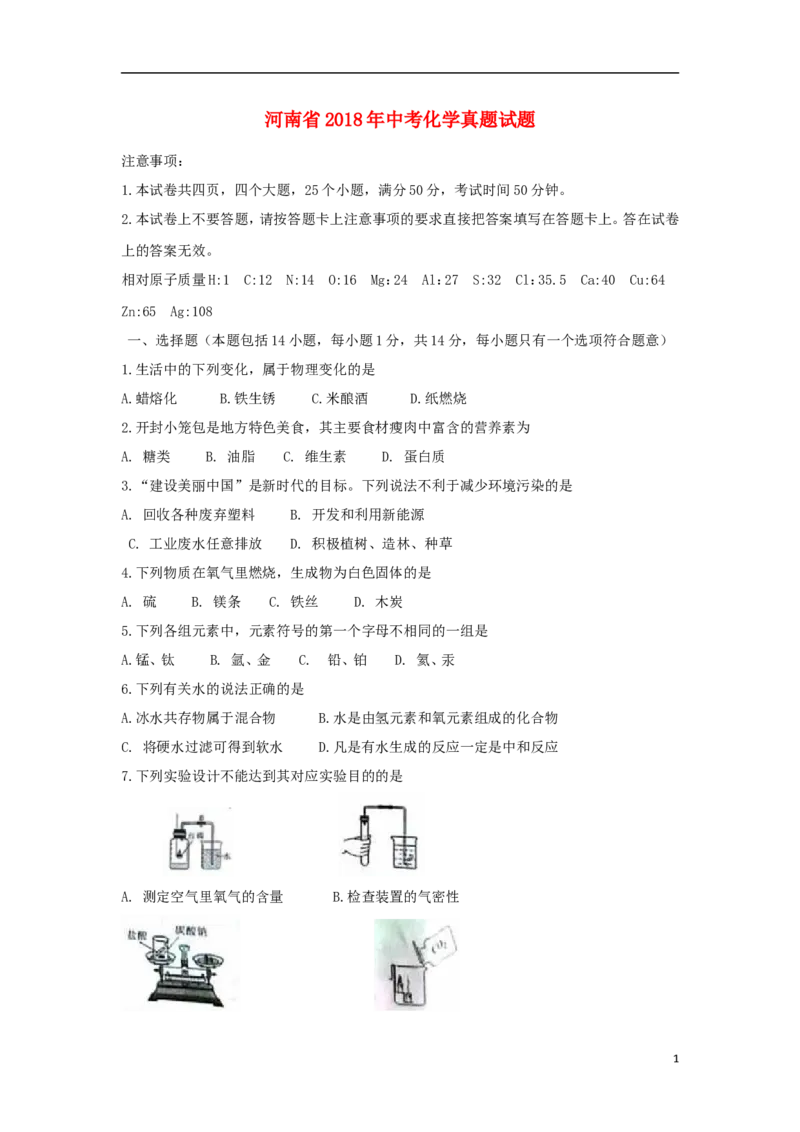
7.下列实验设计不能达到其对应实验目的的是
A. 测定空气里氧气的含量 B.检查装置的气密性
1C. 验证质量守恒定律 D.验证CO 密度比空气的大
2
8.硅是信息技术的关键材料。右图为硅的原子结构示意图,下列说法正确的是
A.硅属于稀有气体元素 B.图中n的值为8
C.硅的相对原子质量为14 D.硅元素位于第三周期
9.室温时将少量干冰放入塑料袋中并密封,塑料袋会快速鼓起,其原因是
A. 分子的体积变大 B.分子分解变成了原子
C. 分子的间隔变大 D. 分子由静止变为运动
10.下列区分物质的方法或试剂不正确的是
A. 用带火星的木条区分氧气和氮气 B. 用熟石灰区分氯化铵和氯化钾
C. 灼烧后闻气味区分羊毛线和腈纶线 D.用酚酞溶液区分硫酸和硫酸钠溶液
11.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是
①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯加水时有水洒出; ④将配制好的溶液装入试剂瓶中有少量溅出。
A. ①② B. ①③ C. ②④ D.③④
12.过氧化钠(NaO)可做呼吸面具中氧气的来源,它与二氧化碳反应后的生成物为
2 2
A. NaCO 和H B. NaO 和O C. NaOH和O D. NaCO 和O
2 3 2 2 2 2 2 3 2
13.甲、乙、丙有如右图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已
略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是
A. C、CO 、CO
2
B. HO、HO、O
2 2 2 2
C.KOH、KCO、KNO
2 3 3
D. FeO、FeCl、Fe(OH)
2 3 3 3
14.有Mg、Al、Zn的混合物共7.2g,与足量盐酸反应,生成H 的质量可能是
2
A. 0.2g B. 0.6g C. 0.8g D. 0.9g
二、填空题(本题包含6个小题,每空1分,共16分)
15.人体中含量最高的金属元素是 ;在尿素、硫酸钾、磷酸二氢铵三种化肥中,属于
复合肥的是 。
216.乙醇完全燃烧的化学方程式为 ;高压水枪灭火所依据的灭火原理是 ;
氢气作燃料的优点是 (答出一条即可)。
17.铜丝作导线是利用了其良好的 性;铁锈(主要成分是FeO)可用硫酸除去,该反
2 3
应的生成物为HO和 ;铝制品耐腐蚀是因为其表面生成了致密的氧化铝薄膜,该反
2
应的化学方程式为 。
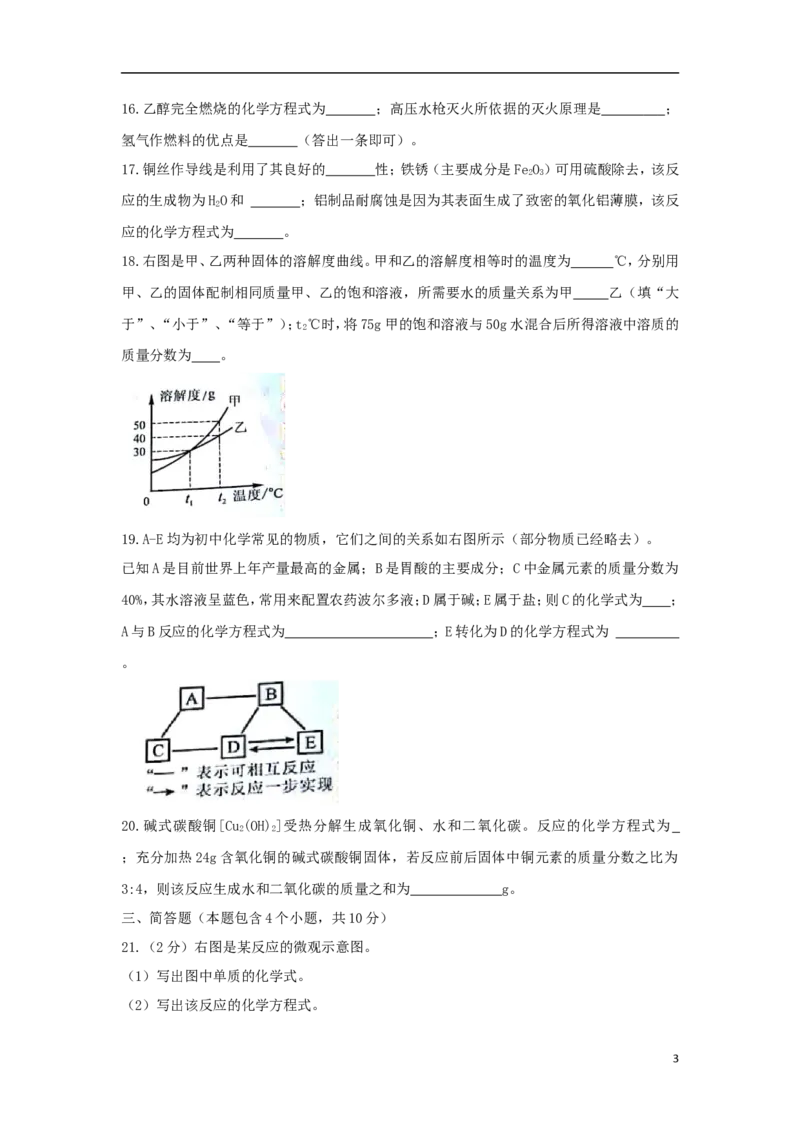
18.右图是甲、乙两种固体的溶解度曲线。甲和乙的溶解度相等时的温度为 ℃,分别用
甲、乙的固体配制相同质量甲、乙的饱和溶液,所需要水的质量关系为甲 乙(填“大
于”、“小于”、“等于”);t℃时,将75g甲的饱和溶液与50g水混合后所得溶液中溶质的
2
质量分数为 。
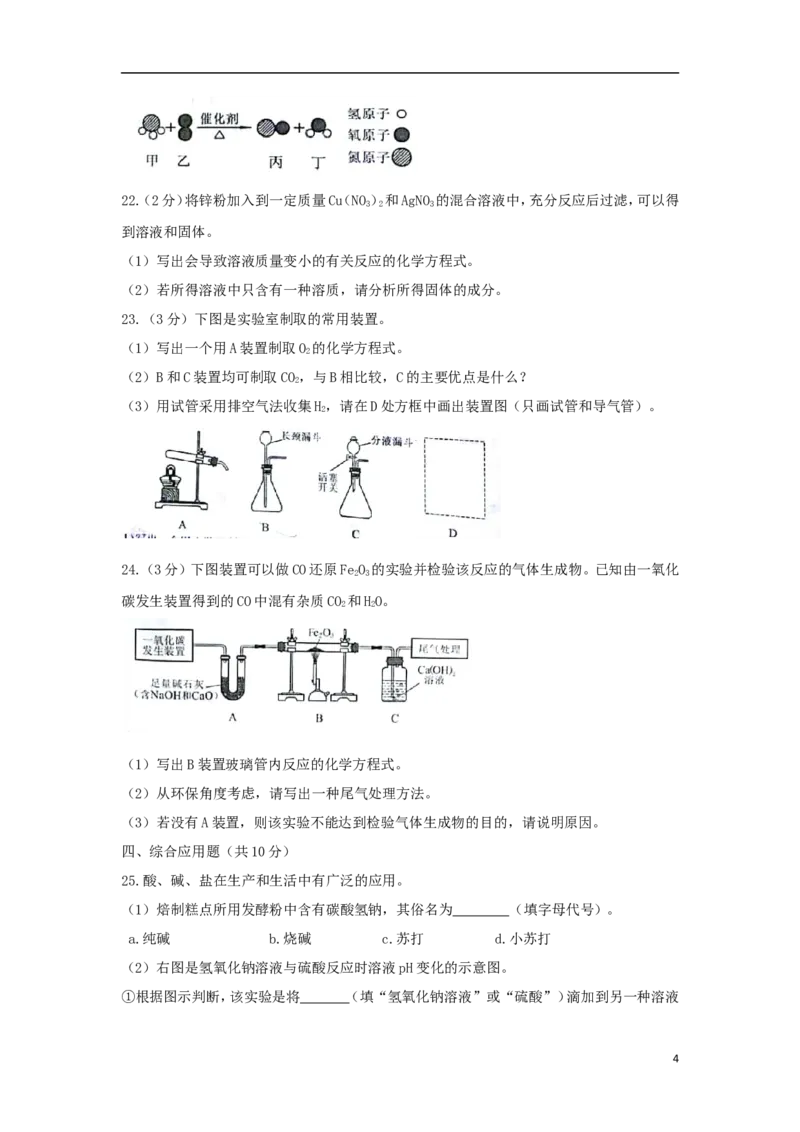
19.A-E均为初中化学常见的物质,它们之间的关系如右图所示(部分物质已经略去)。
已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为
40%,其水溶液呈蓝色,常用来配置农药波尔多液;D属于碱;E属于盐;则C的化学式为 ;
A与B反应的化学方程式为 ;E转化为D的化学方程式为
。
20.碱式碳酸铜[Cu(OH)]受热分解生成氧化铜、水和二氧化碳。反应的化学方程式为
2 2
;充分加热24g含氧化铜的碱式碳酸铜固体,若反应前后固体中铜元素的质量分数之比为
3:4,则该反应生成水和二氧化碳的质量之和为 g。
三、简答题(本题包含4个小题,共10分)
21.(2分)右图是某反应的微观示意图。
(1)写出图中单质的化学式。
(2)写出该反应的化学方程式。
322.(2分)将锌粉加入到一定质量Cu(NO)和AgNO 的混合溶液中,充分反应后过滤,可以得
3 2 3
到溶液和固体。
(1)写出会导致溶液质量变小的有关反应的化学方程式。
(2)若所得溶液中只含有一种溶质,请分析所得固体的成分。
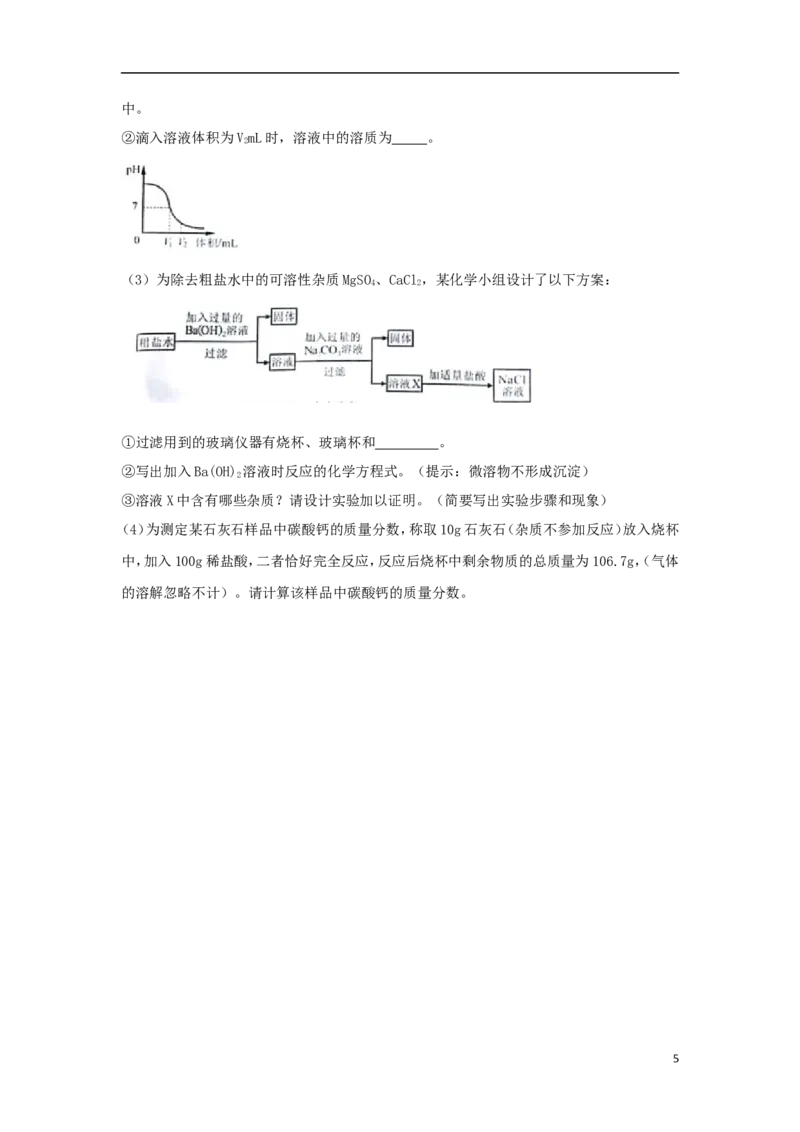
23.(3分)下图是实验室制取的常用装置。
(1)写出一个用A装置制取O 的化学方程式。
2
(2)B和C装置均可制取CO,与B相比较,C的主要优点是什么?
2
(3)用试管采用排空气法收集H,请在D处方框中画出装置图(只画试管和导气管)。
2
24.(3分)下图装置可以做CO还原FeO 的实验并检验该反应的气体生成物。已知由一氧化
2 3
碳发生装置得到的CO中混有杂质CO 和HO。
2 2
(1)写出B装置玻璃管内反应的化学方程式。
(2)从环保角度考虑,请写出一种尾气处理方法。
(3)若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因。
四、综合应用题(共10分)
25.酸、碱、盐在生产和生活中有广泛的应用。
(1)焙制糕点所用发酵粉中含有碳酸氢钠,其俗名为 (填字母代号)。
a.纯碱 b.烧碱 c.苏打 d.小苏打
(2)右图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是将 (填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液
4中。
②滴入溶液体积为VmL时,溶液中的溶质为 。
2
(3)为除去粗盐水中的可溶性杂质MgSO、CaCl,某化学小组设计了以下方案:
4 2
①过滤用到的玻璃仪器有烧杯、玻璃杯和 。
②写出加入Ba(OH) 溶液时反应的化学方程式。(提示:微溶物不形成沉淀)
2
③溶液X中含有哪些杂质?请设计实验加以证明。(简要写出实验步骤和现象)
(4)为测定某石灰石样品中碳酸钙的质量分数,称取10g石灰石(杂质不参加反应)放入烧杯
中,加入100g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7g,(气体
的溶解忽略不计)。请计算该样品中碳酸钙的质量分数。
567