文档内容
五年(2021-2025)高考化学真题分类汇编
专题09 晶体结构与性质
考向 五年考情(2021-2025) 命题趋势
2025·黑吉辽蒙卷、2025·广东卷、2025·河北卷、2025·
晶体结构与性质在高考中常
云南卷、2024·天津卷、2024·广西卷、2024·贵州卷、
见的命题角度有晶体的类
考点01 晶体结构
2024·甘肃卷、2024·湖南卷、2024·山东卷、2023·北京 型、结构与性质的关系,晶
与性质
卷、2022·天津卷、2022·湖北卷、2022·山东卷、2021· 体熔沸点高低的比较,配位
天津卷 数、晶胞模型分析及有关计
2025·陕晋青宁卷、2025·浙江1月卷、2025·安徽卷、 算等是物质结构选考模块的
2025·河北卷、2025·云南卷、2025·黑吉辽蒙卷、2025· 必考点试题侧重晶体类型判
断、物质熔沸点的比较与原
湖北卷、2025·湖南卷、2024·重庆卷、2024·江西卷、
考点02 晶胞分析
因、晶胞中微粒数的判断、
2024·河北卷、2024·湖南卷、2024·湖北卷、2024·安徽
与计算 配位数、晶胞密度计算、晶
卷、2024·吉林卷、2023·河北卷、2023·重庆卷、2023·
胞参数、空间利用率计算的
湖南卷、2023·湖北卷、2023·辽宁卷、2022·湖北卷、
考查。
2021·江苏卷、2021·湖北卷、2021·辽宁卷
考点 一 晶体结构与性质
1.(2025·黑吉辽蒙卷)侯氏制碱法突破西方技术垄断,推动了世界制碱技术的发展,其主要反应为
NaCl+ 。下列有关化学用语或说法正确的是
A. 的电子式: B. 的空间结构:直线形
C. 的晶体类型:离子晶体 D.溶解度:
【答案】C
【解析】
A.CO 中C和O之间有两对共用电子,其结构为 ,A错误;
2
B.HO的中心原子为O,根据价层电子对互斥理论,其外层电子对数为4,VSEPR模型为四面体形,
2
O原子与H原子形成共价键,剩余两对孤电子对,因此,HO为V形分子,B错误;
2
C.NH Cl由NH 和Cl-组成为离子化合物,晶体类型为离子晶体,C正确;
4
D.NH HCO 溶液中含有NH 和HCO ,NH 可以与水分子形成氢键,增大了NH 在水中的溶解度,
4 3
D错误;
故答案选C。
1 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司2.(2025·广东卷)声波封印,材料是音乐存储技术的基础。下列说法错误的是
A.制作黑胶唱片使用的聚氯乙烯,其单体是
B.磁带可由四氧化三铁涂覆在胶带上制成, 具有磁性
C.光碟擦写过程中材料在晶态和非晶态间的可逆转换,涉及物理变化
D.固态硬盘芯片常使用单晶硅作为基础材料,单晶硅是一种共价晶体
【答案】A
【解析】A.聚氯乙烯的单体应为氯乙烯(CH=CHCl),而选项中的CHCHCl是氯乙烷,单体错
2 3 2
误,A错误;
B.四氧化三铁(Fe O)具有磁性,常用于磁带制作,B正确;
3 4
C.光碟擦写时晶态与非晶态转换属于物理变化(无新物质生成),C正确;
D.单晶硅为共价晶体(原子晶体),固态硬盘芯片使用单晶硅,D正确;
故选A。
3.(2025·河北卷)化学研究应当注重宏观与微观相结合。下列宏观现象与微观解释不符的是
选
宏观现象 微观解释
项
A 氮气稳定存在于自然界中 氮分子中存在氮氮三键,断开该共价键需要较多的能量
B 苯不能使溴的 溶液褪色 苯分子中碳原子形成了稳定的大 键
C 天然水晶呈现多面体外形 原子在三维空间里呈周期性有序排列
氯化钠晶体熔点高于氯化铝晶 离子晶体中离子所带电荷数越少,离子半径越大,离子晶体熔点
D
体 越低
【答案】D
【解析】A.氮气的稳定性源于氮分子中的三键,键能高难以断裂,A正确;
B.苯因大π键结构稳定,难以与溴发生加成或取代,B正确;
C.水晶的规则外形由原子三维有序排列(晶体结构)导致,C正确;
D.氯化钠熔点高于氯化铝的真实原因是氯化铝为分子晶体而非离子晶体,选项中将二者均视为离子晶
体并用离子电荷和半径解释,不符合实际,D错误;
故选D。
4.(2025·云南卷)Be及其化合物的转化关系如图。下列说法错误的是
A. 是两性氢氧化物
2 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司B. 和 的晶体类型相同
C. 中Be原子的杂化方式为
D. 与 反应:
【答案】B
【解析】A.由图中转化信息可知, 既能与盐酸反应生成盐和水,又能与氢氧化钠反应生成
盐,因此其是两性氢氧化物,A正确;
B.由题中信息可知, 的熔点远远高于 的,因此 不可能是分子晶体,而 的熔点
和沸点均较低,其为分子晶体,因此两者的晶体类型不相同,B错误;
C. 中 Be 原子与4个羟基形成4个σ键,没有孤电子对,只有4个成键电子对,因
此,其杂化方式为 sp3,C正确;
D. 中的Be化合价为+2,C的化合价为-4,因此其与 反应生成 和 ,该反应的化
学方程式为 ,D正确;
综上所述,本题选B。
5.(2024·天津卷)我国学者在碳化硅 表面制备出超高迁移率半导体外延石墨烯。下列说法正确的是
A. 是离子化合物 B. 晶体的熔点高、硬度大
C.核素 的质子数为8 D.石墨烯属于烯烃
【答案】B
【解析】A.SiC晶体结构与金刚石相似,属于共价晶体,A错误;
B.SiC晶体结构与金刚石相似,属于共价晶体,熔点高、硬度大,B正确;
C.C元素为6号元素,故核素 的质子数为6,C错误;
D.石墨烯是碳元素构成的单质,不属于烯烃,D错误;
故选B。
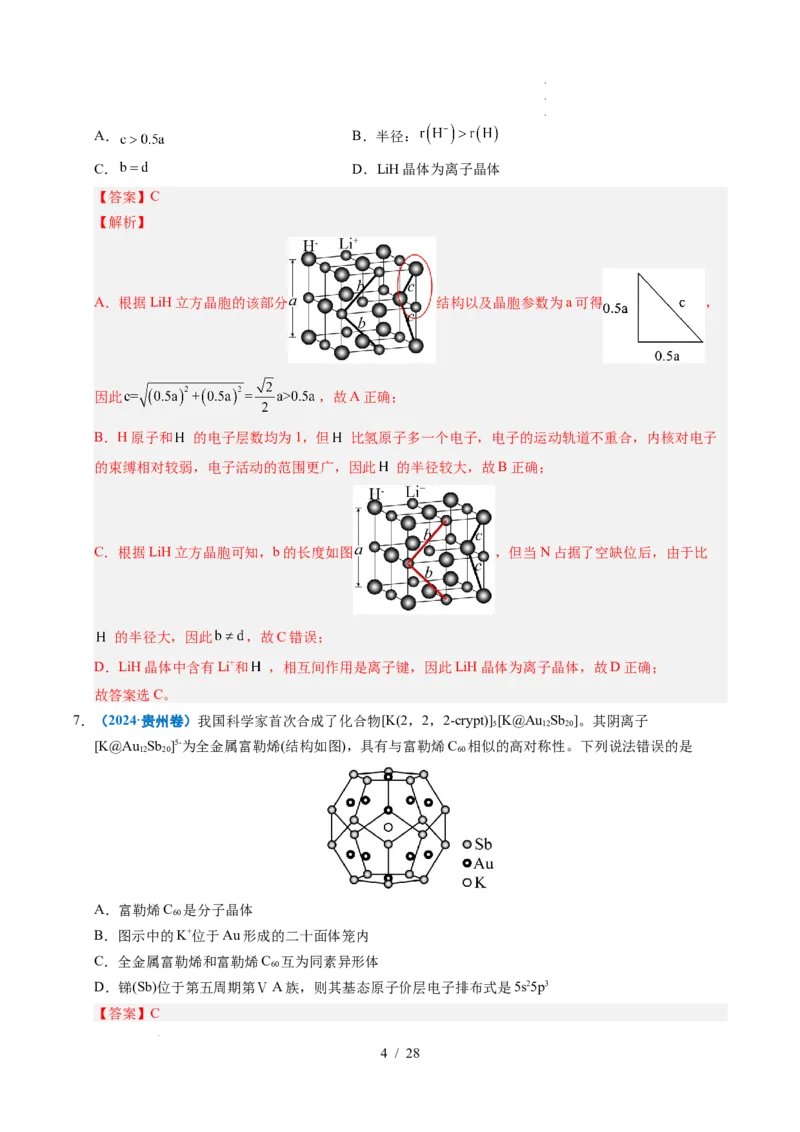
6.(2024·广西卷)一定条件下,存在 缺陷位的LiH晶体能吸附 使其分解为N,随后N占据缺陷位
(如图)。下列说法错误的是
3 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A. B.半径:
C. D.LiH晶体为离子晶体
【答案】C
【解析】
A.根据LiH立方晶胞的该部分 结构以及晶胞参数为a可得 ,
因此 ,故A正确;
B.H原子和 的电子层数均为1,但 比氢原子多一个电子,电子的运动轨道不重合,内核对电子
的束缚相对较弱,电子活动的范围更广,因此 的半径较大,故B正确;
C.根据LiH立方晶胞可知,b的长度如图 ,但当N占据了空缺位后,由于比
的半径大,因此 ,故C错误;
D.LiH晶体中含有Li+和 ,相互间作用是离子键,因此LiH晶体为离子晶体,故D正确;
故答案选C。
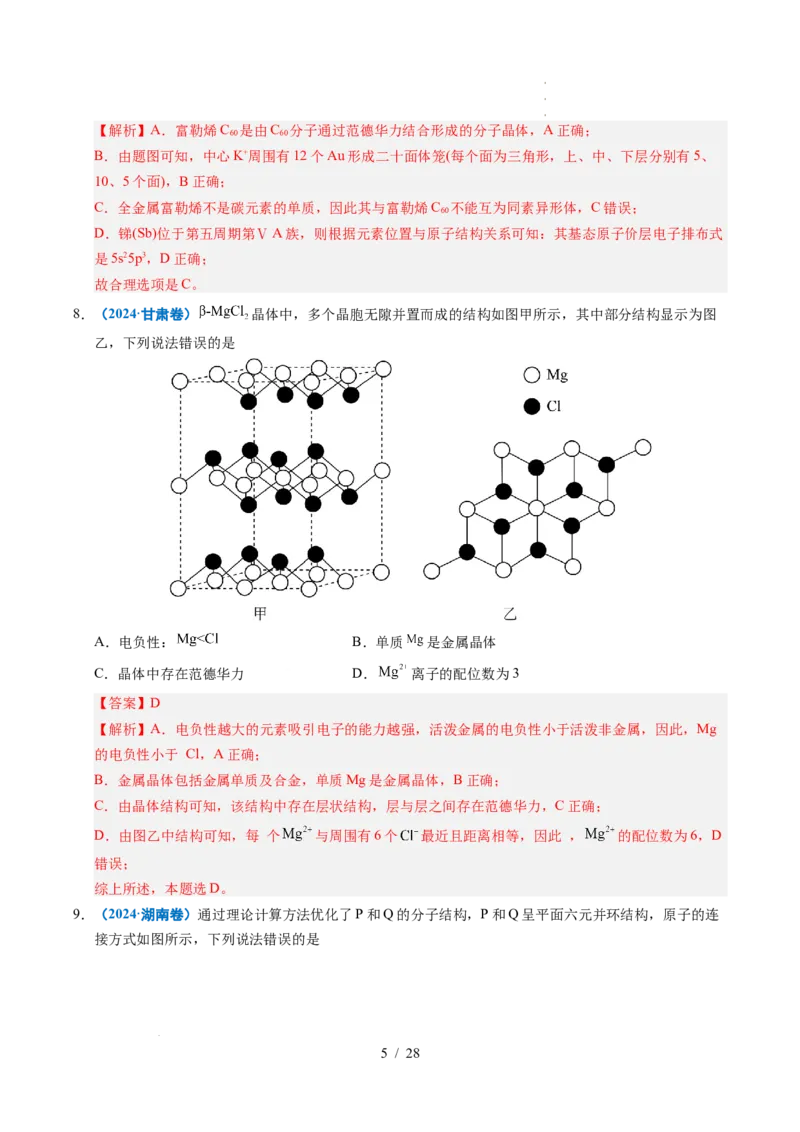
7.(2024·贵州卷)我国科学家首次合成了化合物[K(2,2,2-crypt)] [K@Au Sb ]。其阴离子
5 12 20
[K@Au Sb ]5-为全金属富勒烯(结构如图),具有与富勒烯C 相似的高对称性。下列说法错误的是
12 20 60
A.富勒烯C 是分子晶体
60
B.图示中的K+位于Au形成的二十面体笼内
C.全金属富勒烯和富勒烯C 互为同素异形体
60
D.锑(Sb)位于第五周期第ⅤA族,则其基态原子价层电子排布式是5s25p3
【答案】C
4 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【解析】A.富勒烯C 是由C 分子通过范德华力结合形成的分子晶体,A正确;
60 60
B.由题图可知,中心K+周围有12个Au形成二十面体笼(每个面为三角形,上、中、下层分别有5、
10、5个面),B正确;
C.全金属富勒烯不是碳元素的单质,因此其与富勒烯C 不能互为同素异形体,C错误;
60
D.锑(Sb)位于第五周期第ⅤA族,则根据元素位置与原子结构关系可知:其基态原子价层电子排布式
是5s25p3,D正确;
故合理选项是C。
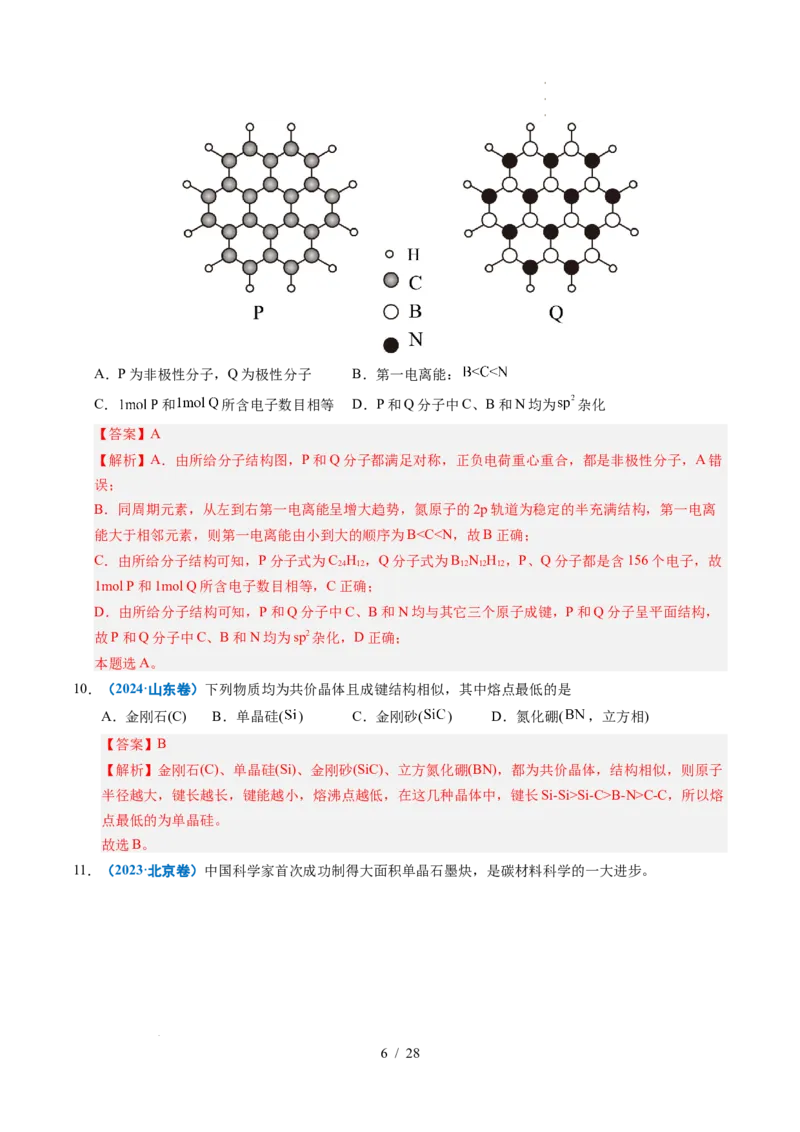
8.(2024·甘肃卷) 晶体中,多个晶胞无隙并置而成的结构如图甲所示,其中部分结构显示为图
乙,下列说法错误的是
A.电负性: B.单质 是金属晶体
C.晶体中存在范德华力 D. 离子的配位数为3
【答案】D
【解析】A.电负性越大的元素吸引电子的能力越强,活泼金属的电负性小于活泼非金属,因此,Mg
的电负性小于 Cl,A正确;
B.金属晶体包括金属单质及合金,单质Mg是金属晶体,B正确;
C.由晶体结构可知,该结构中存在层状结构,层与层之间存在范德华力,C正确;
D.由图乙中结构可知,每 个 与周围有6个 最近且距离相等,因此 , 的配位数为6,D
错误;
综上所述,本题选D。
9.(2024·湖南卷)通过理论计算方法优化了P和Q的分子结构,P和Q呈平面六元并环结构,原子的连
接方式如图所示,下列说法错误的是
5 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.P为非极性分子,Q为极性分子 B.第一电离能:
C. 和 所含电子数目相等 D.P和Q分子中C、B和N均为 杂化
【答案】A
【解析】A.由所给分子结构图,P和Q分子都满足对称,正负电荷重心重合,都是非极性分子,A错
误;
B.同周期元素,从左到右第一电离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,第一电离
能大于相邻元素,则第一电离能由小到大的顺序为BSi-C>B-N>C-C,所以熔
点最低的为单晶硅。
故选B。
11.(2023·北京卷)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
6 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司下列关于金刚石、石墨、石墨炔的说法正确的是
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
【答案】A
【解析】A.原子间优先形成 键,三种物质中均存在 键,A项正确;
B.金刚石中所有碳原子均采用 杂化,石墨中所有碳原子均采用 杂化,石墨炔中苯环上的碳原
子采用 杂化,碳碳三键上的碳原子采用 杂化,B项错误;
C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;
D.金刚石中没有自由移动电子,不能导电,D项错误;
故选A。
12.(2022·天津卷)一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法正确的是
A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨
【答案】D
【解析】A.石墨转化为金刚石吸收能量,则石墨能量低,根据能量越低越稳定,因此石墨比金刚石
稳定,故A错误;
B.金刚石是空间网状正四面体形,键角为109°28′,石墨是层内正六边形,键角为120°,因此碳碳
键的键角不相同,故B错误;
C.金刚石是空间网状正四面体形,石墨是层内正六边形,层与层之间通过范德华力连接,1mol金刚
石有2mol碳碳 键,1mol石墨有1.5mol碳碳 键,因此等质量的石墨和金刚石中,碳碳 键数目之
比为3∶4,故C错误;
D.金刚石和石墨是两种不同的晶体类型,因此可用X射线衍射仪鉴别,故D正确。
综上所述,答案为D。
13.(2022·湖北卷) 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列关于该碳
玻璃的说法错误的是
7 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.具有自范性 B.与 互为同素异形体
C.含有 杂化的碳原子 D.化学性质与金刚石有差异
【答案】A
【解析】A.自范性是晶体的性质,碳玻璃为非晶态,所以没有自范性,A错误;
B.碳玻璃和 均是由碳元素形成的不同的单质,所以是同素异形体,B正确;
C.碳玻璃具有高硬度,与物理性质金刚石类似,因而结构具有一定的相似性,所以含有 杂化的碳
原子形成化学键,C正确;
D.金刚石与碳玻璃属于同素异形体,性质差异主要表现在物理性质上,化学性质上也有着活性的差
异,D正确;
故选A。
14.(2022·山东卷) 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 杂化 D.晶体中所有原子的配位数均相同
【答案】A
【分析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其
为共价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N
原子与其相邻的原子形成3个普通共价键和1个配位键。
【解析】A.因为AlN、GaN为结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小
于N—Ga的,则N—Al的键能较大,键能越大则其对应的共价晶体的熔点越高,故GaN的熔点低于
AlN,A说错误;
B.不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法正
确;
C.金刚石中每个C原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子对,故C
原子均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,
C说法正确;
D.金刚石中每个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、GaN
与金刚石互为等电子体,则其晶体中所有原子的配位数也均为4,D说法正确。
综上所述,本题选A。
15.(2021·天津卷)下列各组物质的晶体类型相同的是
A.SiO 和SO B.I 和NaCl C.Cu和Ag D.SiC和MgO
2 3 2
【答案】C
【解析】A.SiO 为原子晶体,SO 为分子晶体,晶体类型不同,故A错误;
2 3
B.I 为分子晶体,NaCl为离子晶体,晶体类型不同,故B错误;
2
8 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.Cu和Ag都为金属晶体,晶体类型相同,故C正确;
D.SiC为原子晶体,MgO为离子晶体,晶体类型不同,故D错误;
故选C。
考点 二 晶体 分析与计算
16.(2025·陕晋青宁卷)一种负热膨胀材料的立方晶胞结构如图,晶胞密度为 ,阿伏加德罗常数
的值为 ,下列说法错误的是
A.沿晶胞体对角线方向的投影图为
B. 和B均为 杂化
C.晶体中与 最近且距离相等的 有6个
D. 和B的最短距离为
【答案】A
【解析】
A.由晶胞图可知,晶胞中Ag位于体心,B位于顶点,C、N位于体对角线上,沿晶胞体对角线方向
投影,体对角线上的原子投影到中心(重叠),其余6个顶点原子分别投影到六元环的顶点上,其他体
内的C、N原子都投影到对应顶点原子投影与体心的连线上,则投影图为 ,A错误;
B.Ag位于体心,与周围4个N原子原键,价层电子对数为4,且与4个N原子形成正四面体,则Ag
为 杂化;由晶胞中成键情况知,共用顶点B原子的8个晶胞中,有4个晶胞中存在1个C原子与该
B原子成键,即B原子的价层电子对数为4,为 杂化,B正确;
C.晶胞中Ag位于体心,与 最近且距离相等的 就是该晶胞上、下、左、右、前、后6个相邻的
晶胞体心中的 原子,为6个,C正确;
D.B位于顶点,其个数为 ,Ag、C、N均位于晶胞内,个数分别为1、4、4,由晶胞密度可
9 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司知晶胞参数a= , 和B的最短距离为体对角线的一半,即
,D正确;
故选A。
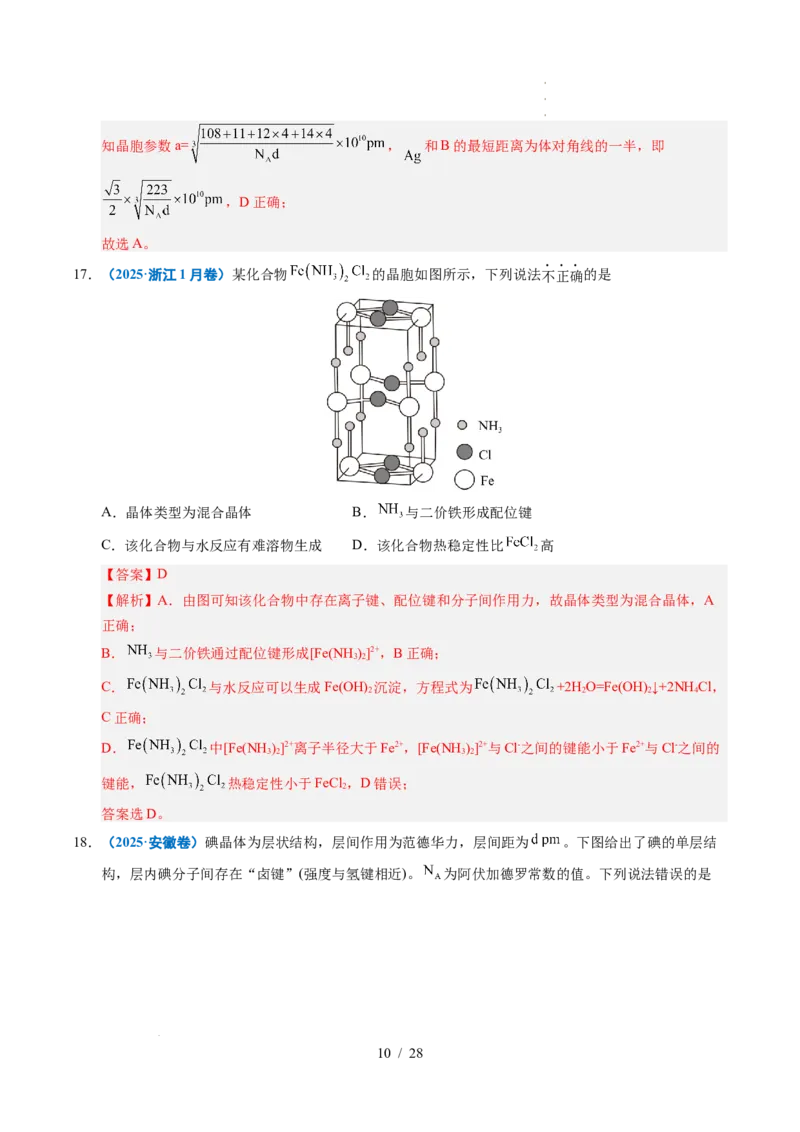
17.(2025·浙江1月卷)某化合物 的晶胞如图所示,下列说法不正确的是
A.晶体类型为混合晶体 B. 与二价铁形成配位键
C.该化合物与水反应有难溶物生成 D.该化合物热稳定性比 高
【答案】D
【解析】A.由图可知该化合物中存在离子键、配位键和分子间作用力,故晶体类型为混合晶体,A
正确;
B. 与二价铁通过配位键形成[Fe(NH )]2+,B正确;
3 2
C. 与水反应可以生成Fe(OH) 沉淀,方程式为 +2H O=Fe(OH) ↓+2NHCl,
2 2 2 4
C正确;
D. 中[Fe(NH )]2+离子半径大于Fe2+,[Fe(NH )]2+与Cl-之间的键能小于Fe2+与Cl-之间的
3 2 3 2
键能, 热稳定性小于FeCl ,D错误;
2
答案选D。
18.(2025·安徽卷)碘晶体为层状结构,层间作用为范德华力,层间距为 。下图给出了碘的单层结
构,层内碘分子间存在“卤键”(强度与氢键相近)。 为阿伏加德罗常数的值。下列说法错误的是
10 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.碘晶体是混合型晶体 B.液态碘单质中也存在“卤键”
C. 碘晶体中有 个“卤键” D.碘晶体的密度为
【答案】A
【解析】A.碘晶体中,分子间是“卤键”(类似氢键),层与层间是范德华力,与石墨不同(石墨层内
只存在共价键)所以碘晶体是分子晶体,A错误;
B.由图可知,题目中的“卤键”类似分子间作用力,只不过强度与氢键接近,则液态碘单质中也存
在类似的分子间作用力,即“卤键”,B正确;
C.由图可知,每个 分子能形成4条“卤键”,每条“卤键”被2个碘分子共用,所以每个碘分子
能形成2个“卤键”, 碘晶体物质的量是0.5mol,“卤键”的个数是 ,
C正确;
D.碘晶体为层状结构,所给区间内4个碘原子处于面心,则每个晶胞中碘原子的个数是 ,晶
胞的体积是 ,密度是 ,D正确;
故选A。
19.(2025·河北卷) 是一种具有优异磁性能的稀土永磁材料,在航空航天等领域中获得重要
应用。 的六方晶胞示意图如下,晶胞参数 、 ,M、N原子的分数坐标分别
为 、 。设 是阿伏加德罗常数的值。
下列说法错误的是
11 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.该物质的化学式为 B.体心原子的分数坐标为
C.晶体的密度为 D.原子Q到体心的距离为
【答案】D
【解析】A.由晶胞图知,白球位于体心,晶胞中数目为1,黑球位于顶角、棱心、体内,六方晶胞
上下表面中一个角60°, 一个角为120°,晶胞中数目为 ,结合题意知,白球
为Sm、黑球为Co,该物质化学式为 ,A正确;
B.体心原子位于晶胞的中心,其分数坐标为 ,B正确;
C.每个晶胞中含有1个“ ”,晶胞底面为菱形,晶胞体积为 ,则晶体密度为
,C正确;
D.原子Q的分数坐标为 ,由体心原子向上底面作垂线,垂足为上底面面心,连接该面心与原
子Q、体心与原子Q可得直角三角形 ,则原子Q到体心的距离
,D错误;
故选D。
20.(2025·云南卷) 是优良的固态电解质材料, 取代部分 后产生空位,可提升
传导性能。取代后材料的晶胞结构示意图( 未画出)及其作为电解质的电池装置如下。下列说法
错误的是
12 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.每个晶胞中 个数为12
B.该晶胞在yz平面的投影为
C. 取代后,该电解质的化学式为
D.若只有 发生迁移,外电路转移的电子数与通过截面MNPQ的 数目相等
【答案】C
【解析】A.由晶胞结构可知,Sc原子分布在晶胞的8个棱心和4个面心,由均摊法算出其原子个数
为 ,由晶体的化学式 可知,O原子的个数是Sc的4倍,因此,每个晶
胞中O2-个数为12,A正确;
B.由晶胞结构可知,该晶胞在yz平面的投影就是其前视图 ,B正确;
C.Ce4+ 取代La3+后,Li+数目减小并产生空位,因此,根据化合价的代数和为0可知,取代后该电解
质的化学式为 ,C错误;
D.Li+与电子所带的电荷数目相同,只是电性不同,原电池中内电路和外电路通过的电量相等,因
此,若只有Li+发生迁移,外电路转移的电子数与通过截面MNPQ的Li+数目相等,D正确;
综上所述,本题选C。
21.(2025·黑吉辽蒙卷) 晶体因x变化形成空位而导致颜色各异,当 时,其立方
晶胞结构如图。设 为阿伏加德罗常数的值,下列说法错误的是
13 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.与W最近且等距的O有6个 B.x增大时,W的平均价态升高
C.密度为 时, D.空位数不同,吸收的可见光波长不同
【答案】B
【解析】A.W位于立方体的顶角,以顶角W为例,在此晶胞内,离该顶角最近且距离相等的O原子
位于该顶角所在3条棱的棱心,由于该顶角在8个晶胞里,而棱上的原子被4个晶胞共有,所以与W
最近且距离相等的O原子有 ,故A正确;
B.O元素化合价为-2价,负化合价总数为-6,设W元素的平均化合价为y,据正负化合价代数和为0
可得:-6+y+x=0,y=6-x,x的值增大y减小,即W元素的平均化合价降低,故B错误;
C. 时,立方晶胞中W个数为 、O个数为 ,若x=0.5,晶胞质量为
,晶胞体积为 ,则密度
,所以密度为 时,x=0.5,故
C正确;
D. 晶体因x变化形成空位而导致颜色各异,即空位数不同,吸收的可见光波长不同,故D
正确;
故答案为:B。
22.(2025·湖北卷) 晶胞是长方体,边长 ,如图所示。下列说法正确的是
14 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.一个晶胞中含有4个O原子
B.晶胞中 分子的取向相同
C.1号和2号S原子间的核间距为
D.每个S原子周围与其等距且紧邻的S原子有4个
【答案】D
【解析】A.由晶胞图可知,SO 分子位于长方体的棱心和体心,1个晶胞中含(12× +1)个SO 分子,
2 2
含有8个O原子,A错误;
B.由图可知晶胞中SO 分子的取向不完全相同,如1和2,B错误;
2
C.1号和2号S原子间的核间距离为上、下面面对角线的一半,即 pm,C错误;
D.以体心的S原子为例,由于a≠b≠c,每个S原子周围与其等距且紧邻(距离最小)的S原子有4个,
D正确;
答案选D。
23.(2025·湖南卷) 掺杂的铋酸钡具有超导性。 替代部分 形成 (摩尔质量为
),其晶胞结构如图所示。该立方晶胞的参数为 ,设 为阿伏加德罗常数的值。下
列说法正确的是
A.晶体中与铋离子最近且距离相等的 有6个
B.晶胞中含有的铋离子个数为8
C.第一电离能:
15 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.晶体的密度为
【答案】A
【解析】A.铋离子位于顶点,与其最近且距离相等的 位于棱心,有6个,分别位于上下、前后、
左右,A正确;
B.晶胞中含有的铋离子个数为 个,B错误;
C.Ba是碱土金属,金属性强于Ca,其易失电子,第一电离能小于O,C错误;
D.晶胞中Ba或K位于体心,个数为总和1, 位于棱心,有 ,所以晶胞的质量是
,晶胞体积是 ,则晶体的密度是: ,D错误;
故选A。
24.(2024·重庆卷)储氢材料 的晶胞结构如图所示, 的摩尔质量为 ,阿伏加德罗常
数的值为 。下列说法正确的是
A. 的配位数为2 B.晶胞中含有2个
C.晶体密度的计算式为 D. (i)和 (ii)之间的距离为
【答案】B
【解析】A.由图可知,与 距离最近且等距离的 的个数是3,则 的配位数为3,A项错误;
B. 位于晶胞的顶点和体心上,该晶胞中 的个数为 ,B项正确;
C.该晶胞体积为 ,该晶胞中 的个数为 ,
的个数为 ,相当于晶胞中含有2个 ,晶体密度为 ,C项
错误;
16 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D. (i)和 (ii)之间的距离等于晶胞体对角线长度的一半,为 ,D项错误;
答案选B。
25.(2024·江西卷)NbO的立方晶胞如图,晶胞参数为anm,P的分数坐标为(0,0,0),阿伏加德罗常数
的值为N ,下列说法正确的是
A
A.Nb的配位数是6
B.Nb和O最短距离为 anm
C.晶体密度
D.M的分数坐标为
【答案】D
【解析】A.由图可知,NbO的立方晶胞中距离Nb原子最近且距离相等的O原子有4个,Nb的配位
数是4,故A错误;
B.由图可知,Nb和O最短距离为边长的 ,晶胞参数为anm,Nb和O最短距离为 anm,故B错
误;
C.根据均摊法计算可知,Nb的个数为6× =3,O的个数为12× =3,即晶胞中含有3个NbO,晶胞
密度为ρ= ,故C错误;
D.P的分数坐标为(0,0,0),M位于正方体的面心,M的分数坐标为( , , ),故D正
确;
故选:D。
26.(2024·河北卷)金属铋及其化合物广泛应用于电子设备、医药等领域。如图是铋的一种氟化物的立方
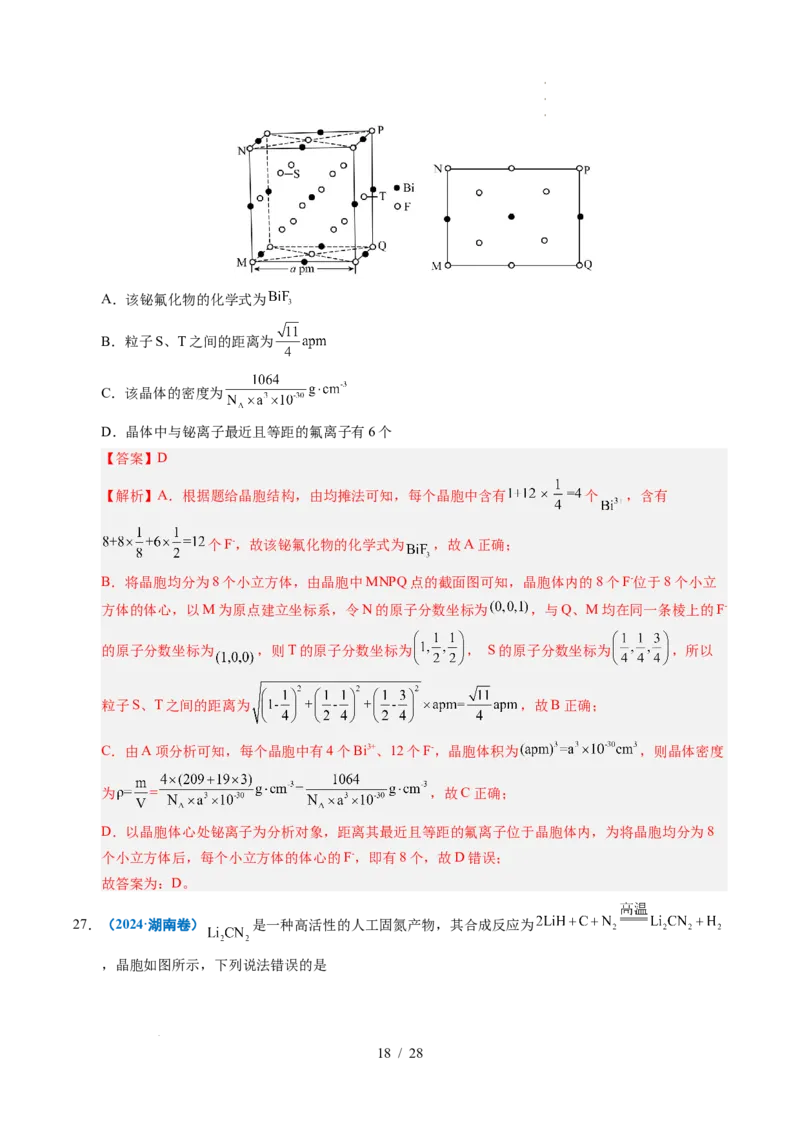
晶胞及晶胞中MNPQ点的截面图,晶胞的边长为 为阿伏加德罗常数的值。下列说法错误的是
17 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.该铋氟化物的化学式为
B.粒子S、T之间的距离为
C.该晶体的密度为
D.晶体中与铋离子最近且等距的氟离子有6个
【答案】D
【解析】A.根据题给晶胞结构,由均摊法可知,每个晶胞中含有 个 ,含有
个F-,故该铋氟化物的化学式为 ,故A正确;
B.将晶胞均分为8个小立方体,由晶胞中MNPQ点的截面图可知,晶胞体内的8个F-位于8个小立
方体的体心,以M为原点建立坐标系,令N的原子分数坐标为 ,与Q、M均在同一条棱上的F-
的原子分数坐标为 ,则T的原子分数坐标为 , S的原子分数坐标为 ,所以
粒子S、T之间的距离为 ,故B正确;
C.由A项分析可知,每个晶胞中有4个Bi3+、12个F-,晶胞体积为 ,则晶体密度
为 = ,故C正确;
D.以晶胞体心处铋离子为分析对象,距离其最近且等距的氟离子位于晶胞体内,为将晶胞均分为8
个小立方体后,每个小立方体的体心的F-,即有8个,故D错误;
故答案为:D。
27.(2024·湖南卷) 是一种高活性的人工固氮产物,其合成反应为
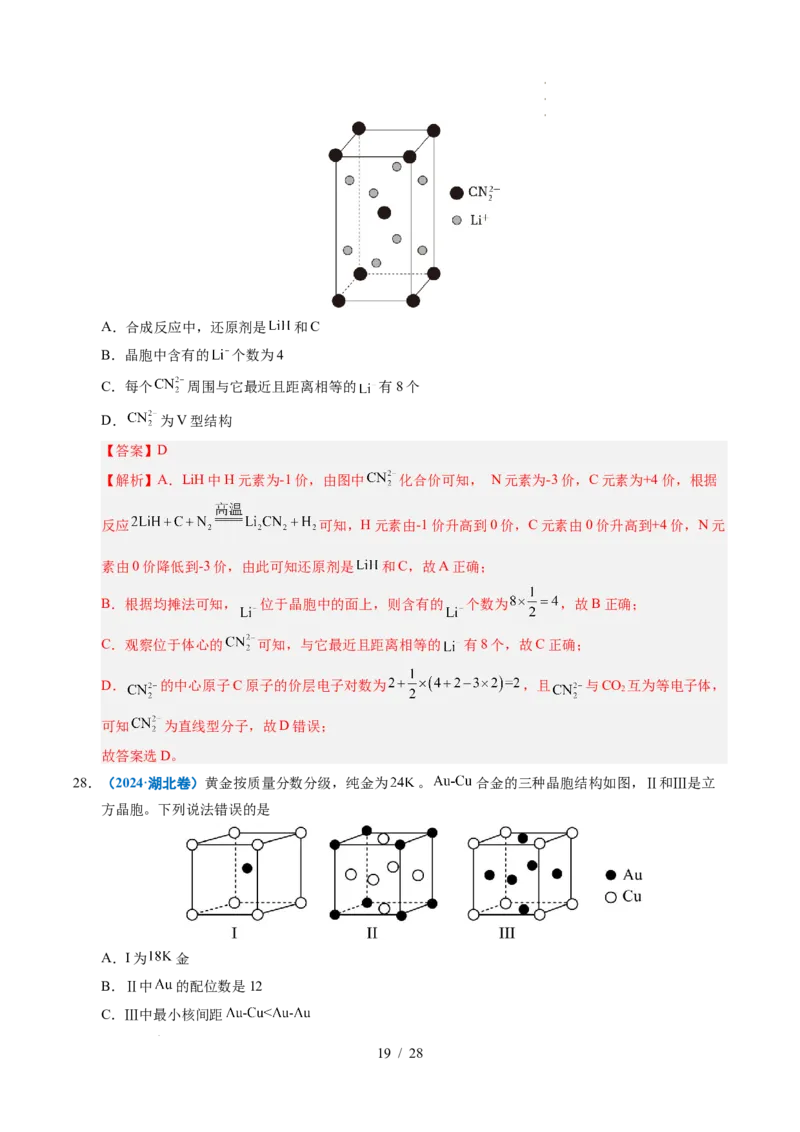
,晶胞如图所示,下列说法错误的是
18 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.合成反应中,还原剂是 和C
B.晶胞中含有的 个数为4
C.每个 周围与它最近且距离相等的 有8个
D. 为V型结构
【答案】D
【解析】A.LiH中H元素为-1价,由图中 化合价可知, N元素为-3价,C元素为+4价,根据
反应 可知,H元素由-1价升高到0价,C元素由0价升高到+4价,N元
素由0价降低到-3价,由此可知还原剂是 和C,故A正确;
B.根据均摊法可知, 位于晶胞中的面上,则含有的 个数为 ,故B正确;
C.观察位于体心的 可知,与它最近且距离相等的 有8个,故C正确;
D. 的中心原子C原子的价层电子对数为 ,且 与CO 互为等电子体,
2
可知 为直线型分子,故D错误;
故答案选D。
28.(2024·湖北卷)黄金按质量分数分级,纯金为 。 合金的三种晶胞结构如图,Ⅱ和Ⅲ是立
方晶胞。下列说法错误的是
A.I为 金
B.Ⅱ中 的配位数是12
C.Ⅲ中最小核间距
19 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.I、Ⅱ、Ⅲ中, 与 原子个数比依次为 、 、
【答案】C
【解析】A.由24K金的质量分数为100%,则18K金的质量分数为: ,I中Au和
Cu原子个数比值为1:1,则Au的质量分数为: ,A正确;
B.Ⅱ中Au处于立方体的八个顶点,Au的配位数指距离最近的Cu,Cu处于面心处,类似于二氧化
碳晶胞结构,二氧化碳分子周围距离最近的二氧化碳有12个,则Au的配位数为12,B正确;
C. 设Ⅲ的晶胞参数为a, 的核间距为 , 的最小核间距也为 ,最小核间距
,C错误;
D. I中, 处于内部, 处于晶胞的八个顶点,其原子个数比为1:1;Ⅱ中, 处于立方体的八
个顶点, 处于面心,其原子个数比为: ;Ⅲ中, 处于立方体的面心, 处于
顶点,其原子个数比为 ;D正确;
故选C。
29.(2024·安徽卷)研究人员制备了一种具有锂离子通道的导电氧化物( ),其立方晶胞和导电
时 迁移过程如下图所示。已知该氧化物中 为 价, 为 价。下列说法错误的是
A.导电时, 和 的价态不变 B.若 , 与空位的数目相等
C.与体心最邻近的O原子数为12 D.导电时、空位移动方向与电流方向相反
【答案】B
【解析】A.根据题意,导电时Li+发生迁移,化合价不变,则Ti和La的价态不变,A项正确;
B.根据“均摊法”,1个晶胞中含Ti:8× =1个,含O:12× =3个,含La或Li或空位共:1个,
若x= ,则La和空位共 ,n(La)+n(空位)= ,结合正负化合价代数和为0,(+1)× +(+3)×n(La)+
(+4)×1+(-2)×3=0,解得n(La)= 、n(空位)= ,Li+与空位数目不相等,B项错误;
20 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.由立方晶胞的结构可知,与体心最邻近的O原子数为12,即位于棱心的12个O原子,C项正确;
D.导电时Li+向阴极移动方向,即与电流方向相同,则空位移动方向与电流方向相反,D项正确;
答案选B。
30.(2024·吉林卷)某锂离子电池电极材料结构如图。结构1是钴硫化物晶胞的一部分,可代表其组成和
结构;晶胞2是充电后的晶胞结构;所有晶胞均为立方晶胞。下列说法错误的是
A.结构1钴硫化物的化学式为 B.晶胞2中S与S的最短距离为
C.晶胞2中距 最近的S有4个 D.晶胞2和晶胞3表示同一晶体
【答案】B
【解析】A.由均摊法得,结构1中含有Co的数目为 ,含有S的数目为 ,Co
与S的原子个数比为9:8,因此结构1的化学式为Co S,故A正确;
9 8
B.由图可知,晶胞2中S与S的最短距离为面对角线的 ,晶胞边长为a,即S与S的最短距离为:
,故B错误;
C.如图: ,以图中的Li为例,与其最近的S共4个,故C正确;
D.如图 ,当2个晶胞2放在一起时,图中红框截取的部分
就是晶胞3,晶胞2和晶胞3表示同一晶体,故D正确;
故选B。
21 / 28
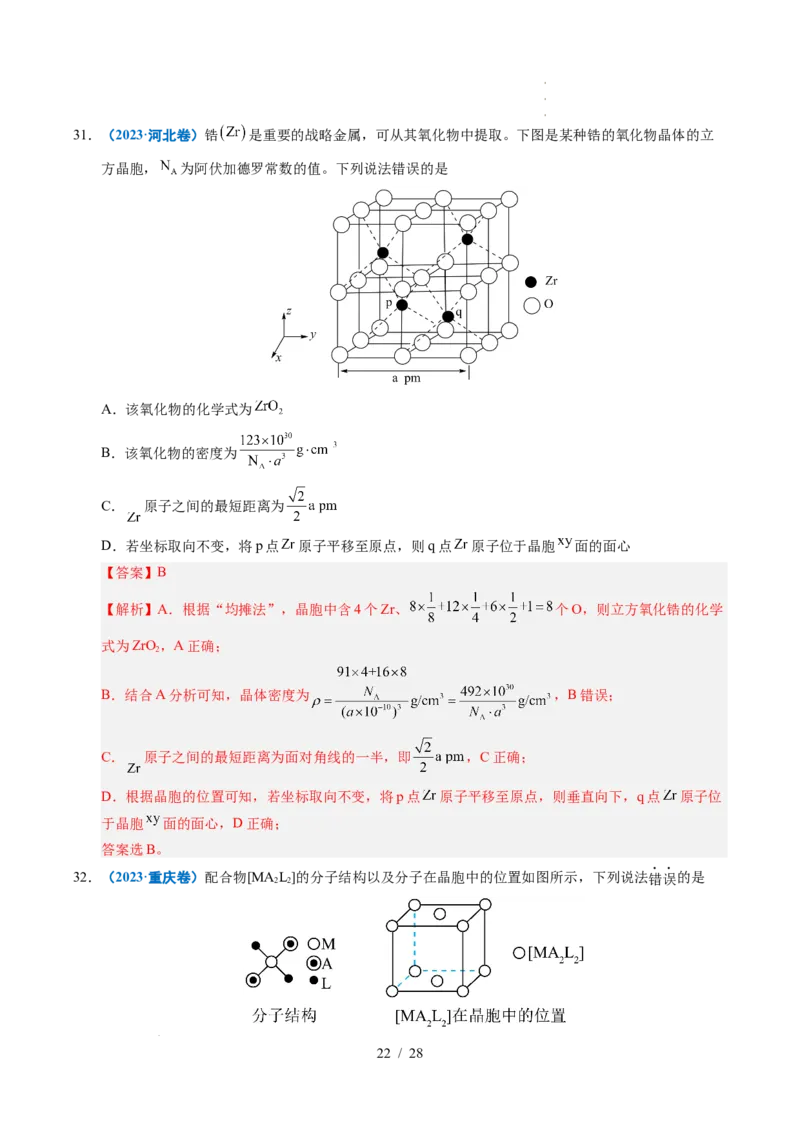
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司31.(2023·河北卷)锆 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立
方晶胞, 为阿伏加德罗常数的值。下列说法错误的是
A.该氧化物的化学式为
B.该氧化物的密度为
C. 原子之间的最短距离为
D.若坐标取向不变,将p点 原子平移至原点,则q点 原子位于晶胞 面的面心
【答案】B
【解析】A.根据“均摊法”,晶胞中含4个Zr、 个O,则立方氧化锆的化学
式为ZrO,A正确;
2
B.结合A分析可知,晶体密度为 ,B错误;
C. 原子之间的最短距离为面对角线的一半,即 ,C正确;
D.根据晶胞的位置可知,若坐标取向不变,将p点 原子平移至原点,则垂直向下,q点 原子位
于晶胞 面的面心,D正确;
答案选B。
32.(2023·重庆卷)配合物[MA L]的分子结构以及分子在晶胞中的位置如图所示,下列说法错误的是
2 2
22 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.中心原子的配位数是4 B.晶胞中配合物分子的数目为2
C.晶体中相邻分子间存在范德华力 D.该晶体属于混合型晶体
【答案】D
【解析】A.由题干配合物[MA L]的分子结构示意图可知,中心原子M周围形成了4个配位键,故中
2 2
心原子M的配位数是4,A正确;
B.由题干图示晶胞结构可知,晶胞中配合物分子的数目为 =2,B正确;
C.由题干信息可知,该晶体为由分子组成的分子晶体,故晶体中相邻分子间存在范德华力,C正
确;
D.由题干信息可知,该晶体为由分子组成的分子晶体,D错误;
故答案为:D。
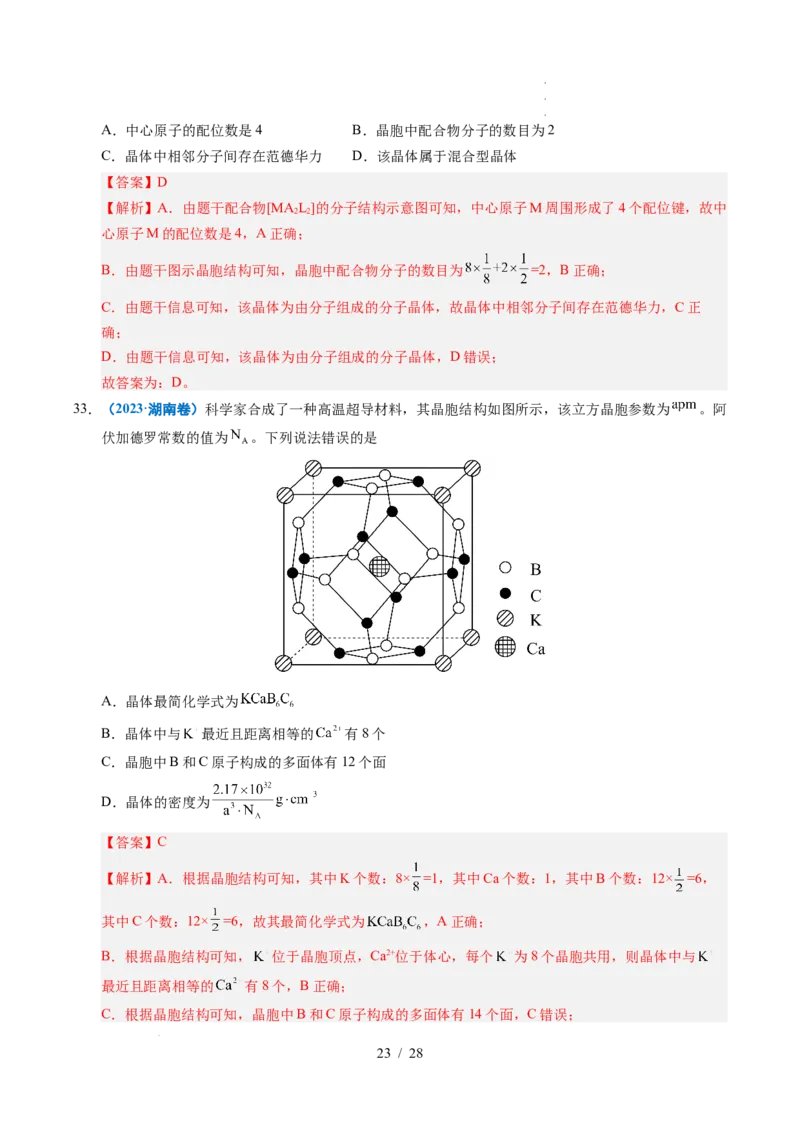
33.(2023·湖南卷)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。阿
伏加德罗常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
【答案】C
【解析】A.根据晶胞结构可知,其中K个数:8× =1,其中Ca个数:1,其中B个数:12× =6,
其中C个数:12× =6,故其最简化学式为 ,A正确;
B.根据晶胞结构可知, 位于晶胞顶点,Ca2+位于体心,每个 为8个晶胞共用,则晶体中与
最近且距离相等的 有8个,B正确;
C.根据晶胞结构可知,晶胞中B和C原子构成的多面体有14个面,C错误;
23 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.根据选项A分析可知,该晶胞最简化学式为 ,则1个晶胞质量为: ,晶胞体积为
a3×10-30cm3,则其密度为 ,D正确;
故选C。
34.(2023·湖北卷)镧La和H可以形成一系列晶体材料 ,在储氢和超导等领域具有重要应用。
属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4个H形成类似
的结构,即得到晶体 。下列说法错误的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
【答案】C
【解析】A.由 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H原
子,若以顶点La研究,与之最近的H原子有8个,则La的配位数为8,故A正确;
B.由 晶胞结构可知,每个H结合4个H形成类似 的结构,H和H之间的最短距离变小,则
晶体中H和H的最短距离: ,故B正确;
C.由题干信息可知,在 晶胞中,每个H结合4个H形成类似 的结构,这样的结构有8个,
顶点数为4 8=32,且不是闭合的结构,故C错误;
D.1个 晶胞中含有5 8=40个H原子,含H质量为 g,晶胞的体积为(484.0 10-10cm)3=(4.84
10-8)3cm3,则 单位体积中含氢质量的计算式为 ,故D正确;
答案选C。
35.(2023·辽宁卷)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),
进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
24 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【解析】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量
为 g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-
30cm3)= g/cm3,A项正确;
B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B项正确;
C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4× =1,Mg的个数小
于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C项错误;
x 1-x
D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生的空位有利
于Li+的传导,D项正确;
答案选C。
36.(2022·湖北卷)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是
A. 的配位数为6 B.与 距离最近的是
C.该物质的化学式为 D.若 换为 ,则晶胞棱长将改变
【答案】B
【解析】A. 配位数为与其距离最近且等距离的F-的个数,如图所示, 位于体心,F-位于面
心,所以 配位数为6,A正确;
25 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司B. 与 的最近距离为棱长的 , 与 的最近距离为棱长的 ,所以与 距离最近的是
,B错误;
C. 位于顶点,所以 个数= =1,F-位于面心,F-个数= =3, 位于体心,所以 个
数=1,综上,该物质的化学式为 ,C正确;
D. 与 半径不同,替换后晶胞棱长将改变,D正确;
故选B。
37.(2021·江苏卷)通过下列实验可从I,的CCl 溶液中回收I。
2 4 2
下列说法正确的是
A.NaOH溶液与I 反应的离子方程式:I+2OH-=I-+IO +H O
2 2 2
B.通过过滤可将水溶液与CCl 分离
4
C.向加酸后的上层清液中滴加AgNO 溶液生成AgI沉淀,1个AgI晶胞(如图)中含14个I-
3
D.回收的粗碘可通过升华进行纯化
【答案】D
【解析】A.选项所给离子方程式元素不守恒,正确离子方程式为:3I+6OH-=5I-+IO +3H O,A错
2 2
误;
B.水溶液与CCl 不互溶,二者应分液分离,B错误;
4
C.根据均摊法,该晶胞中所含I-的个数为 =4,C错误;
D.碘易升华,回收的粗碘可通过升华进行纯化,D正确;
综上所述答案为D。
38.(2021·湖北卷)某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞
结构图,图b表示晶胞的一部分。下列说法正确的是
26 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.该晶胞的体积为a3×10-36cm-3 B.K和Sb原子数之比为3∶1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 apm
【答案】B
【解析】A.该晶胞的边长为 ,故晶胞的体积为 ,A项错误;
B.该晶胞中K的个数为 ,Sb的个数为 ,故K和Sb原子数之比为3∶1,B
项正确;
C.以面心处Sb为研究对象,与Sb最邻近的K原子数为8,C项错误;
D.K和Sb的最短距离为晶胞体对角线长度的 ,即 ,D项错误。
故选B。
39.(2021·辽宁卷)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列说法错误的
是
A.S位于元素周期表p区 B.该物质的化学式为
C.S位于H构成的八面体空隙中 D.该晶体属于分子晶体
【答案】D
【解析】A.S的价电子排布式为:3s23p4,故S位于元素周期表p区,A正确;
B.由该物质形成晶体的晶胞可知:S个数为 ,H个数为: ,故H、S原子个
数比为3:1,故该物质的化学式为 ,B正确;
27 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.S位于H构成的八面体空隙中,如图所示 ,C正确;
D.由于该晶体是一种新型超导材料,说明其是由阴、阳离子构成的,故该晶体属于离子晶体,D错
误;
故答案为:D。
28 / 28
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司