文档内容
秘密★启用前【考试时间2024年11月5日7:45—9:00】
高中 2024 级学生学业发展指导(文化学科)测评
化学
本试卷分为试题卷和答题卡两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)组
成,共6页;答题卡共2页。满分100分,测试时间75分钟。
注意事项:
1.答题前,考生务必将自己的学校、班级、姓名用0.5毫米黑色墨水签字笔填写清楚,同时用
2B铅笔将考号准确填涂在“考号”栏目内。
2.选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,如需改动,用橡皮擦擦干净后再
选涂其它答案;非选择题用0.5毫米黑色墨水签字笔书写在答题卡的对应框内,超出答题区域
书写的答案无效;在草稿纸、试题卷上答题无效。
3.考试结束后将答题卡收回。
可能用到的相对原子质量:
第Ⅰ卷(选择题,共42分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.了解厨房用品的化学成分和性质有助于在家帮厨劳动。下列物质属于电解质的是( )
A.白砂糖 B.食用油 C.氯化钠 D.料酒
2.下列用于物质加热的仪器中,可直接加热的是( )
A.坩埚 B.锥形瓶 C.烧杯 D.蒸馏烧瓶
3.下列物质不能由氯气和单质直接制取的是( )
A. B. C. D.
4.化学变化多种多样,下列变化过程不涉及氧化还原反应的是( )
A.食物腐败变质 B.燃放烟花 C.用发酵粉发面 D.钢铁生锈
5.下列家庭生活用品与其有效成分的化学式、用途的对应关系错误的是( )
选项 A B C D
生活用品 84消毒液 漂白粉 苏打 明矾
有效成分化学式
用途 消毒剂 漂白剂 胃药 净水剂
A.A B.B C.C D.D
6.下列关于胶体的叙述正确的是( )
A.胶体属于化合物
B.胶体、溶液的分类依据是分散系的稳定性
C.丁达尔效应可用于区分 溶液与 胶体
D.气溶胶、液溶胶是按照分散质的状态进行的分类7.在指定溶液中,下列离子能大量共存的是( )
A.含 的溶液中:
B.澄清透明溶液中:
C.使石蕊试液呈蓝色的溶液中:
D.含大量 的溶液中:
8.常温常压下,电化学还原制氨气的总反应方程式为 。若 代表阿
伏加德罗常数的值,下列说法错误的是( )
A.每当消耗标准状况下 时,生成 的分子数为
B.标准状况下, 的电子数为
C.每产生 得到的电子数目为
D. 的 和 的混合物所含氧原子数为
9.以不同类别物质间的转化为线索,认识钠及其化合物。下列分析正确的是( )
A.X一定属于碱性氧化物 B.反应③可充分说明 属于酸性氧化物
C.反应④说明 的稳定性强于Y D.在水中的溶解度Y小于
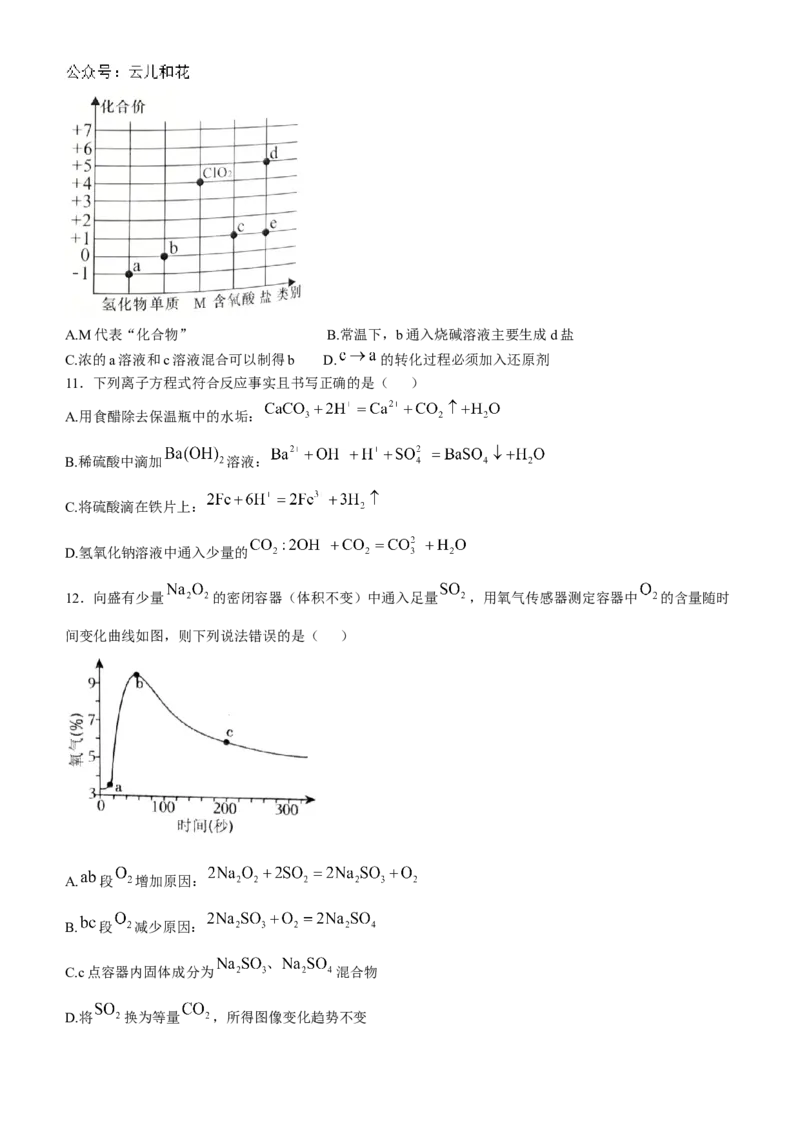
10.右图是氯元素的“价类”二维图。下列说法正确的是( )A.M代表“化合物” B.常温下,b通入烧碱溶液主要生成d盐
C.浓的a溶液和c溶液混合可以制得b D. 的转化过程必须加入还原剂
11.下列离子方程式符合反应事实且书写正确的是( )
A.用食醋除去保温瓶中的水垢:
B.稀硫酸中滴加 溶液:
C.将硫酸滴在铁片上:
D.氢氧化钠溶液中通入少量的
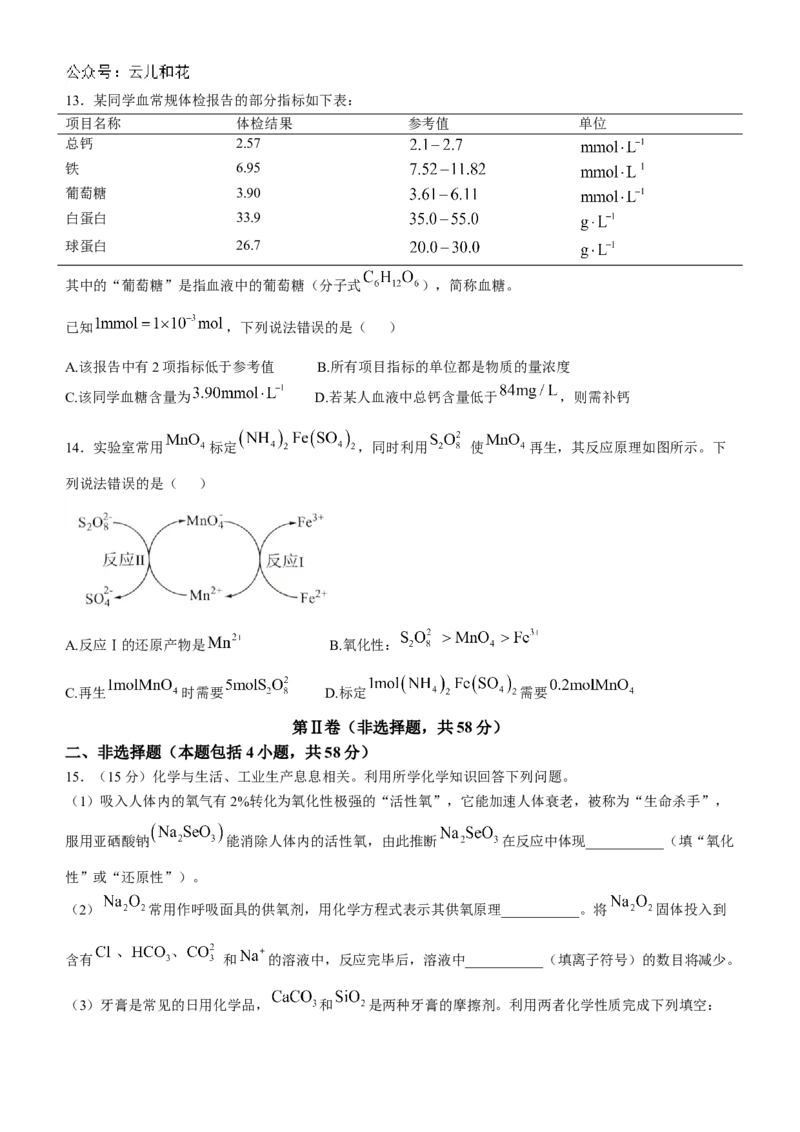
12.向盛有少量 的密闭容器(体积不变)中通入足量 ,用氧气传感器测定容器中 的含量随时
间变化曲线如图,则下列说法错误的是( )
A. 段 增加原因:
B. 段 减少原因:
C.c点容器内固体成分为 混合物
D.将 换为等量 ,所得图像变化趋势不变13.某同学血常规体检报告的部分指标如下表:
项目名称 体检结果 参考值 单位
总钙 2.57
铁 6.95
葡萄糖 3.90
白蛋白 33.9
球蛋白 26.7
其中的“葡萄糖”是指血液中的葡萄糖(分子式 ),简称血糖。
已知 ,下列说法错误的是( )
A.该报告中有2项指标低于参考值 B.所有项目指标的单位都是物质的量浓度
C.该同学血糖含量为 D.若某人血液中总钙含量低于 ,则需补钙
14.实验室常用 标定 ,同时利用 使 再生,其反应原理如图所示。下
列说法错误的是( )
A.反应Ⅰ的还原产物是 B.氧化性:
C.再生 时需要 D.标定 需要
第Ⅱ卷(非选择题,共58分)
二、非选择题(本题包括4小题,共58分)
15.(15分)化学与生活、工业生产息息相关。利用所学化学知识回答下列问题。
(1)吸入人体内的氧气有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,
服用亚硒酸钠 能消除人体内的活性氧,由此推断 在反应中体现___________(填“氧化
性”或“还原性”)。
(2) 常用作呼吸面具的供氧剂,用化学方程式表示其供氧原理___________。将 固体投入到
含有 和 的溶液中,反应完毕后,溶液中___________(填离子符号)的数目将减少。
(3)牙膏是常见的日用化学品, 和 是两种牙膏的摩擦剂。利用两者化学性质完成下列填空:① 具有酸性氧化物的性质,可与强碱反应,写出 与 反应生成 的离子方程式
_______________________________。
②牙膏中的摩擦剂碳酸钙可以用以下两种方案制备:
方案甲:石灰石 生石灰 熟石灰 碳酸钙
方案乙:石灰石 氯化钙 碳酸钙
食品包装袋中常用以上两方案中的物质___________(填化学式)做干燥剂。若步骤③加入纯碱,则该步反应
的化学方程式是____________________________。两种方案相比,方案乙的优势是
______________________________。
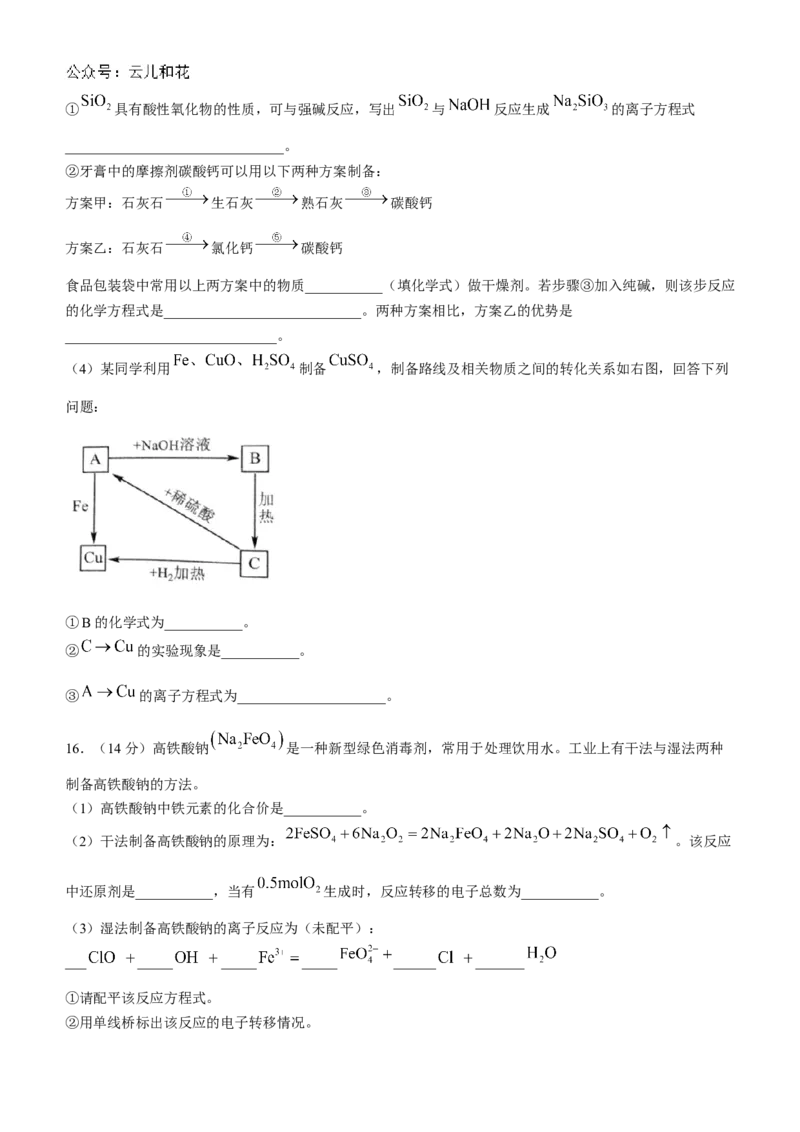
(4)某同学利用 制备 ,制备路线及相关物质之间的转化关系如右图,回答下列
问题:
①B的化学式为___________。
② 的实验现象是___________。
③ 的离子方程式为_____________________。
16.(14分)高铁酸钠 是一种新型绿色消毒剂,常用于处理饮用水。工业上有干法与湿法两种
制备高铁酸钠的方法。
(1)高铁酸钠中铁元素的化合价是___________。
(2)干法制备高铁酸钠的原理为: 。该反应
中还原剂是___________,当有 生成时,反应转移的电子总数为___________。
(3)湿法制备高铁酸钠的离子反应为(未配平):
___ _____ _____ _____ ______ _______
①请配平该反应方程式。
②用单线桥标出该反应的电子转移情况。③被氧化的元素和被还原的元素的物质的量之比为___________。
(4) 处理饮用水时会生成 胶体。实验室用 饱和溶液制备 胶体的操作方
法和现象是______________________________________________________。
(5)工业上常用二氧化氯 、高铁酸钠 等替代传统的 对淡水进行处理。 和
在水处理过程中分别被还原为 和 ,如果以单位质量的氧化剂所得到的电子数来表示消毒
的效率,那么 三种消毒杀菌剂的消毒效率由大到小的顺序是
_____________________________(填化学式)。
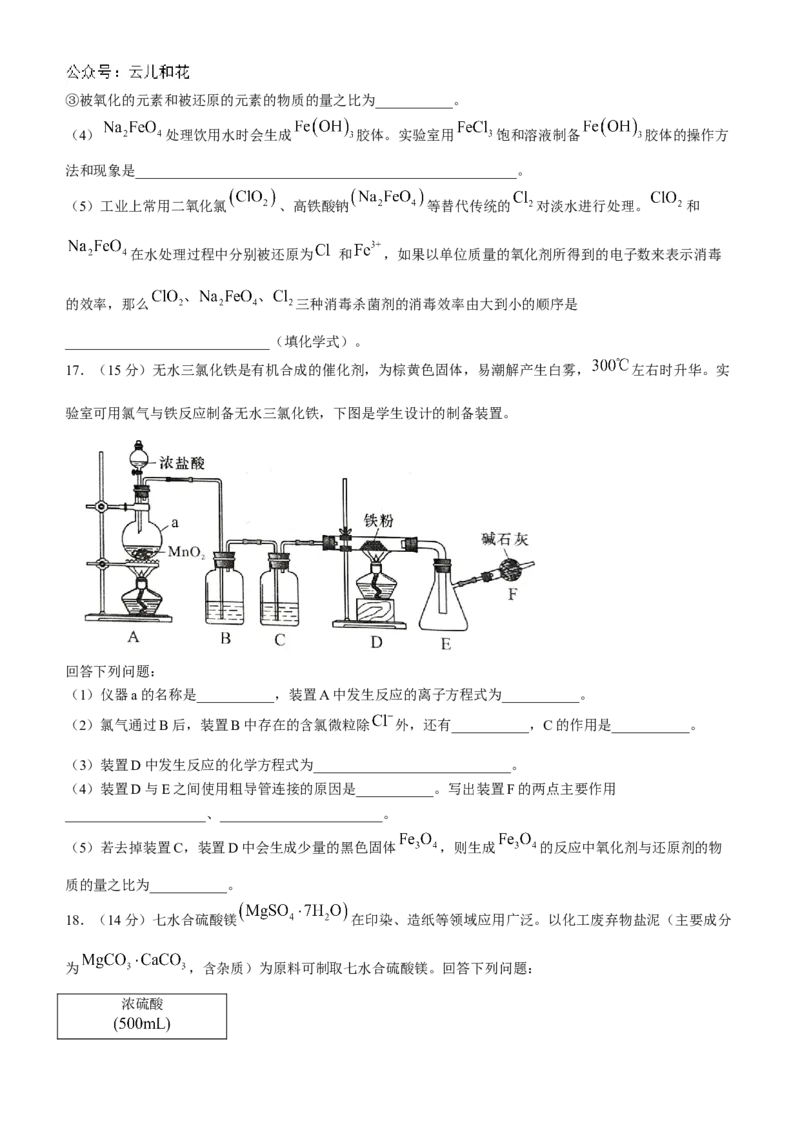
17.(15分)无水三氯化铁是有机合成的催化剂,为棕黄色固体,易潮解产生白雾, 左右时升华。实
验室可用氯气与铁反应制备无水三氯化铁,下图是学生设计的制备装置。
回答下列问题:
(1)仪器a的名称是___________,装置A中发生反应的离子方程式为___________。
(2)氯气通过B后,装置B中存在的含氯微粒除 外,还有___________,C的作用是___________。
(3)装置D中发生反应的化学方程式为____________________________。
(4)装置D与E之间使用粗导管连接的原因是___________。写出装置F的两点主要作用
____________________、_______________________。
(5)若去掉装置C,装置D中会生成少量的黑色固体 ,则生成 的反应中氧化剂与还原剂的物
质的量之比为___________。
18.(14分)七水合硫酸镁 在印染、造纸等领域应用广泛。以化工废弃物盐泥(主要成分
为 ,含杂质)为原料可制取七水合硫酸镁。回答下列问题:
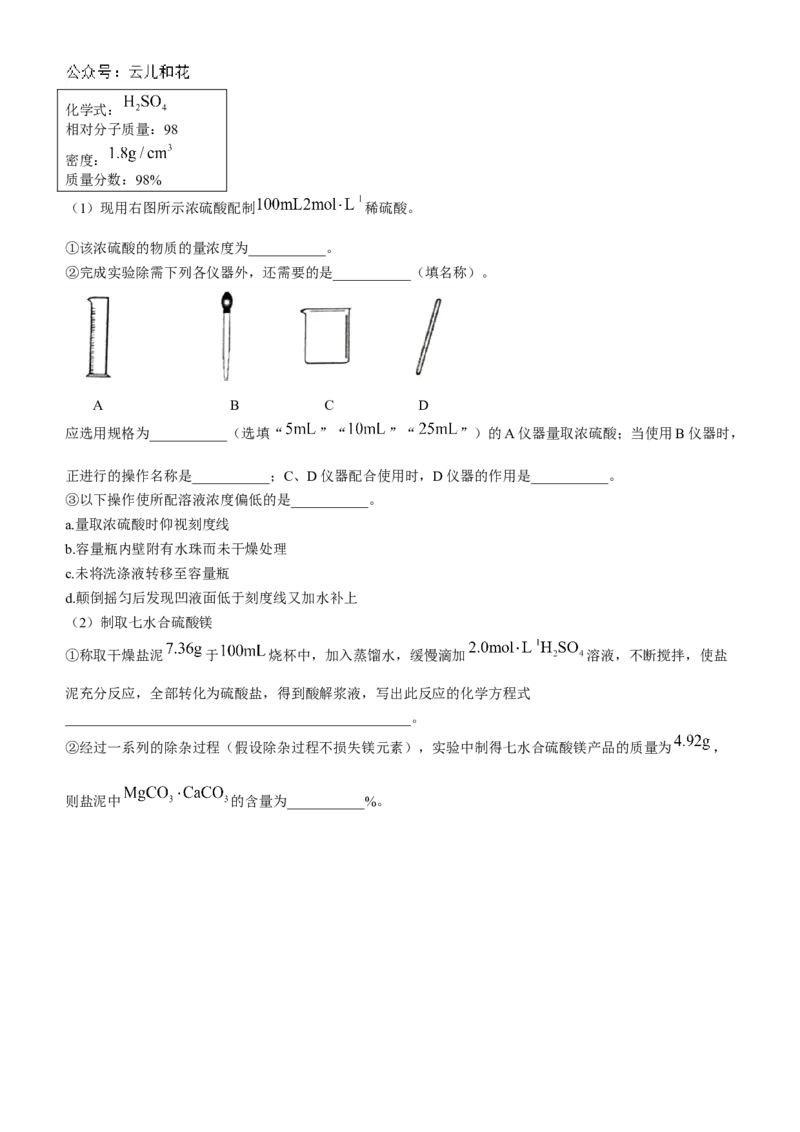
浓硫酸化学式:
相对分子质量:98
密度:
质量分数:98%
(1)现用右图所示浓硫酸配制 稀硫酸。
①该浓硫酸的物质的量浓度为___________。
②完成实验除需下列各仪器外,还需要的是___________(填名称)。
A B C D
应选用规格为___________(选填“ ”“ ”“ ”)的A仪器量取浓硫酸;当使用B仪器时,
正进行的操作名称是___________;C、D仪器配合使用时,D仪器的作用是___________。
③以下操作使所配溶液浓度偏低的是___________。
a.量取浓硫酸时仰视刻度线
b.容量瓶内壁附有水珠而未干燥处理
c.未将洗涤液转移至容量瓶
d.颠倒摇匀后发现凹液面低于刻度线又加水补上
(2)制取七水合硫酸镁
①称取干燥盐泥 于 烧杯中,加入蒸馏水,缓慢滴加 溶液,不断搅拌,使盐
泥充分反应,全部转化为硫酸盐,得到酸解浆液,写出此反应的化学方程式
_________________________________________________。
②经过一系列的除杂过程(假设除杂过程不损失镁元素),实验中制得七水合硫酸镁产品的质量为 ,
则盐泥中 的含量为___________%。