文档内容
山东省德州市五校2025-2026学年高一上学期11月联考
化学试题
一、单选题
1.化学是一门充满神奇色彩的科学,下列说法错误的是
A.化学家可以在微观层面操纵分子和原子,组装分子材料
B.化学家制造出自然界中不存在的新物质、新材料满足人们生产生活需求
C.我国科学家发现并合成了青蒿素,说明化学是一门具有创造性的科学
D.法国科学家拉瓦锡提出原子论,为近代化学的发展奠定了坚实的基础
2.实验室安全至关重要,下列实验安全措施正确的是
A.活泼金属钠燃烧起火,立即用二氧化碳灭火器灭火
B.实验室未用完的钠、钾、白磷不能放回原试剂瓶探究
C.钠与水的反应时,实验安全注意事项图标为
D.如果不慎将酸沾到皮肤上,立即用大量水冲洗,再用氢氧化钠溶液冲洗
3.下列事实及其解释错误的是
A.氯水可以使有色布条褪色,是因为 具有漂白性
B.钠保存在煤油中是因为煤油不与钠反应且密度比钠小,可以隔绝空气和水蒸气
C.为增强漂白能力向漂白粉溶液中加入少量白醋,原因是醋酸的酸性比次氯酸强
D.向包有 的脱脂棉吹气,脱脂棉燃烧,说明 、 与 反应放热且有 生成
4.下列对应离子方程式书写正确的是
A.Fe粉投入 溶液中:
B.向漂白粉溶液中通入过量 :
C. 通入石灰乳中:
D.过量 通入饱和碳酸钠溶液中:5.食盐是日常生活的必需品,也是重要的化工原料。为除去粗盐中的 、 、 以及泥沙等杂质,
实验方案如下,下列说法错误的是
粗盐 滤液 精盐
A.试剂 为 溶液,其目的是除溶液中的
B.若先加盐酸再过滤,将对实验结果产生影响
C.粗盐提纯的整个操作过程中共有两处需要使用玻璃棒
D.加入试剂 的主要目的是除去 和
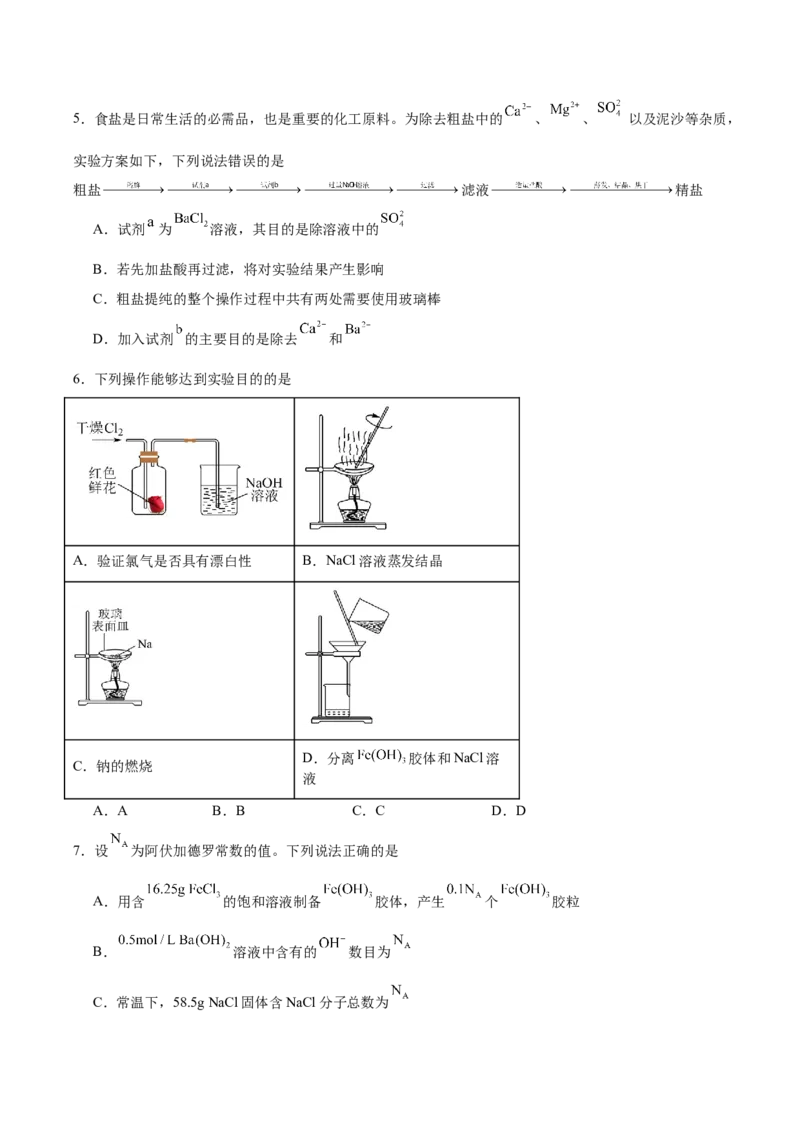
6.下列操作能够达到实验目的的是
A.验证氯气是否具有漂白性 B.NaCl溶液蒸发结晶
D.分离 胶体和NaCl溶
C.钠的燃烧
液
A.A B.B C.C D.D
7.设 为阿伏加德罗常数的值。下列说法正确的是
A.用含 的饱和溶液制备 胶体,产生 个 胶粒
B. 溶液中含有的 数目为
C.常温下,58.5g NaCl固体含NaCl分子总数为D.标准状况下,22.4L NO和 混合气体中氧原子数为
8.下列离子在指定溶液中,一定能大量共存的是
A.某无色澄清透明的溶液中: 、 、 、
B. 溶液中: 、 、 、
C.加入镁条能产生大量氢气的溶液中: 、 、 、
D.澄清透明的溶液中: 、 、 、
9.已知亚磷酸( )与足量NaOH溶液反应生成 ,下列关于物质分类的组合正确的是
碱性氧化
选项 碱 电解质 酸式盐 酸性氧化物
物
A 烧碱 蔗糖 NaHS
B CO
C KOH CaO
D 纯碱
A.A B.B C.C D.D
10.如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。
25℃时向Ⅰ中充入64 g ,Ⅱ中充入64 g ,下列说法正确的是
A.当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为2:1
B.当活塞不再移动时,Ⅰ、Ⅱ两部分密度比为1:2
C.当活塞固定在气缸中间,Ⅰ、Ⅱ两部分压强比为1:2
D.当活塞固定在气缸中间,Ⅰ、Ⅱ两部分原子个数比为4:3
11.下列实验操作得到的现象及结论均正确的是选
实验操作 现象 结论
项
向 胶体中逐滴滴加盐酸至过 胶体带电
A 生成红褐色沉淀
量 荷
将某溶液与稀盐酸反应产生的气体 该溶液中一定含有
B 澄清石灰水变浑浊
通入澄清石灰水
C 取样于试管中,滴加紫色石蕊溶液 溶液呈红色 溶液一定是酸
蛋白质溶液中有一条 此蛋白质溶液属于
D 用激光笔照射烧杯中的蛋白质溶液
光亮的通路 胶体
A.A B.B C.C D.D
12.某无色溶液中只可能含有 中的一种或几种,对其进行如下实
验操作:
①取少量溶液,加入足量 溶液,产生白色沉淀;
②向①所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
③将②)所得混合物过滤,向滤液中加入 溶液,有白色沉淀生成。
下列对该溶液的说法正确的是
A.一定含有 B.可能含有
C.一定含有 D.一定不含
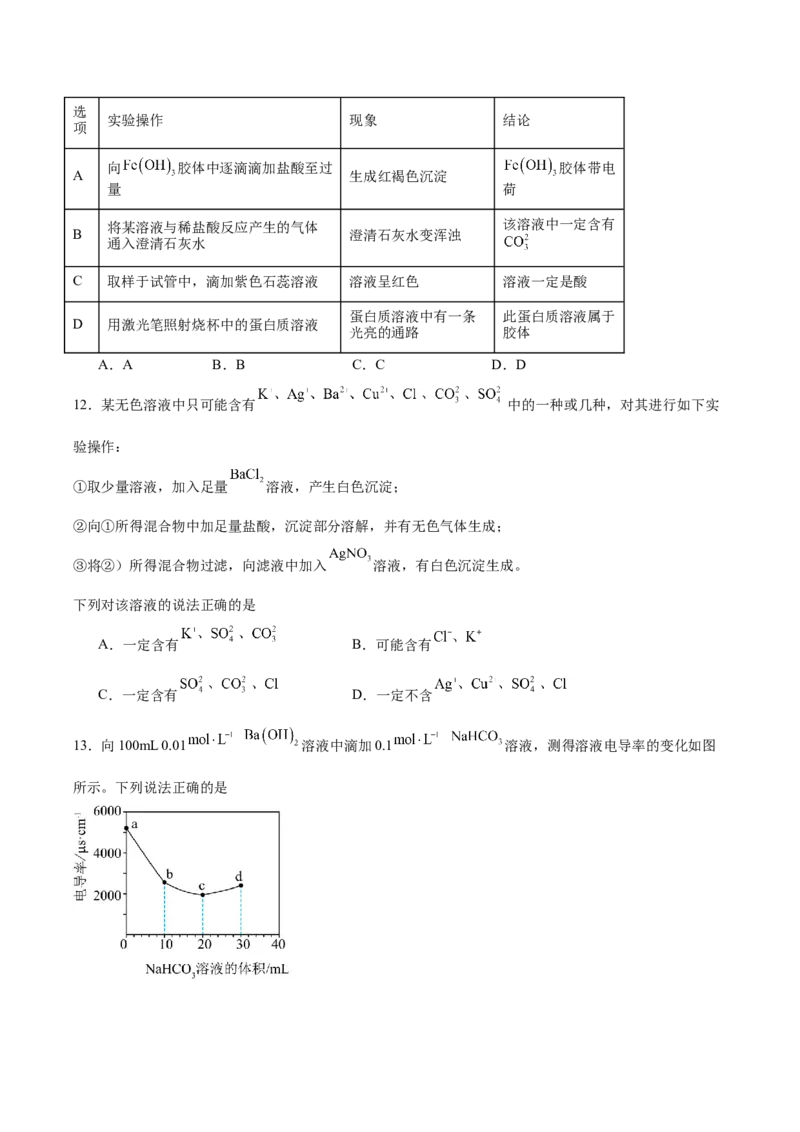
13.向100mL 0.01 溶液中滴加0.1 溶液,测得溶液电导率的变化如图
所示。下列说法正确的是A.a→b电导率下降的主要原因是发生了反应:
B.c点溶液显中性
C.b→c溶液中的 逐渐减小, 逐渐增大
D.c→d溶液电导率逐渐增大的原因是: ,使溶液中离子浓度增大
二、多选题
14.氯及其化合物的“价-类”二维图如图所示,下列说法正确的是
A.乙能使鲜花褪色,说明它具有漂白性
B.丙是新型的自来水消毒剂
C.一定条件下能实现乙→庚的转化
D.相同物质的量的戊和己中所含原子的物质的量之比为3:5
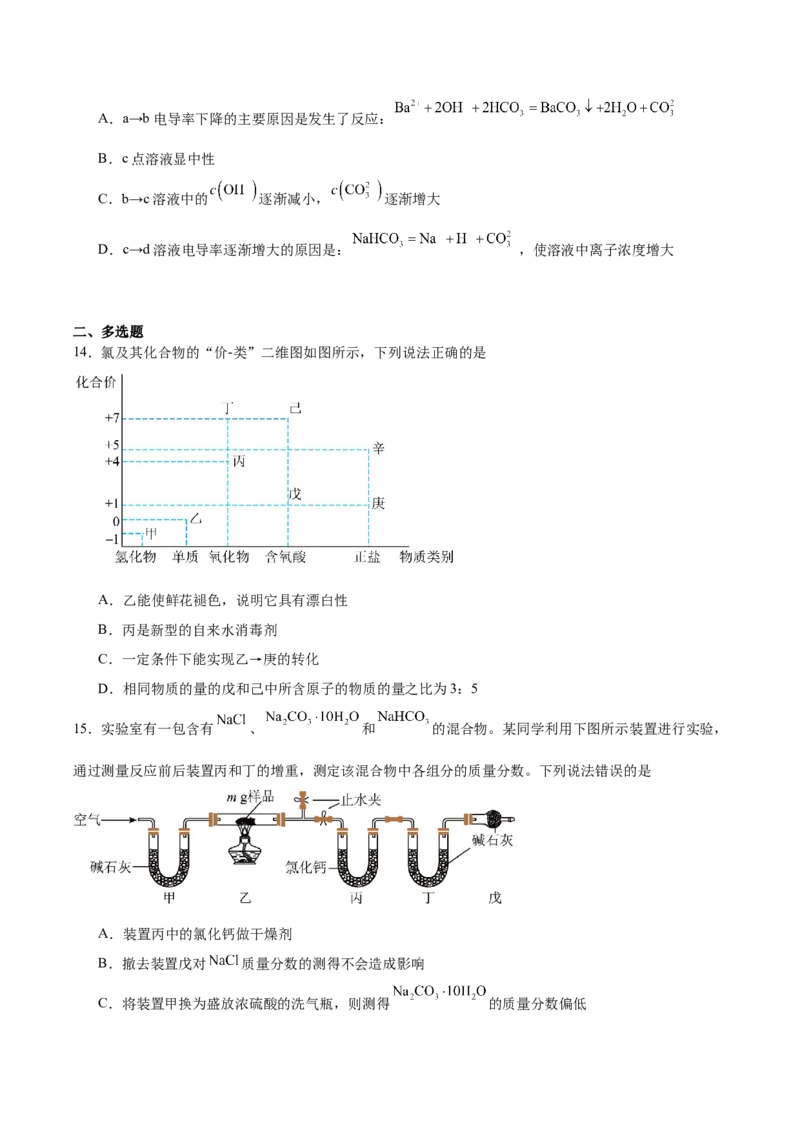
15.实验室有一包含有 、 和 的混合物。某同学利用下图所示装置进行实验,
通过测量反应前后装置丙和丁的增重,测定该混合物中各组分的质量分数。下列说法错误的是
A.装置丙中的氯化钙做干燥剂
B.撤去装置戊对 质量分数的测得不会造成影响
C.将装置甲换为盛放浓硫酸的洗气瓶,则测得 的质量分数偏低D.若能测量样品反应后剩余固体的质量,则撤去装置丁不能达到实验目的
三、填空题
16.下列物质:
①石墨 ②铁 ③液氨 ④ ⑤碳酸氢钠固体 ⑥氢氧化钡溶液 ⑦固态硫酸钡 ⑧熔融氯化钠 ⑨液态氯
化氢
(1)以上物质属于电解质的是 ;属于非电解质的是 ;能导电的是 。
(2)实验室用饱和的 溶液制备 胶体的化学反应方程式 。
(3)将物质⑤配制成溶液,向其溶液中加入少量⑥溶液,写出离子方程式: 。
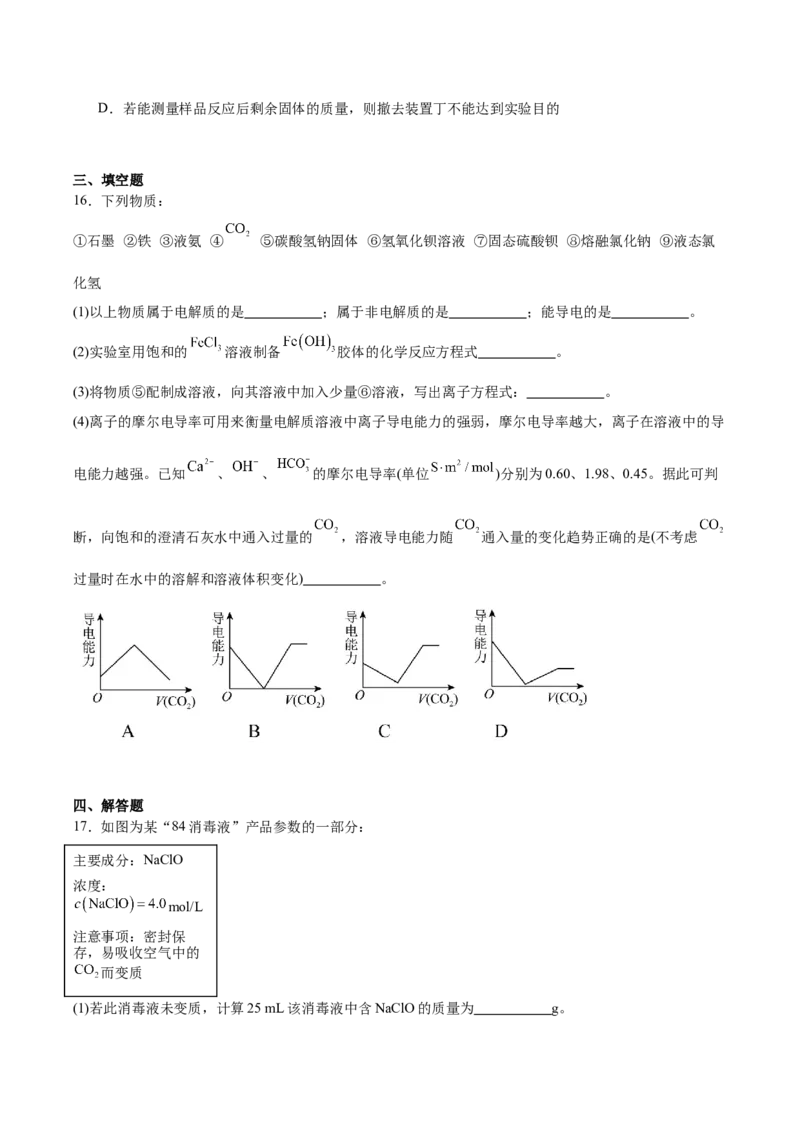
(4)离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导
电能力越强。已知 、 、 的摩尔电导率(单位 )分别为0.60、1.98、0.45。据此可判
断,向饱和的澄清石灰水中通入过量的 ,溶液导电能力随 通入量的变化趋势正确的是(不考虑
过量时在水中的溶解和溶液体积变化) 。
四、解答题
17.如图为某“84消毒液”产品参数的一部分:
主要成分:NaClO
浓度:
mol/L
注意事项:密封保
存,易吸收空气中的
而变质
(1)若此消毒液未变质,计算25 mL该消毒液中含NaClO的质量为 g。(2)变质发生的化学反应方程式 。
(3)取用任意体积的该消毒液时,下列物理量中会随所取体积多少而变化的是___________(填字母)。
A.溶液中NaClO的摩尔质量 B.溶液的浓度
C.溶液中NaClO的物质的量 D.溶液的密度
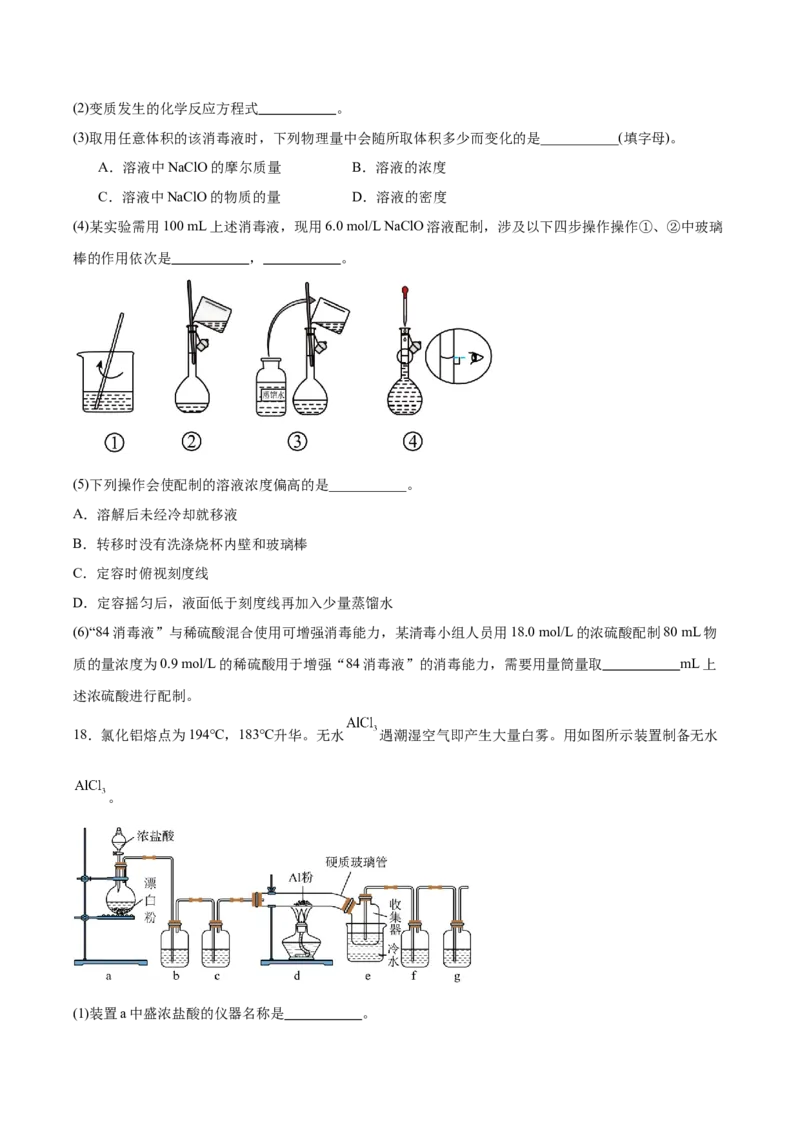
(4)某实验需用100 mL上述消毒液,现用6.0 mol/L NaClO溶液配制,涉及以下四步操作操作①、②中玻璃
棒的作用依次是 , 。
(5)下列操作会使配制的溶液浓度偏高的是___________。
A.溶解后未经冷却就移液
B.转移时没有洗涤烧杯内壁和玻璃棒
C.定容时俯视刻度线
D.定容摇匀后,液面低于刻度线再加入少量蒸馏水
(6)“84消毒液”与稀硫酸混合使用可增强消毒能力,某清毒小组人员用18.0 mol/L的浓硫酸配制80 mL物
质的量浓度为0.9 mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要用量筒量取 mL上
述浓硫酸进行配制。
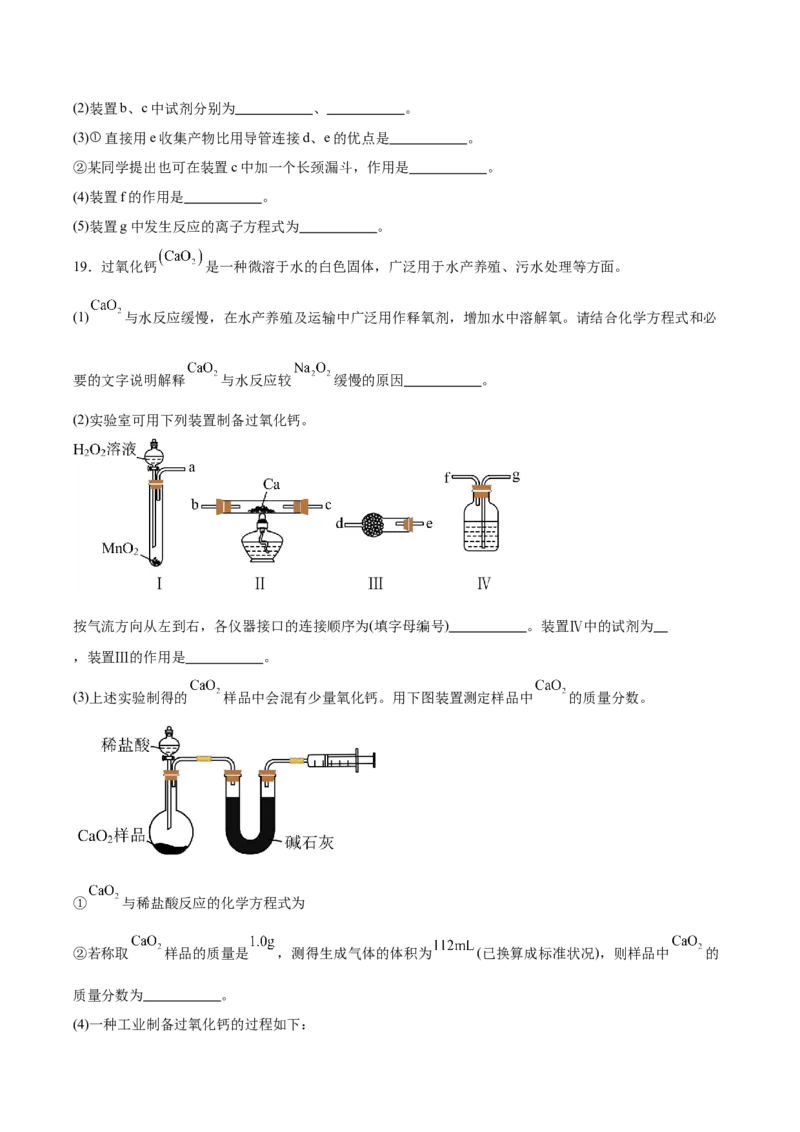
18.氯化铝熔点为194℃,183℃升华。无水 遇潮湿空气即产生大量白雾。用如图所示装置制备无水
。
(1)装置a中盛浓盐酸的仪器名称是 。(2)装置b、c中试剂分别为 、 。
(3)①直接用e收集产物比用导管连接d、e的优点是 。
②某同学提出也可在装置c中加一个长颈漏斗,作用是 。
(4)装置f的作用是 。
(5)装置g中发生反应的离子方程式为 。
19.过氧化钙 是一种微溶于水的白色固体,广泛用于水产养殖、污水处理等方面。
(1) 与水反应缓慢,在水产养殖及运输中广泛用作释氧剂,增加水中溶解氧。请结合化学方程式和必
要的文字说明解释 与水反应较 缓慢的原因 。
(2)实验室可用下列装置制备过氧化钙。
按气流方向从左到右,各仪器接口的连接顺序为(填字母编号) 。装置Ⅳ中的试剂为
,装置Ⅲ的作用是 。
(3)上述实验制得的 样品中会混有少量氧化钙。用下图装置测定样品中 的质量分数。
① 与稀盐酸反应的化学方程式为
②若称取 样品的质量是 ,测得生成气体的体积为 (已换算成标准状况),则样品中 的
质量分数为 。
(4)一种工业制备过氧化钙的过程如下:步骤Ⅰ中反应的化学方程式为 。
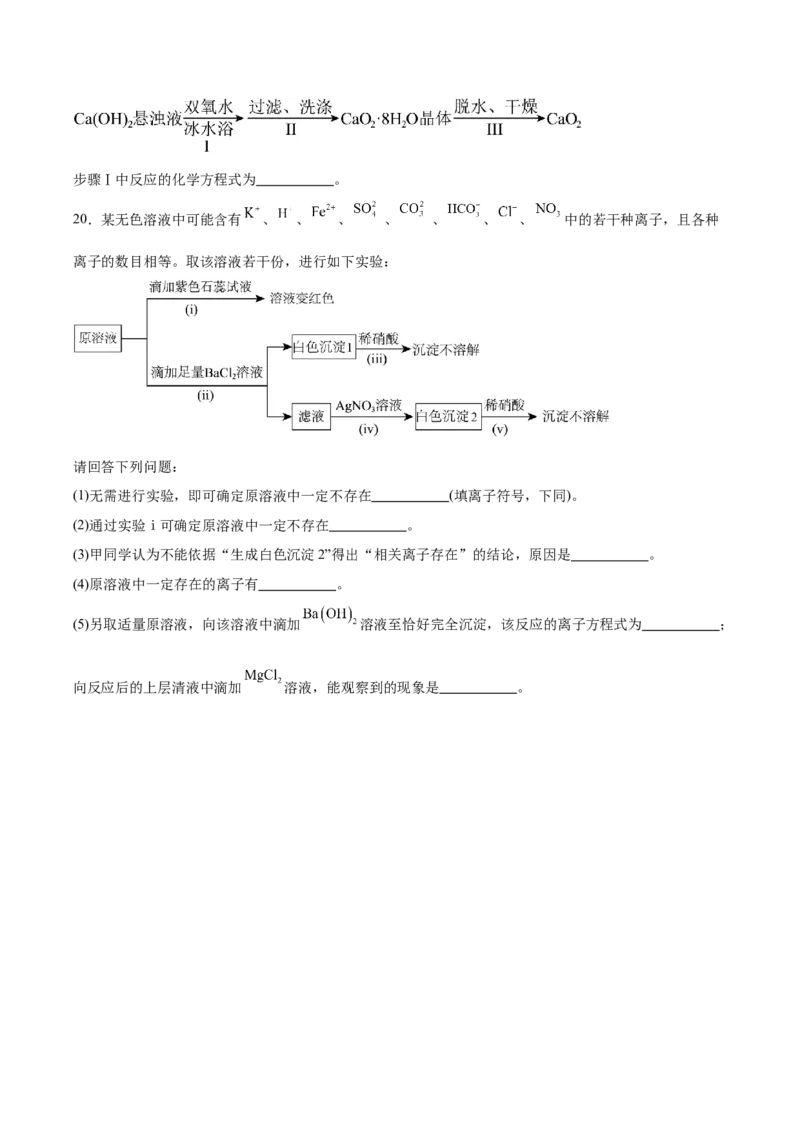
20.某无色溶液中可能含有 、 、 、 、 、 、 、 中的若干种离子,且各种
离子的数目相等。取该溶液若干份,进行如下实验:
请回答下列问题:
(1)无需进行实验,即可确定原溶液中一定不存在 (填离子符号,下同)。
(2)通过实验ⅰ可确定原溶液中一定不存在 。
(3)甲同学认为不能依据“生成白色沉淀2”得出“相关离子存在”的结论,原因是 。
(4)原溶液中一定存在的离子有 。
(5)另取适量原溶液,向该溶液中滴加 溶液至恰好完全沉淀,该反应的离子方程式为 ;
向反应后的上层清液中滴加 溶液,能观察到的现象是 。参考答案
1.D
2.C
3.A
4.D
5.C
6.B
7.D
8.D
9.C
10.C
11.D
12.A
13.C
14.BC
15.BD
16.(1) ⑤⑦⑧⑨ ③④ ①②⑥⑧
(2) (胶体)
(3)
(4)D
17.(1)7.45
(2)
(3)C
(4) 搅拌 引流
(5)AC
(6)5.0
18.(1)分液漏斗
(2) 饱和食盐水 浓硫酸
(3) 防止堵塞 监测实验进行时是否发生堵塞(4)吸水,防止无水 变质(或防止g中水蒸气进入e)
(5)
19.(1)过氧化钙(CaO)微溶于水,在常温下稳定,在潮湿空气及水中发生反应
2
2CaO+2H O=2Ca(OH) +O ↑,生成的Ca(OH) 微溶于水,会覆盖在过氧化钙表面
2 2 2 2 2
(2) agfbced或aggcbed 浓硫酸 防止空气中的水蒸气和二氧化碳进入装置Ⅱ中,使得制得的
过氧化钙不纯
(3) 2CaO +4HCl=2CaCl +2H O+O↑ 72%
2 2 2 2
(4)Ca(OH) +H O+6H O=CaO ·8H O
2 2 2 2 2 2
20.(1)
(2) 、
(3)实验ⅱ中加入 溶液,引入了 干扰
(4) 、 、