文档内容
第二节 氯及其化合物 第1课时 氯气的性质
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.关于氯气的下列说法中不正确的是
A.氯气是黄绿色的有毒气体
B.氯气具有强烈的刺激性
C.相同条件下氯气的密度比空气大
D.氯气溶于水是物理变化过程
2.下列离子方程式正确的是
A. 通入热的NaOH溶液:
B.用醋酸和淀粉-KI溶液检验加碘盐中的
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
3.下列化学用语对事实的表述不正确的是
A.硬脂酸与乙醇的酯化反应:
B.常温时, 氨水的 ,NH •H O +
3 2
⇌
C.次氯酸的结构式为:
D.电解精炼铜的阴极反应:
4.下列实验现象与结论不相符的是
选项 实验现象 实验结论
A 氯水呈黄绿色 氯水中有Cl 分子
2
B 用小刀可以切开钠 钠很软
C 钠可以浮在水面上 钠的密度比水小
D 向饱和NaHCO 溶液中加入足量氯水,有无色气体产生 氯水中有HClO
3A.A B.B C.C D.D
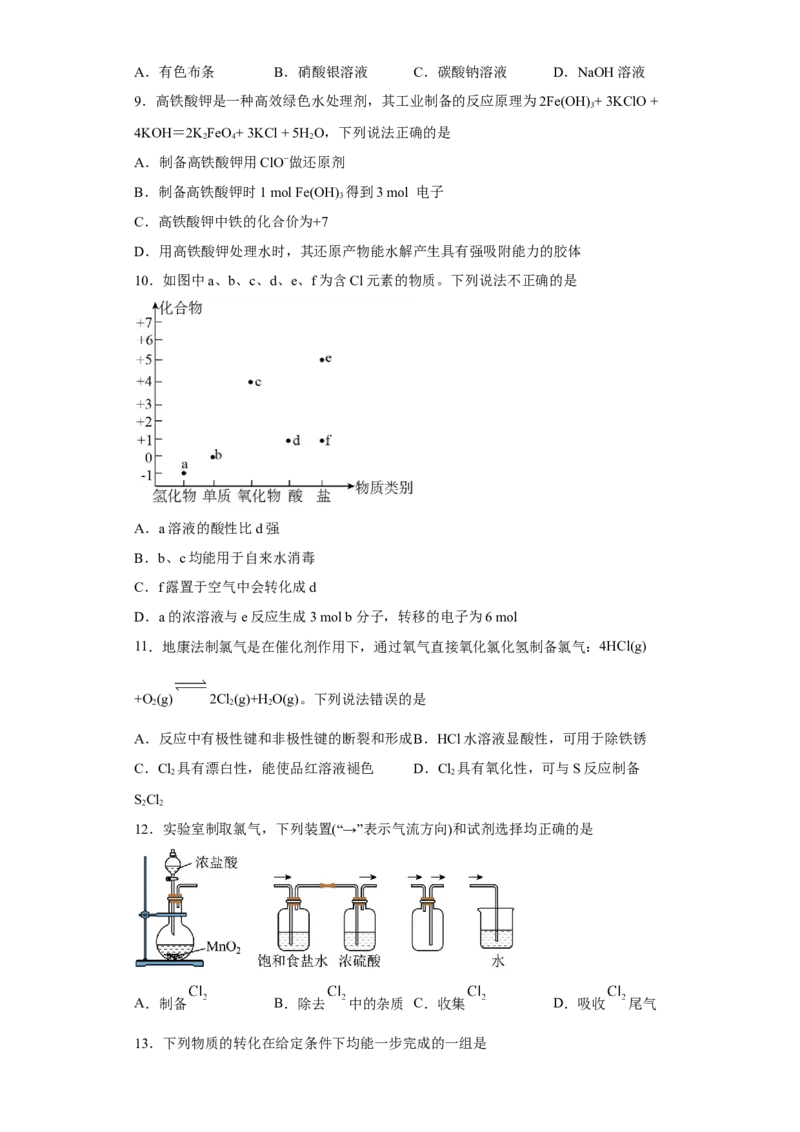
5.将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:
关于溶液中导致变色的微粒I、II、III的判断正确的是
A.H+、HClO、Cl B.H+、Cl-、ClO-
2
C.HCl、ClO-、Cl- D.HClO、HCl、Cl
2
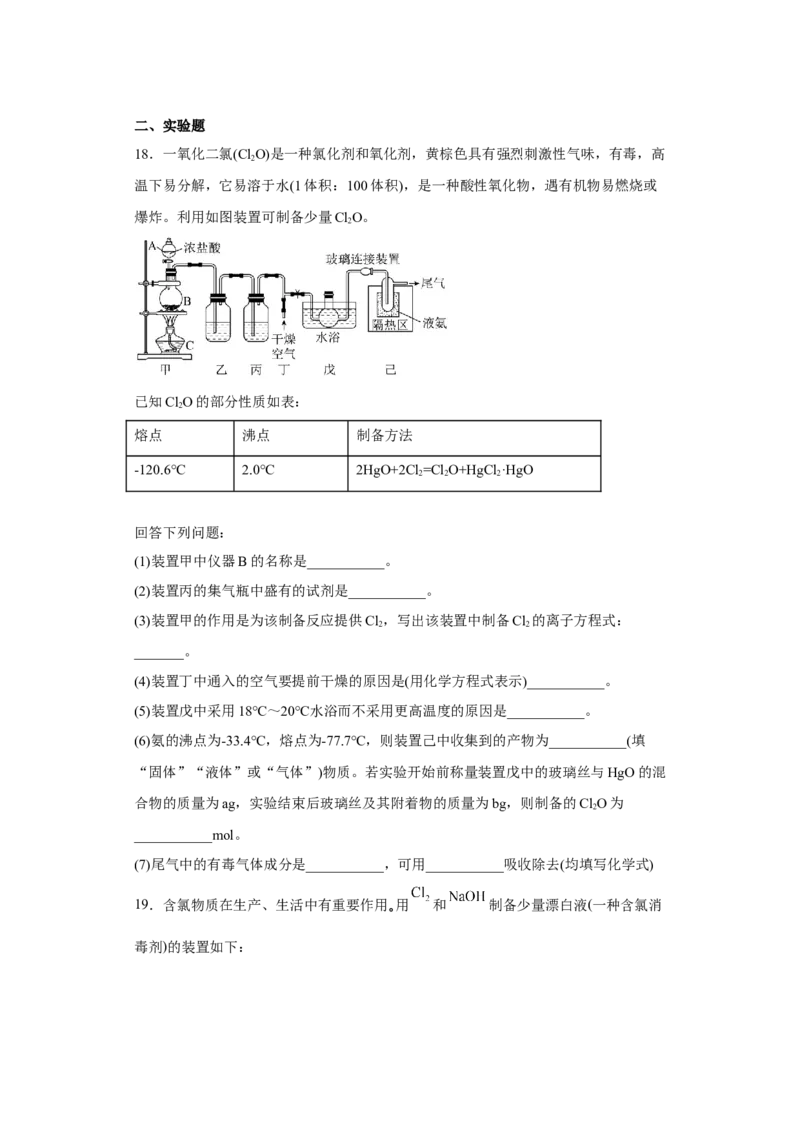
6.将 传感器、氯离子传感器、氧气传感器分别插入盛有氯水的广口瓶中,用强光
照氯水,测得的实验数据如图所示。下列说法正确的是
A.由图甲可推知光照可促进 与水反应
B.由图乙可推知 增大的主要原因是 能电离出
C.由图丙可推知光照可催化水分解
D.由图甲、乙、丙可验证 见光分解的产物
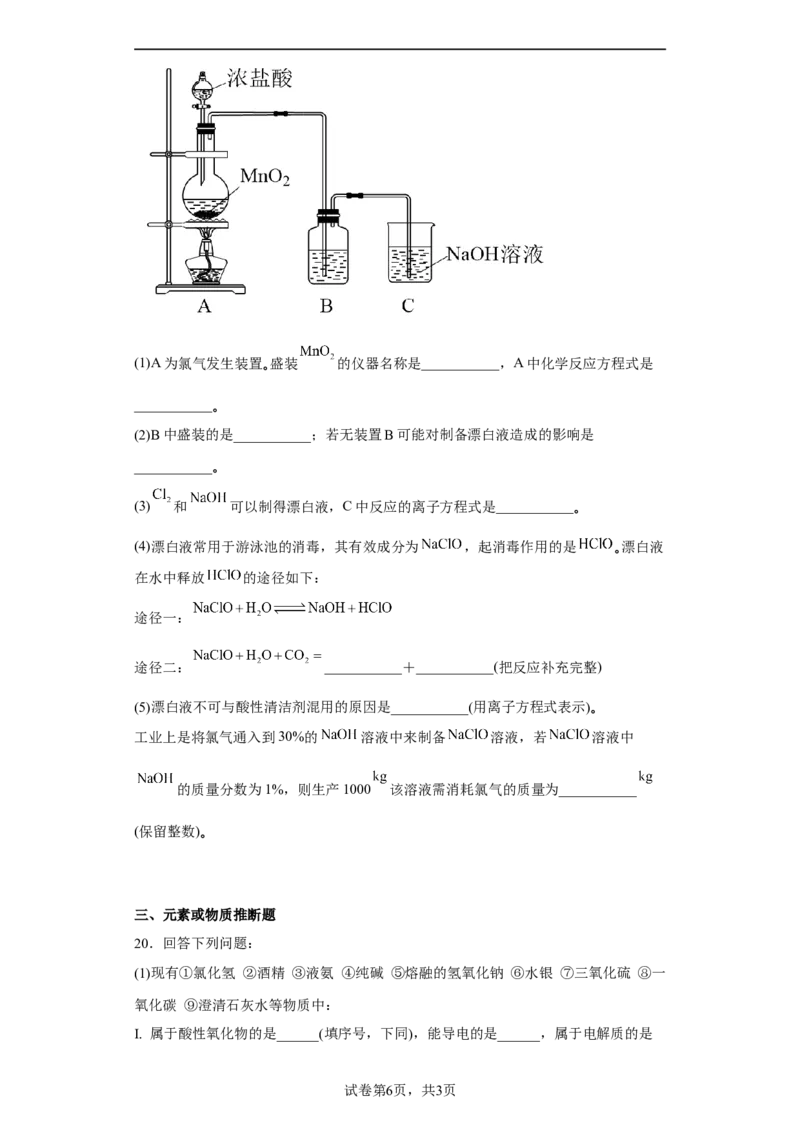
7.如图所示,若关闭阀门I,打开阀门II,让一种含氯气的气体经过甲瓶后,通入乙
瓶,布条不褪色;若关闭阀门II,打开阀门I,再通入这种气体,布条褪色。甲瓶中所
盛的试剂可能是
①浓硫酸 ②饱和氯化钠溶液 ③饱和氢氧化钠溶液
A.①② B.①③ C.②③ D.①②③
8.向漂粉精溶液中加入下列什么物质,可以证明溶液中存在次氯酸分子
试卷第2页,共3页A.有色布条 B.硝酸银溶液 C.碳酸钠溶液 D.NaOH溶液
9.高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为2Fe(OH) + 3KClO +
3
4KOH=2KFeO+ 3KCl + 5H O,下列说法正确的是
2 4 2
A.制备高铁酸钾用ClO−做还原剂
B.制备高铁酸钾时1 mol Fe(OH) 得到3 mol 电子
3
C.高铁酸钾中铁的化合价为+7
D.用高铁酸钾处理水时,其还原产物能水解产生具有强吸附能力的胶体
10.如图中a、b、c、d、e、f为含Cl元素的物质。下列说法不正确的是
A.a溶液的酸性比d强
B.b、c均能用于自来水消毒
C.f露置于空气中会转化成d
D.a的浓溶液与e反应生成3 mol b分子,转移的电子为6 mol
11.地康法制氯气是在催化剂作用下,通过氧气直接氧化氯化氢制备氯气:4HCl(g)
+O (g) 2Cl(g)+HO(g)。下列说法错误的是
2 2 2
A.反应中有极性键和非极性键的断裂和形成B.HCl水溶液显酸性,可用于除铁锈
C.Cl 具有漂白性,能使品红溶液褪色 D.Cl 具有氧化性,可与S反应制备
2 2
SCl
2 2
12.实验室制取氯气,下列装置(“→”表示气流方向)和试剂选择均正确的是
A.制备 B.除去 中的杂质 C.收集 D.吸收 尾气
13.下列物质的转化在给定条件下均能一步完成的一组是A.
B.
C.
D.
14.下列说法不正确的是
A.目前氯气、二氧化氯、臭氧都可用于自来水的消毒
B.氯水、漂白液、漂白粉的溶液都能使有色布条褪色
C.某溶液加入硝酸银溶液产生白色沉淀,加入盐酸沉淀不消失,该溶液一定含Cl-
D.氯气在化学工业中可用来制取高纯度的硅、锗、钛等
15.分离提纯下列物质时选用的试剂和操作方法均正确的是
选项 分离提纯 试剂
A 除去CO 中的HCl 饱和NaCl溶液
2
B 除去Cl 中的水蒸气 碱石灰
2
C 除去FeCl 溶液中的FeCl 氯气
2 3
D 除去Al O 中的Fe O NaOH溶液
2 3 2 3
A.A B.B C.C D.D
16.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,说明氯水中含有Cl-
3
C.向氯水中加入NaCO 粉末,有气泡产生,说明氯水中含有H+
2 3
D.氯水的性质很稳定,保存在无色试剂瓶中
17.下列说法正确的是
①可用Ba(OH) 溶液同时鉴别AgNO、AlCl 、NH Cl、NaCl、NaSO 五种溶液
2 3 3 4 2 4
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③因为氧化性:HClO>HSO ,所以非金属性:Cl>S
2 4
④胶体的本质特征是丁达尔现象
⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
A.①②⑤ B.①②④ C.②④⑤ D.全部
试卷第4页,共3页二、实验题
18.一氧化二氯(Cl O)是一种氯化剂和氧化剂,黄棕色具有强烈刺激性气味,有毒,高
2
温下易分解,它易溶于水(1体积:100体积),是一种酸性氧化物,遇有机物易燃烧或
爆炸。利用如图装置可制备少量ClO。
2
已知ClO的部分性质如表:
2
熔点 沸点 制备方法
-120.6℃ 2.0℃ 2HgO+2Cl =ClO+HgCl ·HgO
2 2 2
回答下列问题:
(1)装置甲中仪器B的名称是___________。
(2)装置丙的集气瓶中盛有的试剂是___________。
(3)装置甲的作用是为该制备反应提供Cl,写出该装置中制备Cl 的离子方程式:
2 2
_______。
(4)装置丁中通入的空气要提前干燥的原因是(用化学方程式表示)___________。
(5)装置戊中采用18℃~20℃水浴而不采用更高温度的原因是___________。
(6)氨的沸点为-33.4℃,熔点为-77.7℃,则装置己中收集到的产物为___________(填
“固体”“液体”或“气体”)物质。若实验开始前称量装置戊中的玻璃丝与HgO的混
合物的质量为ag,实验结束后玻璃丝及其附着物的质量为bg,则制备的ClO为
2
___________mol。
(7)尾气中的有毒气体成分是___________,可用___________吸收除去(均填写化学式)
19.含氯物质在生产、生活中有重要作用。用 和 制备少量漂白液(一种含氯消
毒剂)的装置如下:(1)A为氯气发生装置。盛装 的仪器名称是___________,A中化学反应方程式是
___________。
(2)B中盛装的是___________;若无装置B可能对制备漂白液造成的影响是
___________。
(3) 和 可以制得漂白液,C中反应的离子方程式是___________。
(4)漂白液常用于游泳池的消毒,其有效成分为 ,起消毒作用的是 。漂白液
在水中释放 的途径如下:
途径一:
途径二: ___________+___________(把反应补充完整)
(5)漂白液不可与酸性清洁剂混用的原因是___________(用离子方程式表示)。
工业上是将氯气通入到30%的 溶液中来制备 溶液,若 溶液中
的质量分数为1%,则生产1000 该溶液需消耗氯气的质量为___________
(保留整数)。
三、元素或物质推断题
20.回答下列问题:
(1)现有①氯化氢 ②酒精 ③液氨 ④纯碱 ⑤熔融的氢氧化钠 ⑥水银 ⑦三氧化硫 ⑧一
氧化碳 ⑨澄清石灰水等物质中:
Ⅰ. 属于酸性氧化物的是______(填序号,下同),能导电的是______,属于电解质的是
试卷第6页,共3页______。
Ⅱ.写出下列物质在水溶液中的电离方程式
NaCO :________________
2 3
Ca(OH) :______________
2
HSO :___________________
2 4
(2)有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的1/2,乙元
素原子核内无中子,丙元素原子核内有8个质子,丁元素的最外层电子数是内层电子
数的2倍。
①写出甲元素的离子符号______。
②写出乙、丙两种元素组成的具有10电子的化合物是______(写化学式)。
③表示丁元素(中子数为8)的一种可用于考古断代的核素的原子符号______,丙的阴离
子结构示意图______。参考答案:
1.D
【详解】氯气是一种有刺激性气味的黄绿色有毒气体,相同条件下氯气的密度比空气大,
氯气能溶于水,并能与水反应生成盐酸和次氯酸。故答案为:D
2.C
【详解】A.Cl 通入冷的 NaOH溶液中发生反应生成氯化钠和次氯酸钠,Cl+2OH-=Cl-
2 2
+ClO-+H O,通入热的氢氧化钠溶液会生成氯酸钠,A错误;
2
B.用醋酸和淀粉-KI溶液检验加碘盐中的 的原理是 在酸性条件下与I-发生归中反
应生成I 而遇淀粉变蓝,由于醋酸是弱酸,在离子方程式中不能用H+表示,B错误;
2
C.+2价的铁被双氧水氧化为+3价,反应的离子方程式为2Fe2+
+H O+4H O=2Fe(OH) ↓+4H+,C正确;
2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合后发生反应生成碳酸钡沉淀、碳酸钠和水,
3 2
NaHCO 过量,Ba(OH) 全部参加反应,因此该反应的离子方程式为2 +Ba2++2OH-
3 2
=BaCO ↓+ +2H O,D错误;
3 2
故选C。
3.A
【详解】A. 酯化反应应是“酸脱羟基醇脱氢”,硬脂酸与乙醇的酯化反应:
,故A选;
B. 常温时, 氨水的 ,说明一水合氨是弱碱,NH 3 •H 2 O ⇌ +
,故B不选;
C. 次氯酸中心原子为O,分别与氢和氯各形成一个共价键,次氯酸的结构式为:
,故C不选;
D. 阴极得电子发生还原反应,电解精炼铜的阴极反应: ,故D不选;
故选A。
4.D
【详解】A.Cl 分子呈黄绿色,氯水中含Cl 分子,故氯水呈黄绿色,A相符;
2 2B.钠很软,用小刀可以切开钠,B相符;
C.钠的密度比水小,故钠可以浮在水面上,C相符;
D.向饱和NaHCO 溶液中加入足量氯水,有无色气体产生,是由于氯水中的HCl与
3
NaHCO 反应生成CO,HClO与NaHCO 不反应,D不相符;
3 2 3
故选D。
5.A
【详解】氯气与水反应生成HCl、HClO,HCl具有酸性,HClO具有漂白性,则将氯气持
续通入紫色石蕊试液中先变红后褪色,最后形成饱和氯水溶液显浅黄绿色为溶解的氯气分
子,氯水中H+使紫色石蕊试液变红色,HClO具有漂白性,能将红色变无色,溶解在水中
的Cl 使溶液呈浅黄绿色,微粒I、II、III分别为H+、HClO、Cl,故选:A。
2 2
6.D
【详解】A.图甲中溶液 降低的原因还有 见光分解,A项错误;
B. 不能电离出 ,B项错误;
C.图丙中氧气体积分数增大的主要原因是 见光分解,且光照不易使水分解,C项错
误;
D.综合图甲、乙、丙中信息可推知, 见光分解的产物中有 和 , 在水中
电离出 和 ,D项正确。
故选D。
7.B
【详解】干燥的氯气不具有漂白性,氯气与水反应产生的HClO具有漂白性。根据题意可
知通入的气体中含有潮湿的氯气。但若关闭阀门I,打开阀门II,让该含氯气的气体经过甲
瓶后再通入乙瓶,看到未湿润的有色布条不褪色;说明在装置甲中可能Cl 被反应消耗,则
2
该溶液为饱和氢氧化钠溶液;也可能是Cl 中的水分被吸收,Cl 被干燥,而干燥的氯气不
2 2
具有漂白性,则该试剂是浓硫酸,而氯气在饱和氯化钠溶液中不能反应,出来的气体仍然
是潮湿的氯气,具有漂白性,故甲装置可能所盛的试剂是①浓硫酸、③饱和氢氧化钠溶液,
合理选项是B。
8.A
【详解】A.加入有色布条,可以观察到布条褪色,说明含有具有漂白性的次氯酸分子,A
答案第2页,共2页符合题意;
B.硝酸银溶液可以检验氯离子,不能检验次氯酸,B不符合题意;
C.碳酸钠溶液可以检验氢离子,但次氯酸的酸性弱于碳酸,所以不能检验次氯酸,C不符
合题意;
D.NaOH虽然可以和次氯酸反应,但加入NaOH溶液不会出现明显现象,D不符合题意;
综上所述答案为A。
9.D
【详解】A、反应2Fe(OH) + 3KClO + 4KOH=2KFeO+ 3KCl + 5H O中,Cl元素的化合价
3 2 4 2
由+1价降低为-1价,则KClO为氧化剂,Fe(OH) 为还原剂,故A错误;
3
B、因反应中铁元素的化合价由+3价升高到+6价,则1mol Fe(OH) 失去3mol电子,故B
3
错误;
C、高铁酸钾中铁的化合价为+6价,故C错误;
D、用高铁酸钾处理水时,+6价铁表现出强氧化性,能杀菌消毒,其还原产物为铁离子,
能水解生成氢氧化铁胶体,能吸附水中的悬浮杂质,故D正确;
答案选D。
10.D
【分析】根据所处化合价以及物质类别,推出a为HCl,b为Cl,c为ClO ,d为HClO,e
2 2
为氯酸盐,f为次氯酸盐,据此分析;
【详解】A.a为HCl,盐酸属于一元强酸,d为HClO,次氯酸属于弱酸,因此a溶液的酸
性强于d溶液,故A说法正确;
B.b为为Cl,c为ClO ,两者都具有强氧化性,能使蛋白质变性,因此两者均能用于自
2 2
来水消毒,故B说法正确;
C.f为次氯酸盐,d为HClO,次氯酸的酸性弱于碳酸,次氯酸盐露置在空气中,次氯酸盐
与CO、HO反应生成HClO,故C说法正确;
2 2
D.a为HCl,e为氯酸盐,若e为KClO,两者混合发生KClO+6HCl(浓)
3 3
KCl+3Cl ↑+3H O,该反应中每生成3mol氯气,转移电子物质的量为5mol,故D说法错误;
2 2
答案为D。
11.C
【详解】A.Cl 中含有非极性共价键,HO中含有极性共价键,O 中含有非极性共价键,
2 2 2
HCI中含有极性共价键,则反应有极性共价键、非极性共价键的断裂和形成,A正确;B.HCl水溶液显酸性,可以与Fe O 反应生成易溶于水的FeCl ,从而除去铁锈,B正确;
2 3 3
C.氯气溶于水生成的次氯酸具有漂白性,能使品红溶液褪色,但是氯气无漂白性,C错误;
D.Cl 可与S反应制备SCl,体现了氯气的氧化性,D正确;
2 2 2
故选C。
12.B
【详解】A.浓盐酸和二氧化锰反应需加热,A错误;
B.氯气通过饱和食盐水可以去除HCl杂质气体且氯气在饱和食盐水中损耗少,B正确;
C.氯气的密度大于空气,收集时应向上排空气法,C错误;
D.氯气有毒,用强碱氢氧化钠吸收尾气,D错误;
故选B。
13.A
【详解】A.氯化钠溶液通电电解可以制得氯气,氯气与石灰乳反应可以制得含有氯化钙
和次氯酸钙的漂白粉,物质的转化在给定条件下均能一步完成,故A正确;
B.氯化铝溶液通电电解制得氢氧化铝,不可能制得金属铝,物质的转化在给定条件下不
能一步完成,故B错误;
C.氮气和氧气在高温条件下反应只能生成一氧化氮,不可能生成二氧化氮,物质的转化
在给定条件下均能一步完成,故C错误;
D.硫在高温条件下与氧气反应只能生成二氧化硫,不可能生成三氧化硫,物质的转化在
给定条件下均能一步完成,故D错误;
故选A。
14.C
【详解】A、Cl+H O=HCl+HClO,氯气与水反应生成次氯酸,HClO具有强氧化性,可用
2 2
于杀菌消毒,二氧化氯中氯的化合价为+4价,不稳定,易转变为-1价,从而体现较强的氧
化性,可用于自来水的杀菌消毒,臭氧有强氧化性,能杀菌消毒,故A正确;B、氯水中
含有HClO,具有漂白作用,漂白粉的有效成分为次氯酸钙,能生成具有漂白性的HClO,
可使红色布条褪色,次氯酸钠溶液能生成具有漂白性的HClO,可使红色布条褪色,故B
正确;C、溶液中加入硝酸银溶于生成白色沉淀不一定是氯化银沉淀,再加入盐酸溶液中
含有氯离子,可以发生沉淀转化生成氯化银沉淀,氯化银不溶于酸,所以溶于不一定含氯
离子,故C错误;D.制取高纯硅、锗和钛时,将粗硅、锗和钛先与氯气反应制得SiCl 、
4
GeCl 、TiCl ,然后再使SiCl 、GeCl 、TiCl 分别与氢气反应即可制的高纯的硅、锗和钛,
4 4 4 4 4
故D正确;故选C。
答案第4页,共2页点睛:本题考查了物质性质的分析应用,主要是物质化学性质和反应实质的理解应用,掌
握基础是解题关键。本题的易错点和难点为D,粗硅、锗和钛先与氯气反应制得SiCl 、
4
GeCl 、TiCl ,然后再使SiCl 、GeCl 、TiCl 分别与氢气发生还原反应生成高纯的硅、锗和
4 4 4 4 4
钛,可以联系课本硅的提纯进行解答。
15.A
【详解】A.二氧化碳能溶于水,氯化氢气体极易溶于水,溶于水的氯化氢使溶液呈酸性,
能降低二氧化碳的溶解度,则能用饱和氯化钠溶液除去二氧化碳中的氯化氢气体,故A正
确;
B.氯气能与碱石灰反应,不能用碱石灰干燥氯气,应选用浓硫酸干燥,故B错误;
C.氯气能与氯化亚铁溶液反应生成氯化铁,则不能用氯气除去氯化亚铁溶液中混有的氯
化铁,故C错误;
D.氧化铝能与氢氧化钠溶液反应,氧化铁不能与氢氧化钠溶液反应,则不能用氢氧化钠
溶液除去氧化铝中混有的氧化铁,故D错误;
故选A。
16.D
【分析】氯气溶于水,与水发生反应:Cl+H O HCl+HClO,氯水中含有氯离子、氢离
2 2
子、次氯酸根离子、次氯酸、少量氢氧根离子,只有氯气有颜色,为黄绿色,氯水中含有
氯气而呈浅黄绿色,溶液中HCl与硝酸银反应产生AgCl白色沉淀,而溶液呈酸性,能与
碳酸钠反应生成二氧化碳,溶液中HClO不稳定,光照容易分解。
【详解】A.氯气溶于水,与水发生反应:Cl+H O HCl+HClO,氯水中含有氯离子、氢
2 2
离子、次氯酸根离子、次氯酸、少量氢氧根离子,只有氯气有颜色,为黄绿色,所以氯水
的颜色呈浅黄绿色,说明氯水中含有Cl,A正确;
2
B.氯水与硝酸银溶液反应产生白色沉淀,只能是Cl-与Ag+反应得到AgCl白色沉淀,说明氯
水中含有Cl-,B正确;
C.溶液呈酸性,含有盐酸和次氯酸,次氯酸的酸性比碳酸弱,盐酸与与碳酸钠反应生成二
氧化碳,C正确;
D.溶液中含有的HClO不稳定,光照分解产生HCl和O,所以为防止氯水变质,要把氯水
2
盛放在棕色试剂瓶中,D错误;
故合理选项是D。
【点睛】本题考查氯水的性质,掌握氯气与水的反应,判断氯水中含有的微粒及各种物质
的性质是本题解答的关键,侧重考查元素化合物知识的综合理解和运用。17.A
【详解】试题分析:①加入Ba(OH) 溶液,AgNO 生成灰色沉淀氧化银,AlCl 先生成沉淀,
2 3 3
后溶解,NH Cl生成刺激性气味的气体,NaCl不反应,无明显现象,NaSO 生成白色沉淀,
4 2 4
现象不同,可鉴别,①正确;②蔗糖为非电解质,硫酸钡和水都为电解质,水为极弱的电
解质,硫酸钡为强电解质,②正确;③应从最高价氧化物的水化物的酸性的角度比较非金
属性强弱,③错误;④胶体的本质特征是粒子直径介于之间,④错误;⑤铝可与氢氧化钠
溶液反应,可用于除杂,⑤正确;答案选A。
考点:考查物质的检验与分离。
18.(1)圆底烧瓶
(2)浓硫酸
(3)2Cl-+4H++MnO Cl↑+Mn2++2H O
2 2 2
(4)Cl O+2HO=2HClO
2 2
(5)温度过高ClO分解
2
(6) 液体
(7) Cl 、ClO NaOH溶液
2 2
【分析】甲中浓盐酸和二氧化锰在加热条件下反应生成氯气,乙中用饱和食盐水除氯化氢,
丙中用浓硫酸干燥氯气,丁中通入干燥空气与纯净而干燥的氯气混合,装置戊用来制取
ClO,并在己中收集产物,可选用氢氧化钠溶液来吸收多余的有毒气体,防止污染大气,
2
以此解答该题。
(1)
装置甲中仪器B的名称圆底烧瓶;
(2)
制备的氯气中有杂质HCl、水蒸气,丙装置盛有浓硫酸除去水蒸气;
(3)
题中用MnO 与浓硫酸加热制取氯气,故制备Cl 的离子方程式2Cl-+4H++MnO Cl ↑
2 2 2 2
+Mn2++2HO;
2
答案第6页,共2页(4)
ClO是酸性氧化物、能与水反应生成次氯酸,则装置丁中通入的空气要提前干燥的原因是
2
ClO+2HO=2HClO;
2 2
(5)
水浴的原因是因为温度不能太高也不能太低,温度太低反应速率太慢,温度过高ClO分解;
2
(6)
ClO的熔点-120.6℃、沸点为2.0℃,氨的沸点为-33.4℃,熔点为-77.7℃,则液氨可使ClO
2 2
液化,则装置己中收集到的产物为液体;根据ClO的制备原理
2
2HgO+2Cl =ClO+HgCl ·HgO,运用差量法:每生成1mol Cl O,反应前后固体质量增加
2 2 2 2
(142-87)g=55g,设制备的ClO 的物质的量为x mol,则 ,解得x= ;
2
(7)
结合题目中的信息可知尾气中含有空气、Cl、ClO,其中后两者有毒;这两种有毒气体均
2 2
能被碱液NaOH吸收。
19.(1) 圆底烧瓶
(2) 饱和 溶液 能与 发生中和反应,不利于 的生成。(或
不利于 的生成)
(3)
(4)
(5) 203
【分析】A中二氧化锰和浓盐酸反应生成氯气,浓盐酸易挥发,故氯气中含有氯化氢用饱
和食盐水除掉,B中为饱和食盐水,C中的氢氧化钠吸收氯气尾气,防止污染空气。
(1)
盛装 的仪器名称是圆底烧瓶,A中为二氧化锰和浓盐酸生成氯气的反应,方程式为。
(2)
B为除去氯气中的氯化氢,故应为饱和食盐水;若无装置B则HCl能与NaOH发生中和反
应,不利于NaClO的生成 (或不利于NaClO的生成)。
(3)
Cl 和NaOH反应生成氯化钠、次氯酸钠和水,离子方程式为
2
。
(4)
根据碳酸酸性强于次氯酸的酸性,次氯酸酸性强于碳酸氢根离子的酸性,故反应式为
。
(5)
漂白液和酸反应生成氯气,故离子方程式为 。根据反应:
Cl+2NaOH=NaClO+NaCl+H O,假设反应消耗氯气的质量为x,则根据物质反应转化关系,
2 2
可知反应消耗NaOH的质量为m(NaOH)= ,溶液中剩余NaOH质量m(NaOH)=1000
kg×1%=10 kg,由于NaOH溶液中溶质含量为30 %,则 ,解得
x=203 kg。
20.(1) ⑦ ⑤⑥⑨ ①④⑤ Na CO=2Na++CO Ca(OH) =Ca2++2OH-
2 3 2
HSO =2H++SO
2 4
(2) Na+ HO
2
【分析】有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的0.5,其
答案第8页,共2页M层电子数为1,则甲为Na;乙元素原子核内无中子,则乙为H;丙元素原子核内有8个
质子,则丙为O;丁元素最外层电子数是次外层电子数的2倍,原子只能有2个电子层,
最外层电子数为4,则丁为C;
【详解】(1)Ⅰ.⑦三氧化硫与氢氧化钠反应生成硫酸钠和水,属于碱性氧化物,
⑤熔融的氢氧化钠和⑧澄清石灰水含有自由移动的离子,能够导电;⑥水银含有自由电子
能够导电,
①硫酸④纯碱⑤熔融的氢氧化钠水溶液中或熔融状态下能导电的化合物,属于电解质,
故答案为:⑦;⑤⑥⑧;①④⑤;
Ⅱ. Na CO 在水溶液中完全电离出钠离子和碳酸根离子,电离方程式为:NaCO=2Na++
2 3 2 3
;氢氧化钙为强电解质,完全电离产生钙离子、氢氧根离子,电离方程式:
Ca(OH) =Ca2++2OH-;HSO 为强电解质,水溶液中完全电离产生氢离子、硫酸根离子,电
2 2 4
离方程式:HSO =2H++ ;
2 4
(2)有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的0.5,其M
层电子数为1,则甲为Na;乙元素原子核内无中子,则乙为H;丙元素原子核内有8个质
子,则丙为O;丁元素最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最
外层电子数为4,则丁为C,
①由上述分析可知,甲、乙、丙、丁四种元素的元素符号分别为:Na,H,O,C,甲元素
的离子符号为Na+;故答案为:Na;H;O;C;
②乙为H、丙为O,两种元素组成的具有10电子的化合物是HO;
2
③丁为C,丁元素(中子数为8)则质量数=质子数+中子数=6+8=14,,可用于考古断代的核素
的原子符号为 ;丙为O元素,质子数为8,得到2个电子形成阴离子O2-,其结构示意
图 。答案第10页,共2页