文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
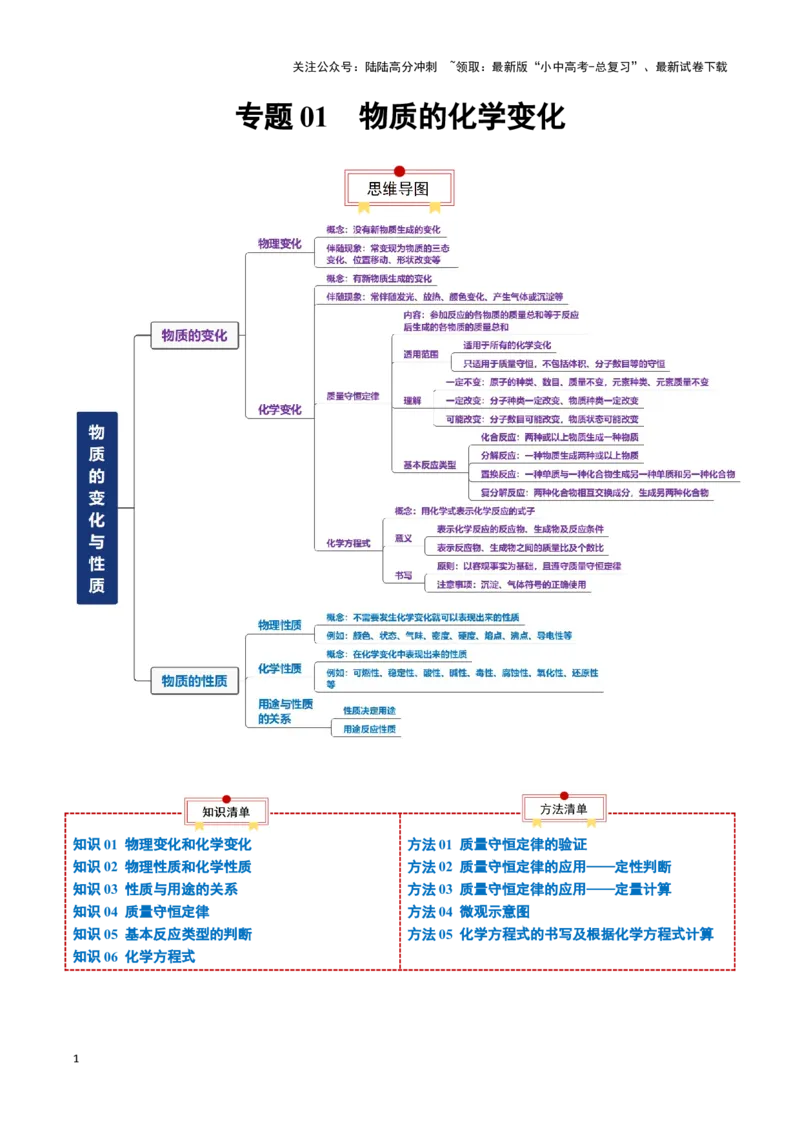
专题 01 物质的化学变化
知识01 物理变化和化学变化 方法01 质量守恒定律的验证
知识02 物理性质和化学性质 方法02 质量守恒定律的应用——定性判断
知识03 性质与用途的关系 方法03 质量守恒定律的应用——定量计算
知识04 质量守恒定律 方法04 微观示意图
知识05 基本反应类型的判断 方法05 化学方程式的书写及根据化学方程式计算
知识06 化学方程式
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识 01 物理变化和化学变化
变化 物理变化 化学变化
概念 没有生成其它物质的变化。 生成其它物质的变化。
本质区别 没有生成其它物质。 生成其它物质。
构成物质的粒子,本身没有变 构成物质的粒子,发生了变化,变成了其
微观理解
化,变化的是粒子之间的间隔。 它物质的粒子。
通常是状态和形状、大小的改 常伴随发光、放热、颜色变化、产生气
宏观现象
变。 体、生成沉淀等现象。
水的三态变化、酒精挥发、灯泡 金属生锈、燃烧、光合作用、呼吸作用,
举例
发光、煤的干馏等。 食物变质、酿酒、酿醋、石油分馏等。
联系 发生化学变化的同时,一定有物理变化。
【例1】(2023·山东淄博·中考真题)物质世界是在不断变化的。下列变化属于物理变化的是( )
A.镁条燃烧 B.冰雪融化 C.光合作用 D.钢铁生锈
知识 2 物理性质和化学性质
变化 物理性质 化学性质
定 义 物质不需要发生化学变化就可以表现出来的性质 物质在化学变化中表现出来的性质
可燃性、助燃性;氧化性、还原性;
常见 颜色、状态、气味;硬度、密度、燃点、沸点、熔
性质 点;溶解性、挥发性、导电性、导热性、吸附性等 稳定性、活泼性;腐蚀性、酸性、碱
性、毒性等
区 别 是否需要经过化学变化才能表现出来
注 意 物质的性质受外界条件影响,在描述物质性质时注明条件。(如液体沸点受大气压影响)
【特别提醒】
(1)物理性质是指不需要发生化学变化就表现出的性质。物理性质包括两个方面:
一个是在物理变化中变现出的性质,如:挥发性、溶解性和吸附性等。
一个是不需要变化就有具有的,如:物质的颜色、气味、状态和密度等。
(2)化学性质是指在化学变化中表现出的性质。如:可燃性、还原性和酸碱性等。
(3)性质和变化的区别:性质是物质固有的属性,是物质基本的特征,是变化的依据;而变化是只一个
过程,是性质的具体体现,即性质决定变化,变化体现性质。性质和变化在描述上是不同的,一般描述物
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质性质的语言中有“可、易、会、能”等表示具有能力的字眼,如“镁条可以燃烧”是性质;而“镁条燃
烧”则是变化。
【例2】(2023·湖北·统考中考真题)下列关于氢气性质的描述,属于化学性质的是( )
A.密度比空气小 B.难溶于水
C.无色无味 D.具有可燃性
知识 3 用途和性质的关系
性质和用途之间的关系,即性质决定用途,用途反映性质;性质与结构之间的关系:即物质的结构特点
决定着物质的性质,性质是结构特点的反映。例:木炭具有可燃性,可以发生燃烧变化,生活中用于作燃料。
【例3】(2022·四川甘孜·统考中考真题)下列物质的用途中,利用其物理性质的是( )
A.乙醇用作燃料 B.氯化钠用于制氯气
C.煤用于火力发电 D.木炭用于吸附色素
知识 4 质量守恒定律
内容 参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
①质量守恒定律只能解释化学变化,不能解释物理变化
②不参加反应的物质不能计算在内
理解
③计算时不能漏掉任何一项,气体和沉淀等都要考虑在内
④只适用于质量守恒,不包括体积守恒、分子数守恒等
实质 分子分裂形成原子,原子重新组合生成新分子,新分子聚集形成物质
宏观:反应物和生成物的总质量不变、元素种类不变、元素总质量不变
“6个不变”
“变 微观:原子的种类、个数、质量不变
与 宏观:物质种类一定改变
“2个一定改变”
不变”
微观:分子种类一定改变
“2个可能改变” 分子数目可能改变,元素化合价可能改变
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①推断物质的元素组成
②推断反应物或生成物的化学式或化学计量数
应用 ③有关密闭容器中化学反应的数据分析
④解释微观示意图
⑤进行有关化学方程式的计算
【例4】(辽宁抚顺)下列说法符合质量守恒定律的是( )
A.10g水与10g酒精混合后质量为20g
B.1L氢气和8L氧气反应,能生成9L水
C.5g硫和5g氧气恰好完全反应,生成物的质量为10g
D.纸在空气中燃烧化为灰烬,灰烬的质量等于纸的质量
知识 5 基本反应类型的判断
反应类型 概念及表达式 特征
概念:由两种或两种以上物质生成另一种物质的反应
化合反应 多变一
表达式:A+B+……→M
概念:由一种反应物生成两种或两种以上其他物质的反应
分解反应 一变多
表达式:A→B+C+……
概念:由两种或两种以上物质生成另一种物质的反应
质量反应 单换单
表达式:A+BC→B+AC
概念:由两种或两种以上物质生成另一种物质的反应
复分解反应 双交换,价不变
表达式:AB+CD→AD+CB
【例5】(2023·海南海口·三模)对于化学反应: ,其反应类型属于( )
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
知识 6 化学方程式
1.化学方程式的意义和书写
定义 用化学式表示化学反应的式子
意义 读法(以C+O =====CO 为例)
2 2
质 表示反应物、生成物和反应条件 碳和氧气在点燃的条件下反应生成二氧化碳
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
每12份质量的碳和32份质量的氧气完全反
宏观:表示反应前后各物质之间的质量关系
应,生成44份质量的二氧化碳
量
1个碳原子和1个氧分子反应生成1个二氧化
微观:表示各物质之间的粒子的相对量的关系
碳分子
2.化学方程式的书写
原则 ①以客观事实为基础②要遵循质量守恒定律(等号两边各原子的种类和数目必须相同)
①写出反应物、生成物的化学式
P+O→PO
2 2 5
②配平化学方程式
4P+5O→2PO
2 2 5
③标明化学反应的条件,标注生成物的状态,把“→”改为“===”
步骤 4P+5O=====2PO
2 2 5
④查:
a.检查化学式是否正确;
b.查是否配平
c.查生成物状态是否标注、标注是否恰当
d.查反应条件是否标明
【特别提醒】①“↑”的标注,当反应物中没有气体时,生成物中的气体标“↑”;
②“↓”的标注:在溶液中进行的反应,当反应物中没有固体时,生成物中的固体或沉淀标“↓”
【例6】(广东揭阳)四位同学正在讨论某一个化学方程式的意义,他们所描述的化学方程式是( )
A.C+O CO B.2CO+O 2CO
2 2 2 2
C.H+Cl 2HCl D.2Mg+O 2MgO
2 2 2
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
方法 1 质量守恒定律的验证
①装置中红热的玻璃管的作用是引燃红磷。
②实验中气球的作用除了使装置密闭之外,还可以防止气体受热膨胀冲开橡胶塞(或平衡气
压)。
实验
1 实验时若取用红磷的量不足,对实验的结果没有(填“有”或“没有”)影响。
③锥形瓶底部铺一层细沙的目的是防止锥形瓶受热不均而炸裂。
④该实验能(填“能”或“不能”)验证质量守恒定律。
①在反应前将装有硫酸铜溶液的锥形瓶和铁钉放在天平左盘,调节天平平衡,然后取下锥形瓶把
铁钉放入锥形瓶中。一段时间后,再把锥形瓶放回天平左盘,最后天平平衡(填“平衡”或“不平
衡”)。
实验
2
②能证明铁钉与硫酸铜发生化学反应的现象是铁钉表面有红色固体析出,溶液颜色变浅。反应后
锥形瓶内溶液的质量减小(填“增大”、“减小”或“不变”)。
③该实验能 (填“能”或“不能”)验证质量守恒定律。
①在反应前调节天平指针居中,观察到反应后天平指针向右偏转,造成该现象的原因是稀盐酸和
实验 碳酸钠反应生成二氧化碳,产生的气体从烧杯中逸出
3 ②该化学反应遵循 (填“遵循”或“不遵循”)质量守恒定律,但该装置不能用于验证质量守恒定
律。
①不能用于验证质量守恒定律,原因是稀硫酸和氯化钠溶液不发生化学反应。
实验
②若将实验4中的氯化钠换为氢氧化钠溶液,该装置能否用于验证质量守恒定律,并说明原因。
4
不能,因为稀硫酸和氢氧化钠溶液反应物明显现象,无法证明二者发生了化学反应。
总结:能验证质量守恒定律的实验必须遵循以下几点
①密闭容器中发生的化学反应
②若不是密闭容器需要反应物和生成物没有气体
③必须有明显的实验现象
④物理变化不能验证质量守恒定律
【例9】(2023·福建莆田·统考一模)质量守恒定律是自然界最基本的规律之一、下列装置及实验(天平未
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
画出)能用来验证质量守恒定律的是( )
A. B. C. D.
方法 2 质量守恒定律的应用——定性判断
本方法有2个考向:
1.根据化学方程式推断未知化学式
2.定性推断物质的元素组成
解题重点:根据化学反应前后原子的种类和数目不变
【例10】(2023·辽宁抚顺·统考模拟预测)已知氯气与热的氢氧化钠溶液反应的化学方程式为
3Cl+6NaOH=5NaCl+X+3H O,则X的化学式是( )
2 2
A.NaClO B.NaClO C.NaClO D.ClO
2 3 2
方法 3 质量守恒定律的应用——定量计算
解题重点:根据反应前后物质的质量守恒和元素的质量守恒
【例11】(2023·河南周口·统考模拟预测)乙醇与乙醛(CHCHO)组成的混合物中,氧元素的质量分数为
3
36%,若100g此混合物完全燃烧,可生成水的质量为( )
A.90 g B.104 g C.92 g D.88 g
方法 4 微观反应示意图
解题重点:根据题中所给出的原子种类判断出反应物和生成物的化学式,然后配平化学方程式,其余问题
就迎刃而解。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【例12】(2023·湖北鄂州·模拟预测)为了缓解碳排放引起的温室效应,我国科学家成功合成新型催化剂,
将二氧化碳转化为甲醇,该过程的微观示意图如图,下列说法正确的是( )
A.甲醇的化学式为CHOH
3
B.甲、丙、丁均为氧化物
C.参加反应的甲和乙分子个数比为1:1
D.生成丙和丁的质量比为9:16
方法 5 化学方程式的书写及根据化学方程式计算
1.化学方程式的书写
①熟悉化学方程式的书写(见以上讲解)
②陌生化学方程式的书写
根据题意分别写出反应物和生成物,然后配平即可,如果发现反应前后元素种类不同或无法配平,则根据
题意一般是溶液中的溶剂如水参加反应。
2.化学方程式的计算
依据 质量守恒定律
以计算32g铜在空气中加热生成氧化铜的质量为例
设:根据题意设未知数 解:设生成氧化铜的质量为x
写:正确书写化学方程式 2Cu+O =====2CuO
2
计
找:找出已知量、未知量的质量关系 2×64 2×80
算
32g x
步
列:列出比例式
骤
求:求出结果 x=40g
答:简明地写出答案 答:生成氧化铜的质量为40g
【例13】(2023·海南·中考真题)镁是一种重要金属,广泛应用于制造火箭、导弹和飞机的部件等。工业
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
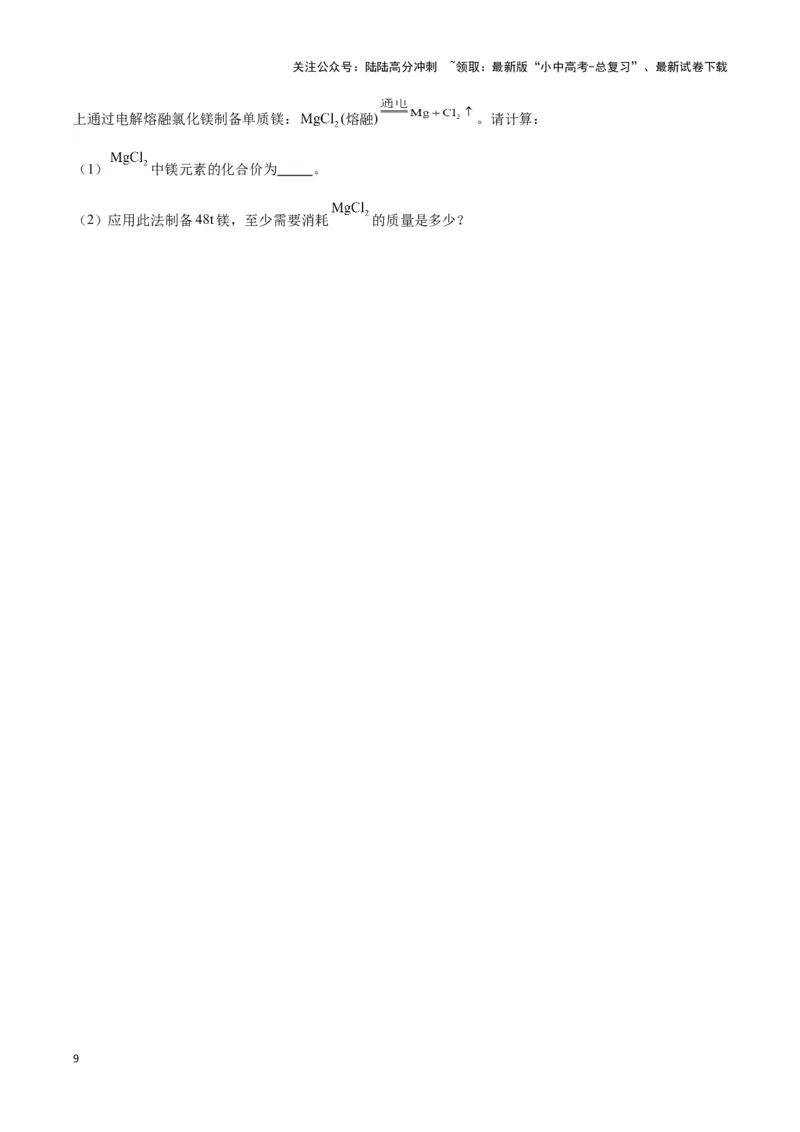
上通过电解熔融氯化镁制备单质镁: (熔融) 。请计算:
(1) 中镁元素的化合价为 。
(2)应用此法制备48t镁,至少需要消耗 的质量是多少?
9