文档内容
2008年高考四川理综化学试题和参考答案
第Ⅰ卷
本卷共21小题,每小题6分,共126分
相对原子质量(原子量):H1 C12 N14 O16 Al 127 Cl 35.5
一.选择题:(本大题共13小题,每小题出的四个选项中,只有一项是符合题目要求的。)
6.下列说法不正确的是
A.1mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4L
B.1mol臭氧和1.5mol氧气含有相同的氧原子数
C.等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3∶1
D.等物质的量的干冰和葡萄糖中所含碳原子数之比为1∶6,氧原子数之比为1∶3
7.下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H SO 和Ca(OH) 反应的中和热
2 4 2
ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO (g) =2CO(g)+O (g)反应的
2 2
ΔH=2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量
是甲烷燃烧热
8.在密闭容器中进行如下反应:H (g) +I (g) 2HI(g),在温
2 2
度 T
1
T 和T 时,产物的量与反应时间的关系如下图所示.符合图
1 2
示
的正确判断是
A.T >T ,ΔH>0 B.T >T ,ΔH<0
1 2 1 2
C.T <T ,ΔH>0 D.T <T ,ΔH<0
1 2 1 2
9.下列叙述中正确的是
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的租序数
B.除点周期外,其他周期均有18个元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
10.下列说法中正确的是
A.离子晶体中每个离子周围均吸引着6个带相反电荷的离子
B.金属导电的原因是在外电场作用下金属产生自由电子,电子定向移动
C.分子晶体的熔沸点很低,常温下都呈液态或气态
D.原子晶体中的各相邻原子都以共价键相结合
11.能正确表示下列反应的离子方程式是
A.足量硫酸铝与纯碱反应:
B.硫酸铜与烧碱反应:
C.苯酚与碳酸钠反应:
量的氢化碘
T
2
时 间D.碳酸钡与硫酸反应:
12.胡椒粉是植物挥发油的成分之一。它的结构式为HO— —CH CH=CH ,下列叙
2 2
述中不正确的是
A.1mol胡椒粉最多可与4mol氢气发生反应
B.1mol胡椒粉最多可与4mol溴发生反应
C.胡椒粉可与甲酸发生反应,生成聚合物
D.胡椒粉在水中的溶解度小于苯酚在水中的溶解度
13.在aLAl (SO ) 和(NH ) SO 的混合物溶液中加入b molBaCl ,恰好使溶液中的 离
2 4 3 4 2 4 2
子完全沉淀;如加入足量强碱并加热可得到c molNH 气,则原溶液中的Al3+离子浓度
3
(mol/L)为
A. B. C. D.
第Ⅱ卷(本卷共10题,共174分。)
26.(14分)
某固体混合物可能含有MgCO 、Al (SO ) 、Na SO 、Ba(NO ) 、AgNO 和CuSO 。将该混
3 2 4 3 2 4 3 2 3 4
合物进行如下实验,根据所给实验现象完成表格(对于能确定的物质在相应位置写化
学式,暂不能确定的物质在相应位置填“无”):
(1)将少许混合物放入水中得到无色溶液和白色沉淀。
肯定存在的物质 肯定不存在的物质 理由
(2)取溶液进行焰色反应,火焰呈黄色;
肯定存在的物质 肯定不存在的物质 理由
(3)取白色沉淀加入稀盐酸,沉淀完全溶解并放出气体。
肯定存在的物质 肯定不存在的物质 理由
(4)通过上述实验仍无法确定的物质是______________。
27.(15分)
D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大。它们的最简氢化物
分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回
答下列问题:
(1)Y的最高价氧化物的化学式为__________;
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是___________,写出该元素的任
意3种含氧酸的化学式:___________________________________;
(3)D和Y形成的化合物,其分子的空间构型为____________;
(4)D 和X形成的化合物,其化学键类型属___________,其晶体类型属__________;(5)金属镁和E的单质在高温下反应得到的产物是___________,此产物与水反应生成两
种碱,该反应的化学方程式是____________________;
(6)试比较D和X的最高价氧化物熔点的高低并说明理由:
__________________________________________________________
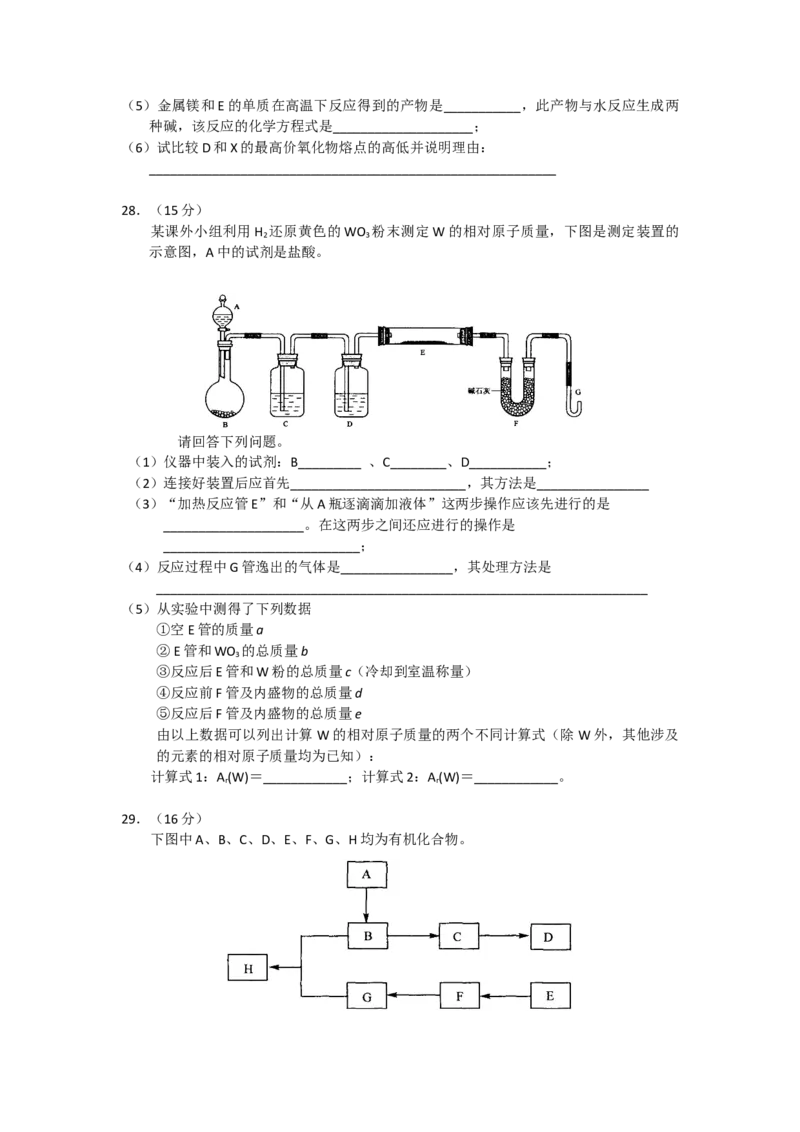
28.(15分)
某课外小组利用H 还原黄色的WO 粉末测定W的相对原子质量,下图是测定装置的
2 3
示意图,A中的试剂是盐酸。
请回答下列问题。
(1)仪器中装入的试剂:B_________ 、C________、D___________;
(2)连接好装置后应首先_________________________,其方法是________________
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是
____________________。在这两步之间还应进行的操作是
____________________________;
(4)反应过程中G管逸出的气体是________________,其处理方法是
______________________________________________________________________
(5)从实验中测得了下列数据
①空E管的质量a
②E管和WO 的总质量b
3
③反应后E管和W粉的总质量c(冷却到室温称量)
④反应前F管及内盛物的总质量d
⑤反应后F管及内盛物的总质量e
由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其他涉及
的元素的相对原子质量均为已知):
计算式1:A(W)=____________;计算式2:A(W)=____________。
r r
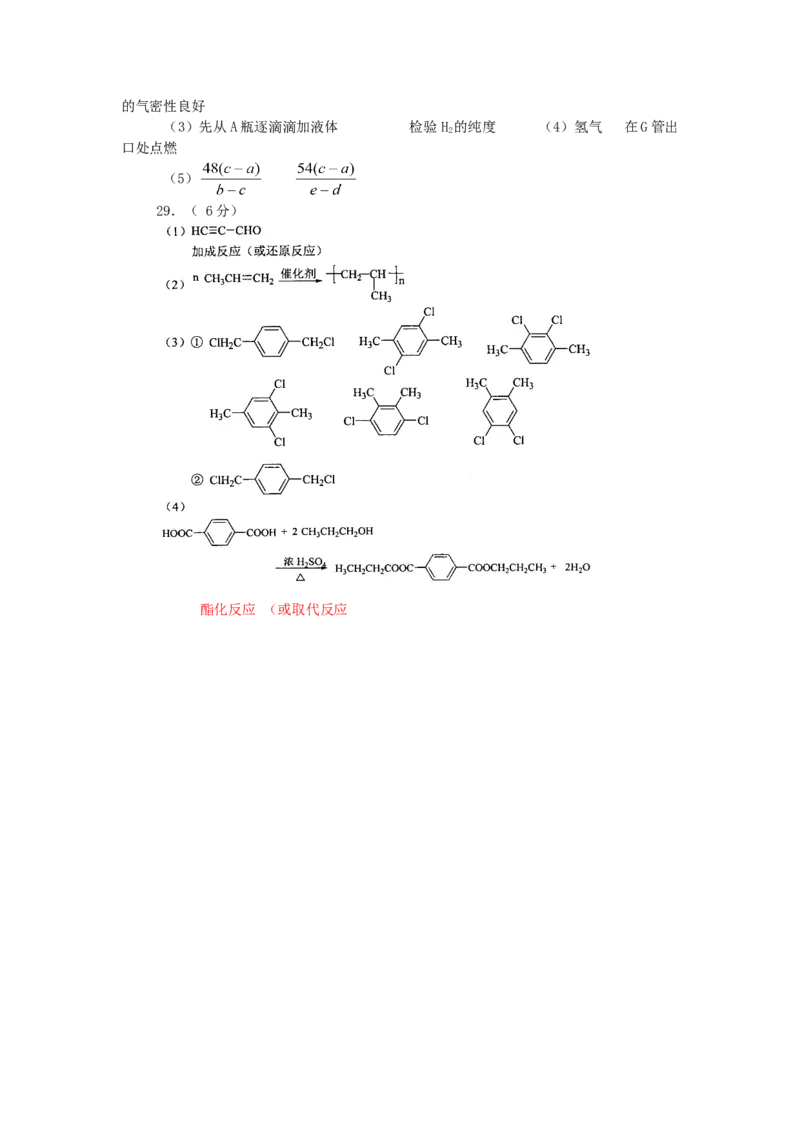
29.(16分)
下图中A、B、C、D、E、F、G、H均为有机化合物。回答下列问题:
(1)有机化合物 A的相对分子质量小于60,A能发生银镜反应,1molA在催化剂作用下
能与3 mol H 反应生成B,则A的结构简式是___________________,
2
由A生成B的反应类型是 ;
(2)B在浓硫酸中加热可生成C,C在催化剂作用下可聚合生成高分子化合物D,由C生成
D的化学方程式是__________________________;
(3)①芳香化合物E的分于式是C H Cl 。E的苯环上的一溴取代物只有一种,则E的所有
8 8 2
可能的结构简式是。_______________________________________________
②E在NaOH溶液中可转变为F,F用高锰酸钾酸性溶液氧化生成 G(C H O )。1
8 6 4
mol G与足量的 NaHCO 溶液反应可放出 44.8 L CO (标准状况),由此确定E的
3 2
结构简式是__________________________________________________
(4)G和足量的B在浓硫酸催化下加热反应可生成H,则由G和B生成H的化学方程式
是_____________________________________________________________________,
该反应的反应类型是__________________________________________。
2008理科综合能力测试参考答案
第Ⅰ卷共21小题,每小题6分,共126分。
一、选择题:
6.C 7.B 8.D 9.C 10.D 11.A 12.B 13.C
26.(14分)
(l)
无 CuSO 溶液无色,而CuSO 溶液为蓝色
4 4
(2)
NaSO 无 钠的焰色反应呈黄色
2 4
(3)
MgCO Ba(NO) AgNO MgCO 沉淀溶于盐酸,有气体放出;如有
3 3 2 3 3
Ba(NO) ,生成的BaSO 沉淀不溶于盐酸;
3 2 4
如有AgNO,生成的沉淀在盐酸中不消失。
3
(4)Al(SO)
2 4 3
27.(15分) (1)SO (2)Cl,HClO HclO HclO HclO (任写 3
3 2 3 4
种酸)
(3)直线形 (4)共价键 原子晶体 (5)MgN MgN
3 2 3 2
十8HO = 3Mg(OH)↓+2NH·HO
2 2 3 2
(MgN 十6HO = 3Mg(OH)↓+2NH↑)
3 2 2 2 3
(6)D的最高价氧化物是CO,X的最高价氧化物是SiO,前者比后者的熔点低。因为
2 2
前者为分子晶体,由分子间力结合,而后者为原子晶体,由共价键结合;共价键强度大于
分子间力。
28.(15分) (1)锌粒 水 浓硫酸 (2)检查气密性
将G弯管浸没在盛有水的烧杯中,温热烧瓶B,观察G管口,若有气泡逸出,说明装置的气密性良好
(3)先从A瓶逐滴滴加液体 检验H 的纯度 (4)氢气 在G管出
2
口处点燃
(5)
29.( 6分)
酯化反应 (或取代反应