文档内容
2008年普通高等学校招生全国统一考试(山东卷) 13、N 代表阿伏加德罗常数,下列叙述错误的是
A
理科综合能力测试化学部分 A.l0mL质量分数为98%的H SO ,用水稀释至l00 mL,H SO 的质量分数为9 .8%
2 4 2 4
第Ⅰ卷
B.在H O +Cl =2HCI+O :反应中,每生成32 g氧气,则转移2N 个电子
2 2 2 2 A
以下数据可供答题时参考:
C.标准状况下,分子数为的N 的CO、C H 混合气体体积约为22 .4 L,质量为28 g
A 2 4
相对原于质量(原子量):H l C l2 N 14 O16 Na 23 S 32 C1 35.5
一、选择题 D.一定温度下,l L0 .50mol·L1 NH
4
Cl 溶液与2 L0 .25 mol·L1 NH
4
Cl 溶液含NH
4
物质的量不同
9、下列叙述合理的是 c(CO)c H O
14、高温下,某反应达平衡,平衡常数K= 2 。恒容时,温度升高,H 浓度减小。下列说法正确的
c(CO )c H 2
A.金属材料都是导体,非金属材料都是绝缘体 2 2
B.棉、麻、丝、毛及合成纤维完全燃烧都只生成CO 和H O
是
2 2
A.该反应的焓变为正值
C.水电站把机械能转化成电能,而核电站把化学能转化成电能
B.恒温恒容下,增大压强,H 浓度一定减小
D.我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染” 2
10、下列由事实得出的结论错误的是 C.升高温度,逆反应速率减小
A.维勒用无机物合成了尿素,突破了无机物与有机物的界限
D.该反应化学方程式为COH O CO H
2 2 2
B、门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新
15、某温度时,BaSO 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
4
C 、C 是英国和美国化学家共同发现的,体现了国际科技合作的重要性
60
D、科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研 究为主的学科
11、下列说法正确的是
A.SiH 比CH .稳定
4 4
B.O2半径比F的小
C.Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强
D.P和As属于第ⅤA族元素,H PO 酸性比H AsO 的弱
3 4 3 4
12、下列叙述正确的是
提示:BaSO (s) Ba2(aq)SO2(aq)的平衡
4 4
A.汽油、柴油和植物油都是碳氢化合物
常数K c(Ba2)c(SO2)称为溶度积常数
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应 ap 4
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
A.加入Na SO 可以使溶液由a点变到b点
2 4
D.含5个碳原子的有机物.每个分子中最多可形成4个C—C单键B.通过蒸发可以使溶液由d点变到c点
提供的试剂:稀盐酸 稀硫酸 KSCN溶 液 KMnO 溶液
4
C.d点无BaSO 沉淀生成
4 NaOH溶液 碘水
D.a点对应的K 大于c点对应的K 所选试剂为
sp sp
证明炉渣中含有FeO的实验现象为 。
第Ⅱ卷
29、(12分)北京奥运会“祥云”火炬燃料是丙烷(C H ),亚特兰大奥运会火炬燃料是丙烯 (C H )。
28、(14分)黄铜矿(CuFeS )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。 3 8 3 6
2
(1)丙烷脱氢可得丙烯。
(1)冶炼铜的反应为
高温
已知:C H (g) CH (g) (g)H (g) H 156.6kJ mol1
3 8 4 2 1
8CuFeS 21O 8Cu4FeO2Fe O 16SO
2 2 2 3 2
CH CH CH (g) CH (g)HC CH (g)H (g) H 32.4kJ mol1
若CuFeS 中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。 3 2 4 2 2 1
2
则相同条件下,反应C H (g) CH CH CH (g)H (g)的H = kJmol1
(2)上述冶炼过程产生大量SO 。下列 处理方案中合理的是 (填代号)。 3 3 3 2 2
2
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O 和CO ,负极通入丙烷,电解质是熔融碳酸盐。电
a.高空排放 2 2
b.用于制备硫酸 池反应方程式为 ;放电时,CO2移向电池的 (填 “正”或“负”)极。
3
c.用纯碱溶液吸收制Na SO
2 3 (3)碳氢化合物完全燃烧生成CO 和H O。常温常压下,空气中的CO 溶于水.达到平衡时,溶液的
2 2 2
d.用浓硫酸吸收
pH=5.60,c(H CO )=1.5×10-5mol·L-1。若忽略水的电离及H CO 第二级电离,则H CO
2 3 2 3 2 3
(3)过二硫酸钾(K S O )具有强氧化性,可将I氧化为I :
2 2 8 2
HCO H的平衡常数K (已知:10-5.60=2 5×10-6)
3 1
S O 2 2I 2SO2 I
2 8 4 2
(4)常温下,0.l mol· L-1NaHCO ,溶液的pH大于8.则溶液中c(H CO ) c(CO2) (填、
3 2 3 3
通过改变反应途径,Fe3、Fe2均可催化上述反应。试用离子方程式表示Fe3对上述反应催化的过
“﹥” “=”或 “<” ,原因是 (用离子方程式和必要的文字说明)。
程。 、 (不必配平)
30、(16分)食盐是日常生活的必需品,也是重要的化工原料。
(4)利用黄铜矿冶炼铜产生的炉渣(Fe O 、FeO、SiO 、Al O )可制备Fe O 。方法为
2 3 2 2 3 2 3 (1)粗食盐常含有少量K+、Ca 2+、Mg 2+、Fe 3+、SO2等杂质离子,实验室提纯NaCl的流程如下:
4
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液。过滤,将沉淀洗涤、干燥、煅烧得Fe O 。据以上信息回答下列
2 3
问题:
a.除去Al3的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:饱和Na CO 溶液 饱和K CO 溶液 NaOH溶液 BaCl 溶液 Ba(NO ) 溶液
2 3 2 3 2 3 275%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca 2+、Mg 2+、Fe 3+、SO2离子,选出a所代表的试剂,按滴加顺序依次为
4
(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为 。
(2)用提纯的NaCl配制500 mL4.00 mol· L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有 (填仪器
名称)。
(3)电解饱和食盐水的装置如图所示,若收集的H 为2 L,则同样条件下收集的Cl (填 “>”、“=” 或
2 2
“< ” )2 L,原因是 . 装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法
为 。
【选做部分】
31、(8分)【化学一化学与技术】
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在 部分发生反应,在 部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为 ;加入硅、锰和铝的目的是 。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹 (填 “前” 或 “后” )加入,原因是 。
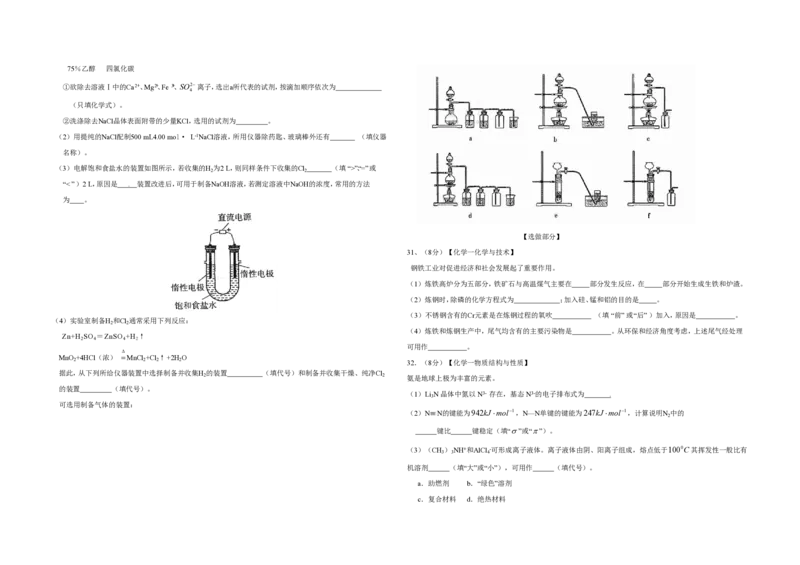
(4)实验室制备H 和Cl 通常采用下列反应:
2 2
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是 。从环保和经济角度考虑,上述尾气经处理
Zn+H SO =ZnSO +H ↑
2 4 4 2
可用作 。
MnO +4HCl(浓) MnCl +Cl ↑+2H O
2 2 2 2 32.(8分)【化学一物质结构与性质】
据此,从下列所给仪器装置中选择制备并收集H 的装置 (填代号)和制备并收集干燥、纯净Cl
2 2 氨是地球上极为丰富的元素。
的装置 (填代号)。
(1)Li N晶体中氮以N3- 存在,基态N3-的电子排布式为 .
3
可选用制备气体的装置:
(2)N N的键能为942kJ mol1,N—N单键的键能为247kJ mol1,计算说明N 中的
2
键比 键稳定(填“”或“”)。
(3)(CH ) NH+和AlCl -可形成离子液体。离子液体由阴、阳离子组成,熔点低于1000C其挥发性一般比有
3 3 4
机溶剂 (填“大”或“小”),可用作 (填代号)。
a.助燃剂 b.“绿色”溶剂
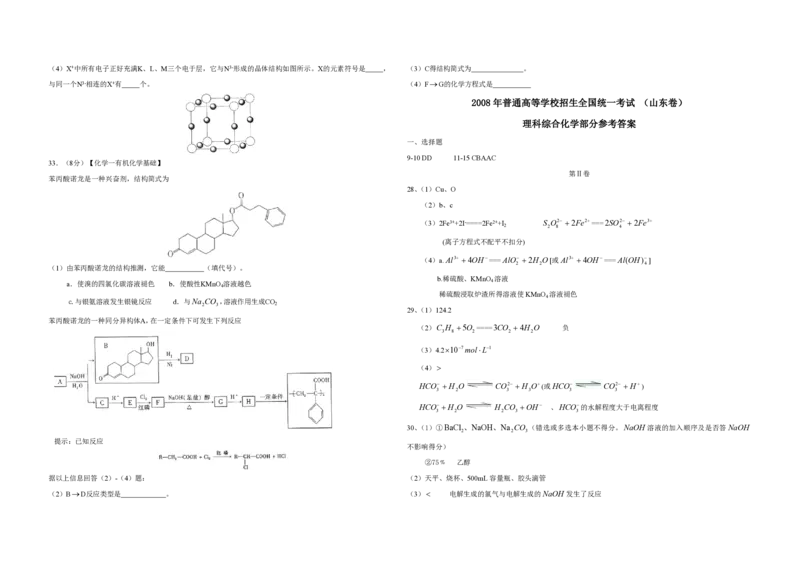
c.复合材料 d.绝热材料(4)X+中所有电子正好充满K、L、M三个电于层,它与N3-形成的晶体结构如图所示。X的元素符号是 , (3)C得结构简式为 。
与同一个N3-相连的X+有 个。 (4)FG的化学方程式是
2008 年普通高等学校招生全国统一考试 (山东卷)
理科综合化学部分参考答案
一、选择题
9-10 DD 11-15 CBAAC
33.(8分)【化学一有机化学基础】
第Ⅱ卷
苯丙酸诺龙是一种兴奋剂,结构简式为
28、(1)Cu、O
(2)b、c
(3)2Fe3++2I-====2Fe2++I S O2 2Fe2===2SO2 2Fe3
2 2 8 4
(离子方程式不配平不扣分)
(4)a.Al3 4OH===AlO 2H O[或Al3 4OH===Al(OH)]
2 2 4
(1)由苯丙酸诺龙的结构推测,它能 (填代号)。
b.稀硫酸、KMnO 溶液
a.使溴的四氯化碳溶液褪色 b.使酸性KMnO 溶液越色 4
4
稀硫酸浸取炉渣所得溶液使KMnO 溶液褪色
4
c.与银氨溶液发生银镜反应 d.与Na CO ,溶液作用生成CO
2 3 2
29、(1)124.2
苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应
(2)C H 5O ====3CO 4H O 负
3 8 2 2 2
(3)4.2107molL1
(4)
HCO H O CO2 H O(或HCO CO2 H)
3 2 3 3 3 3
HCO H O H CO OH 、HCO的水解程度大于电离程度
3 2 2 3 3
30、(1)①BaCl 、NaOH、Na CO (错选或多选本小题不得分。NaOH 溶液的加入顺序及是否答NaOH
2 2 3
提示:已知反应
不影响得分)
②75﹪ 乙醇
据以上信息回答(2)-(4)题: (2)天平、烧杯、500mL容量瓶、胶头滴管
(2)BD反应类型是 。 (3) 电解生成的氯气与电解生成的NaOH 发生了反应酸碱中和滴定
(4)e d
31、(1)炉身 炉腰
(2)2P5FeO3CaO高温Ca PO 5Fe
4 2
脱氧和调整钢的成分
(3)后 避免Cr被氧化(或“氧吹前加入Cr会形成炉渣被除去”)
(4)CO 燃料(或还原剂)
32、(1)1s22s22p6
(2)
(3)小 b
(4)Cu 6
33、(1)a、b
(2)加成反应(或还原反应)