文档内容
2009 年普通高等学校招生全国统一考试(重庆卷)
理科综合能力测试试题卷(化学部分及其解析)
以下数据可供解题时参考:
相对原子质量:H 1 C 12 O 16 Na 23 Si 28 Cl 35.5
第一部分(选择题共48分)
6.材料与化学密切相关,表中对应系错误的是
材料 主要化学成分
A 刚玉、金刚石 三氧化二铝
B 大理石、石灰石 碳酸钙
C 普通水泥、普通玻璃 硅酸盐
D 沙子、石英 二氧化硅
答案A
【解析】金刚石是由碳元素组成的单质,而不是三氧化铝,A项错误。
【考点分析】本题考查考生对物质组成成分的认识。
7.有关实验的叙述,正确的是
A.将固体加入容量瓶中溶解并稀释至刻度,配置成一定物质的量浓度的溶液
B.用玻璃棒蘸取溶液,点在湿润的pH是指上测定其pH
C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应
D.读取滴定管内液体的体积,俯视读数导致读数偏小
答案D
【解析】A项容量瓶不能用来直接盛装固体配置溶液,要将固体先在烧杯中溶解,冷却至室
温转移到容量瓶中,A项错误;B项pH不能润湿,润湿后会改变待测夜的浓度,从而测定不
准,B项错误;C项进行焰色反应时铂丝用浓盐酸洗涤并灼烧,如用NaOH洗涤会使NaOH
粘附在铂丝上,干扰检验其它金属元素的焰色反应,C项错误;D项正确。
【考点分析】本题考查化学基本实验操作、仪器使用等。
8.下列各组离子,能在溶液中大量共存的是
A. B
C. D
答案D
【解析】A项Mg2+水解呈酸性,AlO—水解呈碱性,Mg2+与AlO—发生双水解,Mg2++2AlO —
2 2 2
+4H O====2Al(OH)↓+Mg(OH)↓不能大量共存;A项错误;B项在酸性条件下NO —具
2 3 2 3
有强氧化性,Fe2+与NO —不能大量共存B项错误;C项NH +与OH—结合成弱电解质
3 4
NH ·HO不能大量共存,C项错误;答案选D。
3 2
【考点分析】本题考查离子的大量共存。
9.下列叙述正确的是
A.SO 具有还原性,故可作漂白剂
2
B.Na的金属活性比Mg强,故可用Na与MgCl 溶液反应制Mg
2
C.浓硝酸中的HNO 见光会分解,故有时在实验室看到的浓硝酸呈黄色
3
D.Fe在Cl 中燃烧生成FeCl,故在与其它非金属反应的产物中的Fe也显+3价
2 3
答案C【解析】A项SO 具有还原性和氧化性,在作漂白剂时并不发生氧化还原反应,而是与品红
2
中的有色物质发生化合而褪色;B项Na是活泼金属,Na与MgCl 溶液反应时,先与水反应
2
得到H,D项Fe与其它非金属反应的产物的化合价取决于非金属的氧化性强弱,并不一定
2
是+3价,如Fe与S反应生成FeS中Fe显+2价,D错误;答案选C。
【考点分析】本题考查化学反应及其物质的性质。
10.物质的量浓度相同的下列溶液,pH由大到小排列正确的是w.w.w.k.s.5.u.c.o.m
A.Ba(OH) 、 NaSO 、FeCl 、KCl
2 2 3 3
B.NaSiO、NaSO 、KNO、NH Cl
2 3 2 3 3 4
C.NH ·H O、HPO 、NaSO 、HSO
3 2 3 4 2 4 2 4
D.NaHCO 、C HCOOH、C HOH、HCl
3 6 5 2 5
答案B
【解析】A项FeCl 是强酸弱碱盐溶液呈酸性,KCl是强碱强酸盐溶液呈中性,A错误;C项
3
HPO 显酸性,C错误;D项C HOH呈中性,C HCOOH呈酸性,D错误;答案选B。
3 4 2 5 6 5
【考点分析】本题考查溶液的酸碱性。
11.下列对有机物结构或性质的描述,错误的是
A.一定条件下,Cl 可在甲苯的苯环或侧链上发生取代反应
2
B.苯酚钠溶液中通入CO 生成苯酚,则碳酸的酸性比苯酚弱
2
C.乙烷和丙烯的物质的量各1mol,完成燃烧生成3molHO
2
D.光照下2,2—二甲基丙烷与Br 反应其一溴取代物只有一种
2
答案B
【解析】B项CO + H O + C HONa C HOH + NaHCO,则碳酸的酸性比苯酚强,B错
2 2 6 5 6 5 3
误。
【考点分析】本题考查化学反应、化学反应方程式、同分异构、物质的量等。
12.下列热化学方程式数学正确的是( 的绝对值均正确)
A.C HOH(l)+3O (g)==2CO (g)+3H O(g);△H=—1367.0 kJ/mol(燃烧热)
2 5 2 2 2
B. NaOH(aq)+HCl(aq)==NaCl(aq)+H O(l);△H=+57.3kJ/mol(中和热)
2
C.S(s)+O (g)===SO(g);△H=—269.8kJ/mol(反应热)
2 2
D. 2NO ==O +2NO;△H=+116.2kJ/mol(反应热)
2 2
答案C
【解析】A项燃烧热要求可燃物的物质的量必须为1mol,得到的氧化物必须是稳定的氧化物,
HO的状态必须为液态,A项错误;中和反应是放热反应,△H应小于0,B项错误;热化学
2
反应方程式要注明物质在反应时的状态,D项错误;答案C正确。
【考点分析】本题考查燃烧热以及热化学方程式的书写正误判断。
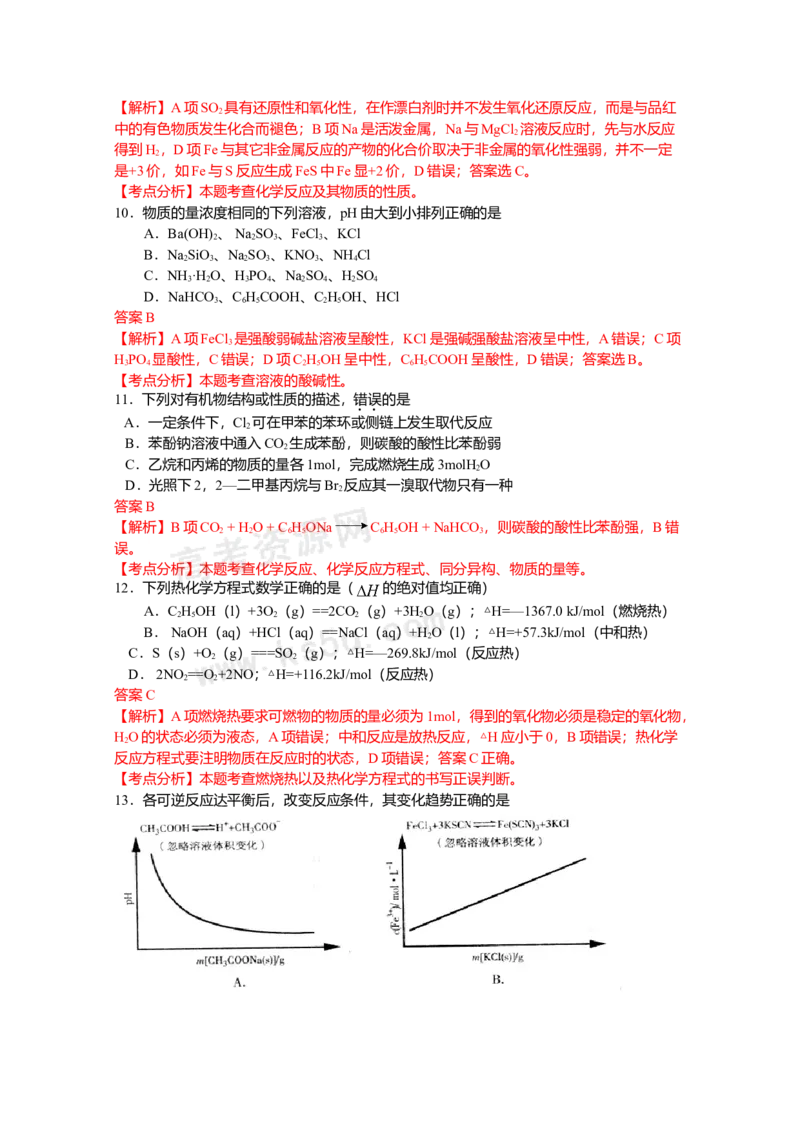
13.各可逆反应达平衡后,改变反应条件,其变化趋势正确的是答案D
【解析】A项CHCOOH溶液中加入CHCOONa固体,CHCOOH溶液中CHCOO—浓度增加,
3 3 3 3
电离平衡逆向移动,c(H+)减小,pH逐渐增大,A错误;B项加入KCl对平衡体系无影响,化
学平衡不移动,B错误;C项恒温恒压,加入Ar,各反应物的物质的量不变,体积变大,各
物质的量浓度成倍减小(等效于减压),化学平衡朝体积增大方向移动,H 的改变量减小,
2
起始量不变,转化率减小,C错误;大暗暗选D。
【考点分析】本题考查化学平衡的移动与化学平衡图像。
第二部分(非选择题共 60 分)
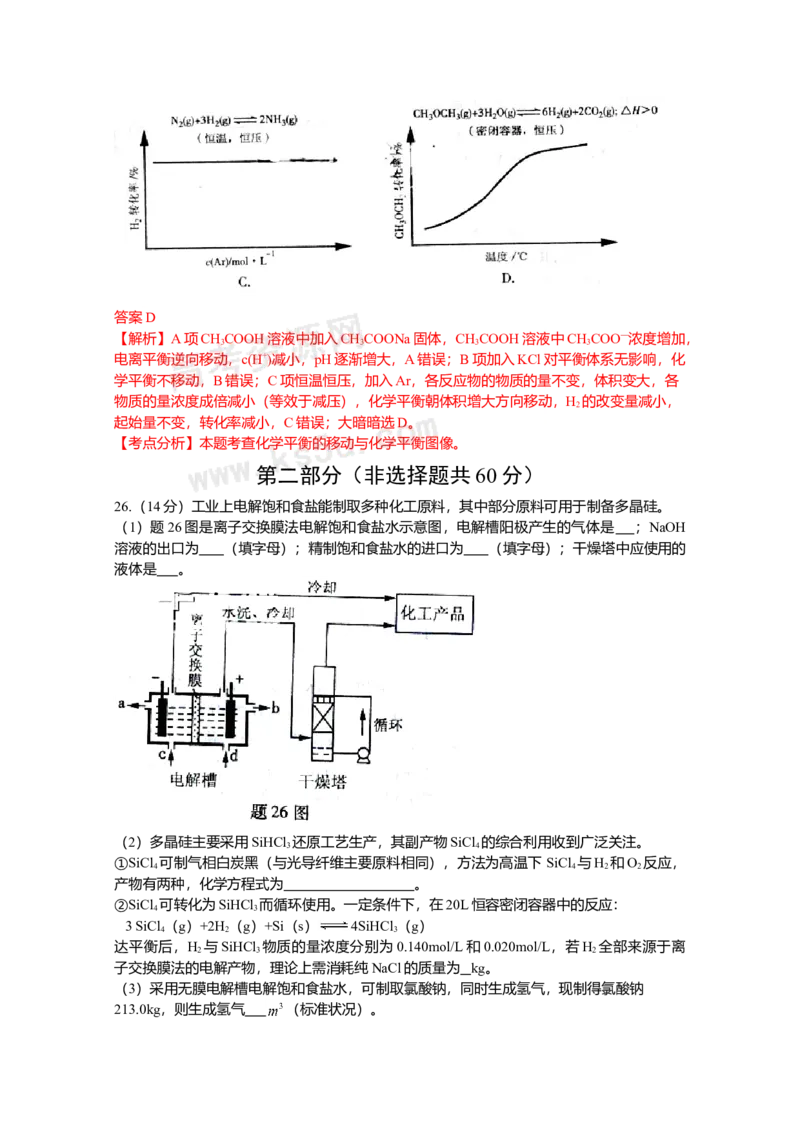
26.(14分)工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ;NaOH
溶液的出口为 (填字母);精制饱和食盐水的进口为 (填字母);干燥塔中应使用的
液体是 。
(2)多晶硅主要采用SiHCl 还原工艺生产,其副产物SiCl 的综合利用收到广泛关注。
3 4
①SiCl 可制气相白炭黑(与光导纤维主要原料相同),方法为高温下 SiCl 与H 和O 反应,
4 4 2 2
产物有两种,化学方程式为 。
②SiCl 可转化为SiHCl 而循环使用。一定条件下,在20L恒容密闭容器中的反应:
4 3
3 SiCl (g)+2H (g)+Si(s) 4SiHCl (g)
4 2 3
达平衡后,H 与SiHCl 物质的量浓度分别为0.140mol/L和0.020mol/L,若H 全部来源于离
2 3 2
子交换膜法的电解产物,理论上需消耗纯NaCl的质量为 kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠
213.0kg,则生成氢气 (标准状况)。答案(1)①氯气;a;d;浓硫酸(2)①SiCl +2H+O 高温 S iO+4HCl②0.35(3)134.4
4 2 2 2
【解析】(1)电解饱和食盐时阳极阴离子Cl—、OH—放电,Cl—的放电能力强于OH—,阳极
发生的方程式为:2Cl——2e—===Cl ↑;阴极:2H++2e—===H↑;总反应为:2NaCl+2H O
2 2 2
电解 C l↑+H ↑+2NaOH。H 、2NaOH在阴极,NaOH溶液的出口为a,Cl 在阳极,精制饱
2 2 2 2
和食盐水从阳极进入,选d;要干燥Cl 需要用酸性干燥剂HSO 或PO 等,中性干燥剂无水
2 2 4 2 5
CaCl 。(2)①SiCl 与H 和O 反应,产物有两种,光导纤维的主要成分是SiO ,H、Cl元
2 4 2 2 2
素必在另一产物中,H、Cl 元素结合成 HCl,然后配平即可。发生的化学方程式为:
SiCl +2H+O 高温 S iO+4HCl。②
4 2 2 2
由3 SiCl (g)+2H (g)+Si(s) 4SiHCl (g)
4 2 3
起始量(mol) n 0
变化量(mol) 3x 2x x 4x
平衡量(mol) n—2x 4x
4x=0.020mol/L×20L=0.4mol,n—2x=0.140mol/L20L=2.8mol,n=3.0mol,由 2NaCl+2H O
2
电解 C l↑+H ↑+2NaOH,( 2×58.5)g:1mol=m(NaCl)g:3mol;m(NaCl)
2 2
=351g=0.351kg。
(3)由NaCl转化为NaClO,失去电子数为6,HO转化为H,得到的电子数为2,设产生
3 2 2
的H 体积为V,由得失电子守恒有:6× ;
2
V=134.4m3。
【考点分析】本题考查电解、氯碱工业、化学平衡的计算、化学方程式书写、化学计算等知
识。
27.(15分)两个学习小组用题27图装置探究乙二酸(HOOC—COOH)受热分解的部分产
物。(1)甲组:w.w.w.k.s.5.u.c.o.m
①按接口顺序:a—b—c—d—e—f—g—h连接装置进行实验。B中溶液变浑浊,证明分解产
物有 ;装置C的作用是 ;E中溶液变浑浊,D中的现象是 ,证明分解产物
有 。
②乙二酸受热分解的化学方程式为 。
(2)乙组:
①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,则F中最主要
反应的化学方程式为 。
②从A~F中选用装置进行实验,证明甲组通入D的气体能否与NaO 反应。最简单的装置接
2 2
口连接顺序是 ;实验后用F中的固体进行验证的方法是 (可另
选试剂)。
答案
【解析】(1)①B中澄清石灰水变浑浊,证明分解产物有CO 产生;装置C的作用是充分除
2
去CO,防止对后继实验产物检验的干扰;E中澄清石灰水变浑浊,说明有CO 产生,乙二
2 2
酸产生的CO 在C装置中已经被NaOH吸收完全,CO 的产生来源于D装置中高锰酸钾对
2 2
CO的氧化,D中现象为溶液褪色(或变浅),证明分解产物有CO。②乙二酸受热分解的化
学方程式为:HOOC—COOH △ CO↑+CO↑+H O。(2)①接口a与j连接进行实验,观察
2 2
到F中生成的气体可使带火星的木条复燃,说明有氧气产生,通过冷凝管后出来主要是
CO,CO 与NaO 反应的化学方程式为:2CO+Na O=== 2NaCO+O 。②先要制备气体,
2 2 2 2 2 2 2 2 3 2
将产生的CO 吸收,再通入到NaO 中证明。连接顺序为:a→d→e→j;要证明发生了反应,
2 2 2即证明F中的物质是NaCO,方法较多。
2 3
【考点分析】本题综合考查化学实验、实验现象、实验设计、化学反应等知识。
28.(16分)星形聚合物SPLA可经下列反应路线得到(部分反应条件未注明)。
(1)淀粉是 糖(填“单”或“多”);A的名称是 。
(2)乙醛由不饱和烃制备的方法之一是 (用化学方程式表示,可多步)。
(3)D E的化学反应类型属于 反应;D结构中有3个相同的基团,且1molD能与
2molAg(NH ) OH反应,则D的结构简式是 ;D与银氨溶液反应的化学方程式为
3 2
。
(4)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO 溶液反应,又不能与新
3
制Cu(OH) 反应,且1molG与足量Na反应生成1mol H,则G的结构简式为 。
2 2
(5)B有多种脱水产物,其中两种产物的结构简式为 和 。答案
【解析】(1)由框图可以知道淀粉水解成A,A是葡萄糖,A转化为乳酸B,根据所学知识
知道淀粉是一种多糖。(2)乙醛的制备方法较多,可以用乙烯水化法转化为乙醇,乙醇氧
化成乙醛,或用乙炔与水发生加成反应也可,此题方法较多。(3)由D、E的化学式可以看
出E比D多2个H原子,加氢叫还原,加氢也是加成反应,1molD能与2molAg(NH )OH
3 2
反应,说明1molD中有1mol—CHO,D结构中有3个相同的基团,经分析相同的3个基团为
—(CHOH),分子式C H O 就剩下一个—C,D的结构简式 ,D与银氨溶
2 5 10 4
液反应的化学方程式为:
。
(4)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO 溶液反应,又不能与新
3
制Cu(OH) 反应,且1molG与足量Na反应生成1mol H,G中无—COOH,无—CHO,
2 2
1molG中有2mol—OH,即可得G的结构简式为: 。
(5)B是乳酸,由其官能团的反应机理即可得到答案。 、、 、 。
【考点分析】本题是考查有机物的综合推断、同分异构体的书写、有机化学反应类型、有机
化学反应方程式的书写等知识。
29(15分)化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1) X的单质既可与盐酸反应,又可与NaOH溶液反应,X的原子结构示意图为
。
(2) X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为
(3) 一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与HO 反应,其产物之一是Y的单质,Y的单质地电子式为 ;Z分子的结构
2 2
呈
②A的化学式是
(4)X的单质、石墨和二氧化钛(TiO )按比例混合,高温下反应得到的化合物均由两种元
2
素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是
答案
【解析】(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X为Al元素,X的原子
结构示意图为
+13
(2)铝盐与过量NaOH溶液反应转化为偏铝酸盐,发生的离子反应方程式为:
Al3++4OH—===AlO—+2H O。
2 2
(3)①A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子个电子,可以推测Z是
一种氢化物,常见的氢化物由NH 、CH、HF等;Z与HO 反应,其产物之一是Y的单质,
3 4 2 2
知道Z是NH 。②A具有良好的耐热冲击性能,由以上几种元素与Al构成的化合物来看只有
3
N与Al构成AlN。(4)由题意可以得到答案。
【考点分析】本题考查元素及其化合物的综合推断。
w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m