文档内容
第I卷(选择题)
1.下列属于酸性氧化物的是
A.CO B.CaO C.K SO D.NaOH
2 2 4
2.仪器名称为“容量瓶”的是
A. B. C. D.
3.常温下能与水反应的金属单质是
A.SiO B.Br C.Na O D.Na
2 2 2
4.HCl+NaOH=NaCl+H O的反应类型是
2
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
5.下列物质中,属于可再生的能源是
A.氢气 B.石油 C.煤 D.天然气
6.硅元素在周期表中的位置是
A.第二周期ⅣA族 B.第三周期ⅣA族
C.第三周期ⅥA族 D.第二周期ⅥA族
7.下列化学用语表述正确的是
A.水分子的结构式: B.氯化钠的电子式:
C.氯气的比例模型: D.硫原子的结构示意图:
8.能产生“丁达尔效应”的是
A.饱和食盐水 B.Fe(OH) 胶体 C.盐酸 D.硫酸铜溶液
3
9.下列说法不正确的是
A.核素2H的中子数是0 B.12C和14C互为同位素
1
C.金刚石、石墨和富勒烯互为同素异形体 D.CH CH OH和CH OCH 互为同分异构体
3 2 3 3
10.实验室有两瓶失去标签的溶液,其中一瓶是H SO ,另一瓶是蔗糖溶液。鉴别时,下列选用的试纸或试
2 4
剂不正确的是( )
第1页 | 共9页A.pH试纸 B.KCl溶液
C.BaCl 溶液 D.Na CO 溶液
2 2 3
11.下列物质的水溶液因水解呈酸性的是
A.NaOH B.Na CO C.NH Cl D.HCl
2 3 4
12.已知1 mol CH 气体完全燃烧生成气态CO 和液态H O,放出890.3 kJ热量,则表示该反应的热化学方
4 2 2
程式正确的是
A.CH (g)+2O (g)=CO (g)+2H O(g) △H=+890.3 kJ·mol-1
4 2 2 2
B.CH (g)+2O (g)=CO (g)+2H O(l) △H=-890.3 kJ·mol-1
4 2 2 2
C.CH (g)+2O (g)=CO (g)+2H O(l) △H=+890.3 kJ·mol-1
4 2 2 2
D.CH (g)+2O (g)=CO (g)+2H O(g) △H=-890.3 kJ·mol-1
4 2 2 2
13.有关SO 的性质,下列说法不正确的是
2
A.能使品红溶液褪色 B.能与NaOH溶液反应
C.能与H O反应生成H SO D.一定条件下能与O 反应生成SO
2 2 4 2 3
14.有关苯的结构和性质,下列说法正确的是
A.分子中含有碳碳双键
B.易被酸性KMnO 溶液氧化
4
C.与溴水发生加成反应而使溴水褪色
D.在一定条件下可与浓硝酸和浓硫酸的混合酸反应生成硝基苯
15.下列说法正确的是
A.HCl属于共价化合物,溶于水能电离出H+和Cl-
B.NaOH是离子化合物,该物质中只含离子键
C.HI气体受热分解的过程中,只需克服分子间作用力
D.石英和干冰均为原子晶体
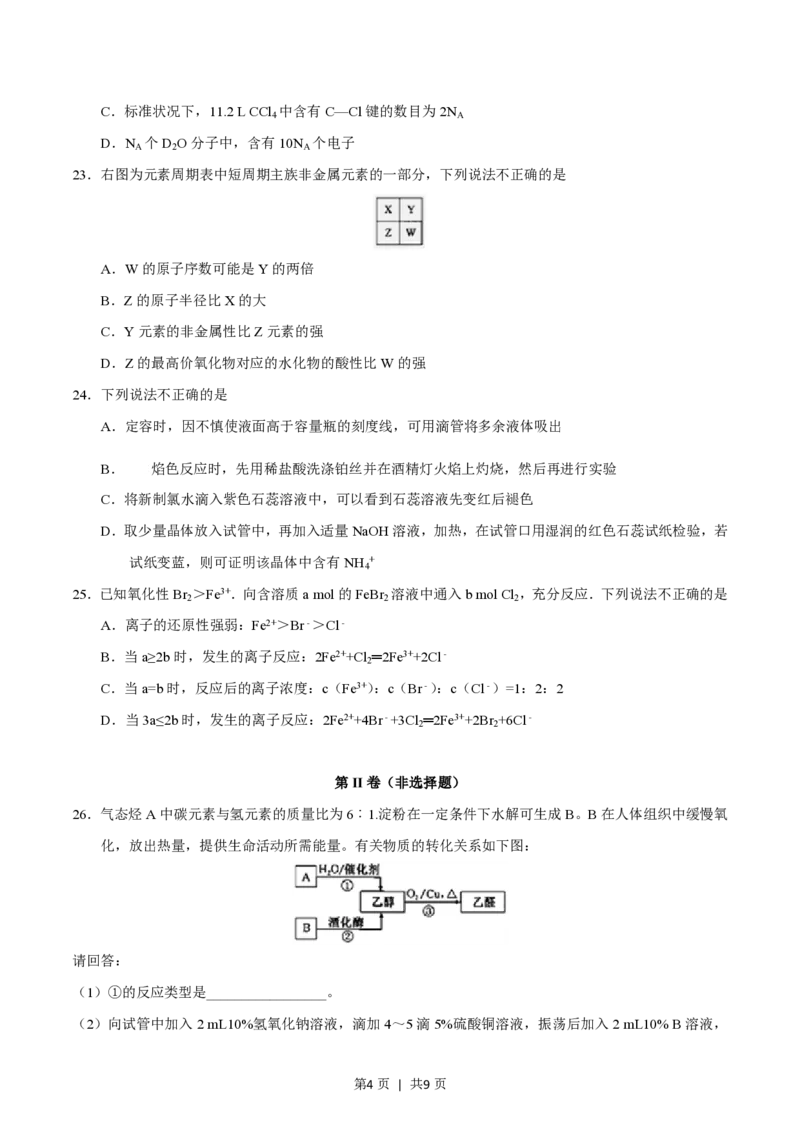
16.按如图所示装置进行实验,下列说法不正确的是( )
A.装置甲的锌片上和装置乙的铜片上均可观察到有气泡产生
第2页 | 共9页B.甲、乙装置中的能量变化均为化学能转化为电能
C.装置乙中的锌、铜之间用导线连接电流计,可观察到电流计指针发生偏转
D.装置乙中负极的电极反应式:Zn-2e-===Zn2+
17.关于常温下浓度均为0.1 mol·L-1 的盐酸和醋酸溶液,下列说法正确的是
A.醋酸溶液的pH小于盐酸
B.醋酸的电离方程式:CH COOH=CH COO-+H+
3 3
C.c(CH COOH)+c(CH COO-)=c(Cl-)
3 3
D.0.1 mol·L-1 的醋酸溶液与等物质的量浓度、等体积的氢氧化钠溶液混合后:c(H+)>c(OH-)
18.下列离子方程式正确的是
A.硫酸钠溶液与氢氧化钡溶液反应:SO 2-+Ba2+=BaSO ↓
4 4
B.大理石与稀硝酸反应:CO 2-+2H+=CO ↑+H O
3 2 2
C.氯化铁溶液与碘化钾溶液反应:Fe3++2I-=Fe2++I
2
D.氯化镁容液与氨水反应:Mg2++2OH-=Mg(OH) ↓
2
19.下列说法不正确的是
A.钠和钾的合金可用于快中子反应堆作热交换剂
B.可用超纯硅制造的单晶硅来制芯片
C.可利用二氧化碳制造全降解塑料
D.氯气有毒,不能用于药物的合成
20.某温度时,2NO(g)+O (g)=2NO (g)反应到2 s后,NO的浓度减少了0.06 mol·L-1,则以O 表示该时段
2 2 2
的化学反应速率是
A.0.03 mol·L-1·s-1 B.0.015 mol·L-1·s-1
C.0.12 mol·L-1·s-1 D.0.06 mol·L-1·s-1
21.下列说法正确的是
A.棉花和蚕丝的主要成分都是纤维素
B.蛋白质在一定条件发生水解反应生成葡萄糖
C.煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程
D.食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物
22.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.N 个氧分子与N 个氢分子的质量之比为8∶1
A A
B.100 mL 1.0 mol·L-1FeCl 溶液与足量Cu反应,转移的电子数为0.2N
3 A
第3页 | 共9页C.标准状况下,11.2 L CCl 中含有C—Cl键的数目为2N
4 A
D.N 个D O分子中,含有10N 个电子
A 2 A
23.右图为元素周期表中短周期主族非金属元素的一部分,下列说法不正确的是
A.W的原子序数可能是Y的两倍
B.Z的原子半径比X的大
C.Y元素的非金属性比Z元素的强
D.Z的最高价氧化物对应的水化物的酸性比W的强
24.下列说法不正确的是
A.定容时,因不慎使液面高于容量瓶的刻度线,可用滴管将多余液体吸出
B. 焰色反应时,先用稀盐酸洗涤铂丝并在酒精灯火焰上灼烧,然后再进行实验
C.将新制氯水滴入紫色石蕊溶液中,可以看到石蕊溶液先变红后褪色
D.取少量晶体放入试管中,再加入适量NaOH溶液,加热,在试管口用湿润的红色石蕊试纸检验,若
试纸变蓝,则可证明该晶体中含有NH +
4
25.已知氧化性Br >Fe3+.向含溶质a mol的FeBr 溶液中通入b mol Cl ,充分反应.下列说法不正确的是
2 2 2
A.离子的还原性强弱:Fe2+>Br﹣>Cl﹣
B.当a≥2b时,发生的离子反应:2Fe2++Cl ═2Fe3++2Cl﹣
2
C.当a=b时,反应后的离子浓度:c(Fe3+):c(Br﹣):c(Cl﹣)=1:2:2
D.当3a≤2b时,发生的离子反应:2Fe2++4Br﹣+3Cl ═2Fe3++2Br +6Cl﹣
2 2
第II卷(非选择题)
26.气态烃A中碳元素与氢元素的质量比为6︰1.淀粉在一定条件下水解可生成B。B在人体组织中缓慢氧
化,放出热量,提供生命活动所需能量。有关物质的转化关系如下图:
请回答:
(1)①的反应类型是_________________。
(2)向试管中加入2 mL10%氢氧化钠溶液,滴加4~5滴5%硫酸铜溶液,振荡后加入2 mL10% B溶液,
第4页 | 共9页加热。写出加热后观察到的现象_____________________________。
(3)反应③的化学方程式是__________________________________________________。
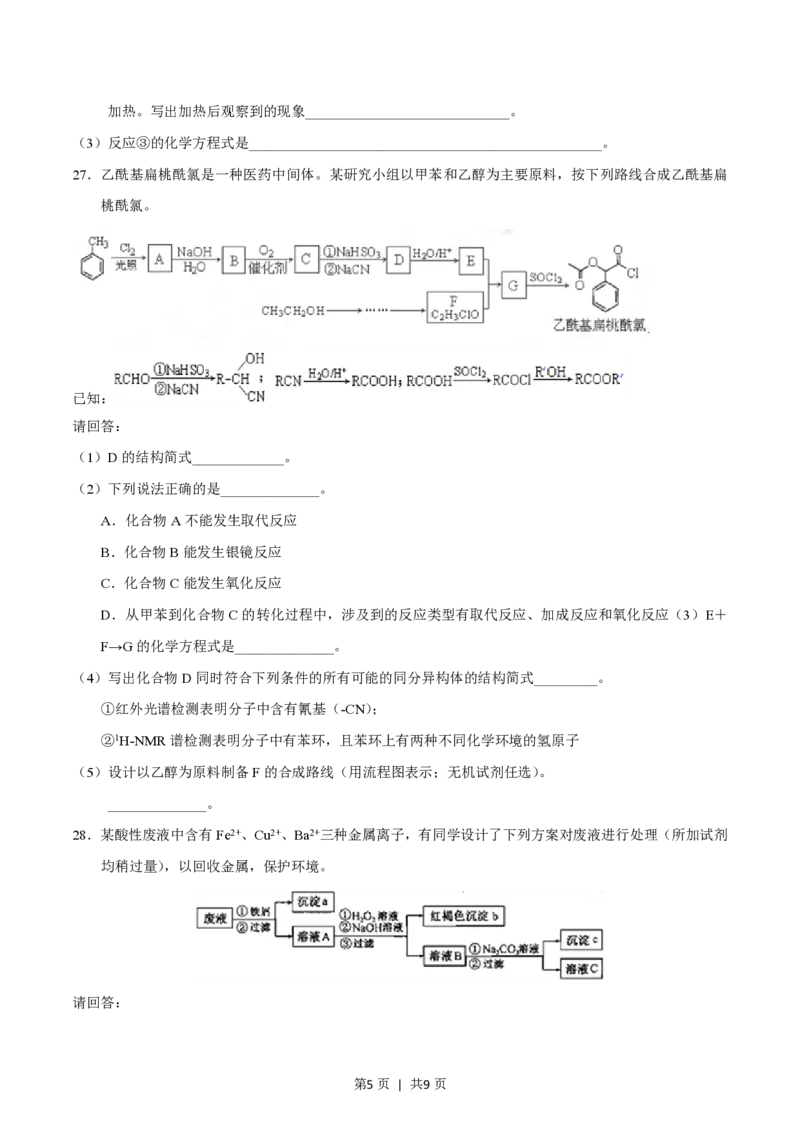
27.乙酰基扁桃酰氯是一种医药中间体。某研究小组以甲苯和乙醇为主要原料,按下列路线合成乙酰基扁
桃酰氯。
已知:
请回答:
(1)D的结构简式_____________。
(2)下列说法正确的是______________。
A.化合物A不能发生取代反应
B.化合物B能发生银镜反应
C.化合物C能发生氧化反应
D.从甲苯到化合物C的转化过程中,涉及到的反应类型有取代反应、加成反应和氧化反应(3)E+
F→G的化学方程式是______________。
(4)写出化合物D同时符合下列条件的所有可能的同分异构体的结构简式_________。
①红外光谱检测表明分子中含有氰基(-CN);
②1H-NMR谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子
(5)设计以乙醇为原料制备F的合成路线(用流程图表示;无机试剂任选)。
______________。
28.某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂
均稍过量),以回收金属,保护环境。
请回答:
第5页 | 共9页(1)沉淀a中含有的单质是_____________。
(2)沉淀c的化学式是___________________。
(3)溶液A与H O 溶液在酸性条件下反应的离子方程式是_________________________。
2 2
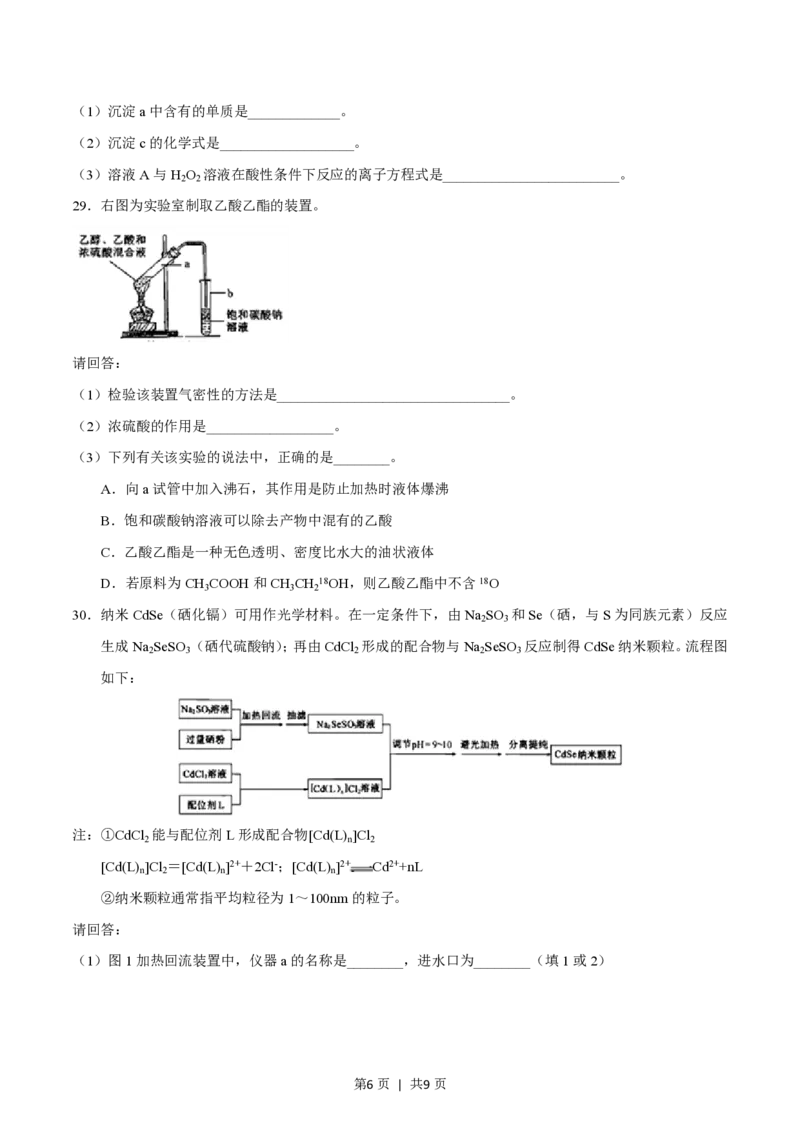
29.右图为实验室制取乙酸乙酯的装置。
请回答:
(1)检验该装置气密性的方法是_________________________________。
(2)浓硫酸的作用是__________________。
(3)下列有关该实验的说法中,正确的是________。
A.向a试管中加入沸石,其作用是防止加热时液体爆沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明、密度比水大的油状液体
D.若原料为CH COOH和CH CH 18OH,则乙酸乙酯中不含18O
3 3 2
30.纳米CdSe(硒化镉)可用作光学材料。在一定条件下,由Na SO 和Se(硒,与S为同族元素)反应
2 3
生成Na SeSO (硒代硫酸钠);再由CdCl 形成的配合物与Na SeSO 反应制得CdSe纳米颗粒。流程图
2 3 2 2 3
如下:
注:①CdCl 能与配位剂L形成配合物[Cd(L) ]Cl
2 n 2
[Cd(L) ]Cl =[Cd(L) ]2++2Cl-;[Cd(L) ]2+ Cd2++nL
n 2 n n
②纳米颗粒通常指平均粒径为1~100nm的粒子。
请回答:
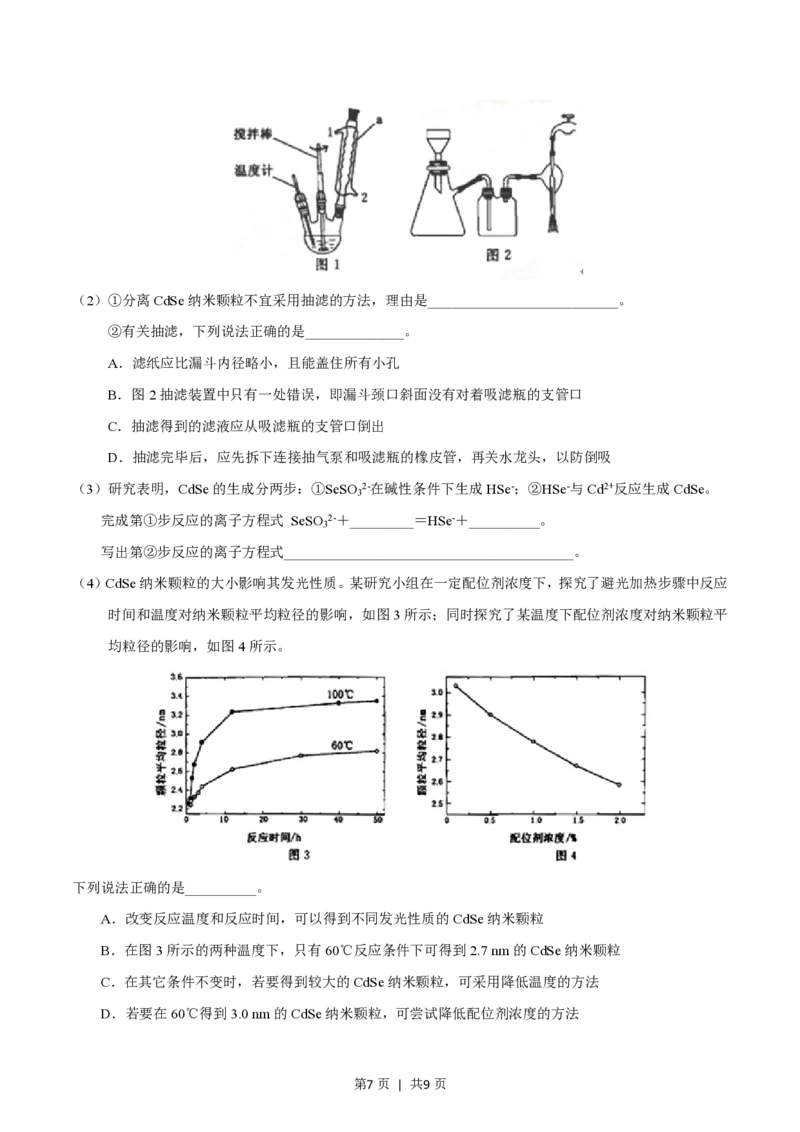
(1)图1加热回流装置中,仪器a的名称是________,进水口为________(填1或2)
第6页 | 共9页(2)①分离CdSe纳米颗粒不宜采用抽滤的方法,理由是___________________________。
②有关抽滤,下列说法正确的是______________。
A.滤纸应比漏斗内径略小,且能盖住所有小孔
B.图2抽滤装置中只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
C.抽滤得到的滤液应从吸滤瓶的支管口倒出
D.抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
(3)研究表明,CdSe的生成分两步:①SeSO 2-在碱性条件下生成HSe-;②HSe-与Cd2+反应生成CdSe。
3
完成第①步反应的离子方程式 SeSO 2-+_________=HSe-+__________。
3
写出第②步反应的离子方程式_________________________________________。
(4)CdSe纳米颗粒的大小影响其发光性质。某研究小组在一定配位剂浓度下,探究了避光加热步骤中反应
时间和温度对纳米颗粒平均粒径的影响,如图3所示;同时探究了某温度下配位剂浓度对纳米颗粒平
均粒径的影响,如图4所示。
下列说法正确的是__________。
A.改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒
B.在图3所示的两种温度下,只有60℃反应条件下可得到2.7 nm的CdSe纳米颗粒
C.在其它条件不变时,若要得到较大的CdSe纳米颗粒,可采用降低温度的方法
D.若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法
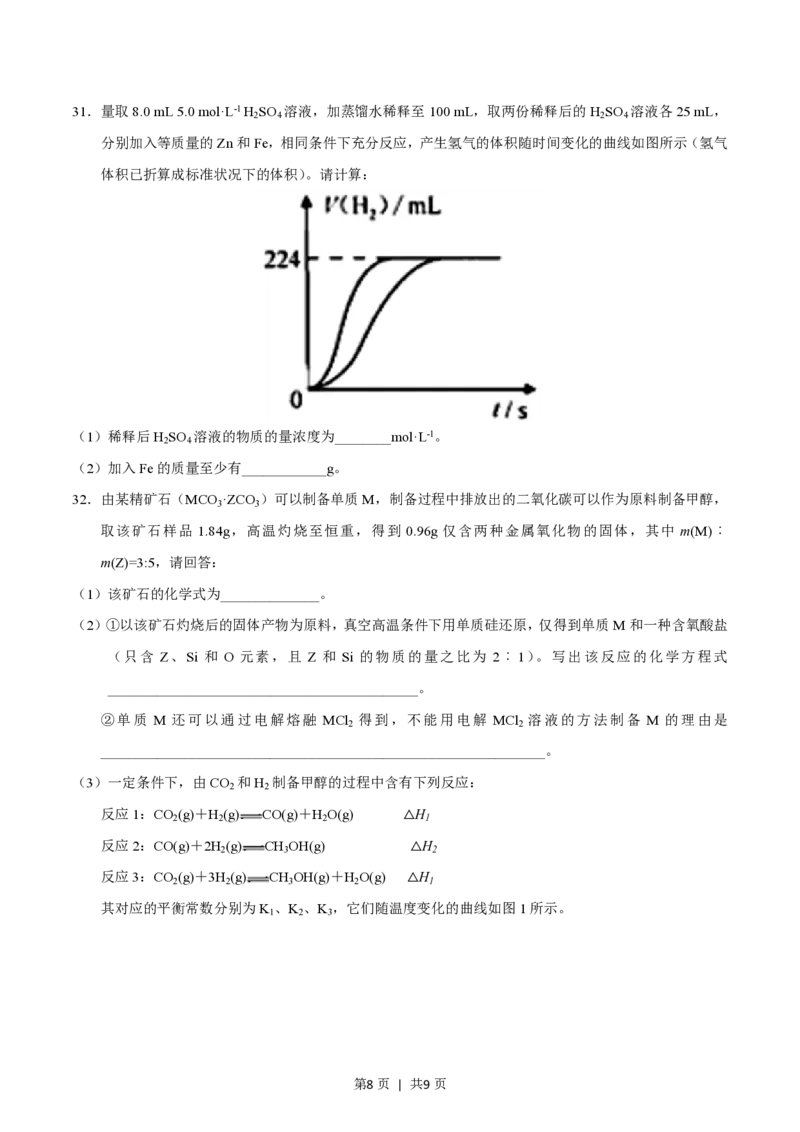
第7页 | 共9页31.量取8.0 mL 5.0 mol·L-1 H SO 溶液,加蒸馏水稀释至100 mL,取两份稀释后的H SO 溶液各25 mL,
2 4 2 4
分别加入等质量的Zn和Fe,相同条件下充分反应,产生氢气的体积随时间变化的曲线如图所示(氢气
体积已折算成标准状况下的体积)。请计算:
(1)稀释后H SO 溶液的物质的量浓度为________mol·L-1。
2 4
(2)加入Fe的质量至少有____________g。
32.由某精矿石(MCO ·ZCO )可以制备单质M,制备过程中排放出的二氧化碳可以作为原料制备甲醇,
3 3
取该矿石样品 1.84g,高温灼烧至恒重,得到 0.96g 仅含两种金属氧化物的固体,其中 m(M)︰
m(Z)=3:5,请回答:
(1)该矿石的化学式为______________。
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐
(只含 Z、Si 和 O 元素,且 Z 和 Si 的物质的量之比为 2︰1)。写出该反应的化学方程式
____________________________________________。
②单质 M 还可以通过电解熔融 MCl 得到,不能用电解 MCl 溶液的方法制备 M 的理由是
2 2
_______________________________________________________________。
(3)一定条件下,由CO 和H 制备甲醇的过程中含有下列反应:
2 2
反应1:CO (g)+H (g) CO(g)+H O(g) △H
2 2 2 1
反应2:CO(g)+2H (g) CH OH(g) △H
2 3 2
反应3:CO (g)+3H (g) CH OH(g)+H O(g) △H
2 2 3 2 1
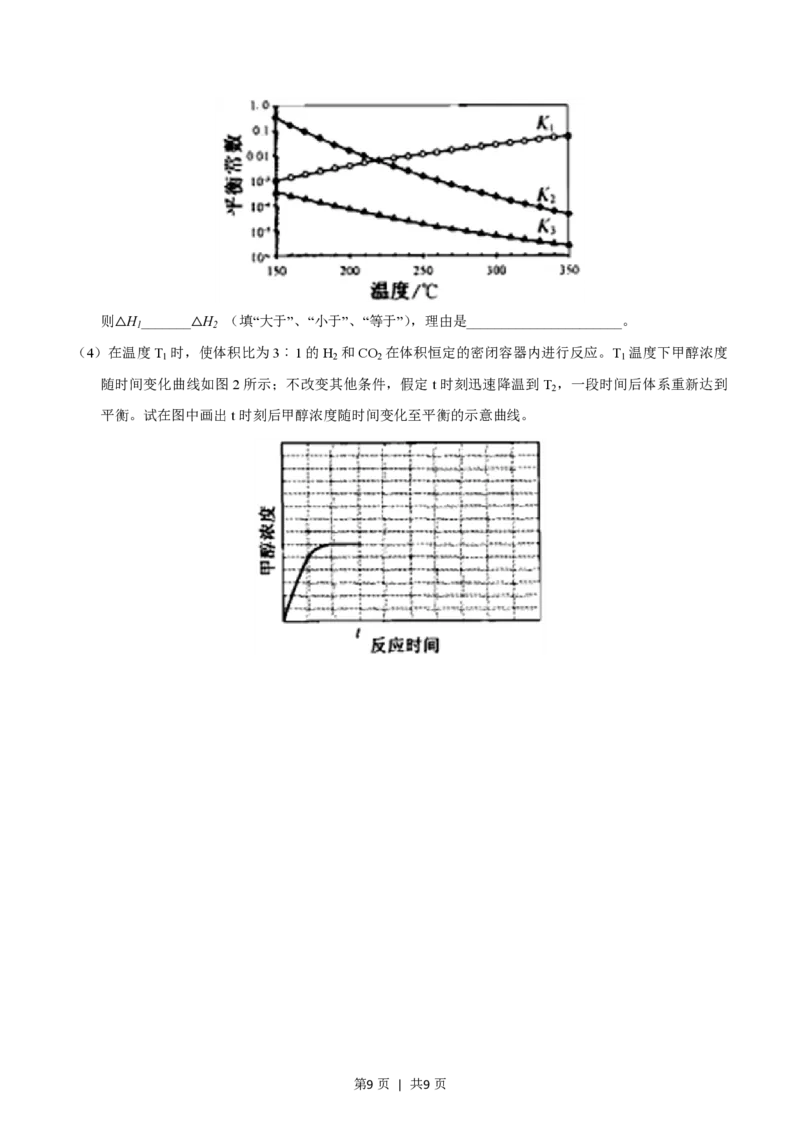
其对应的平衡常数分别为K 、K 、K ,它们随温度变化的曲线如图1所示。
1 2 3
第8页 | 共9页则△H _______△H (填“大于”、“小于”、“等于”),理由是______________________。
1 2
(4)在温度T 时,使体积比为3︰1的H 和CO 在体积恒定的密闭容器内进行反应。T 温度下甲醇浓度
1 2 2 1
随时间变化曲线如图2所示;不改变其他条件,假定t时刻迅速降温到T ,一段时间后体系重新达到
2
平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。
第9页 | 共9页