文档内容
向盛有FeCl 溶液的试管中加过量铁粉,
2019 年普通高等学校招生全国统一考试·全国Ⅱ卷 D 3 黄色逐渐消失,加KSCN后溶液颜色不变
充分振荡后加1滴KSCN溶液
11.下列化学方程式中,不能正确表达反应颜色变化的是( )
理科综合(化学部分)
A.向CuSO 溶液中加入足量Zn粉,溶液蓝色消失
4
Zn+CuSO ==Cu+ZnSO
4 4
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。 B.澄清的石灰水久置后出现白色固体
7.“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法 Ca(OH) 2 +CO 2 ==CaCO 3 ↓+H 2 O
错误的是( ) C.Na 2 O 2 在空气中放置后由淡黄色变为白色
A.蚕丝的主要成分是蛋白质 2Na
2
O
2
==2Na
2
O+O
2
↑
B.蚕丝属于天然高分子材料 D.向Mg(OH)
2
悬浊液中滴加足量FeCl
3
溶液出现红褐色沉淀3Mg(OH)
2
+2FeCl
3
==2Fe(OH)
3
+3MgCl
2
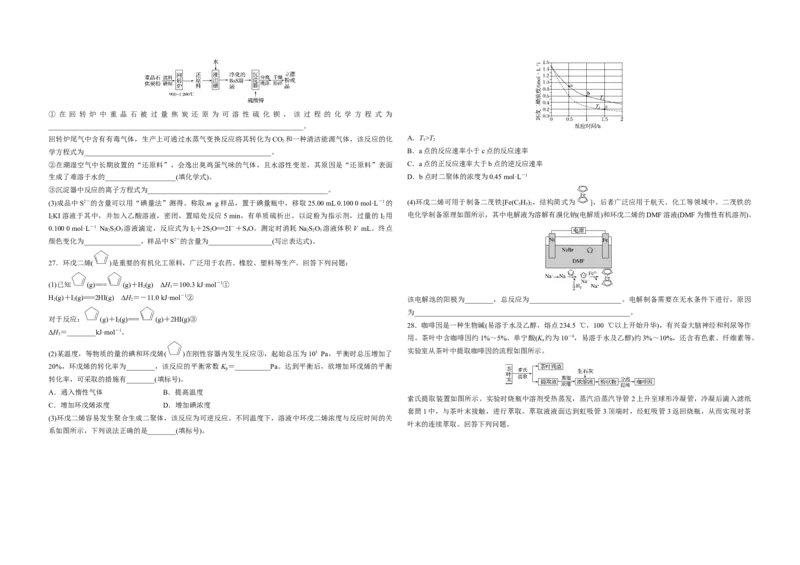
C.“蜡炬成灰”过程中发生了氧化反应 12.绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其
D.古代的蜡是高级脂肪酸酯,属于高分子聚合物 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
8.已知N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A.3 g 3He含有的中子数为1N
A
B.1 L 0.1 mol·L-1磷酸钠溶液含有的PO数目为0.1N
A
C.1 mol K Cr O 被还原为Cr3+转移的电子数为6N
2 2 7 A
D.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13N A.图中a和b分别为T、T 温度下CdS在水中的溶解度
A 1 2
9.今年是门捷列夫发现元素周期律150周年。如表是元素周期表的一部分,W、X、Y、Z为短周期主族元素, B.图中各点对应的K 的关系为:K (m)=K (n)T
2
学方程式为_____________________________________________________。 B.a点的反应速率小于c点的反应速率
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面 C.a点的正反应速率大于b点的逆反应速率
生成了难溶于水的____________________(填化学式)。 D.b点时二聚体的浓度为0.45 mol·L-1
③沉淀器中反应的离子方程式为___________________________________________________。
(3)成品中S2-的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.100 0 mol·L-1的 (4)环戊二烯可用于制备二茂铁[Fe(C 5 H 5 ) 2 ,结构简式为 ],后者广泛应用于航天、化工等领域中。二茂铁的
IKI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉为指示剂,过量的I 用 电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
2 2
0.100 0 mol·L-1 Na SO 溶液滴定,反应式为I +2SO==2I-+SO。测定时消耗NaSO 溶液体积V mL。终点
2 2 3 2 2 4 2 2 3
颜色变化为________________,样品中S2-的含量为__________________(写出表达式)。
27.环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知 (g)=== (g)+H(g) ΔH=100.3 kJ·mol-1①
2 1
H 2 (g)+I 2 (g)===2HI(g) ΔH 2 =-11.0 kJ·mol-1② 该电解池的阳极为________,总反应为__________________________。电解制备需要在无水条件下进行,原因
为_____________________________________________________________。
对于反应: (g)+I(g)=== (g)+2HI(g)③
2
28.咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5 ℃,100 ℃以上开始升华),有兴奋大脑神经和利尿等作
ΔH=________kJ·mol-1。
3 用。茶叶中含咖啡因约1%~5%、单宁酸(K 约为10-6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。
a
实验室从茶叶中提取咖啡因的流程如图所示。
(2)某温度,等物质的量的碘和环戊烯( )在刚性容器内发生反应③,起始总压为105 Pa,平衡时总压增加了
20%,环戊烯的转化率为________,该反应的平衡常数K =__________Pa。达到平衡后,欲增加环戊烯的平衡
p
转化率,可采取的措施有________(填标号)。
A.通入惰性气体 B.提高温度
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管 2上升至球形冷凝管,冷凝后滴入滤纸
C.增加环戊烯浓度 D.增加碘浓度
套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶
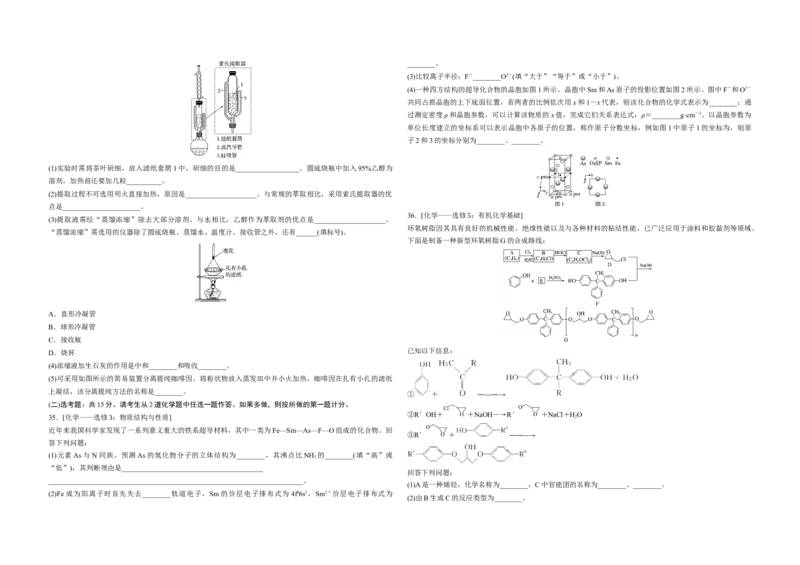
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关
叶末的连续萃取。回答下列问题。
系如图所示,下列说法正确的是________(填标号)。________。
(3)比较离子半径:F-________O2-(填“大于”“等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-
共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为________;通
过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=________g·cm-3。以晶胞参数为
单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为,则原
子2和3的坐标分别为________、________。
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是__________________。圆底烧瓶中加入95%乙醇为
溶剂,加热前还要加几粒__________。
(2)提取过程不可选用明火直接加热,原因是____________________。与常规的萃取相比,采用索氏提取器的优
点是______________________。
36.[化学——选修5:有机化学基础]
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是____________________。
环氧树脂因其具有良好的机械性能、绝缘性能以及与各种材料的粘结性能,已广泛应用于涂料和胶黏剂等领域。
“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏水、温度计、接收管之外,还有______(填标号)。
下面是制备一种新型环氧树脂G的合成路线:
A.直形冷凝管
B.球形冷凝管
C.接收瓶
已知以下信息:
D.烧杯
(4)浓缩液加生石灰的作用是中和________和吸收________。
(5)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸
上凝结,该分离提纯方法的名称是________。
① + ―---―→
(二)选考题:共15分。请考生从2道化学题中任选一题作答。如果多做,则按所做的第一题计分。
②R′OH+ +NaOH―→R′ +NaCl+HO
35.[化学——选修3:物质结构与性质] 2
近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe—Sm—As—F—O组成的化合物。回
③R′ + ――--→
答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为________,其沸点比NH 的________(填“高”或
3
“低”),其判断理由是________________________________________
回答下列问题:
________________________________________________________________________。
(1)A是一种烯烃,化学名称为________,C中官能团的名称为________、________。
(2)Fe成为阳离子时首先失去________轨道电子,Sm的价层电子排布式为 4f66s2,Sm3+价层电子排布式为
(2)由B生成C的反应类型为________。(3)由C生成D的反应方程式为__________________________________________________。
(4)E的结构简式为________。
(5)E的二氯代物有多种同分异构体,请写出其中能同时满足以下条件的芳香化合物的结构简式________、
________。
①能发生银镜反应:②核磁共振氢谱有三组峰,且峰面积比为3∶2∶1。
(6)假设化合物D、F和NaOH恰好完全反应生成1 mol单一聚合度的G,若生成的NaCl和HO的总质量为765
2
g,则G的n值理论上应等于________。