文档内容
A.原子半径:WT
1 2
应未达到平衡,b点的正反应速率大于逆反应速率,故a点的正反应速率大于b点的逆反应速率,C项正确;b
B.a点的反应速率小于c点的反应速率
点时,环戊二烯的浓度减小0.9 mol·L-1,结合生成的二聚体浓度为环戊二烯浓度变化量的,可知二聚体的浓
C.a点的正反应速率大于b点的逆反应速率
度为0.45 mol·L-1,D项正确。(4)结合图示电解原理可知,Fe电极发生氧化反应,为阳极;在阴极上有H 生成,
D.b点时二聚体的浓度为0.45 mol·L-1 2
故电解时的总反应为Fe+2 +H↑或Fe+2C H==Fe(C H) +H↑。结合相关反应可知,电解制备需
(4)环戊二烯可用于制备二茂铁[Fe(C H) ,结构简式为 ],后者广泛应用于航天、化工等领域中。二茂铁的 2 5 6 5 5 2 2
5 5 2
在无水条件下进行,否则水会阻碍中间产物 Na的生成,水电解生成 OH-,OH-会进一步与Fe2+反应生成
电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
Fe(OH) ,从而阻碍二茂铁的生成。
2
28.咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5 ℃,100 ℃以上开始升华),有兴奋大脑神经和利尿等作
用。茶叶中含咖啡因约1%~5%、单宁酸(K 约为10-6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。
a
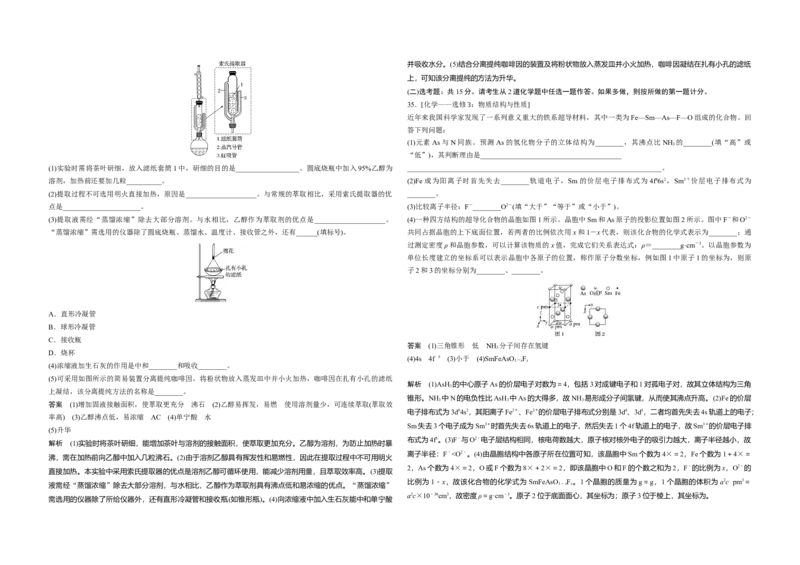
实验室从茶叶中提取咖啡因的流程如图所示。
该电解池的阳极为________,总反应为__________________________。电解制备需要在无水条件下进行,原因
为_____________________________________________________________。 索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管 2上升至球形冷凝管,冷凝后滴入滤纸
套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶
答案 (1)89.3 (2)40% 3.56×104 BD (3)CD (4)Fe电极 Fe+2 +H↑(或Fe+2C H==Fe(C H) 叶末的连续萃取。回答下列问题。
2 5 6 5 5 2
+H↑) 水会阻碍中间物Na的生成;水会电解生成OH-,进一步与Fe2+反应生成Fe(OH)
2 2
解析 (1)根据盖斯定律,由反应①+反应②得反应③,则ΔH =ΔH +ΔH =(100.3-11.0)kJ·mol-1=89.3 kJ·mol
3 1 2并吸收水分。(5)结合分离提纯咖啡因的装置及将粉状物放入蒸发皿并小火加热,咖啡因凝结在扎有小孔的滤纸
上,可知该分离提纯的方法为升华。
(二)选考题:共15分。请考生从2道化学题中任选一题作答。如果多做,则按所做的第一题计分。
35.[化学——选修3:物质结构与性质]
近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe—Sm—As—F—O组成的化合物。回
答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为________,其沸点比NH 的________(填“高”或
3
“低”),其判断理由是________________________________________
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是__________________。圆底烧瓶中加入95%乙醇为 ________________________________________________________________________。
溶剂,加热前还要加几粒__________。 (2)Fe成为阳离子时首先失去________轨道电子,Sm的价层电子排布式为 4f66s2,Sm3+价层电子排布式为
(2)提取过程不可选用明火直接加热,原因是____________________。与常规的萃取相比,采用索氏提取器的优 ________。
点是______________________。 (3)比较离子半径:F-________O2-(填“大于”“等于”或“小于”)。
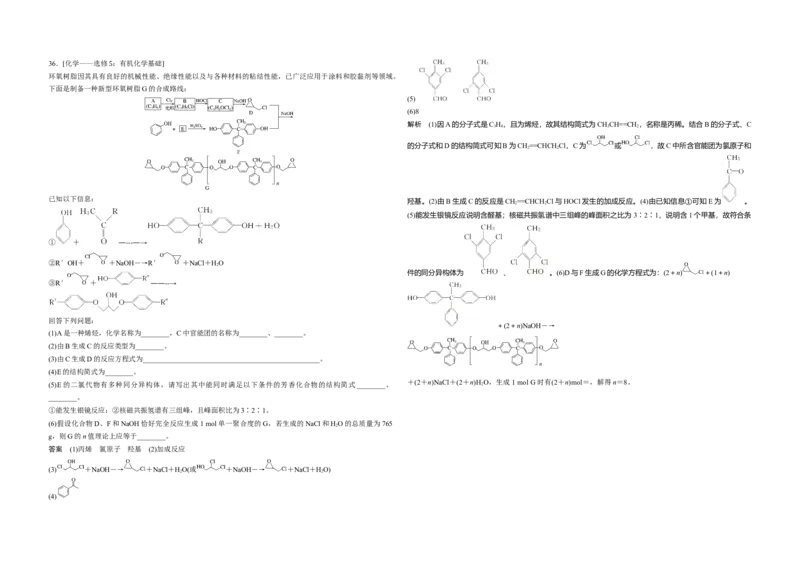
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是____________________。 (4)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-
“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏水、温度计、接收管之外,还有______(填标号)。 共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为________;通
过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=________g·cm-3。以晶胞参数为
单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为,则原
子2和3的坐标分别为________、________。
A.直形冷凝管
B.球形冷凝管
C.接收瓶
答案 (1)三角锥形 低 NH 分子间存在氢键
3
D.烧杯
(4)4s 4f 5 (3)小于 (4)SmFeAsO F
1-x x
(4)浓缩液加生石灰的作用是中和________和吸收________。
(5)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸
解析 (1)AsH 的中心原子As的价层电子对数为=4,包括3对成键电子和1对孤电子对,故其立体结构为三角
3
上凝结,该分离提纯方法的名称是________。
锥形。NH 中N的电负性比AsH 中As的大得多,故NH 易形成分子间氢键,从而使其沸点升高。(2)Fe的价层
3 3 3
答案 (1)增加固液接触面积,使萃取更充分 沸石 (2)乙醇易挥发,易燃 使用溶剂量少,可连续萃取(萃取效
电子排布式为3d64s2,其阳离子Fe2+、Fe3+的价层电子排布式分别是3d6、3d5,二者均首先失去4s轨道上的电子;
率高) (3)乙醇沸点低,易浓缩 AC (4)单宁酸 水
Sm失去3个电子成为Sm3+时首先失去6s轨道上的电子,然后失去1个4f轨道上的电子,故Sm3+的价层电子排
(5)升华
布式为4f5。(3)F-与O2-电子层结构相同,核电荷数越大,原子核对核外电子的吸引力越大,离子半径越小,故
解析 (1)实验时将茶叶研细,能增加茶叶与溶剂的接触面积,使萃取更加充分。乙醇为溶剂,为防止加热时暴
离子半径:F-