文档内容
2022年上海市高考化学试卷
一、选择题(本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.(2分)北京2022年冬奥会上,我国短道速滑队取得了良好成绩。短道速滑所用冰刀
的材料是合金。下列选项正确的是( )
A.该合金熔点比纯铁低 B.该合金硬度比纯铁低
C.该合金含碳量比生铁高 D.该合金延展性比生铁差
2.(2分)雪蜡是冰雪运动的重要材料,主要成分为石蜡。以下关于石蜡的说法正确的是
( )
A.常温下是气态 B.易溶于水
C.是纯净物 D.是石油分馏产物
3.(2分)Na O的电子式为( )
2
A. B.
C. D.
4.(2分)二氧化碳在一定条件下可以转化为乙酸,下列有关二氧化碳性质的说法正确的
是( )
A.为共价化合物 B.为电解质
C.为折线形分子 D.含非极性共价键
5.(2分)苯是不饱和烃,但不能使溴的四氯化碳溶液褪色,是因为( )
A.苯是非极性分子
B.苯溶于四氯化碳
C.苯不能发生取代反应
D.苯中不存在烯烃典型的碳碳双键
6.(2分)下列物质中所有原子均共面的是( )
A.二氯甲烷 B.1,1,2,2﹣四氯乙烷
C.1,2﹣二氯乙烯 D.乙醛
7.(2分)关于CH C≡CCH 的说法错误的是( )
3 3
A.是乙炔同系物
B.和1,3﹣丁二烯互为同分异构体C.可以使酸性高锰酸钾溶液褪色
D.1mol该物质能和3molH 加成
2
8.(2分)常温下,在pH=1的溶液中可以大量共存的是( )
A.Al3+、 、Cl﹣ B.OH﹣、Al3+、Na+
C.Fe2+、K+、S2﹣ D.Fe2+、 、Cl﹣
9.(2分)下列属于原子晶体的是( )
A.CO B.金刚石 C.NaCl D.氦气
2
10.(2分)下列关于硫酸工业的说法正确的是( )
A.在纯氧中煅烧黄铁矿 B.在高压条件下制SO
3
C.用98%浓硫酸吸收SO D.用澄清石灰水吸收尾气
3
11.(2分)下列事实不能说明C的非金属性大于Si的是( )
A.稳定性:CH >SiH
4 4
B.酸性:H CO >H SiO
2 3 2 3
C.熔沸点:CO <SiO
2 2
D.CH 中C为﹣4价,SiH 中Si为+4价
4 4
12.(2分)制备二氧化硫并检验其性质,用铜和浓硫酸在试管中制得二氧化硫,先通到
品红溶液中,然后通到新制氯水中,最后尾气处理,下列说法正确的是( )
A.SO 是氧化产物
2
B.品红溶液褪色体现SO 的漂白性
2
C.新制氯水褪色体现SO 的氧化性
2
D.用饱和亚硫酸钠溶液处理尾气
13.(2分)将Mg加入稀NH Cl溶液中,发生反应Mg+2NH Cl═MgCl +2NH ↑+H ↑,
4 4 2 3 2
下列说法正确的是( )
A.用湿润的蓝色石蕊试纸检验NH
3
B.经过一段时间之后可能生成Mg(OH) 沉淀
2
C.NH 和H 均为还原产物
3 2
D.1molMg充分反应生成22.4L气体(标准状况下)
14.(2分)下列四组物质中,不能用溴水鉴别的是( )
A.SO 和CO B.NaOH和NaCl
2 2
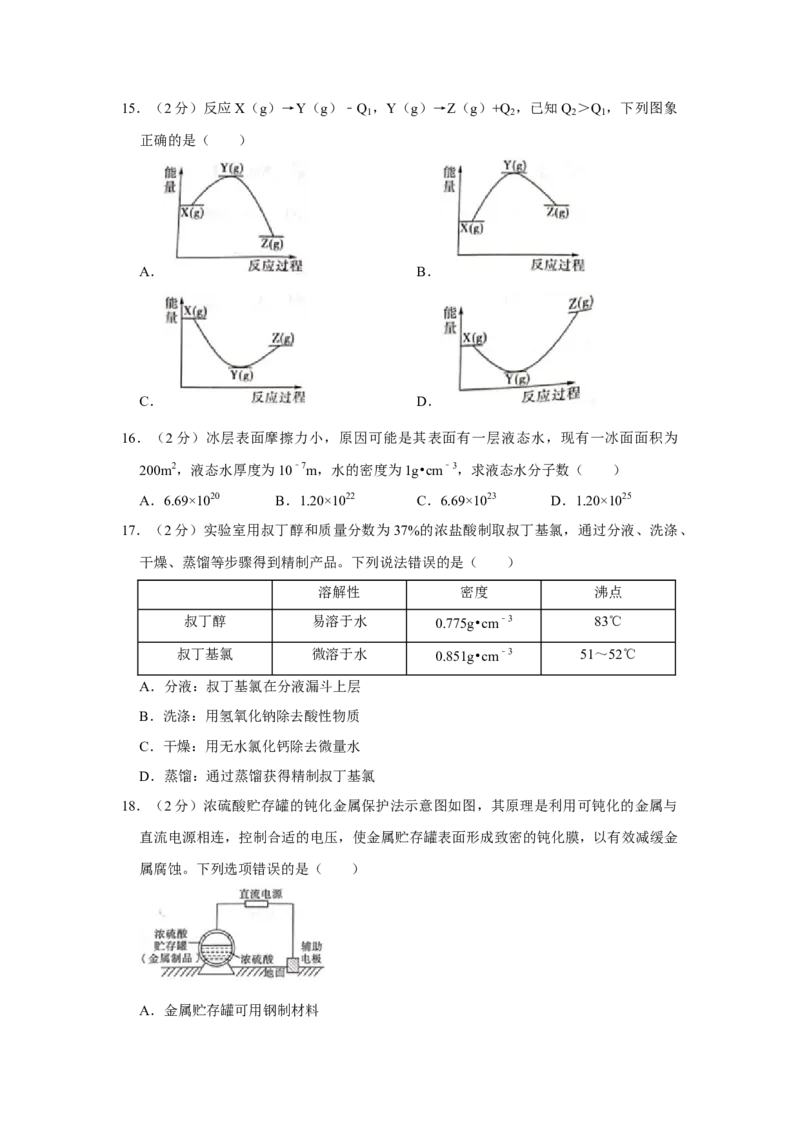
C.乙烷和乙烯 D.正戊烷和正己烷15.(2分)反应X(g)→Y(g)﹣Q ,Y(g)→Z(g)+Q ,已知Q >Q ,下列图象
1 2 2 1
正确的是( )
A. B.
C. D.
16.(2分)冰层表面摩擦力小,原因可能是其表面有一层液态水,现有一冰面面积为
200m2,液态水厚度为10﹣7m,水的密度为1g•cm﹣3,求液态水分子数( )
A.6.69×1020 B.1.20×1022 C.6.69×1023 D.1.20×1025
17.(2分)实验室用叔丁醇和质量分数为37%的浓盐酸制取叔丁基氯,通过分液、洗涤、
干燥、蒸馏等步骤得到精制产品。下列说法错误的是( )
溶解性 密度 沸点
叔丁醇 易溶于水 0.775g•cm﹣3 83℃
叔丁基氯 微溶于水 0.851g•cm﹣3 51~52℃
A.分液:叔丁基氯在分液漏斗上层
B.洗涤:用氢氧化钠除去酸性物质
C.干燥:用无水氯化钙除去微量水
D.蒸馏:通过蒸馏获得精制叔丁基氯
18.(2分)浓硫酸贮存罐的钝化金属保护法示意图如图,其原理是利用可钝化的金属与
直流电源相连,控制合适的电压,使金属贮存罐表面形成致密的钝化膜,以有效减缓金
属腐蚀。下列选项错误的是( )
A.金属贮存罐可用钢制材料B.电子沿导线流入辅助电极
C.贮存浓硫酸的金属罐与电源负极相连
D.电压高到一定程度有可能会加剧腐蚀
19.(2分)向10mL浓度为0.1mol•L﹣1的二元弱酸H A中逐滴加入VmL0.1mol•L﹣1的
2
NaOH溶液。下列离子关系错误的是( )
A.V=5,2[Na+]=[H A]+[HA﹣]+[A2﹣]
2
B.V=10,[H A]+[H+]=[OH﹣]+2[A2﹣]
2
C.V=15,且测得此时溶液pH<7,[Na+]>[A2﹣]>[HA﹣]
D.V=20,[Na+]>2[HA﹣]>2[H A]
2
20.(2分)向体积为1L的容器中充入4molA,发生反应:2A(s) 2B(g)+C(?),
不同温度下的平衡常数与达到平衡时B的物质的量如下: ⇌
温度 T T
1 2
K 4 1
n(B)/mol x y
下列说法正确的是( )
A.容器中气体的平均摩尔质量不变时,该反应达到平衡
B.T 时,若平衡时剩余2molA,则C必为气体
1
C.T 时,当反应达到平衡后,容器内剩余A的物质的量为3mol
2
D.T 时,若容器的体积变为2L,则平衡时n(B)=2ymol
2
二、(本题共15分)
21.(15分)利用Al O 催化氮气合成氨气,并生成CO、H 等燃料气的方程式如下所示:
2 3 2
反应①:Al O (s)+N (g)+3CH (g) 3CO(g)+6H (g)+2AlN(s)
2 3 2 4 2
反应②:2AlN(s)+3H
2
O(g) Al
2
O
3
(s⇌)+2NH
3
(g)
(1)氮原子核外电子排布式为:⇌ 。
(2)比较C、N、O原子的半径大小: 。
(3)反应①的进程如图所示,则p 和p 的大小为: 。
1 2(4)某一2L恒温恒容装置,反应前充入3mol甲烷,10min后,甲烷为1.2mol,求前
10min氮气的反应速率为: 。
(5)写出反应①和反应②的总反应方程式: 。
(6)这个制取氨气的方法和工业制取氨气相比,优点是: 、
。
三、(本题共15分)
22.(15分)铵态氮肥的过度使用会导致水体的富营养化,研究发现,可以用化学方法和
生物方法去除氨氮。现探究去除溶液中氨氮的最适宜条件。
(1)化学方法一般用次氯酸钠氧化。次氯酸钠可以和水中溶解的氨气反应得到无毒无
害物质,其离子方程式为3ClO﹣+2NH ═3Cl﹣+N ↑+3H O。次氯酸钠溶液中含氯的微
3 2 2
粒有 。
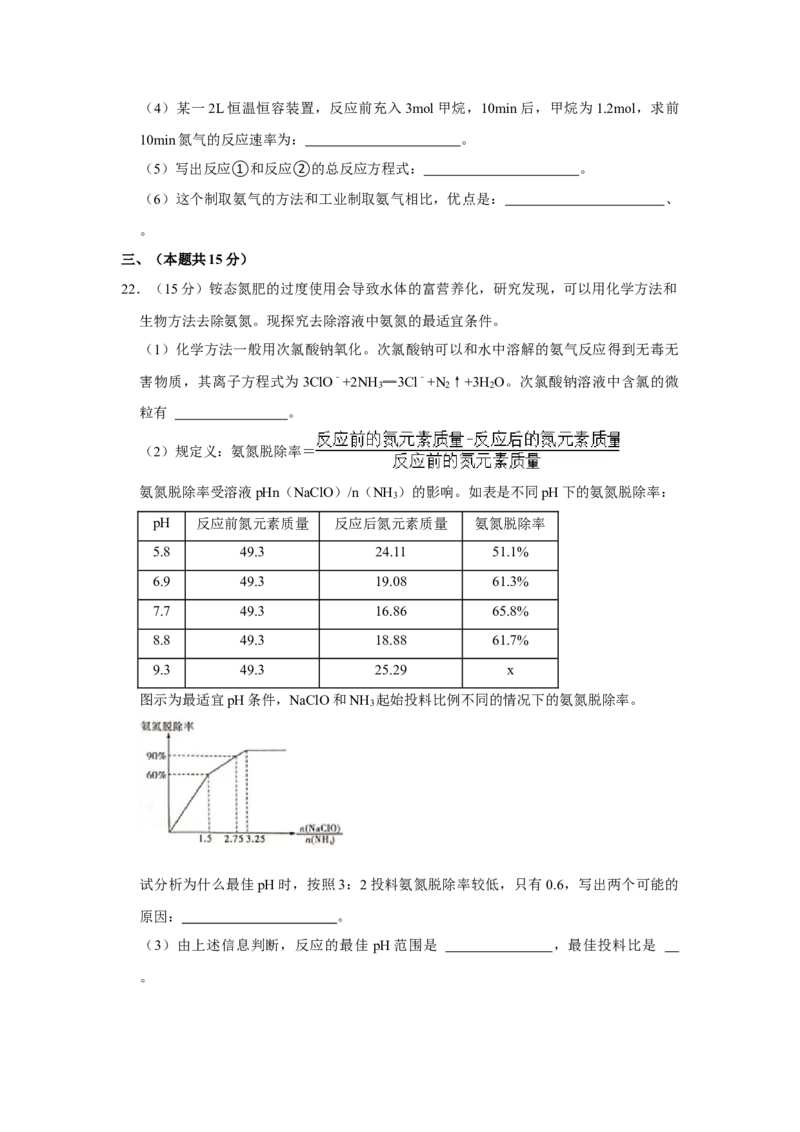
(2)规定义:氨氮脱除率=
氨氮脱除率受溶液pHn(NaClO)/n(NH )的影响。如表是不同pH下的氨氮脱除率:
3
pH 反应前氮元素质量 反应后氮元素质量 氨氮脱除率
5.8 49.3 24.11 51.1%
6.9 49.3 19.08 61.3%
7.7 49.3 16.86 65.8%
8.8 49.3 18.88 61.7%
9.3 49.3 25.29 x
图示为最适宜pH条件,NaClO和NH 起始投料比例不同的情况下的氨氮脱除率。
3
试分析为什么最佳pH时,按照3:2投料氨氮脱除率较低,只有0.6,写出两个可能的
原因: 。
(3)由上述信息判断,反应的最佳 pH范围是 ,最佳投料比是
。生物方法是利用硝化细菌,将土壤中的 转化为 后,土壤中的O 进一步将 氧
2
化为 。之后,在氧气较少的环境下, 又可以在反硝化细菌的作用下与 反应,
使氮以N 形式放出。
2
(4)氧气与 反应时,反应物 与O 的物质的量之比为 。写出 与
2
作用生成N 的离子方程式: 。
2
(5)在VLamol•L﹣1的氨水中滴加等体积0.01mol•L﹣1的盐酸,使pH=7,则产物中一
水合氨浓度为 。
四、(本题共15分)
23.(15分)惕各酸及其酯类在香精配方中有着广泛的用途,已知惕各酸香叶醇酯的结构
如图所示:
其合成方法如图所示:
C H NO(A) C H O (B)→惕各酸
5 9 5 10 3
已知:RCHO
(1)反应①为 反应,有机物B中的官能团名称为 。
(2)反应②③的反应试剂与条件为 。
(3)写出分子式为C H O ,满足下列条件的结构简式: 。
5 10 3
①能水解且能发生银镜反应②不与Na反应
③有3种化学环境不同的氢原子
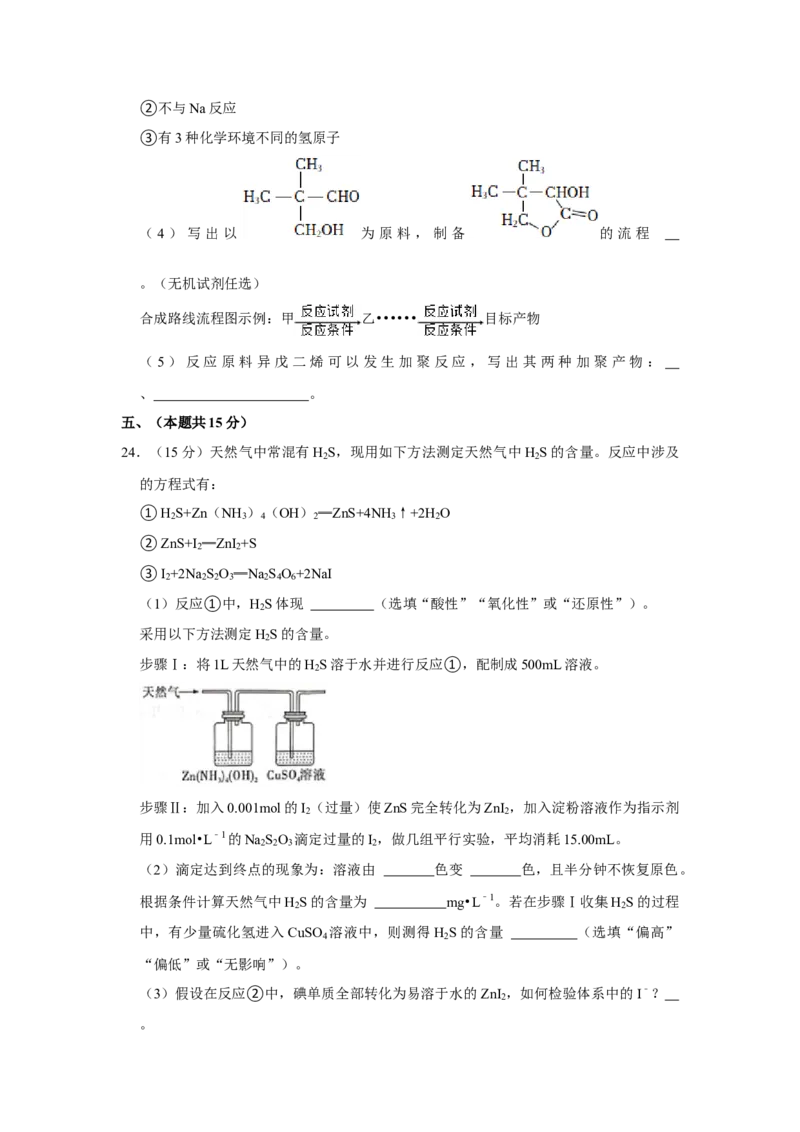
(4)写出以 为原料,制备 的流程
。(无机试剂任选)
合成路线流程图示例:甲 乙•••••• 目标产物
(5)反应原料异戊二烯可以发生加聚反应,写出其两种加聚产物:
、 。
五、(本题共15分)
24.(15分)天然气中常混有H S,现用如下方法测定天然气中H S的含量。反应中涉及
2 2
的方程式有:
①H S+Zn(NH ) (OH) ═ZnS+4NH ↑+2H O
2 3 4 2 3 2
②ZnS+I ═ZnI +S
2 2
③I +2Na S O ═Na S O +2NaI
2 2 2 3 2 4 6
(1)反应①中,H S体现 (选填“酸性”“氧化性”或“还原性”)。
2
采用以下方法测定H S的含量。
2
步骤Ⅰ:将1L天然气中的H S溶于水并进行反应①,配制成500mL溶液。
2
步骤Ⅱ:加入0.001mol的I (过量)使ZnS完全转化为ZnI ,加入淀粉溶液作为指示剂
2 2
用0.1mol•L﹣1的Na S O 滴定过量的I ,做几组平行实验,平均消耗15.00mL。
2 2 3 2
(2)滴定达到终点的现象为:溶液由 色变 色,且半分钟不恢复原色。
根据条件计算天然气中H S的含量为 mg•L﹣1。若在步骤Ⅰ收集H S的过程
2 2
中,有少量硫化氢进入CuSO 溶液中,则测得H S的含量 (选填“偏高”
4 2
“偏低”或“无影响”)。
(3)假设在反应②中,碘单质全部转化为易溶于水的ZnI ,如何检验体系中的I﹣?
2
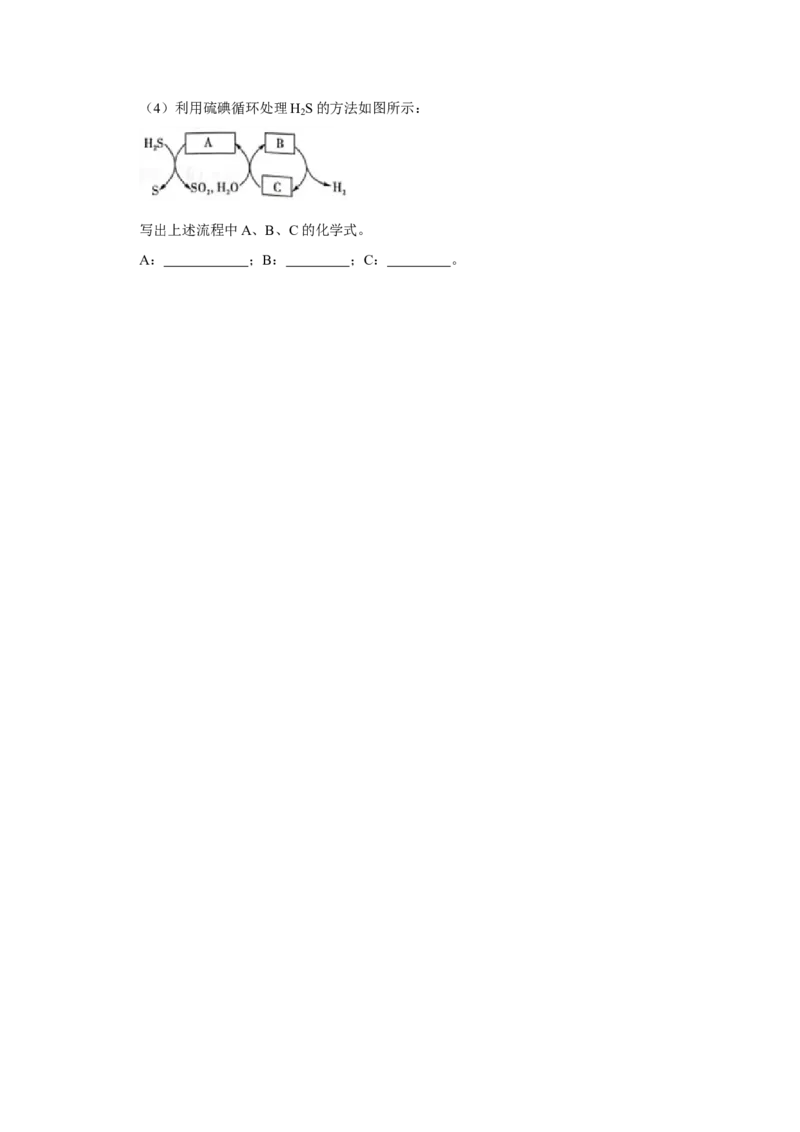
。(4)利用硫碘循环处理H S的方法如图所示:
2
写出上述流程中A、B、C的化学式。
A: ;B: ;C: 。