文档内容
绵阳南山中学 2024 年春季高 2022 级期末热身化学试题
命题人:宗靖浩 审题人:杜红帅
本试卷分为试题卷和答题卡两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)
组成,共6页;答题卡共2页。满分100分,考试时间75分钟。
注意事项:
1. 答题前,考生务必将自己的学校、班级、姓名用0.5毫米黑色墨水签字笔填写清楚,
同时用2B铅笔将考号准确填涂在“考号”栏目内。
2. 选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,如需改动,用橡皮擦擦干
净后再选涂其它答案;非选择题用0.5毫米黑色墨水签字笔书写在答题卡的对应框内,超出
答题区域书写的答案无效;在草稿纸、试题卷上答题无效。
3. 考试结束后将答题卡收回。
相对原子质量:H1 C12 N14 O16 Si28 Mn55
第Ⅰ卷(选择题,共 42 分)
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项最符合题意)
1.化学与生活、生产、科技、环境等密切相关。下列说法正确的是
A.乙二醇的水溶液凝固点很高,可作汽车发动机的抗冻剂
B.长征四号丙运载火箭使用了属于离子晶体的氮化硅高温陶瓷材料
C.医用酒精可用于杀菌消毒是因为乙醇与细菌蛋白质发生氧化反应
D.酚醛树脂主要用于绝缘、隔热、阻燃、隔音材料和复合材料
2.下列化学用语使用正确的是
A.K的结构示意图: B.基态Mn原子的电子排布式:[Ar]3d54s2
C.基态Si原子的价层电子轨道表示式: D.N H 的电子式:
2 4
3.下列各项说法正确的是
A.凡是能发生银镜反应的物质一定是醛
B.人造脂肪中的反式脂肪酸是引发动脉硬化的因素之一
C.乙二醇和丙三醇具有相同的官能团互为同系物
D.苯酚不慎沾到皮肤上,用氢氧化钠溶液擦拭
4.设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.常温常压下,60g二氧化硅中Si—O键数为2N
A
B.标准状况下,2.24LC H O含有的C—H键数为0.6N
3 6 A
第1页,共6页C.1mol乙酸与足量乙醇发生酯化反应,生成的乙酸乙酯分子数为N
A
D.0.1molC H 和C H O的混合气体完全燃烧,消耗的O 分子数为0.3N
2 4 2 6 2 A
5.下列各组物质形成的晶体中,化学键和晶体类型完全相同的是
A.CS 和SiO B.C 和S C.HClO和C H D.H O 和Na O
2 2 60 8 2 4 2 2 2 2
6.下列关于晶体性质描述正确的是
A.SiO 、NaCl、干冰的熔沸点依次减小
2
B.CO 、H O等分子晶体均为分子密堆积,一个分子周围有12个紧邻的分子
2 2
C.自然界中的玻璃、炭黑、蜡状的白磷(P )等属于非晶体
4
D.离子晶体Cu(NH ) SO ·5H O中微粒间的相互作用力仅含有离子键和共价键
3 4 4 2
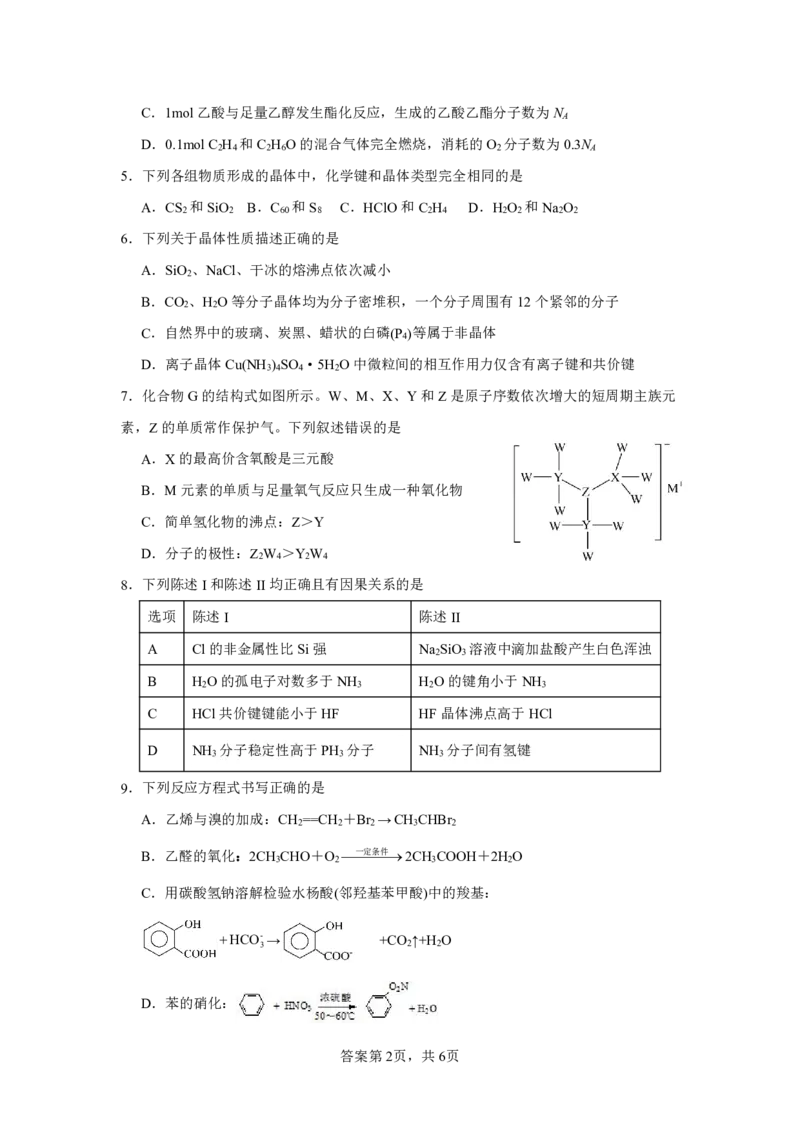
7.化合物G的结构式如图所示。W、M、X、Y和Z是原子序数依次增大的短周期主族元
素,Z的单质常作保护气。下列叙述错误的是
A.X的最高价含氧酸是三元酸
B.M元素的单质与足量氧气反应只生成一种氧化物
C.简单氢化物的沸点:Z>Y
D.分子的极性:Z W >Y W
2 4 2 4
8.下列陈述I和陈述II均正确且有因果关系的是
选项 陈述I 陈述II
A Cl的非金属性比Si强 Na SiO 溶液中滴加盐酸产生白色浑浊
2 3
B H O的孤电子对数多于NH H O的键角小于NH
2 3 2 3
C HCl共价键键能小于HF HF晶体沸点高于HCl
D NH 分子稳定性高于PH 分子 NH 分子间有氢键
3 3 3
9.下列反应方程式书写正确的是
A.乙烯与溴的加成:CH ==CH +Br →CH CHBr
2 2 2 3 2
B.乙醛的氧化:2CH CHO+O 一定条件2CH COOH+2H O
3 2 3 2
C.用碳酸氢钠溶解检验水杨酸(邻羟基苯甲酸)中的羧基:
+HCO-→ +CO ↑+H O
3 2 2
D.苯的硝化:
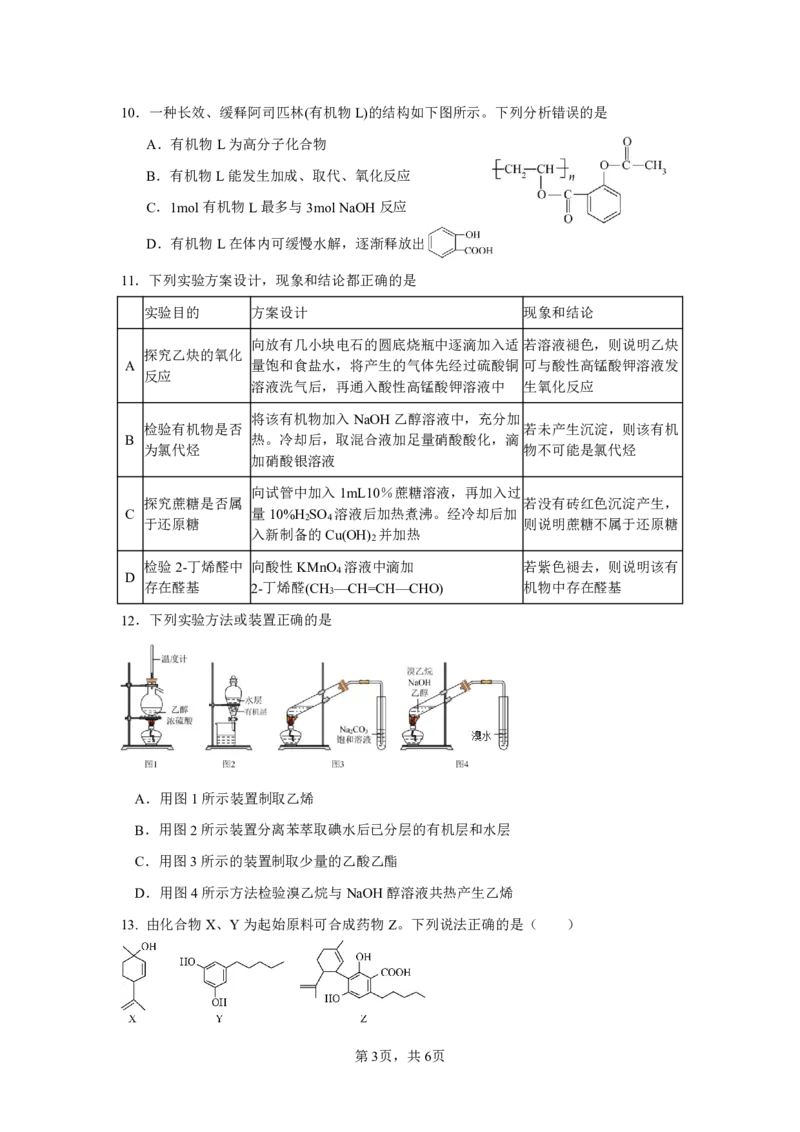
答案第2页,共6页10.一种长效、缓释阿司匹林(有机物L)的结构如下图所示。下列分析错误的是
A.有机物L为高分子化合物
B.有机物L能发生加成、取代、氧化反应
C.1mol有机物L最多与3molNaOH反应
D.有机物L在体内可缓慢水解,逐渐释放出
11.下列实验方案设计,现象和结论都正确的是
实验目的 方案设计 现象和结论
向放有几小块电石的圆底烧瓶中逐滴加入适 若溶液褪色,则说明乙炔
探究乙炔的氧化
A 量饱和食盐水,将产生的气体先经过硫酸铜 可与酸性高锰酸钾溶液发
反应
溶液洗气后,再通入酸性高锰酸钾溶液中 生氧化反应
将该有机物加入NaOH乙醇溶液中,充分加
检验有机物是否 若未产生沉淀,则该有机
B 热。冷却后,取混合液加足量硝酸酸化,滴
为氯代烃 物不可能是氯代烃
加硝酸银溶液
向试管中加入1mL10%蔗糖溶液,再加入过
探究蔗糖是否属 若没有砖红色沉淀产生,
C 量10%H SO 溶液后加热煮沸。经冷却后加
于还原糖 2 4 则说明蔗糖不属于还原糖
入新制备的Cu(OH) 并加热
2
检验2-丁烯醛中 向酸性KMnO 溶液中滴加 若紫色褪去,则说明该有
4
D
存在醛基 2-丁烯醛(CH —CH=CH—CHO) 机物中存在醛基
3
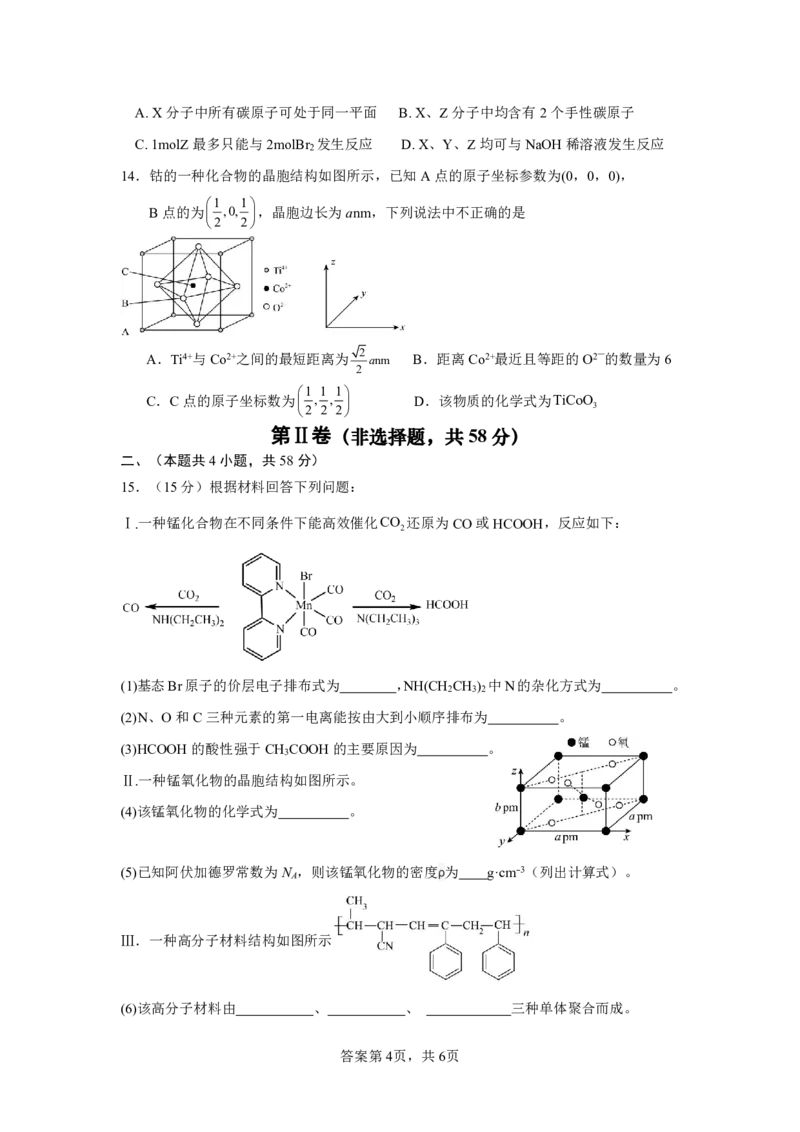
12.下列实验方法或装置正确的是
A.用图1所示装置制取乙烯
B.用图2所示装置分离苯萃取碘水后已分层的有机层和水层
C.用图3所示的装置制取少量的乙酸乙酯
D.用图4所示方法检验溴乙烷与NaOH醇溶液共热产生乙烯
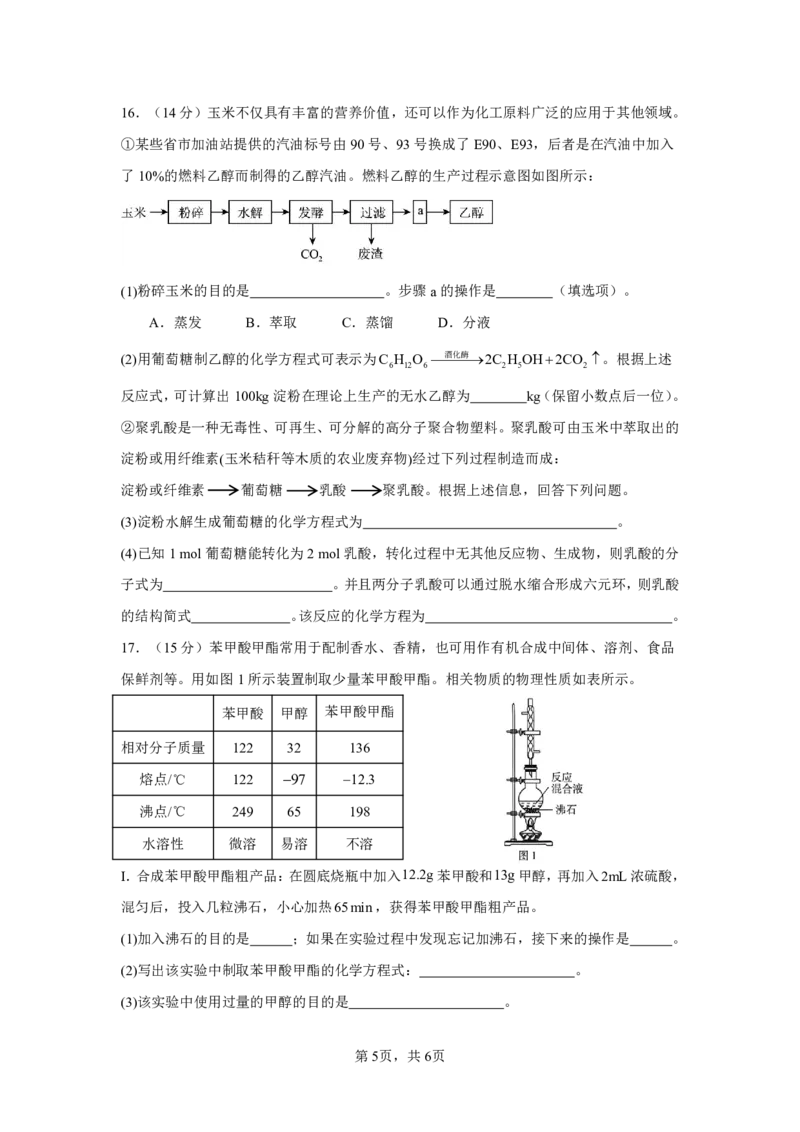
13. 由化合物X、Y为起始原料可合成药物Z。下列说法正确的是( )
第3页,共6页A.X分子中所有碳原子可处于同一平面 B.X、Z分子中均含有2个手性碳原子
C.1molZ最多只能与2molBr 发生反应 D.X、Y、Z均可与NaOH稀溶液发生反应
2
14.钴的一种化合物的晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),
1 1
B点的为 ,0, ,晶胞边长为anm,下列说法中不正确的是
2 2
A.Ti4+与Co2+之间的最短距离为 2 anm B.距离Co2+最近且等距的O2—的数量为6
2
1 1 1
C.C点的原子坐标数为 , , D.该物质的化学式为TiCoO
2 2 2 3
第Ⅱ卷
(非选择题,共 58 分)
二、(本题共4小题,共58分)
15.(15分)根据材料回答下列问题:
Ⅰ.一种锰化合物在不同条件下能高效催化CO 还原为CO或HCOOH,反应如下:
2
(1)基态Br原子的价层电子排布式为 ,NH(CH CH ) 中N的杂化方式为 。
2 3 2
(2)N、O和C三种元素的第一电离能按由大到小顺序排布为 。
(3)HCOOH的酸性强于CH COOH的主要原因为 。
3
Ⅱ.一种锰氧化物的晶胞结构如图所示。
(4)该锰氧化物的化学式为 。
(5)已知阿伏加德罗常数为N
A
,则该锰氧化物的密度ρ为 g·cm-3(列出计算式)。
Ⅲ.一种高分子材料结构如图所示
(6)该高分子材料由 、 、 三种单体聚合而成。
答案第4页,共6页16.(14分)玉米不仅具有丰富的营养价值,还可以作为化工原料广泛的应用于其他领域。
①某些省市加油站提供的汽油标号由90号、93号换成了E90、E93,后者是在汽油中加入
了10%的燃料乙醇而制得的乙醇汽油。燃料乙醇的生产过程示意图如图所示:
(1)粉碎玉米的目的是 。步骤a的操作是 (填选项)。
A.蒸发 B.萃取 C.蒸馏 D.分液
(2)用葡萄糖制乙醇的化学方程式可表示为C H O 酒化酶2C H OH2CO 。根据上述
6 12 6 2 5 2
反应式,可计算出100kg淀粉在理论上生产的无水乙醇为 kg(保留小数点后一位)。
②聚乳酸是一种无毒性、可再生、可分解的高分子聚合物塑料。聚乳酸可由玉米中萃取出的
淀粉或用纤维素(玉米秸秆等木质的农业废弃物)经过下列过程制造而成:
淀粉或纤维素 葡萄糖 乳酸 聚乳酸。根据上述信息,回答下列问题。
(3)淀粉水解生成葡萄糖的化学方程式为 。
(4)已知1mol葡萄糖能转化为2mol乳酸,转化过程中无其他反应物、生成物,则乳酸的分
子式为 。并且两分子乳酸可以通过脱水缩合形成六元环,则乳酸
的结构简式 。该反应的化学方程为 。
17.(15分)苯甲酸甲酯常用于配制香水、香精,也可用作有机合成中间体、溶剂、食品
保鲜剂等。用如图1所示装置制取少量苯甲酸甲酯。相关物质的物理性质如表所示。
苯甲酸 甲醇 苯甲酸甲酯
相对分子质量 122 32 136
熔点/℃ 122 97 12.3
沸点/℃ 249 65 198
水溶性 微溶 易溶 不溶
I.合成苯甲酸甲酯粗产品:在圆底烧瓶中加入12.2g苯甲酸和13g甲醇,再加入2mL浓硫酸,
混匀后,投入几粒沸石,小心加热65min,获得苯甲酸甲酯粗产品。
(1)加入沸石的目的是 ;如果在实验过程中发现忘记加沸石,接下来的操作是 。
(2)写出该实验中制取苯甲酸甲酯的化学方程式: 。
(3)该实验中使用过量的甲醇的目的是 。
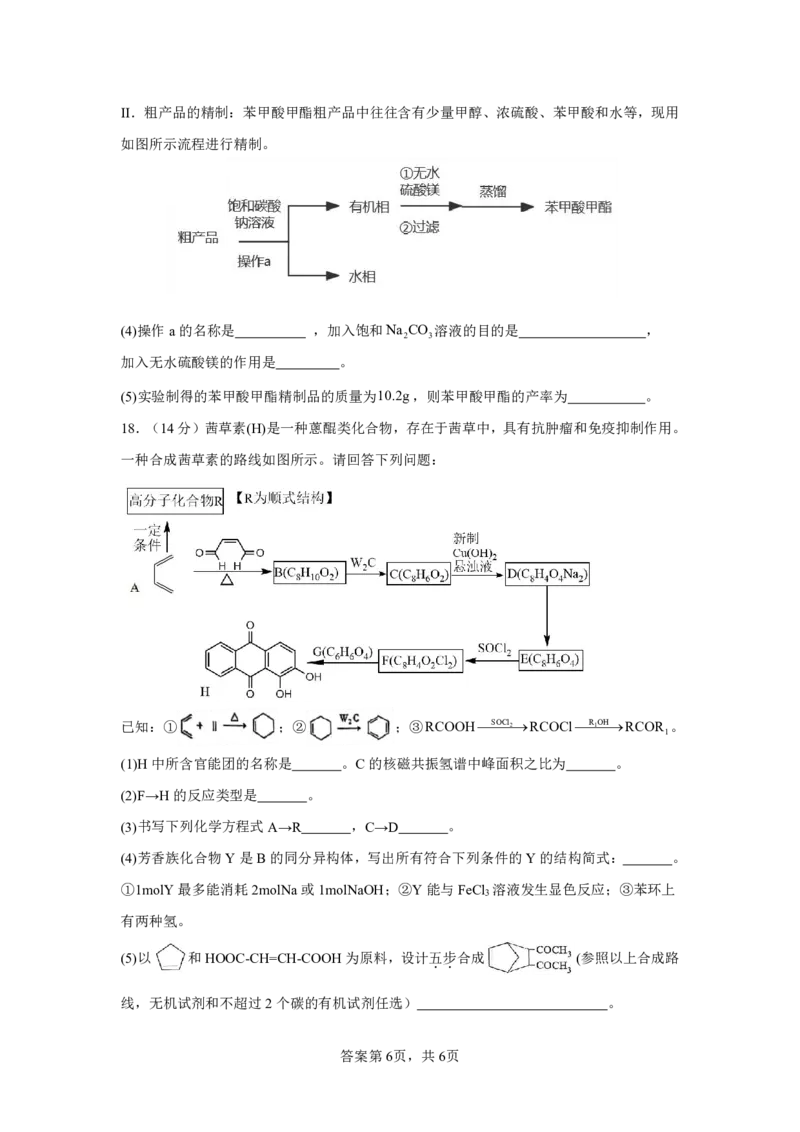
第5页,共6页II.粗产品的精制:苯甲酸甲酯粗产品中往往含有少量甲醇、浓硫酸、苯甲酸和水等,现用
如图所示流程进行精制。
(4)操作a的名称是 ,加入饱和Na CO 溶液的目的是 ,
2 3
加入无水硫酸镁的作用是 。
(5)实验制得的苯甲酸甲酯精制品的质量为10.2g,则苯甲酸甲酯的产率为 。
18.(14分)茜草素(H)是一种蔥醌类化合物,存在于茜草中,具有抗肿瘤和免疫抑制作用。
一种合成茜草素的路线如图所示。请回答下列问题:
已知:① ;② ;③RCOOHSOCl2RCOClR1OHRCOR 。
1
(1)H中所含官能团的名称是 。C的核磁共振氢谱中峰面积之比为 。
(2)F→H的反应类型是 。
(3)书写下列化学方程式A→R ,C→D 。
(4)芳香族化合物Y是B的同分异构体,写出所有符合下列条件的Y的结构简式: 。
①1molY最多能消耗2molNa或1molNaOH;②Y能与FeCl 溶液发生显色反应;③苯环上
3
有两种氢。
(5)以 和HOOC-CH=CH-COOH为原料,设计五
.
步
.
合成 (参照以上合成路
线,无机试剂和不超过2个碳的有机试剂任选) 。
答案第6页,共6页