文档内容
大兴区 2020—2021 学年度第一学期期末检测试卷
初 三 化 学
2020.1
考生须知
1.本试卷共8页,共两部分,39道小题,满分70分。考试时间:70 分钟。
2.在试卷和答题卡上准确填写学校、班级、姓名、考号。
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.考试结束,将本试卷、答题卡和草稿纸一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27
第一部分 选择题(共25分)
每小题1分。在每小题列出的四个选项中,选出符合题目要求的一项。
1. 下列变化中,属于化学变化的是
A. 石蜡熔化 B. 河水结冰 C. 岩石粉碎 D. 食物腐败
2. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
3. 根据“原子量”递增的顺序,绘制了第一张元素周期表的科学家是
A. 阿伏加德罗 B. 拉瓦锡
C. 门捷列夫 D. 道尔顿
4. 将厨房中的下列物质放入足量水中,充分搅拌,不能形成溶液的是
A. 面粉 B. 味精 C. 白糖 D. 食盐
5. 我国最近又启动了“酱油加铁”工程。这里的铁是指
A. 分子 B. 原于 C. 单质 D. 元素
6. 下列有关酒精灯的使用方法中,正确的是A. B. C. D.
7. 下列物质在氧气中燃烧,火星四射、生成黑色固体的是
A. 铁丝 B. 氢气 C. 蜡烛 D. 红磷
8. 下列图标中,表示“禁止烟火”的是
A. B. C. D.
9. 下列元素中,属于非金属元素的是
A. Cu B. Fe C. Zn D. C
10. 决定元素种类的是
A. 中子数 B. 质子数 C. 核外电子数 D. 最外层电子数
11. 下列物质属于纯净物的是
A. 加碘食盐 B. 泥水 C. 空气 D. 高锰酸钾
12. 下列不属于二氧化碳用途的是
A. 用作制冷剂 B. 用作气体肥料
C. 用作燃料 D. 生产碳酸饮料
13. 吸烟有害健康,烟气中的一种有毒气体是( )
A. N B. CO C. O D. CO
2 2 2
14. 下列化学符号中,表示2个氢分子的是
A. H B. 2H C. 2H D. 2H+
2 2
15. 下列物质中,属于氧化物的是( )
A. NaCl B. MnO C. NaOH D. H SO
2 2 4
16. 区别空气、氧气、二氧化碳三瓶气体,最好且简便的方法是( )
A. 用带火星的木条
B. 用澄清石灰水
C. 用紫色石蕊溶液
D. 用燃着的木条
的
17. 下列物质由分子构成 是A. 金刚石 B. 二氧化碳 C. 氯化钠 D. 铁
18. 自来水厂常用二氧化氯(ClO )杀菌消毒,其中氯元素的化合价为
2
A. +2 B. +4 C. -2 D. -4
19. 下列物质的用途中,利用其物理性质的是
A. 氧气用于炼钢 B. 氮气用作保护气
C. 氧化钙用作干燥剂 D. 氢气用于填充探空气球
20. 如图摘自元素周期表,据此判断下列叙述不正确 的是
A. 碳原子的质子数为6
B. 氮原子的核外电子数为14
C. 氧的相对原子质量为16.00
D. 碳、氮 、氧三种原子的原子序数依次递增
21. 下列清洗方法是利用乳化功能的是( )
A. 用汽油除去衣服上的油污 B. 用水洗去盘子上的水果渣
C. 用醋洗去水壶中的水垢 D. 用洗洁精清洗餐具上的油污
22. 氨催化氧化是制硝酸的主要反应之一、该反应前后分子种类变化的微观示意图如下。下列说法不正确
的是
A. 甲中氮、氢原子个数比为1:3 B. 乙的相对分子质量为32
C. 两种生成物的分子个数比为1:1 D. 丙中氮、氧元素的质量比为7:8
23. 40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。①中溶液的质
量为A. 30 g B. 100 g C. 130 g D. 140 g
24. 40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。形成的溶液为
不饱和溶液的是
A. ① B. ② C. ③ D. ①②
25. 40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。将②中的溶液
升温至70℃,下列说法不正确的是
A. 溶液中溶质质量增加 B. 溶液中溶质与溶剂的质量比为2:5
C. 溶液的溶质质量分数不变 D. 若再加入5 g KCl固体会完全溶解第二部分 非选择题(共45分)
39题3分,其余每空1分。
〖生活现象解释〗
26. 自然界中的氧循环如图所示。
(1)图示物质中含有氧分子的是_____(填序号)。
A O B H O C CO
2 2 2
(2)自然界中产生氧气的主要途径为_____。
27. 水是生命之源。
(1)电解水可制得氢气。该反应的化学方程式为_____。
(2)生活中常用来区分硬水和软水的物质是_____。
(3)请任举1例生活中节约用水的具体做法:_____。
28. 化学与生活息息相关。
(1)影视舞台上经常见到云雾缭绕,使人如入仙境的景象。产生这种景象可用的物质是_____。
(2)发生森林火灾时,消防员开辟防火隔离带的主要目的是_____。
(3)湿衣服在烈日下比在阴凉处干得快,请用微粒的观点解释其原因:_____。
29. 生产生活离不开能源。
(1)目前使用的燃料大多来自化石燃料,如煤、_____、天然气等。
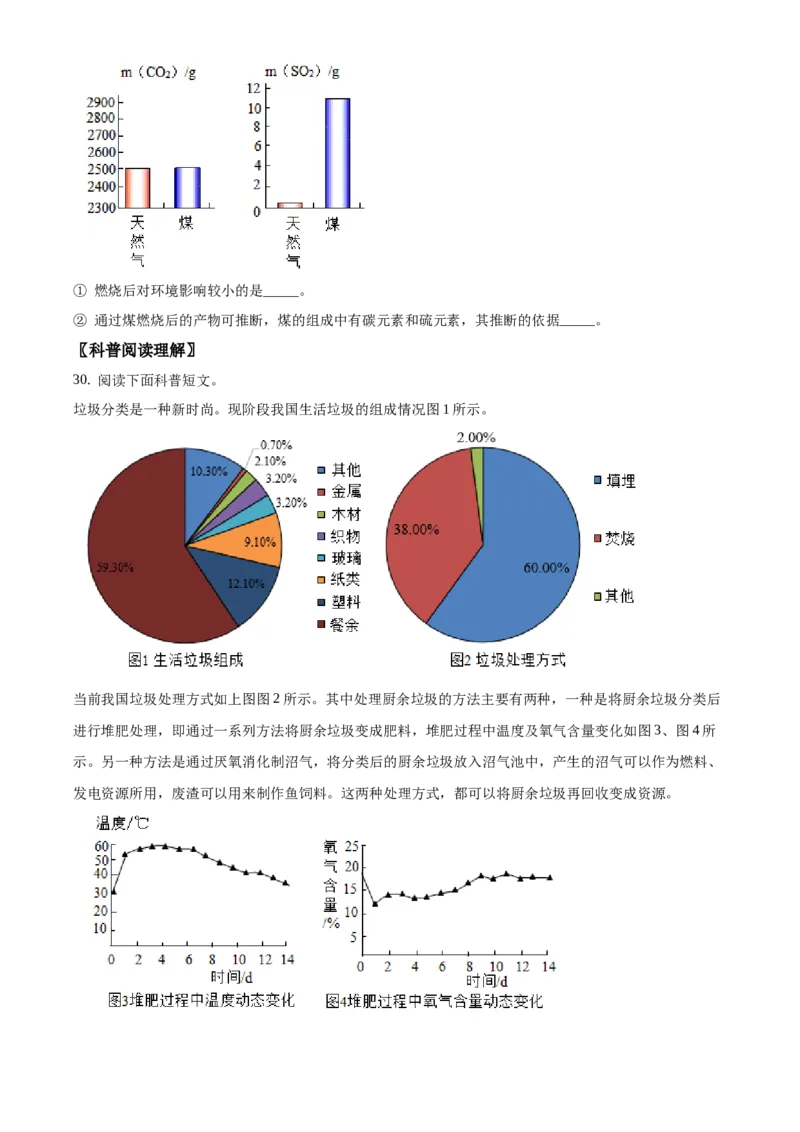
(2)充分燃烧1 kg天然气和煤产生的CO 和SO 气体的质量如图所示。
2 2① 燃烧后对环境影响较小的是_____。
② 通过煤燃烧后的产物可推断,煤的组成中有碳元素和硫元素,其推断的依据_____。
〖科普阅读理解〗
30. 阅读下面科普短文。
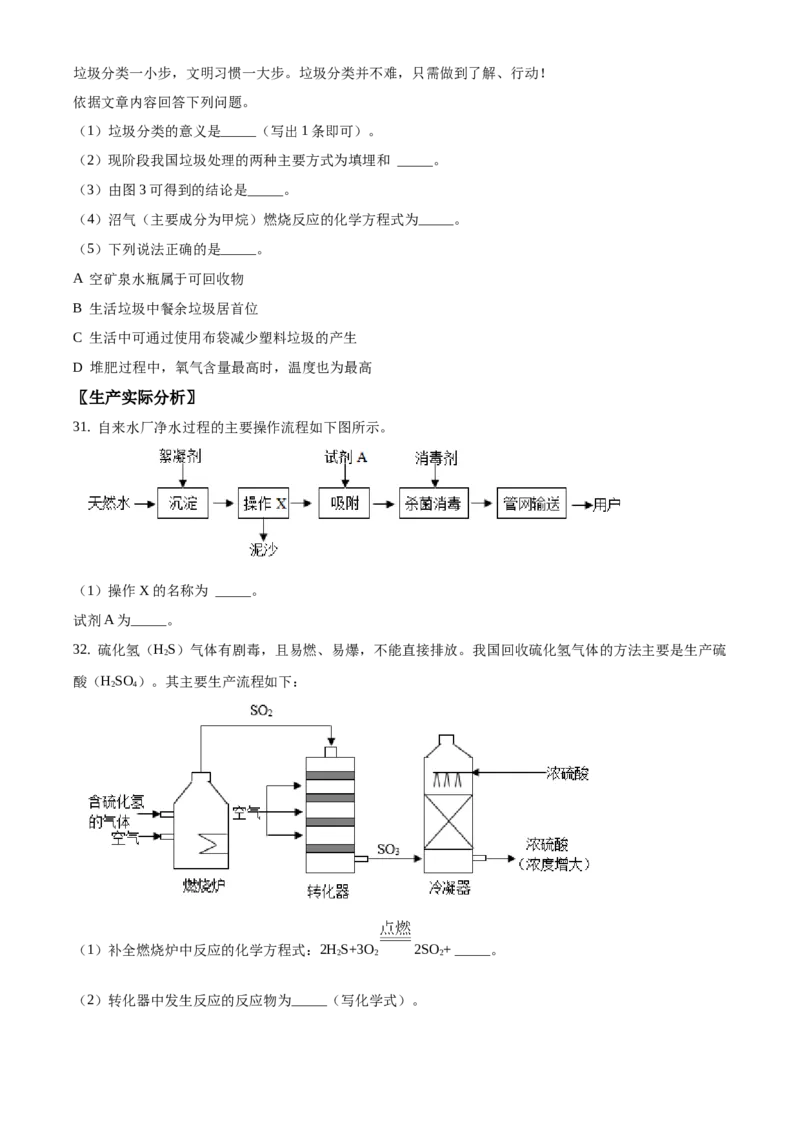
垃圾分类是一种新时尚。现阶段我国生活垃圾的组成情况图1所示。
当前我国垃圾处理方式如上图图2所示。其中处理厨余垃圾的方法主要有两种,一种是将厨余垃圾分类后
进行堆肥处理,即通过一系列方法将厨余垃圾变成肥料,堆肥过程中温度及氧气含量变化如图3、图4所
示。另一种方法是通过厌氧消化制沼气,将分类后的厨余垃圾放入沼气池中,产生的沼气可以作为燃料、
发电资源所用,废渣可以用来制作鱼饲料。这两种处理方式,都可以将厨余垃圾再回收变成资源。垃圾分类一小步,文明习惯一大步。垃圾分类并不难,只需做到了解、行动!
依据文章内容回答下列问题。
(1)垃圾分类的意义是_____(写出1条即可)。
(2)现阶段我国垃圾处理的两种主要方式为填埋和 _____。
(3)由图3可得到的结论是_____。
(4)沼气(主要成分为甲烷)燃烧反应的化学方程式为_____。
(5)下列说法正确的是_____。
A 空矿泉水瓶属于可回收物
B 生活垃圾中餐余垃圾居首位
C 生活中可通过使用布袋减少塑料垃圾的产生
D 堆肥过程中,氧气含量最高时,温度也为最高
〖生产实际分析〗
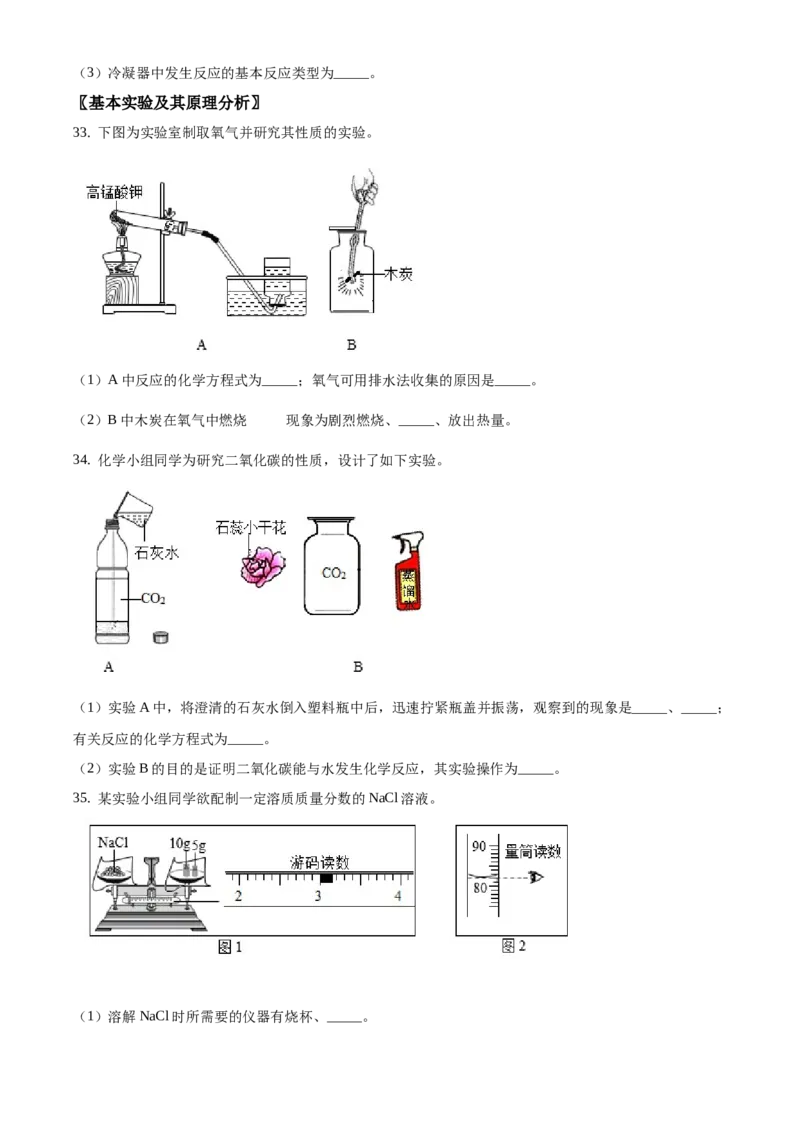
31. 自来水厂净水过程的主要操作流程如下图所示。
(1)操作X的名称为 _____。
试剂A为_____。
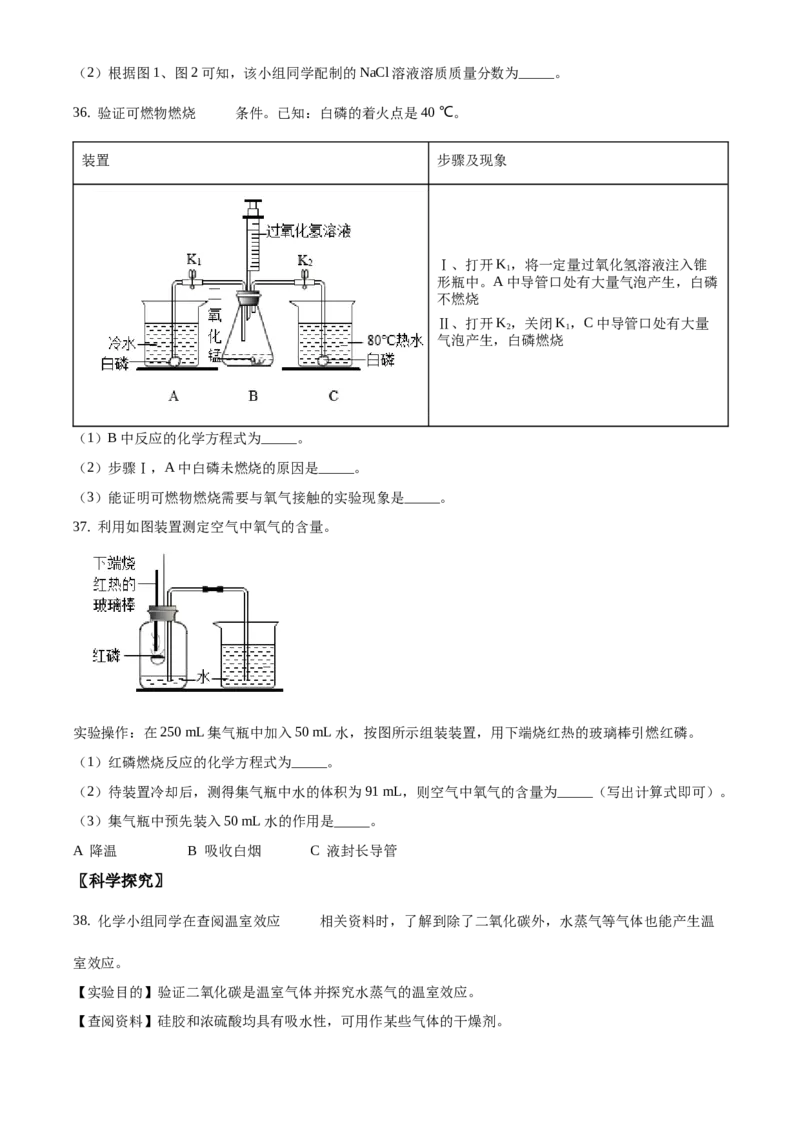
32. 硫化氢(HS)气体有剧毒,且易燃、易爆,不能直接排放。我国回收硫化氢气体的方法主要是生产硫
2
酸(HSO )。其主要生产流程如下:
2 4
(1)补全燃烧炉中反应的化学方程式:2HS+3O 2SO + _____。
2 2 2
(2)转化器中发生反应的反应物为_____(写化学式)。(3)冷凝器中发生反应的基本反应类型为_____。
〖基本实验及其原理分析〗
33. 下图为实验室制取氧气并研究其性质的实验。
(1)A中反应的化学方程式为_____;氧气可用排水法收集的原因是_____。
的
(2)B中木炭在氧气中燃烧 现象为剧烈燃烧、_____、放出热量。
34. 化学小组同学为研究二氧化碳的性质,设计了如下实验。
(1)实验A中,将澄清的石灰水倒入塑料瓶中后,迅速拧紧瓶盖并振荡,观察到的现象是_____、_____;
有关反应的化学方程式为_____。
(2)实验B的目的是证明二氧化碳能与水发生化学反应,其实验操作为_____。
35. 某实验小组同学欲配制一定溶质质量分数的NaCl溶液。
(1)溶解NaCl时所需要的仪器有烧杯、_____。(2)根据图1、图2可知,该小组同学配制的NaCl溶液溶质质量分数为_____。
的
36. 验证可燃物燃烧 条件。已知:白磷的着火点是40℃。
装置 步骤及现象
Ⅰ、打开K,将一定量过氧化氢溶液注入锥
1
形瓶中。A中导管口处有大量气泡产生,白磷
不燃烧
Ⅱ、打开K,关闭K,C中导管口处有大量
2 1
气泡产生,白磷燃烧
(1)B中反应的化学方程式为_____。
(2)步骤Ⅰ,A中白磷未燃烧的原因是_____。
(3)能证明可燃物燃烧需要与氧气接触的实验现象是_____。
37. 利用如图装置测定空气中氧气的含量。
实验操作:在250 mL集气瓶中加入50 mL水,按图所示组装装置,用下端烧红热的玻璃棒引燃红磷。
(1)红磷燃烧反应的化学方程式为_____。
(2)待装置冷却后,测得集气瓶中水的体积为91 mL,则空气中氧气的含量为_____(写出计算式即可)。
(3)集气瓶中预先装入50 mL水的作用是_____。
A 降温 B 吸收白烟 C 液封长导管
〖科学探究〗
的
38. 化学小组同学在查阅温室效应 相关资料时,了解到除了二氧化碳外,水蒸气等气体也能产生温
室效应。
【实验目的】验证二氧化碳是温室气体并探究水蒸气的温室效应。
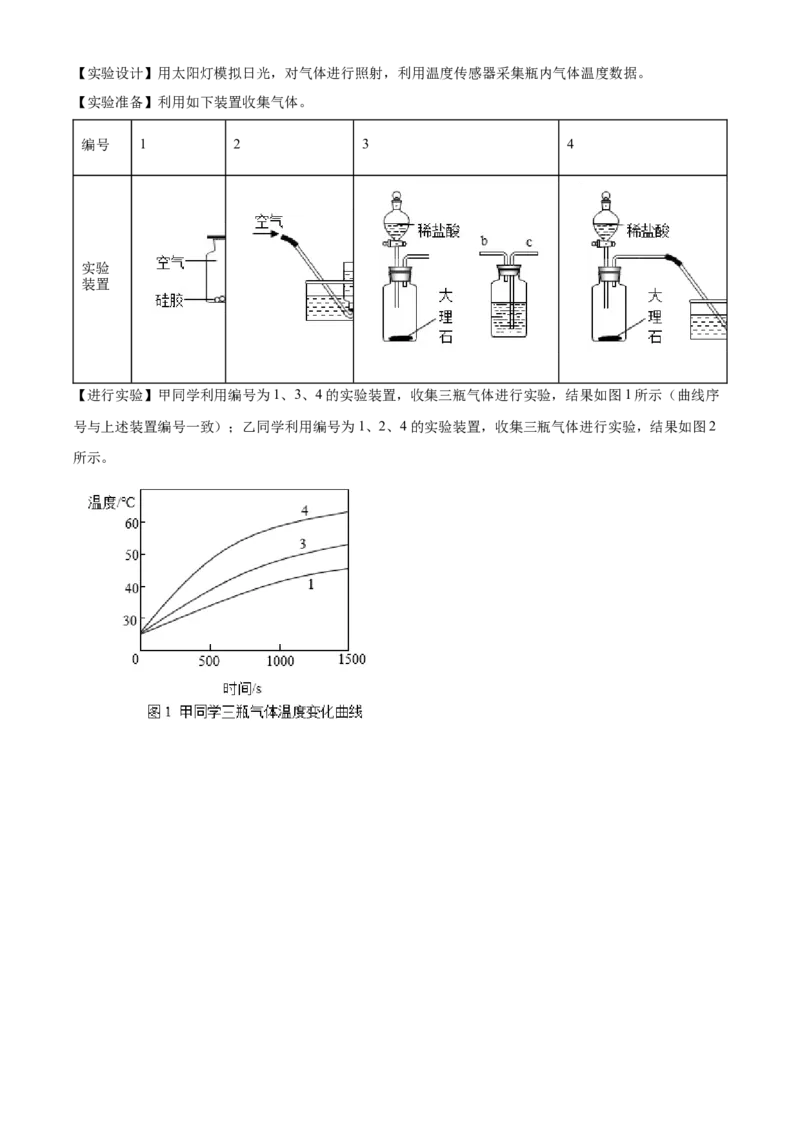
【查阅资料】硅胶和浓硫酸均具有吸水性,可用作某些气体的干燥剂。【实验设计】用太阳灯模拟日光,对气体进行照射,利用温度传感器采集瓶内气体温度数据。
【实验准备】利用如下装置收集气体。
编号 1 2 3 4
实验
装置
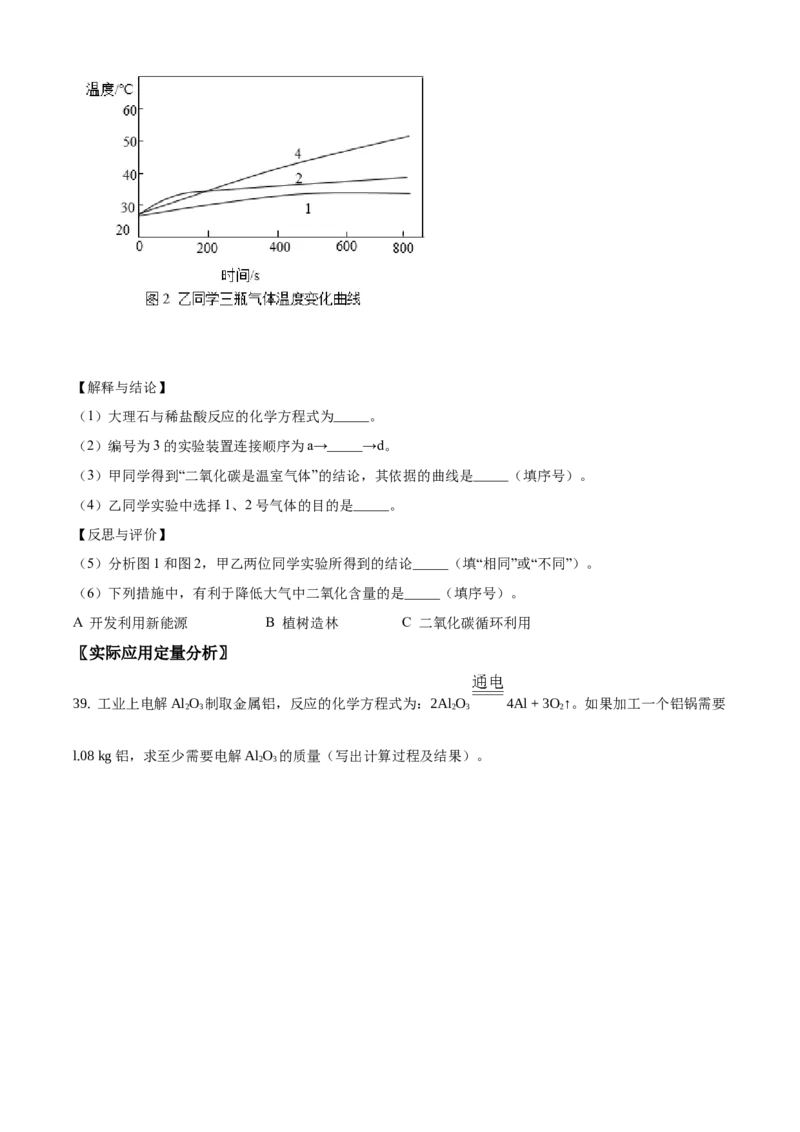
【进行实验】甲同学利用编号为1、3、4的实验装置,收集三瓶气体进行实验,结果如图1所示(曲线序
号与上述装置编号一致);乙同学利用编号为1、2、4的实验装置,收集三瓶气体进行实验,结果如图2
所示。【解释与结论】
(1)大理石与稀盐酸反应的化学方程式为_____。
(2)编号为3的实验装置连接顺序为a→_____→d。
(3)甲同学得到“二氧化碳是温室气体”的结论,其依据的曲线是_____(填序号)。
(4)乙同学实验中选择1、2号气体的目的是_____。
【反思与评价】
(5)分析图1和图2,甲乙两位同学实验所得到的结论_____(填“相同”或“不同”)。
(6)下列措施中,有利于降低大气中二氧化含量的是_____(填序号)。
A 开发利用新能源 B 植树造林 C 二氧化碳循环利用
〖实际应用定量分析〗
39. 工业上电解Al O 制取金属铝,反应的化学方程式为:2Al O 4Al + 3O ↑。如果加工一个铝锅需要
2 3 2 3 2
l.08 kg铝,求至少需要电解Al O 的质量(写出计算过程及结果)。
2 3本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网(http://zujuan.xkw.com)是学科网旗下智能题库,拥有小初高全学科超千万精品试题。
微信关注组卷网,了解更多组卷技能
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635