文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 23 化学计算题
考点01 文字叙述型
考点02 坐标曲线型
考点03 表格数据型
考点04 综合型
考点01 文字叙述型
1.(2025·天津·中考真题)现有一定质量的硫酸钠和硫酸铜的混合粉末,其中含钠元素2.3g。向该混合粉
末中加入81.8g水,完全溶解后,逐滴滴入50g溶质质量分数为8%的氢氧化钠溶液,恰好完全反应,得到
沉淀和溶液。计算:
(1)混合粉末中硫酸铜的质量;
(2)反应后所得溶液中溶质的质量分数;
(3)若用20%的氢氧化钠溶液(密度为 )配制上述50g质量分数为8%的氢氧化钠溶液,需要
20%的氢氧化钠溶液多少毫升( ;结果精确至0.1)。
【答案】(1)8g;
(2)10%;
(3)16.7mL。
【解析】(1)解:设混合粉末中硫酸铜的质量为x,生成氢氧化铜的质量为y,硫酸钠的质量为z。
参加反应的氢氧化钠质量:
答:混合粉末中硫酸铜的质量为8g;
(2)设原混合粉末中硫酸钠的质量为m。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
所得溶液中溶质的质量:
所得溶液的质量:
所得溶液中溶质的质量分数:
答:反应后所得溶液中溶质的质量分数为10%;
(3)需要20%的氢氧化钠溶液的体积:
答:需要20%的氢氧化钠溶液16.7mL。
2.(2025·河北·中考真题)炉甘石洗剂可用于皮肤止痒,其中的炉甘石主要成分为 。为测定某炉甘
石洗剂中 的质量分数,从混合均匀的洗剂中取出100g,向其中加入过量稀硫酸,充分反应后,生成
4.4g二氧化碳(只有 与稀硫酸反应生成二氧化碳,且二氧化碳全部逸出)。请回答:
(1)稀硫酸过量时,所得溶液中溶质主要为 和 (写化学式)。
(2)该洗剂中 的质量分数。(要求有必要的化学方程式和计算步骤)
【答案】(1)
(2)12.5%。
【解析】(1)从混合均匀的洗剂中取出100g,向其中加入过量稀硫酸,碳酸锌与稀硫酸反应生成硫酸
锌、二氧化碳和水,则反应后所得溶液中溶质主要为 和 ;
(2)解:设100g洗剂中碳酸锌的质量为x。
则该洗剂中 的质量分数为
答:该洗剂中 的质量分数为12.5%。
3.(2025·湖北·中考真题)我国研制了世界最大口径碳化硅单体反射镜,应用于深空探测、气象观测等。
碳化硅可用硅与碳在高温下反应制备:Si+C SiC。
(1)SiC中硅、碳元素的质量比为 。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)若要制得40kgSiC,至少需要Si的质量是多少?(写出计算过程)
【答案】(1)7:3
(2)28kg。
【解析】(1)SiC中硅、碳元素的质量比为:28:12=7:3;
(2)解:设若要制得40kgSiC,至少需要Si的质量是x
x=28kg
答:若要制得40kgSiC,至少需要Si的质量是28kg。
4.(2025·湖南长沙·中考真题)小化同学在老师的指导下进行“氧气的实验室制取与性质”的实验活动。
高锰酸钾制氧气的化学方程式为: 。请计算:
(1)高锰酸钾( )中钾元素、锰元素的质量比为 ;
(2)实验中需要0.64g氧气,如果一药匙高锰酸钾的质量为3g,他取两药匙高锰酸钾完全反应制得的氧气
是否足够实验所需?(写出计算过程及结果)
【答案】(1)
(2)制得的氧气不足以满足实验所需。
【解析】(1)K的相对原子质量为39,Mn的相对原子质量为55,高锰酸钾( )中钾元素、锰元
素的质量比为 。
(2)根据氧气的质量计算,解:设制取0.64g氧气需要高锰酸钾的质量为x。
x=6.32g
两药匙高锰酸钾的质量为
答:制得的氧气不足以满足实验所需。
5.(2025·福建·中考真题)“84”消毒液(含NaClO)常用于环境消毒,其生产原理是:
。欲生产100t质量分数为14.9%的NaClO溶液以配制“84”消毒液,请回答下
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
列问题:
(1)100t该NaClO溶液含NaClO t。
(2)理论上需NaCl的质量是 (写出计算过程)。
【答案】(1)14.9
(2)11.7t。
【解析】(1)100t该NaClO溶液含NaClO的质量为: ;
(2)解:设理论上需NaCl的质量为x
答:理论上需NaCl的质量为11.7t。
6.(2024·山东威海·中考真题)某品牌“发热鞋垫”中发热剂的主要成分为铁粉、活性炭和氯化钠等。为
测定其中铁粉的含量,小明同学进行如下实验:取5g发热剂样品于烧杯中,逐滴加入稀硫酸至不再产生
气泡,测得加入稀硫酸的质量为23.4g,反应后烧杯内剩余物的总质量为28.3g,计算发热剂中铁粉的质量
分数(假设其他成分不与酸反应)。
【答案】56%。
【解析】解:设发热剂中铁粉的质量为 ,铁和稀硫酸反应有氢气生成,生成氢气的质量
=5g+23.4g-28.3g=0.1g
发热剂中铁粉的质量分数=
答:发热剂中铁粉的质量分数为56%。
7.(2023·四川甘孜·中考真题)中国空间站利用太阳能电池板提供电力,电解水制备氧气。
(1)电解水时,产生的氧气与氢气的体积比约等于化学方程式中化学计量数之比。若产生 氧气,则
生成的氢气体积约为 。
(2)若需制取 氧气,理论上至少需要电解水的质量是多少?(根据化学方程式进行计算,写出计算
步骤)
【答案】(1)20
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)7.2kg
【解析】(1)电解水时,产生的氢气和氧气的体积比为2:1,若产生10 L 氧气,则生成的氢气的体积约
为10mL×2=20mL。
(2)解:设需要水的质量为
答:需要水的质量为7.2kg。
考点02 坐标曲线型
8.(2025·甘肃兰州·中考真题)为测定某抗酸药(含碳酸氢钠)中碳酸氢钠的质量分数。称取14.0g该药片
充分溶解后(假设其他成分不溶于水,也不与酸反应),向其中逐滴加入7.3%的稀盐酸,用pH传感器测得
实验数据如图所示。
请计算该抗酸药中碳酸氢钠的质量分数。(写出计算过程,结果精确到0.1%)
【答案】60.0%。
【解析】碳酸氢钠溶液呈碱性,pH>7。加入稀盐酸,发生的反应是 ,随
着反应的进行,溶液pH不断减小,根据图像,pH=7时,消耗50g稀盐酸,此时恰好完全反应,根据稀盐
酸的质量计算,解:设该抗酸药中碳酸氢钠的质量分数为x
x=60.0%
答:该抗酸药中碳酸氢钠的质量分数为60.0%。
9.(2025·黑龙江·中考真题)向 和NaCl的混合物中加入167g水充分溶解,再逐滴加入一定溶
质质量分数的 溶液。实验过程中,生成沉淀质量与加入 溶液的质量关系如图所示。请计算下列
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
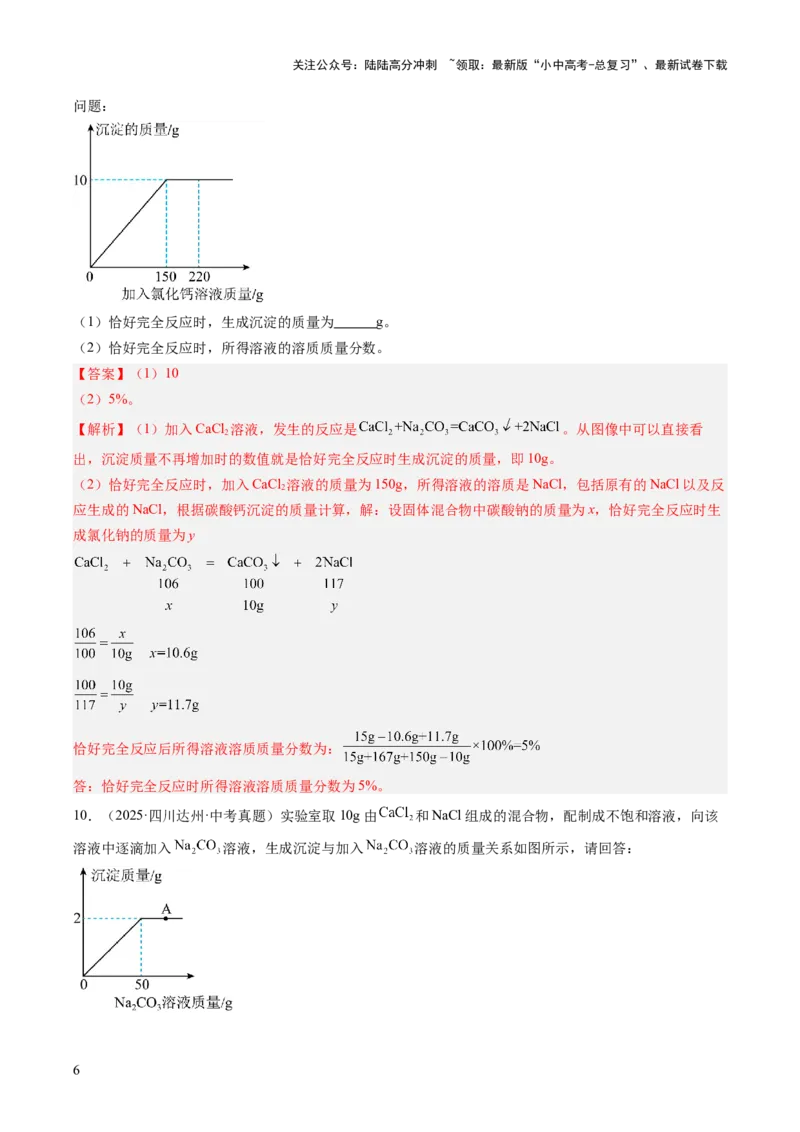
问题:
(1)恰好完全反应时,生成沉淀的质量为 g。
(2)恰好完全反应时,所得溶液的溶质质量分数。
【答案】(1)10
(2)5%。
【解析】(1)加入CaCl 溶液,发生的反应是 。从图像中可以直接看
2
出,沉淀质量不再增加时的数值就是恰好完全反应时生成沉淀的质量,即10g。
(2)恰好完全反应时,加入CaCl 溶液的质量为150g,所得溶液的溶质是NaCl,包括原有的NaCl以及反
2
应生成的NaCl,根据碳酸钙沉淀的质量计算,解:设固体混合物中碳酸钠的质量为x,恰好完全反应时生
成氯化钠的质量为y
恰好完全反应后所得溶液溶质质量分数为:
答:恰好完全反应时所得溶液溶质质量分数为5%。
10.(2025·四川达州·中考真题)实验室取10g由 和NaCl组成的混合物,配制成不饱和溶液,向该
溶液中逐滴加入 溶液,生成沉淀与加入 溶液的质量关系如图所示,请回答:
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1) 完全反应后生成 的质量为 g。
(2)A点对应的溶液中溶质为 。
(3)求原混合物中 的质量分数(写出计算过程)。
【答案】(1)2
(2)NaCl、NaCO
2 3
(3)22.2%。
【解析】(1)加入NaCO 溶液,发生的反应是 ,根据图像,CaCl 完全
2 3 2
反应后生成CaCO 的质量为2g。
3
(2)A点NaCO 溶液过量,溶液中含有原有的NaCl以及生成的NaCl,还有过量的NaCO,则溶质是
2 3 2 3
NaCl和NaCO。
2 3
(3)根据CaCO 沉淀的质量计算,解:设原混合物中CaCl 的质量分数为x
3 2
x=22.2%
答:原混合物中CaCl 的质量分数为22.2%。
2
11.(2025·山东烟台·中考真题)化学小组同学在实践基地发现一袋久置的熟石灰,标签显示其含少量杂
质(杂质不溶于水也不与酸反应)。同学们为探究其变质程度,进行以下实验。取该熟石灰样品10 g于锥
形瓶中,加入40 g水,振荡,然后逐滴加入一定溶质质量分数的稀盐酸,边加边振荡。加入稀盐酸的质量
与锥形瓶中物质的总质量关系如下图所示。(忽略 在水中的溶解)
请完成下列问题:
(1)10 g该熟石灰样品产生 的质量是 g。
(2)计算所加入的稀盐酸的溶质质量分数。(写出计算过程,结果精确至0.1%)
(3)10 g该熟石灰样品中氢氧化钙的质量是 g。(不写计算过程)
【答案】(1)0.88
(2)14.6%。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)7.4
【解析】(1)根据图像,久置的熟石灰中含有碳酸钙和氢氧化钙,当加入50g 稀盐酸时,氢氧化钙和盐
酸先反应,后加入 60g -50g稀盐酸时,碳酸钙和盐酸反应;则生成质量为 50g+60g−109.12g=0.88g,答
案: 0.88。
(2)解:根据图像分析,与碳酸钙反应的稀盐酸质量是60g−50g=10g;
设10g稀盐酸中HCl质量为x。
,x=1.46g。
稀盐酸溶质质量分数 ×100%=14.6%
答:稀盐酸溶质质量分数为14.6%。
(3)与氢氧化钙反应的稀盐酸质量是50g,含HCl质量为50g×14.6%=7.3g。
设氢氧化钙质量为y。
,y=7.4g。
12.(2025·四川遂宁·中考真题)化学是一门以实验为基础的自然学科,阳阳同学在实验室用100g一定溶
质质量分数的过氧化氢溶液和二氧化锰制取氧气,完全反应后,生成氧气的质量与反应时间的关系如图:
(1)反应生成氧气的质量为 g。
(2)二氧化锰起 作用。
(3)计算参加反应的过氧化氢溶液的溶质质量分数(用方程式计算,写出解题过程)。
【答案】(1)3.2
(2)催化
(3)6.8%。
【解析】(1)由图可知,反应生成氧气的质量为3.2g,故填:3.2;
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,二氧化锰为该反应的催化剂,起催化作用,
故填:催化;
(3)解:设参加反应的过氧化氢溶液中溶质的质量为x。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
解得:
则参加反应的过氧化氢溶液的溶质质量分数为
答:参加反应的过氧化氢溶液的溶质质量分数为6.8%。
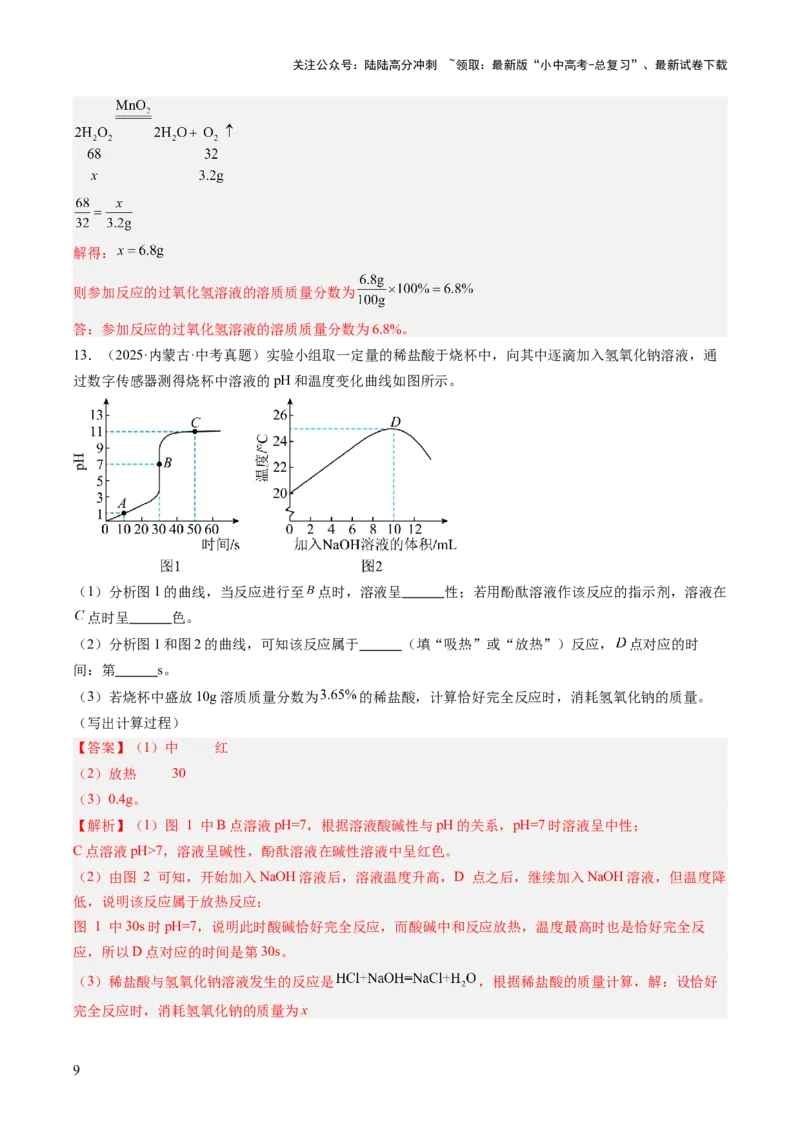
13.(2025·内蒙古·中考真题)实验小组取一定量的稀盐酸于烧杯中,向其中逐滴加入氢氧化钠溶液,通
过数字传感器测得烧杯中溶液的pH和温度变化曲线如图所示。
(1)分析图1的曲线,当反应进行至 点时,溶液呈 性;若用酚酞溶液作该反应的指示剂,溶液在
点时呈 色。
(2)分析图1和图2的曲线,可知该反应属于 (填“吸热”或“放热”)反应, 点对应的时
间:第 s。
(3)若烧杯中盛放10g溶质质量分数为 的稀盐酸,计算恰好完全反应时,消耗氢氧化钠的质量。
(写出计算过程)
【答案】(1)中 红
(2)放热 30
(3)0.4g。
【解析】(1)图 1 中B点溶液pH=7,根据溶液酸碱性与pH的关系,pH=7时溶液呈中性;
C点溶液pH>7,溶液呈碱性,酚酞溶液在碱性溶液中呈红色。
(2)由图 2 可知,开始加入NaOH溶液后,溶液温度升高,D 点之后,继续加入NaOH溶液,但温度降
低,说明该反应属于放热反应;
图 1 中30s时pH=7,说明此时酸碱恰好完全反应,而酸碱中和反应放热,温度最高时也是恰好完全反
应,所以D点对应的时间是第30s。
(3)稀盐酸与氢氧化钠溶液发生的反应是 ,根据稀盐酸的质量计算,解:设恰好
完全反应时,消耗氢氧化钠的质量为x
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
x=0.4g
答:恰好完全反应时,消耗氢氧化钠的质量为0.4g。
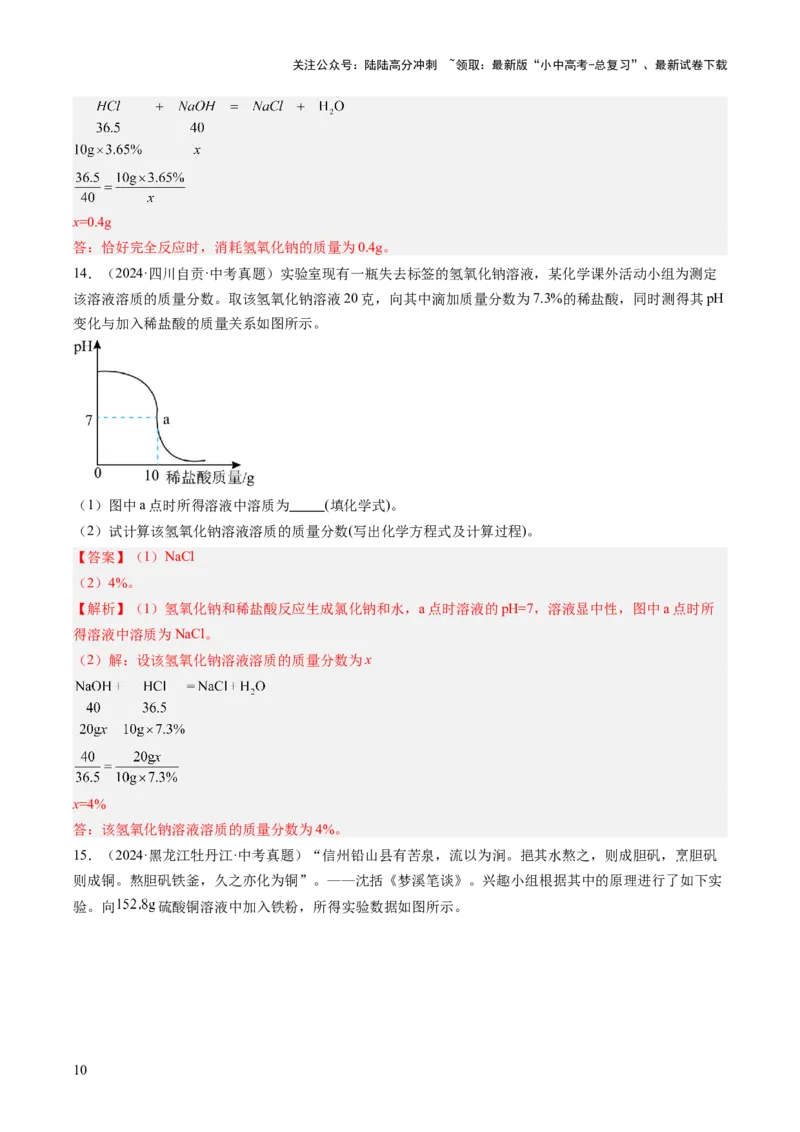
14.(2024·四川自贡·中考真题)实验室现有一瓶失去标签的氢氧化钠溶液,某化学课外活动小组为测定
该溶液溶质的质量分数。取该氢氧化钠溶液20克,向其中滴加质量分数为7.3%的稀盐酸,同时测得其pH
变化与加入稀盐酸的质量关系如图所示。
(1)图中a点时所得溶液中溶质为 (填化学式)。
(2)试计算该氢氧化钠溶液溶质的质量分数(写出化学方程式及计算过程)。
【答案】(1)NaCl
(2)4%。
【解析】(1)氢氧化钠和稀盐酸反应生成氯化钠和水,a点时溶液的pH=7,溶液显中性,图中a点时所
得溶液中溶质为NaCl。
(2)解:设该氢氧化钠溶液溶质的质量分数为x
x=4%
答:该氢氧化钠溶液溶质的质量分数为4%。
15.(2024·黑龙江牡丹江·中考真题)“信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾,烹胆矾
则成铜。熬胆矾铁釜,久之亦化为铜”。——沈括《梦溪笔谈》。兴趣小组根据其中的原理进行了如下实
验。向 硫酸铜溶液中加入铁粉,所得实验数据如图所示。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)b点固体的成分是 (用化学式表示)。
(2)计算恰好完全反应时,所得溶液中溶质的质量分数。
【答案】(1)
(2)10%
【解析】(1)向硫酸铜溶液中加入铁粉,铁和硫酸铜反应生成硫酸亚铁和铜,b点时铁粉过量,故b点固
体的成分是:Fe、Cu;
(2)解:设反应生成硫酸亚铁的质量为x,反应生成铜的质量为y
x=15.2g
y=6.4g
则恰好完全反应时,所得溶液中溶质的质量分数为:
答:所得溶液中溶质的质量分数为 。
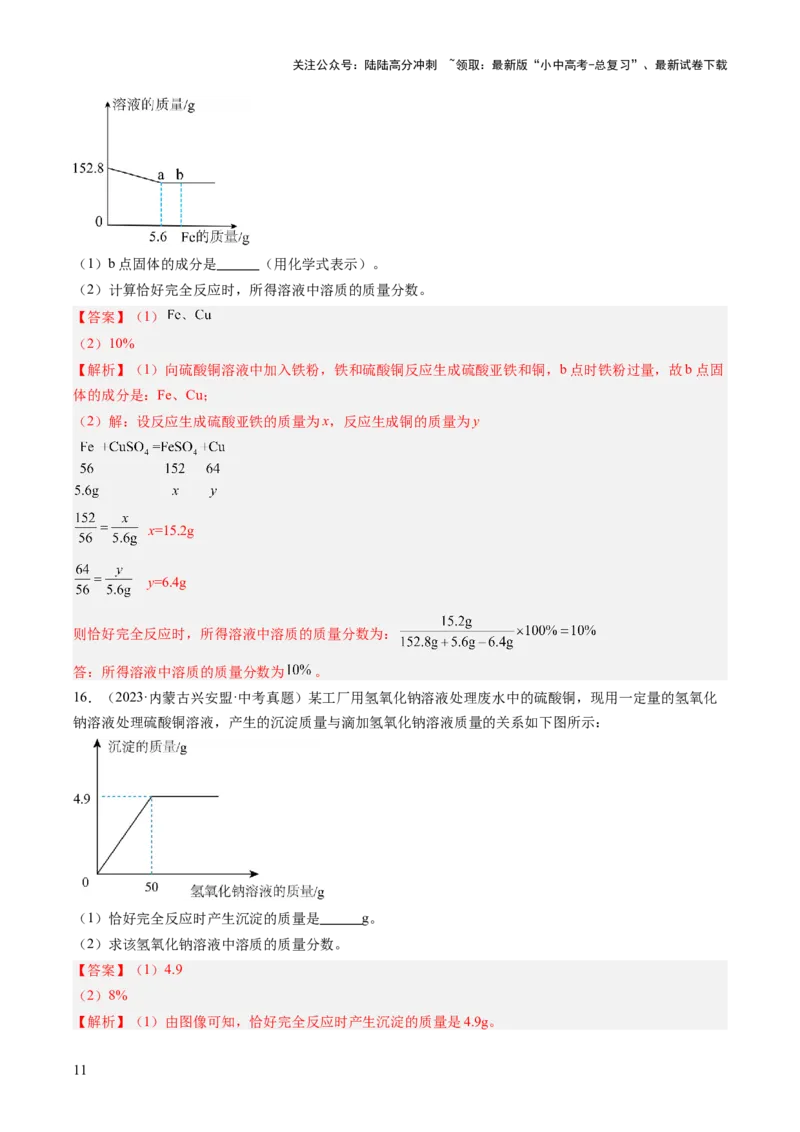
16.(2023·内蒙古兴安盟·中考真题)某工厂用氢氧化钠溶液处理废水中的硫酸铜,现用一定量的氢氧化
钠溶液处理硫酸铜溶液,产生的沉淀质量与滴加氢氧化钠溶液质量的关系如下图所示:
(1)恰好完全反应时产生沉淀的质量是 g。
(2)求该氢氧化钠溶液中溶质的质量分数。
【答案】(1)4.9
(2)8%
【解析】(1)由图像可知,恰好完全反应时产生沉淀的质量是4.9g。
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)解:设该氢氧化钠溶液中溶质的质量为x。
,x=4g
该该氢氧化钠溶液中溶质的质量分数为: =8%
答:氢氧化钠溶液中溶质的质量分数为8%
考点03 表格数据型
17.(2025·黑龙江绥化·中考真题)碳酸钾 俗称钾碱,主要用于印染、玻璃的生产等。为测定某
钾碱样品中碳酸钾的质量分数,化学兴趣小组同学称取28.0g钾碱样品于烧杯中,将200.0g一定溶质质量
分数的稀硫酸平均分成五份,依次加入上述烧杯中,充分反应,测得实验数据如下表。
1 2 3 4 5
加入稀硫酸的质量/g 40 40 40 40 40
烧杯中剩余物质的质量/g 65.8 103.6 141.4 m 219.2
(1)m的值为 ,完全反应后生成二氧化碳的总质量为 g。
(2)计算该钾碱样品中碳酸钾的质量分数(写出计算过程,结果精确到0.1%)。
(3)第5次加入稀硫酸后所得溶液中 和 的个数比 (填“>”“<”或“=”)。
【答案】(1)179.2 8.8
(2)98.6%。
(3)<
【解析】(1)分析表中数据可知,第一次加入40g稀硫酸,反应生成二氧化碳的质量为
,第二次加入40g稀硫酸,反应生成二氧化碳的质量为
,即每加入40g稀硫酸,就会生成2.2g的二氧化碳。且
,即该反应在第4次加入稀硫酸后,碳酸钾就完全反应,则
;
根据质量守恒定律,完全反应后生成二氧化碳的总质量为 ;
故填:179.2;8.8;
(2)解:设参加反应的 的质量为x。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
解得:
则该钾碱样品中碳酸钾的质量分数
答:该钾碱样品中碳酸钾的质量分数是98.6%。
(3)由(1)分析可知,该反应在第4次加入稀硫酸后,碳酸钾就完全反应(碳酸钾与稀硫酸反应生成硫
酸钾、水和二氧化碳),则第5次加入稀硫酸后所得溶液中的溶质为硫酸钾(KSO )和硫酸(HSO ),
2 4 2 4
则此时所得溶液中 和 的个数比小于2:1,故填:<。
18.(2025·四川宜宾·中考真题)实验小组取20g石灰石样品于烧杯中,将100g稀盐酸分四次加入,充分
反应后测得实验数据如下表(杂质不参与反应,生成的气体全部逸出)。
第一次 第二次 第三次 第四次
加入稀盐酸的质量/g 25 25 25 25
烧杯中剩余物质的质量/g 42 64 88.4 113.4
回答下列问题:
(1)实验中发生反应的化学方程式是 。
(2)反应中产生气体的总质量是 g。
(3)该石灰石样品中碳酸钙的质量分数为 (写出计算过程)。
【答案】(1)
(2)6.6
(3)75%。
【解析】(1)石灰石主要成分CaCO 与稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为
3
。
(2)加入100g稀盐酸时,产生CO 的质量一定最大。根据质量守恒定律,反应前物质总质量为
2
,反应后剩余物质质量为113.4g,所以生成二氧化碳质量为 。
(3)第三次加入25g稀盐酸,产生CO 的质量为 ,第四次加入25g稀盐酸,产生
2
CO 的质量也为6.6g,可知样品中的碳酸钙完全反应后产生CO 的质量为6.6g,据此计算,解:设该石灰
2 2
石样品中碳酸钙的质量分数为x
x=75%
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答:该石灰石样品中碳酸钙的质量分数为75%。
19.(2024·甘肃兰州·中考真题)兴趣小组同学得知鸡蛋壳的主要成分是碳酸钙,就用它来测定某瓶标签
破损的稀盐酸中溶质的质量分数。称取5.5g干燥的鸡蛋壳(杂质不参加反应)于烧杯中,再将75g该稀盐
酸分3次加入,充分反应后得到实验数据如下:
第一次 第二次 第三次
稀盐酸的质量/g 25 25 25
剩余固体的质量/g 3 0.5 0.5
请计算:
(1)鸡蛋壳中碳酸钙的质量为 g。
(2)该稀盐酸中溶质的质量分数是多少?(结果精确到0.1%)
【答案】(1)5
(2)7.3%
【解析】(1)鸡蛋壳主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,杂质不参与
反应,则由表格数据可知,鸡蛋壳中碳酸钙的质量为 ;
(2)由表格数据可知,第一次加入25g稀盐酸反应后剩余固体的质量为3g,则消耗碳酸钙的质量为
,第二次加入25g稀盐酸反应后剩余固体的质量为0.5g,则消耗碳酸钙的质量为
,第三次加入25g稀盐酸反应后剩余固体的质量仍为0.5g,说明第二次加入25g稀盐酸时碳酸钙与稀盐酸
恰好完全反应,则共消耗稀盐酸的质量为25g+25g=50g,
解:设稀盐酸中盐酸的质量为x。
则稀盐酸中溶质的质量分数为
答:稀盐酸中溶质的质量分数为7.3%。
20.(2023·湖北鄂州·中考真题)为测定某瓶稀盐酸的溶质质量分数,取4.0g石灰石样品于烧杯中,将该
稀盐酸40.0g分4次加入烧杯中,充分反应后经过滤、洗涤、干燥、称重,得实验数据如下:
第一 第三
第二次 第四次
次 次
加入稀盐酸的质量/g 10.0 10.0 10.0 10.0
剩余固体的质量/g 3.0 2.0 1.0 0.6
已知:石灰石样品中的杂质既不与盐酸反应,也不溶于水。请计算:
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)4.0g石灰石中碳酸钙的质量是 g。
(2)求该瓶稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
【答案】(1)3.4
(2)7.3%
【解析】(1)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,杂质不与稀盐酸反应,由表格数据分析
可知,第一次加入的10.0g稀盐酸能与4.0g-3.0g=1.0g碳酸钙完全反应;第二次加入的10.0g稀盐酸能与
3.0g-2.0g=1.0g碳酸钙完全反应;第三次加入的10.0g稀盐酸能与2.0g-1.0g=1.0g碳酸钙完全反应;第四次
加入的10.0g稀盐酸只能与1.0g-0.6g=0.4g碳酸钙反应,说明此时碳酸钙已经完全反应,最终剩余的0.6g为
石灰石样品中的杂质,故4.0g石灰石中碳酸钙的质量是4.0g-0.6g=3.4g;
(2)解:通过数据比较可知:10.0g稀盐酸完全反应可以消耗碳酸钙的质量为1.0g,
设10.0g稀盐酸中溶质质量为x
x=0.73 g
则该瓶稀盐酸的溶质质量分数为: ,
答:该瓶稀盐酸的溶质质量分数为7.3%。
21.(2023·黑龙江绥化·中考真题)某同学取MgC1 和KC1固体混合物10.8g,向其中加入115g的水,使
2
其完全溶解。将100g一定质量分数的KOH溶液平均分成5等份,依次加入到上述溶液中,生成沉淀的质
量与KOH溶液的质量关系如下表:
第二 第四
实验次数 第一次 第三次 第五次
次 次
KOH溶液的质量/g 20 20 20 20 20
产生沉淀的质量/g 1.45 m 4.35 5.8 5.8
请分析计算。
(1)表中m的值是 。
(2)所用KOH溶液中溶质的质量分数是 。
(3)计算恰好完全反应时,所得溶液中溶质的质量分数(要写出计算过程)。
【答案】(1)2.9
(2)14%
(3)8.1%
【解析】(1)根据前四次,每次对应的沉淀的质量为1.45g,所以第三次m=1.45×2=2.9,且第四次为恰好
完全反应;
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)解:第四次恰好完全反应,此时加入氢氧化钾溶液的质量为80g,生成沉淀氢氧化镁的质量为5.8g,
设80g氢氧化钾溶液中氢氧化钾的质量为
所用KOH溶液中溶质的质量分数= ;
答:所用KOH溶液中溶质的质量分数14%;
(3)解:计算恰好完全反应时,设参加反应的MgC1 的质量为y,生成KC1的质量为z
2
所得溶液是氯化钾溶液,质量分数=
答:恰好完全反应时,所得溶液的溶质质量分数是8.1%。
考点04 综合型
22.(2025·江西·中考真题)实践小组为测定某品牌纯碱样品中NaCO 的质量分数,进行了如图实验(杂
2 3
质不参与反应)。
(1)实验室取用纯碱粉末需用到的仪器为 ,加入稀盐酸观察到的现象是 。
(2)充分反应后生成气体的质量是 g。
(3)计算样品中NaCO 的质量分数。(写出计算过程,结果精确到0.1%)
2 3
(4)由于二氧化碳能溶于水,该实验测得样品中NaCO 的质量分数会 (选填“偏大”“偏小”或
2 3
“不变”)。
【答案】(1)药匙 产生大量气泡
(2)2.2
(3)88.3%。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)偏小
【解析】(1)实验室取用纯碱(粉末状 )需用到的仪器为药匙 ,药匙用于取用粉末状或小颗粒状的固
体药品 。纯碱(NaCO)与稀盐酸反应生成氯化钠、水和二氧化碳,所以加入稀盐酸观察到的现象是有
2 3
气泡产生。
(2)根据质量守恒定律,减少的质量是生成二氧化碳的质量,反应前总质量:6g+61.7g=67.7g;反应后总
质量:65.5g ,则生成气体的质量是67.7g−65.5g=2.2g。
(3)设纯碱样品中碳酸钠的质量为 。
x=5.3g
纯碱样品中碳酸钠的质量分数= ×100%=88.3%
答:纯碱样品中碳酸钠的质量分数为88.3%。
(4)由于二氧化碳能溶于水,会导致测得的二氧化碳质量偏小(部分二氧化碳溶解在水中,未全部逸
出)。根据化学方程式计算时,二氧化碳质量偏小,会使计算出的碳酸钠质量偏小,所以该实验测得样品
中碳酸钠的质量分数会偏小 。
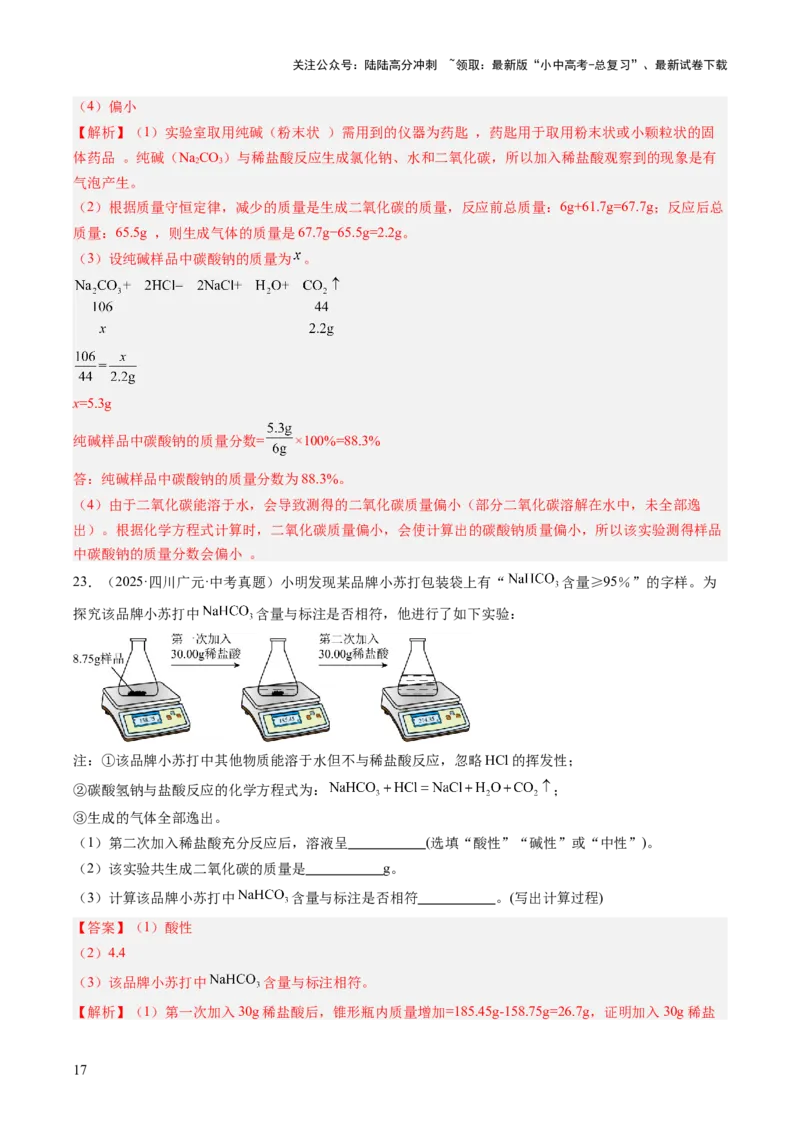
23.(2025·四川广元·中考真题)小明发现某品牌小苏打包装袋上有“ 含量≥95%”的字样。为
探究该品牌小苏打中 含量与标注是否相符,他进行了如下实验:
注:①该品牌小苏打中其他物质能溶于水但不与稀盐酸反应,忽略HCl的挥发性;
②碳酸氢钠与盐酸反应的化学方程式为: ;
③生成的气体全部逸出。
(1)第二次加入稀盐酸充分反应后,溶液呈 (选填“酸性”“碱性”或“中性”)。
(2)该实验共生成二氧化碳的质量是 g。
(3)计算该品牌小苏打中 含量与标注是否相符 。(写出计算过程)
【答案】(1)酸性
(2)4.4
(3)该品牌小苏打中 含量与标注相符。
【解析】(1)第一次加入30g稀盐酸后,锥形瓶内质量增加=185.45g-158.75g=26.7g,证明加入30g稀盐
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
酸反应生成30g-26.7g=3.3g气体,第二次加入30g稀盐酸,质量增加214.35g-185.45g=28.9,第二次加入稀
盐酸只生成气体30g-28.9g=1.1g气体,证明第二次加入酸过量,故第二次加入稀盐酸充分反应后,溶液呈
酸性;
(2)由(1)分析可知,该实验共生成二氧化碳的质量=3.3g+1.1g=4.4g;
(3)解:设样品中碳酸氢钠质量为x
故碳酸氢钠含量= >95%,故含量与标注相符。
答:该品牌小苏打中 含量与标注相符。
24.(2025·黑龙江齐齐哈尔·中考真题)化学兴趣小组用某碳酸氢钠样品(杂质只含氯化钠)进行下图所示实
验:
请计算:
(1)恰好完全反应时,生成气体的质量是 g。
(2)加入15.3g水后,所得不饱和溶液中溶质的质量分数是多少?
【答案】(1)8.8
(2)10%。
【解析】(1)由质量守恒定律可知,反应生成二氧化碳气体的质量为:100g+17.5g-108.7g=8.8g;
(2)解:设样品中碳酸氢钠的质量为 ,生成氯化钠的质量为 。
方法一:
方法二:
答:所得不饱和溶液中溶质的质量分数是10%。
25.(2025·黑龙江大庆·中考真题)小庆和小铁同学利用实验室的粗盐,模拟侯氏制碱法制备碳酸钠。操
作过程如下:
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)粗盐提纯
除去难溶性杂质后的食盐水中还含有少量可溶性杂质,为除去其中的NaSO 、CaCl 和MgCl ,选用的除
2 4 2 2
杂试剂为①过量NaOH溶液、②过量NaCO 溶液、③过量BaCl 溶液,请写出一种合理的加入顺序
2 3 2
(仅填序号)。过滤后向滤液中加适量的盐酸,蒸发结晶得到NaCl固体。
(2)配制饱和食盐水
已知20℃时NaCl的溶解度为36.0g,配制50g饱和食盐水需量取水的体积为 mL(水的密度可近似看作
1g/cm3,结果保留一位小数)。
(3)模拟侯氏制碱法
具体原理为:NaCl+H O+CO+NH=NaHCO↓+NHCl,2NaHCO NaCO+H O+CO↑
2 2 3 3 4 3 2 3 2 2
取一定量的饱和食盐水,通入足量的氨气和二氧化碳充分反应,过滤后得到8.4g碳酸氢钠固体,加热完全
分解生成碳酸钠的质量为多少克?(写出计算过程)
【答案】(1)①③②(或③②①或③①②)
(2)36.8
(3)5.3g。
【解析】(1)氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡能与硫酸钠反应生成硫酸钡
沉淀和氯化钠,碳酸钠能与氯化钙反应生成碳酸钙沉淀,同时碳酸钠能与氯化钡反应生成碳酸钡沉淀和氯
化钠,故①用于除去氯化镁杂质,②用于除去氯化钙杂质,③用于除去硫酸钠杂质,过滤后向滤液中加适
量的盐酸,盐酸能除去过量的氢氧化钠、碳酸钠,不能除去过量的氯化钡,所以②还用于除去过量的氯化
钡,则②应放在③的后面,故正确顺序为①③②或③②①或③①②;
(2)20℃时NaCl的溶解度为36.0g,则20℃时饱和食盐水的溶质质量分数为 ,则配制
50g饱和食盐水需要氯化钠的质量为 ,需要水的质量为
50g-13.2g=36.8g,则需要水的体积为 ;
(3)解:设加热8.4g碳酸氢钠固体生成碳酸钠的质量为x
答:加热8.4g碳酸氢钠固体,加热完全分解生成碳酸钠的质量为5.3g。
26.(2025·甘肃武威·中考真题)“金粉”( 合金)是一种金属颜料,可用于文物修复。某化学兴趣
小组为测定“金粉”中铜的含量,进行了下图所示的实验。请根据图示数据计算:
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)生成氢气的质量为 。
(2)该“金粉”中铜的质量分数(写出计算过程)。
(3)所用稀硫酸中溶质的质量分数(写出计算过程)。
【答案】(1)0.2g
(2)74%;
(3)9.8%。
【解析】(1)根据质量守恒定律,化学反应前后物质的总质量不变,则生成氢气的质量是:
25g+100g-124.8g=0.2g;
(2)解:设该“金粉”中锌的质量为x
x=6.5g
则该“金粉”中铜的质量分数为:
答:该“金粉”中铜的质量分数为74%;
(3)解:设所用稀硫酸中溶质的质量分数为y
y=9.8%
答:所用稀硫酸中溶质的质量分数为9.8%。
27.(2024·陕西·中考真题)学习小组用一瓶长久放置、标签标示溶质质量分数为5%的过氧化氢溶液制取
氧气,并用下图所示方法测定实验产生氧气的质量。
请完成下列分析及计算:
(1)二氧化锰在反应前后的质量 (填“变大”“变小”或“不变”)。
(2)实验产生氧气的质量是 g。
(3)通过计算说明实验所用过氧化氢溶液中溶质质量分数与标签标示的5%是否一致。
【答案】(1)不变
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)1.6
(3)不一致。
【解析】(1)过氧化氢在二氧化锰的催化下分解生成氧气和水,二氧化锰作为该反应的催化剂,在反应
前后质量不变;
(2)根据质量守恒定律,实验产生氧气的质量是400.0g-398.4g=1.6g;
(3)解:设参加反应的过氧化氢的质量为x,
x=3.4g
则实验所用过氧化氢溶液中溶质质量分数为 ≠5%,
答:实验所用过氧化氢溶液中溶质质量分数与标签标示的5%不一致。
28.(2023·山东潍坊·中考真题)航母舰体需要定期除锈维护,为实现对除锈废液(溶质主要成分为
、其他杂质忽略)的综合利用,需测定废液中 的质量分数,取 废液样品,依次加入
溶质质量分数相同的 溶液,过滤,称重,相关数据如图。
回答下列问题:
(1)第③次过滤后,滤液中溶质的成分为 (用化学式表示)。
(2)所用 溶液溶质的质量分数(写出计算过程)。
(3)废液样品中 的质量分数为 (结果精确至0.1%)。
【答案】(1)
(2)24%
(3)
【解析】(1)第一次加入的氢氧化钠溶液先与盐酸反应生成氯化钠和水,盐酸反应完,再与氯化铁反应
生成氢氧化铁沉淀和氯化钠,第一次加入 氢氧化钠溶液,产生氢氧化铁沉淀 ;第二次加入
氢氧化钠溶液,产生氢氧化铁沉淀 ;第三次加入 氢氧化钠溶液,产生氢氧化铁沉淀 ;说明
氢氧化钠溶液与氯化铁溶液完全反应能生成 氢氧化铁沉淀。第三次加入 氢氧化钠溶液,只
21关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
生成了 沉淀,说明氯化铁已经完全反应,氢氧化钠有剩余,则第③次过滤后,滤液中溶质的成分为
。
(2)解:根据题意, 氢氧化钠溶液与氯化铁溶液完全反应能生成 氢氧化铁沉淀。
设参加反应的氢氧化钠的质量为x。
所用 溶液溶质的质量分数 。
答:所用 溶液溶质的质量分数为 。
(3)第一次加入 氢氧化钠溶液,产生氢氧化铁沉淀 ;第二次加入 氢氧化钠溶液,产生氢
氧化铁沉淀 ;说明与稀盐酸反应的氢氧化钠溶液的质量为 ,溶质的质量为 。
设参加反应的稀盐酸中溶质的质量为y。
废液样品中 的质量分数为 。
22