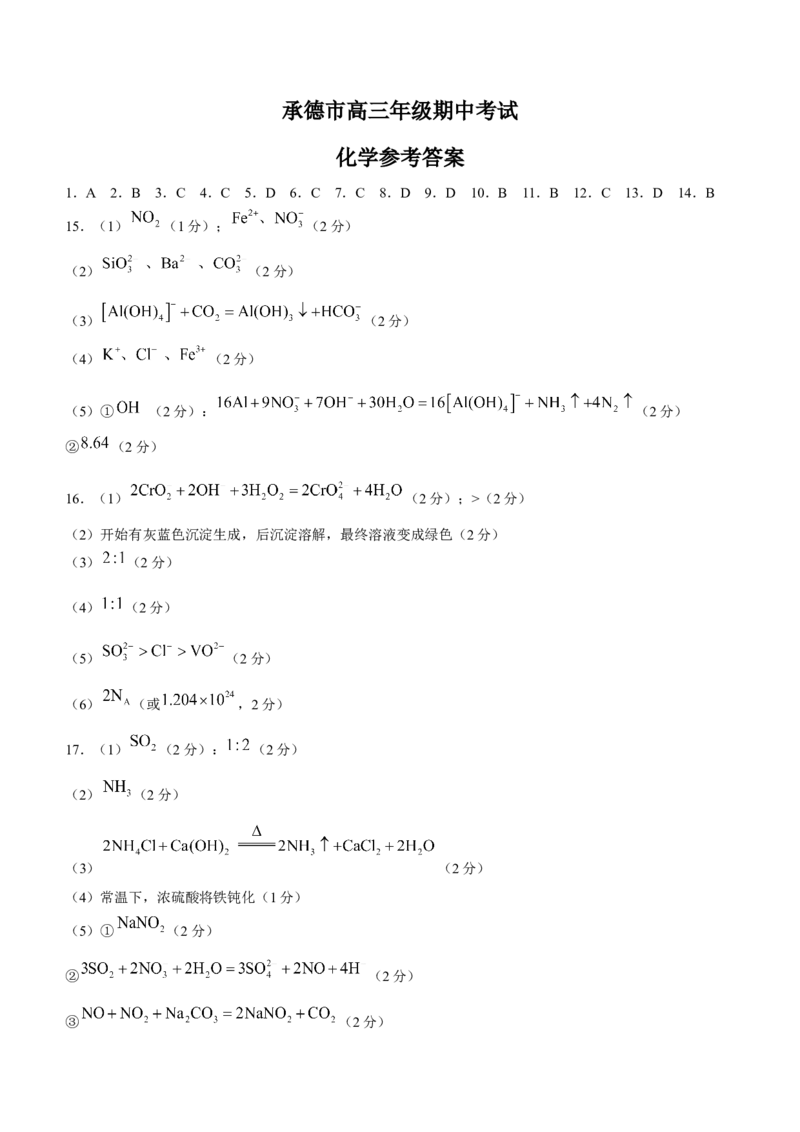文档内容
承德市高三年级期中考试
化学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将白己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷
上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是行合题目要求的。
1.化学与科学、技术、社会、生活等密切相关。下列有关说法错误的是( )
A. 可用于丝织品漂白是由于其能氧化丝织品中的有色成分
B.现代化肥种类丰富,施用方法依据其对象营养状况而定
C.液晶用途广泛,已经获得实际应用的热致液晶均为刚性棒状强极性分子
D.规范使用防腐剂可以减缓食物变质速率,保持食品营养价值
2.下列表示正确的是( )
A. 和 互为同位素
B. 的电子式:
C. 的结构示意图:
D.基态N原子的价层电子排布图:
3.生活中处处有化学。下列物质的俗名和化学式对应不正确的是( )
A.刚玉— B.氯仿— C.重晶石— D.消石灰—
4.在给定条件下,下列选项所示的物质间的转化能实现的是( )
A.浓缩海水
B.C.石油
D. 悬浊液
5,下列实验操作中选用仪器错误的是( )
制备硝基苯时冷凝回流 用铁坩埚加热熔化 用分液漏斗分离乙酸乙 用滴定管量取
用冷凝管 酯和水的混合物
固体 溶液
A B C D
A.A B.B C.C D.D
6.钠和钠的化合物有许多重要的用途,如碳酸钠可用于从海水中提取溴,涉及的反应为
。下列说法错误的是( )
A.用双线桥法标出电子的转移:
B.该反应中氧化剂与还原剂的物质的量之比是
C.等物质的量的 和 分别与足量的盐酸反应,在相同条件下 产生 的体积小于
产生的
D.碳酸氢钠溶于水显碱性,可用于去除油污
7.下列实验对应的离子方程式正确的是( )
A.将少量 通入 溶液中:
B.酸性条件下 溶液与 溶液反应生成
C.将碳酸氢钙溶液与过量的澄清石灰水混合:
D.将 和 的混合溶液与足量 反应:
8.设 为阿伏加德罗常数的值,下列说法错误的是( )A.电解精炼铜时,当阴极增重 ,阳极失去的电子总数为
B. 由乙烯和环丙烷组成的混合气体中含 键的数目为
C. 时, 的 溶液中含有 的数目为
D. 的中心原子的价层电子对数为
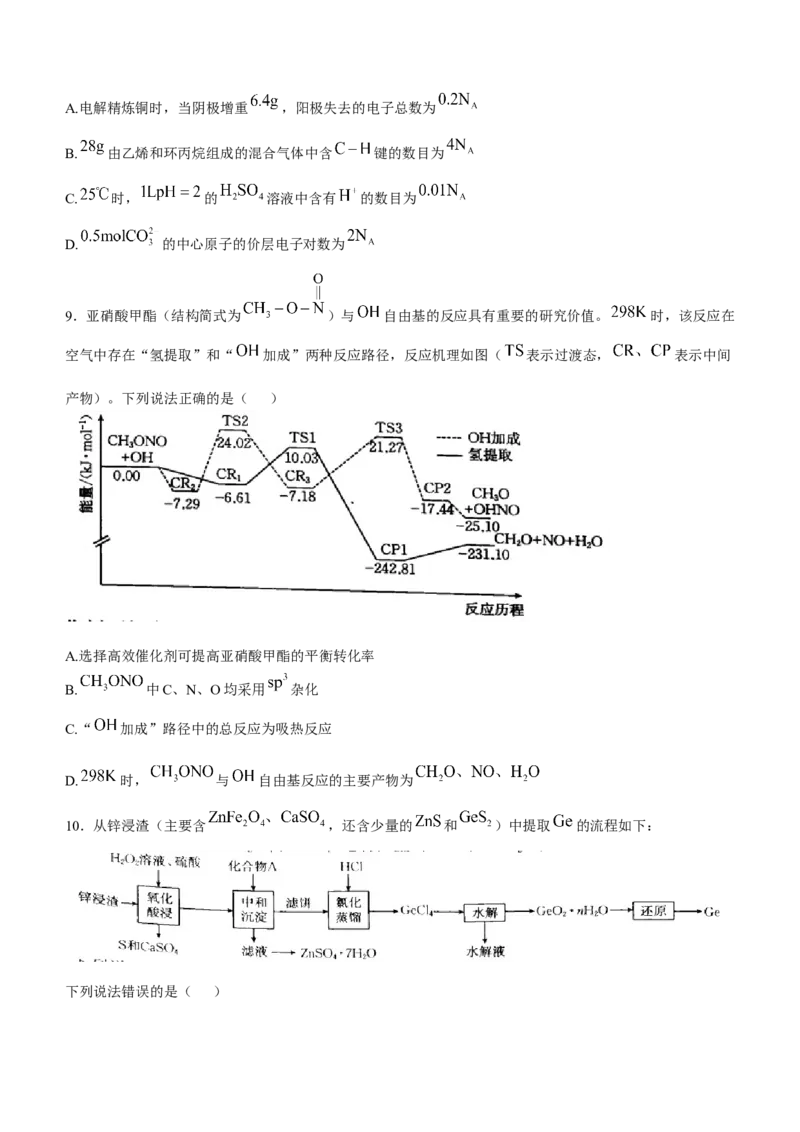
9.亚硝酸甲酯(结构简式为 )与 自由基的反应具有重要的研究价值。 时,该反应在
空气中存在“氢提取”和“ 加成”两种反应路径,反应机理如图( 表示过渡态, 表示中间
产物)。下列说法正确的是( )
A.选择高效催化剂可提高亚硝酸甲酯的平衡转化率
B. 中C、N、O均采用 杂化
C.“ 加成”路径中的总反应为吸热反应
D. 时, 与 自由基反应的主要产物为
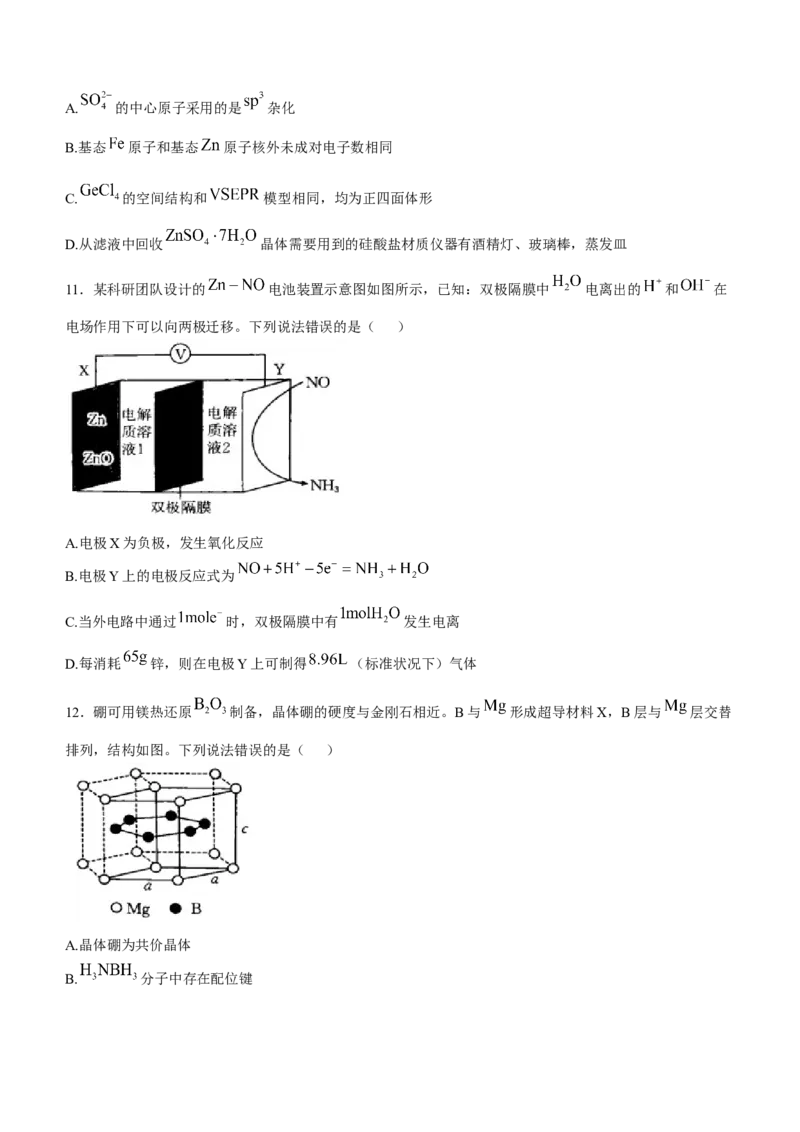
10.从锌浸渣(主要含 ,还含少量的 和 )中提取 的流程如下:
下列说法错误的是( )A. 的中心原子采用的是 杂化
B.基态 原子和基态 原子核外未成对电子数相同
C. 的空间结构和 模型相同,均为正四面体形
D.从滤液中回收 晶体需要用到的硅酸盐材质仪器有酒精灯、玻璃棒,蒸发皿
11.某科研团队设计的 电池装置示意图如图所示,已知:双极隔膜中 电离出的 和 在
电场作用下可以向两极迁移。下列说法错误的是( )
A.电极X为负极,发生氧化反应
B.电极Y上的电极反应式为
C.当外电路中通过 时,双极隔膜中有 发生电离
D.每消耗 锌,则在电极Y上可制得 (标准状况下)气体
12.硼可用镁热还原 制备,晶体硼的硬度与金刚石相近。B与 形成超导材料X,B层与 层交替
排列,结构如图。下列说法错误的是( )
A.晶体硼为共价晶体
B. 分子中存在配位键C.超导材料X的化学式为
D. (中的 键角为
阅读下列材料完成13~14题。
铁是一种变价元素,常见的化合价有 价和 价。铁是工业和日常生活中不可或缺的材料。由于其良好的
导电性和导热性,铁广泛用于电气和热传导设备。此外,铁的氧化物在颜料、磁性材料和催化剂等方面有重
要应用,铁盐在工业和生活中有多种用途:硫酸铁盐、氯化铁盐和硝酸铁盐常用于制造油漆、墨水、防锈剂、
净水剂等。
13.探究铁及其化合物的性质,下列实验方案、现象和结论都正确的是( )
选项 实验方案 现象 结论
溶液逐渐变蓝
A 往 溶液中加人 片 的氧化能力比 强
溶液先变成红色,后红色变浅
稀释了溶液,红色变
往 溶液中滴加 溶
B
浅
液,再加入少量 固体
先用盐酸浸泡带有铁锈的铁钉, 有特征蓝色沉淀出现
铁锈的主要成分为
C
再滴加 溶液
液体先变成红褐色,然后析出
向 沸水中逐滴加入5~6滴
先水解得 胶
红褐色沉淀
D
饱和 溶液,持续煮沸
体,再聚沉成 沉
淀
A.A B.B C.C D.D
14.铁盐法是处理含陣废水的主要方法之一,已知 (Ⅲ)比 (Ⅴ)毒性大且不易沉降,碑(Ⅴ)酸铁、
砷(Ⅴ)酸钙的溶解度很小。硫酸厂酸性废水[主要含有硫酸和含砷(Ⅲ)化合物]的处理步骤如下:
(1)向废水中加入消石灰,调节废水的 至5~6,过滤后再加入一定量绿矾,得到混合溶液;
(2)向上述混合溶液中加入高浓度双氧水作为氧化剂,搅拌,至溶液变为黄褐色浑浊液;
(3)再加入碱调节反应后的浑浊液 至7~9,出现大量褐色沉淀,搅拌,充分反应后,静置、过滤.向收
滤渣,检测滤液中砷含量,达标后外排。
下列说法错误的是( )
A.步骤(1)中过滤出的滤渣的主要成分是
B.步骤(2)中双氧水的作用只是将三价砷氧化为五价砷
C.亚砷酸( )和砷酸( )均为弱酸
D.步骤(3)中,工业上调节反应后的浑浊液的 所用的碱最好是
二、非选择题:本题共4小题,共58分。15.(15分)某溶液A中可能含有
中的几种,现对该溶液进行如下实验:
步骤1:取少量溶液A于试管中,向试管中滴加浓盐酸,有少量无色气体生成,气体遇空气立即变为红棕色,
将所得溶液分成两等份,分别为溶液 、溶液 。
步骤2:向溶液 中加入 溶液,有白色沉淀生成。
步骤3:向溶液 中加入过量的 溶液,有红褐色沉淀生成,过滤,向所得滤液中通入过量的 ,有
白色絮状沉淀生成。
依据上述实验,回答下列问题:
(1)步骤1中得到的红棕色气体为_______(填化学式),由此可推出溶液A中一定含有_______(填离子
符号)。
(2)结合步骤1和步骤2可知,该溶液A中一定不含的离子为_______(填离子符号)。
(3)步骤3中生成白色絮状沉淀反应的离子方程式为________________________________________。
(4)结合上述实验,可知溶液A中可能含有的离子为_______(填离子符号)。
(5)已知:在碱性条件下, 单质能与 反应,生成氨气和氮气,发生反应的离子方程式为_______
______ ______ ______ ______ (未配平,Y代表一种离
子)。
①Y代表_______(填离子符号);配平上述离子方程式:_______(Y用具体离子符号表示)。
②若该反应中生成标准状况下 气体,则消耗的 单质的质量为_______g。
16.(14分)过渡金属在日常生活、工业生产和医疗化工中随处可见,它们渗透到我们生活的方方面面。请
回答下列问题:
Ⅰ.几种铬( )的化合物的转化关系如图所示:
(1)反应②的离子方程式为_______;碱性条件下,氧化性: _______(填“>”或“<”) 。
(2)已知铬的化合物色彩众多,如 (紫色)、 (灰蓝色沉淀)、 (绿色)等。
向 溶液中滴加 溶液至过量,可观察到的现象是_______。
(3)已知 晶体{配合物化学式可表示为 }有3种不同颜色,其配位数均为6,实验测得 不同颜色的晶体分别与足量的硝酸银溶液反应,生成沉淀的物质的量如表所
示:
晶体颜色 深绿色 浅绿色 紫色
沉淀的物质的量 1 2 3
若晶体为深绿色,则 _______。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。
(4)将废钒催化剂(主要成分为 )与稀硫酸、 溶液混合,充分反应后生成 ,该反应中氧
化剂和还原剂的物质的量之比为_______。
(5) 能与盐酸反应生成 和一种黄绿色气体,该黄绿色气体能与 溶液反应而被吸收,则
的还原性由强到弱的顺序是_______。
(6) 在氮气氛围、碳高温条件下还原氨化制备 ,还生成一种具有还原性的气体,则生成标准状况
下 该还原性气体时,反应转移的电子数为_______。
17.(15分)氮、硫及其化合物的“价-类”二维图如图所示。
请回答下列问题:
(1)g与i在一定条件下可发生反应生成淡黄色固体和水,反应中作氧化剂的是_______(填化学式),氧化
剂和还原剂的物质的量之比为_______。
(2) 四种粒子中 模型不是平面三角形的是_______。
(3)实验室利用加热固体药品制备a的化学方程式为______________________________________。
(4)常温下,k的浓溶液可储存在铁罐中,其原因是___________________________。
(5)工业上利用氮、硫及其化合物的“价-类”二维图中的部分物质生产e的流程如图所示:已知:Ⅰ.理论上控制“分解塔”的反应条件(如i的流速、反应温度、d溶液的浓度等),使
,才能获得高纯度的产品e;Ⅱ.b单独与 溶液不反应。
①e为_______(填化学式)。
②气体i通入稀的d溶液中时,只生成气体b,写出反应的离子方程式:________________________________。
③“吸收塔”中b、c与足量的碳酸钠溶液反应的化学方程式为_____________________________________。
18.(14分)含氮化合物在现代工业、环境治理中有重要地位。请回答下列问题:
(1)已知:
则反应 的 _______ 。
(2)使用 催化剂,利用 将 还原为 ,可以消除烟气中的氨氧化物对环境
的污染,反应机理如图所示。
①根据图示, 在有氧条件下总反应的化学方程式是_______________________________。
②将一定比例的 和 的混合气体,匀速通入装有催化剂的反应器中反应(装置如图甲)。反应
相同时间,测得 的去除率随反应温度的变化曲线如图乙所示,在 范围内随着温度的升高,
的去除率先迅速上升后上升缓慢的主要原因是_______________________;当反应温度高于 时,的去除率迅速下降的原因可能是_____________________________。
甲 乙
③利用模拟烟气测试系统,在氨氮比为 和 条件下,保持 的气体流量,研究氧气浓
度对催化剂活性的影响,测得不同浓度下 对 转化为 的转化率影响如图所示。由图可知,在反应气
体中不含氧气时,催化剂也能催化一定量的一氧化氮进行转化,原因是_____________________。随着氧气浓
度
氧量气浓度的增加,催化剂的活性逐渐提高,但氧气浓度大于 后,再增加氧气的浓度,催化剂的催化效
率提升不明显,其原因是____________________________。
(3) 时,反应 在恒容密闭容器中进行, 和 的初始
分压分别为 和 ,起始时容器中只含 和 ,假设当反应达到平衡后, 和 的平
衡分压分别为 和 ,则该反应在 时的 为_______ 。承德市高三年级期中考试
化学参考答案
1.A 2.B 3.C 4.C 5.D 6.C 7.C 8.D 9.D 10.B 11.B 12.C 13.D 14.B
15.(1) (1分); (2分)
(2) (2分)
(3) (2分)
(4) (2分)
(5)① (2分): (2分)
② (2分)
16.(1) (2分);>(2分)
(2)开始有灰蓝色沉淀生成,后沉淀溶解,最终溶液变成绿色(2分)
(3) (2分)
(4) (2分)
(5) (2分)
(6) (或 ,2分)
17.(1) (2分): (2分)
(2) (2分)
(3) (2分)
(4)常温下,浓硫酸将铁钝化(1分)
(5)① (2分)
② (2分)
③ (2分)18.(1) (2分)
(2)① (2分)
②迅速上升段是因为温度升高,催化剂的活性增大,反应速率加快, 的去除率迅速上升,上升缓慢段是
因为温度升高,催化剂的活性降低(或其他合理答案,2分); 与 反应生成了 (或催化剂失活,
2分)
③在催化剂表面存在一定比例的活泼氧,可以在反应中充当氧气的作用或催化剂具有足够强的氧化能力(2
分);吸附氧达到了饱和(2分)
(3) (2分)