文档内容
石景山区 2022-2023 学年第一学期初三期末试卷
化 学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ca-40
第一部分
本部分共25题,每题1分,共25分。在每题列出的四个选项中,选出最符合题目要求的一
项。
1. 垃圾分类人人有责。果皮属于( )
A. 可回收物 B. 其他垃圾 C. 厨余垃圾 D. 有害垃圾
2. 84消毒液是一种含氯消毒剂。这里的“氯”指的是
A. 元素 B. 单质 C. 分子 D. 原子
3. 走过花圃会闻到花香。用微粒的观点解释其原因是
A. 分子在不断运动 B. 分子的质量小
C. 分子之间有间隔 D. 分子的体积小
4. 化石燃料是不可再生的能源,下列不属于化石燃料的是
A. 煤 B. 石油 C. 乙醇 D. 天然气
5. 下列物质的用途中,利用其化学性质的是
A. 干冰用于人工降雨 B. 液氢用作火箭燃料
C. 液氮用作冷冻剂 D. 石墨用于制铅笔芯
6. 赤铁矿(主要成分是Fe O)用于工业炼铁。Fe O 中铁元素的化合价为
2 3 2 3
A. -3 B. -2 C. +2 D. +3
7. 尿素[CO(NH )]是农业上常使用的一种化肥。CO(NH ) 中质量分数最大的元素是
2 2 2 2
A. C B. O C. N D. H
8. 生活中需要对天然水进行净化,下列净水方法中,净化程度最高的是
A. 沉淀 B. 蒸馏 C. 吸附 D. 消毒
的
9. 下列物质中,属于纯净物 是
A. 氧气 B. 糖水 C. 食醋 D. 大理石
10. 下列物质属于单质的是
A. Cl B. ClO C. HClO D. NaClO
2 2 3
11. 下列物质属于氧化物的是
A. O B. NO C. KClO D. NaOH
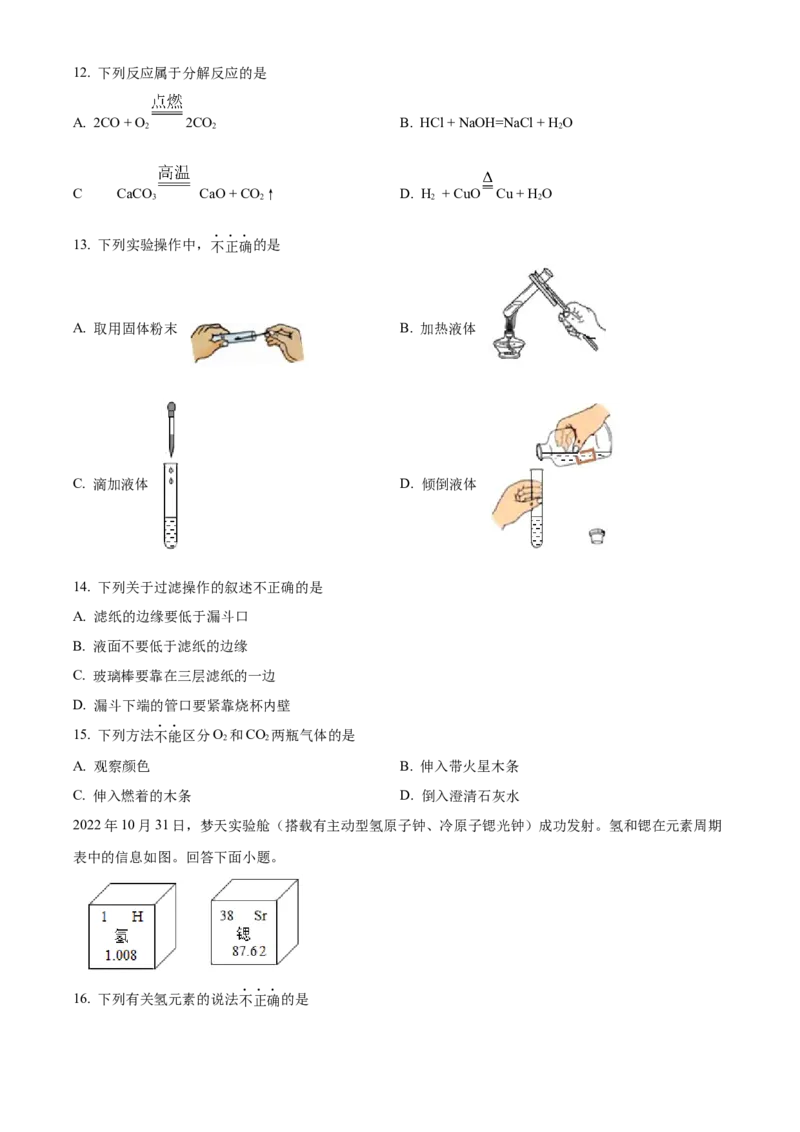
3 2 5 312. 下列反应属于分解反应的是
A. 2CO + O 2CO B. HCl + NaOH=NaCl + H O
2 2 2
C . CaCO CaO + CO ↑ D. H + CuO Cu + H O
3 2 2 2
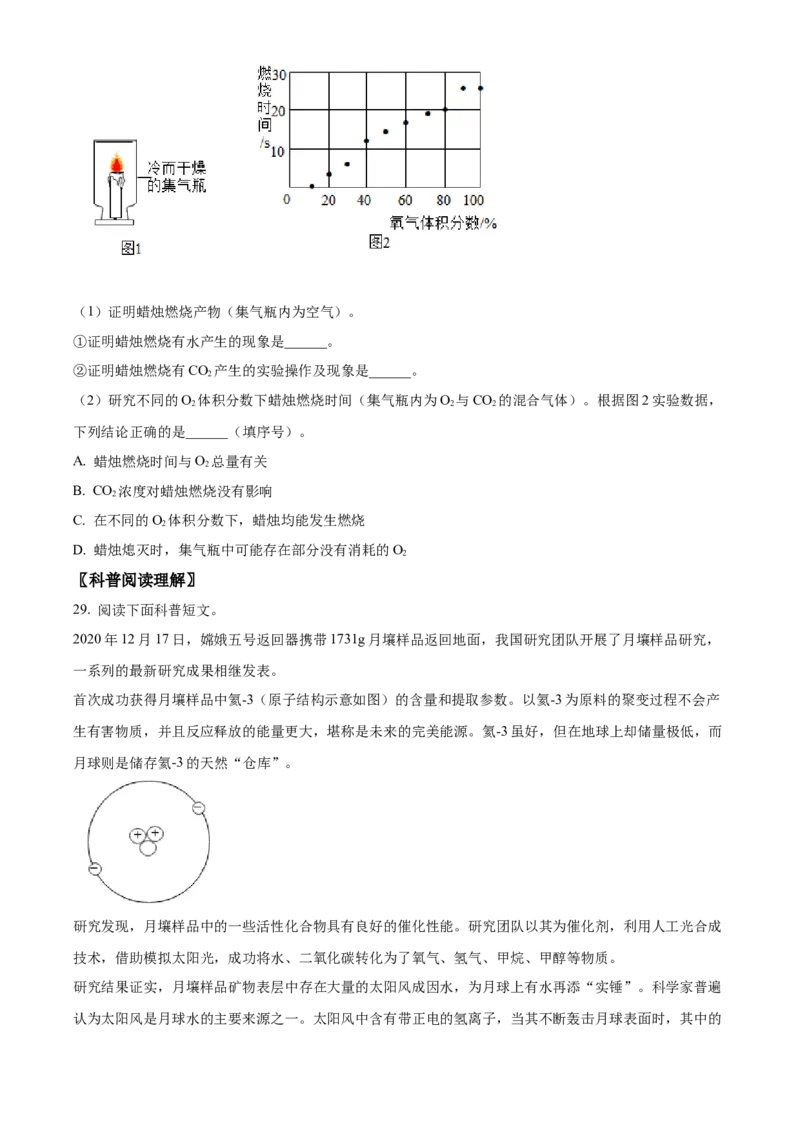
13. 下列实验操作中,不正确的是
A. 取用固体粉末 B. 加热液体
C. 滴加液体 D. 倾倒液体
14. 下列关于过滤操作的叙述不正确的是
A. 滤纸的边缘要低于漏斗口
B. 液面不要低于滤纸的边缘
C. 玻璃棒要靠在三层滤纸的一边
D. 漏斗下端的管口要紧靠烧杯内壁
15. 下列方法不能区分O 和CO 两瓶气体的是
2 2
A. 观察颜色 B. 伸入带火星木条
C. 伸入燃着的木条 D. 倒入澄清石灰水
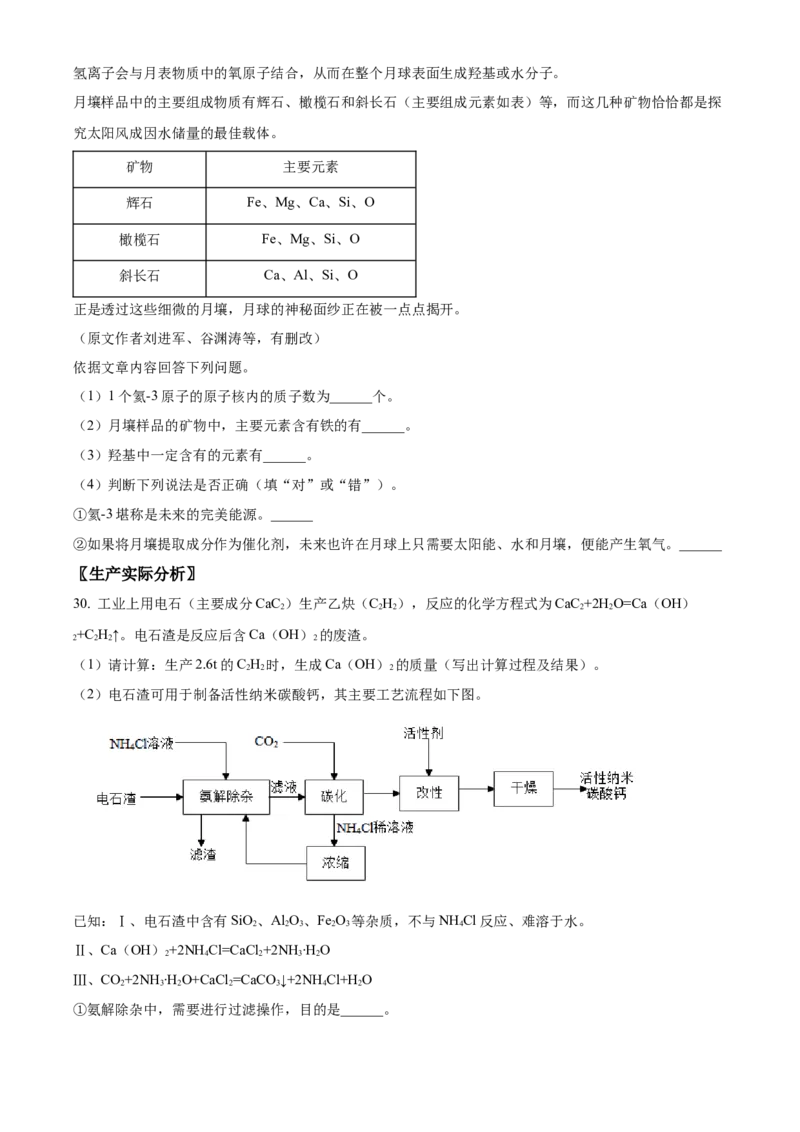
2022年10月31日,梦天实验舱(搭载有主动型氢原子钟、冷原子锶光钟)成功发射。氢和锶在元素周期
表中的信息如图。回答下面小题。
16. 下列有关氢元素的说法不正确的是A. 原子序数是1 B. 属于非金属元素
C. 元素符号是H D. 1个氢原子的质量为1.008 g
17. 1个锶原子的核外电子数是
A. 36 B. 38 C. 50 D. 88
18. 氢元素与锶元素的本质区别是
A. 质子数不同 B. 电子数不同 C. 中子数不同 D. 原子质量不同
19. 下列元素的元素符号书写不正确的是
A. 铜 Cu B. 钾 K C. 锌 Xn D. 汞 Hg
20. 下列符号中,既能表示一种元素,又能表示一个原子的是
A. H B. 2H+ C. H D. 2H
2
21. 下列物质的化学式书写正确的是
A. 氧化镁 MgO B. 硫酸 SO
2 4
C. 氯化钠 NaCl D. 碳酸钠 NaCO
3
22. 从化学式“SO ”中不能获取 的信息是
2
A. 表示二氧化硫这种物质 B. 二氧化硫有刺激性气味
C. 硫元素与氧元素质量比为1:1 D. 表示一个二氧化硫分子
23. 下列化学方程式书写不正确的是
A. C+O CO B. 2P+5O PO
2 2 2 2 5
C. CH+2O 2HO+CO D. CO+Ca(OH)=CaCO ↓+H O
4 2 2 2 2 2 3 2
24. 下列关于2H+O 2HO的说法不正确的是
2 2 2
A. 表示氢气与氧气在点燃条件下反应生成水
B. 参加反应的氢气和氧气的分子个数比为2:1
C. 反应前后原子总个数不变
D. 反应前后氢气、氧气、水之间的质量比为1:16:18
25. 氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如下、下列说法不正确
的是A. 甲中氮、氢原子个数比为1:3
为
B. 丙 NO分子
C. 反应前后甲和丙中氮元素质量相等
D. 生成的丙和丁的分子个数比为1:2
第二部分
本部分共11题,共45分。
〖生活现象解释〗
26. 空气是一种重要的自然资源。
(1)空气的成分中,体积分数最大的是______。
(2)O 具有重要的作用,请举一例说明O 具有的用途及体现的化学性质:______。
2 2
(3)空气中含有一定量的水蒸气,是自然界水循环的重要组成部分。水由液体变为水蒸气,用分子的观
点解释发生改变的是______。
(4)现代大气发展形成的前期,地球温度高,大气中水蒸气和CO 含量高;后期,地球温度降低,使很
2
大一部分CO 转化为碳酸盐岩,水中溶解CO 量也不断增多。CO 转化为CaCO 过程中碳元素化合价
2 2 2 3
______(填“发生”或“未发生”)改变,CO 与水反应的化学方程式为______。
2
27. 烙画是通过控制烙铁的温度在木质材料、宣纸、丝绢上烫出黑、焦、褐等不同颜色而作的画。
(1)在木质材料上烫出黑色的画,此过程发生的是______(填“物理”或“化学”)变化。
(2)烙画创作时,木质材料没有燃烧,原因是______。
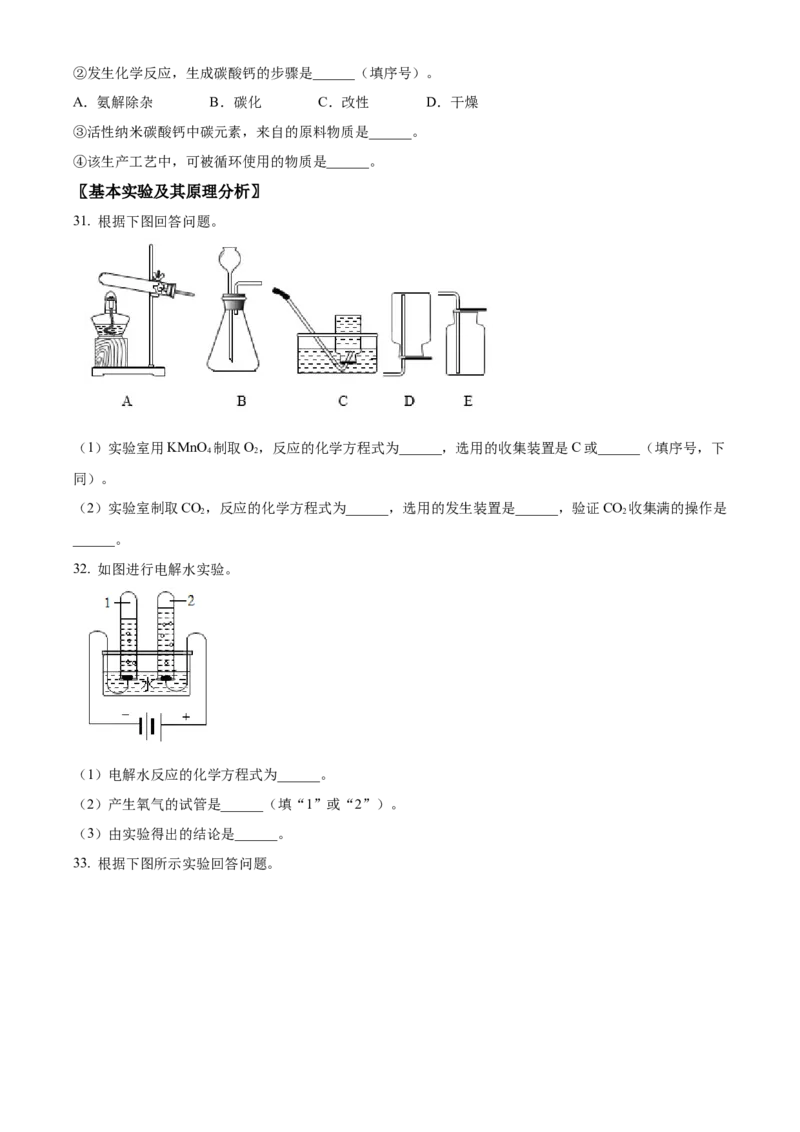
28. 用图1装置进行蜡烛燃烧的实验。(1)证明蜡烛燃烧产物(集气瓶内为空气)。
①证明蜡烛燃烧有水产生的现象是______。
②证明蜡烛燃烧有CO 产生的实验操作及现象是______。
2
(2)研究不同的O 体积分数下蜡烛燃烧时间(集气瓶内为O 与CO 的混合气体)。根据图2实验数据,
2 2 2
下列结论正确的是______(填序号)。
A. 蜡烛燃烧时间与O 总量有关
2
B. CO 浓度对蜡烛燃烧没有影响
2
C. 在不同的O 体积分数下,蜡烛均能发生燃烧
2
D. 蜡烛熄灭时,集气瓶中可能存在部分没有消耗的O
2
〖科普阅读理解〗
29. 阅读下面科普短文。
2020年12月17日,嫦娥五号返回器携带1731g月壤样品返回地面,我国研究团队开展了月壤样品研究,
一系列的最新研究成果相继发表。
首次成功获得月壤样品中氦-3(原子结构示意如图)的含量和提取参数。以氦-3为原料的聚变过程不会产
生有害物质,并且反应释放的能量更大,堪称是未来的完美能源。氦-3虽好,但在地球上却储量极低,而
月球则是储存氦-3的天然“仓库”。
研究发现,月壤样品中的一些活性化合物具有良好的催化性能。研究团队以其为催化剂,利用人工光合成
技术,借助模拟太阳光,成功将水、二氧化碳转化为了氧气、氢气、甲烷、甲醇等物质。
研究结果证实,月壤样品矿物表层中存在大量的太阳风成因水,为月球上有水再添“实锤”。科学家普遍
认为太阳风是月球水的主要来源之一。太阳风中含有带正电的氢离子,当其不断轰击月球表面时,其中的氢离子会与月表物质中的氧原子结合,从而在整个月球表面生成羟基或水分子。
月壤样品中的主要组成物质有辉石、橄榄石和斜长石(主要组成元素如表)等,而这几种矿物恰恰都是探
究太阳风成因水储量的最佳载体。
矿物 主要元素
辉石 Fe、Mg、Ca、Si、O
橄榄石 Fe、Mg、Si、O
斜长石 Ca、Al、Si、O
正是透过这些细微的月壤,月球的神秘面纱正在被一点点揭开。
(原文作者刘进军、谷渊涛等,有删改)
依据文章内容回答下列问题。
(1)1个氦-3原子的原子核内的质子数为______个。
(2)月壤样品的矿物中,主要元素含有铁的有______。
(3)羟基中一定含有的元素有______。
(4)判断下列说法是否正确(填“对”或“错”)。
①氦-3堪称是未来的完美能源。______
②如果将月壤提取成分作为催化剂,未来也许在月球上只需要太阳能、水和月壤,便能产生氧气。______
〖生产实际分析〗
30. 工业上用电石(主要成分CaC )生产乙炔(C H),反应的化学方程式为CaC +2H O=Ca(OH)
2 2 2 2 2
+C H↑。电石渣是反应后含Ca(OH) 的废渣。
2 2 2 2
(1)请计算:生产2.6t的C H 时,生成Ca(OH) 的质量(写出计算过程及结果)。
2 2 2
(2)电石渣可用于制备活性纳米碳酸钙,其主要工艺流程如下图。
已知:Ⅰ、电石渣中含有SiO、Al O、Fe O 等杂质,不与NH Cl反应、难溶于水。
2 2 3 2 3 4
Ⅱ、Ca(OH)+2NHCl=CaCl +2NH∙H O
2 4 2 3 2
Ⅲ、CO+2NH∙H O+CaCl =CaCO ↓+2NHCl+H O
2 3 2 2 3 4 2
①氨解除杂中,需要进行过滤操作,目的是______。②发生化学反应,生成碳酸钙的步骤是______(填序号)。
A.氨解除杂 B.碳化 C.改性 D.干燥
③活性纳米碳酸钙中碳元素,来自的原料物质是______。
④该生产工艺中,可被循环使用的物质是______。
〖基本实验及其原理分析〗
31. 根据下图回答问题。
(1)实验室用KMnO 制取O,反应的化学方程式为______,选用的收集装置是C或______(填序号,下
4 2
同)。
(2)实验室制取CO,反应的化学方程式为______,选用的发生装置是______,验证CO 收集满的操作是
2 2
______。
32. 如图进行电解水实验。
(1)电解水反应的化学方程式为______。
(2)产生氧气的试管是______(填“1”或“2”)。
(3)由实验得出的结论是______。
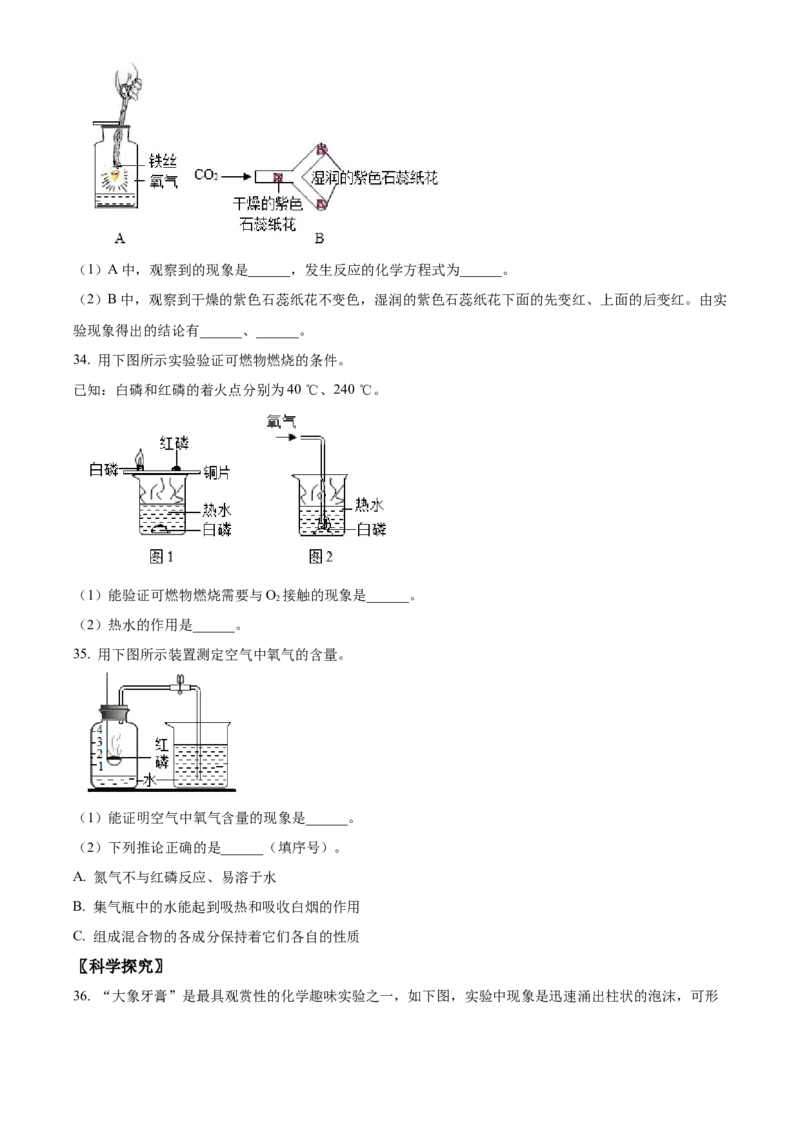
33. 根据下图所示实验回答问题。(1)A中,观察到的现象是______,发生反应的化学方程式为______。
(2)B中,观察到干燥的紫色石蕊纸花不变色,湿润的紫色石蕊纸花下面的先变红、上面的后变红。由实
验现象得出的结论有______、______。
34. 用下图所示实验验证可燃物燃烧的条件。
已知:白磷和红磷的着火点分别为40℃、240℃。
(1)能验证可燃物燃烧需要与O 接触的现象是______。
2
(2)热水的作用是______。
35. 用下图所示装置测定空气中氧气的含量。
(1)能证明空气中氧气含量的现象是______。
(2)下列推论正确的是______(填序号)。
A. 氮气不与红磷反应、易溶于水
B. 集气瓶中的水能起到吸热和吸收白烟的作用
C. 组成混合物的各成分保持着它们各自的性质
〖科学探究〗
36. “大象牙膏”是最具观赏性的化学趣味实验之一,如下图,实验中现象是迅速涌出柱状的泡沫,可形象地称为“大象牙膏”。
(1)该实验原理主要是HO 在催化剂作用下迅速分解产生水和氧气,反应的化学方程式为______。
2 2
【实验探究】实验小组用500 mL平底烧瓶对“大象牙膏”喷射、成形的影响因素进行研究。数据如下:
现象
实
HO HO
验 2 2 2 2 催化剂 发泡剂种类及 是是
溶液浓 溶液体
序 种类 体积/mL 否 否
度/% 积/mL 其他
号 喷 成
射 形
① 30 80 KI溶液 皂液/20 否 否 泡沫缓慢流出
② 30 80 KI溶液 洗衣液/20 否 否 泡沫缓慢流出
③ 30 80 KI溶液 洗洁精/20 否 否 泡沫大量涌出
CuSO 溶
④ 30 80 4 洗洁精/20 否 否 无明显反应现象
液
FeCl 溶 反应激烈,来不及形
⑤ 30 80 3 洗洁精/20 是 否
液 成泡沫
KMnO
⑥ 30 x 4 洗洁精/20 是 是 反应快,喷射时间短
溶液
⑦ 50 50 KI溶液 洗洁精/20 是 是 喷射力度不足
喷射力强、时间长且
⑧ 50 50 KI溶液 洗洁精/12 是 是
连续
⑨ 50 50 KI溶液 洗洁精/10 是 是 喷射最高,但不连续
【解释与结论】
(2)实验①②③探究的影响因素是______。
(3)实验⑥中,HO 溶液体积x为______mL。
2 2
(4)该探究中,能使HO 的分解较长时间进行的催化剂是______。
2 2
(5)依据实验数据分析,实验③没有喷射、没有成形的最主要原因是______。(6)实验探究得出,实验效果最好的实验是______(填序号,下同)。
【反思与评价】
(7)实验中,还需要控制的实验条件是______。
A. 催化剂用量 B. 温度 C. 催化剂溶液的颜色