文档内容
辽宁省重点高中沈阳市郊联体
2024~2025 学年度上学期 10 月月考高三年级试题
化学
命题人:沈阳市第五十六中学 桓静静 审题人:康平县高级中学 赵明月
考试时间75分钟 试卷总分:100分
可能用到的相对原子质量:
第Ⅰ卷 选择题(45分)
一、单选题(每小题只有一个正确选项,共15小题,每题3分,共45分)
1.党的二十大报告指出“推动绿色发展,促进人与自然和谐共生”。下列做法不合理的是( )。
A.开发利用天然纤维,停止使用合成材料 B.多采用太阳能风能发电,减少火力发电
C.研发新能源汽车,降低汽油柴油消耗 D.研究开发生物农药,减少作物农药残留
2.下列反应不符合哲学中“量变引起质变”观点的是( )。
A.锌与硫酸 B.过氧化钠和
C. 溶液和氯水 D.铜和硝酸
3.元素及其化合物的转化在工业生产中具有极其重要的用途。下列物质间转化能实现的是( )。
A.用Fe制取 :
B.工业尾气中的 处理:
C.工业制取漂白粉:饱和食盐水 漂白粉
D.铝土矿制铝:铝土矿 Al
4.室温下,根据下列实验操作及现象得出的实验结论正确的是( )。
选项 实验操作及现象 实验结论
A 向 溶液中滴加几滴溴水, 非金属性:Br>S
振荡,产生乳白色浑浊
B 向 溶液中滴加酸性 溶
溶液具有漂白性
液,溶液紫红色褪去
用洁净的嵌有铂丝的玻璃棒蘸取某溶液在酒精灯火
C 该溶液中一定不含钾元素
焰上灼烧,火焰颜色呈黄色
向盛有等体积、等浓度的 溶液的两支试管中分
D
别加入 等浓度的 溶液和 溶 比 的催化效果好
液,加 溶液的试管中产生气泡的速率更快
A.A B.B C.C D.D5.实验改进与优化应遵循科学性、易操作性、安全性的原则,提升化学实验效率。下列有关实验改进分
析不正确的是( )。
A、使用恒压滴液漏斗可防止浓氨水污染环境,并使漏斗内液体顺利流下
B.用点燃的木条靠近肥皂泡,听到爆鸣声,可检验产物中有氢气
C.利用该装置可制取 ,并进行 性质的探究实验
D.利用该装置可较长时间看到白色絮状沉淀
6.这周末,高中生小汪帮家里做家务。下列劳动项目与所涉及的化学原理不相符的是( )。
选项 劳动项目 化学原理
A 用盐卤和豆浆制作豆腐 胶体的聚沉
B 用加水稀释的“84”消毒液拖地面 氧化还原反应
C 用白醋清洗水壶中的水垢 分解反应
D 用热的纯碱溶液洗涤餐具 水解反应
A.A B.B C.C D.D
7.我国化工专家侯德榜将合成氨与纯碱工业联合,发明了联合制碱法,使原料氯化钠的利用率从70%提
高到90%以上,该生产方法在制得纯碱的同时,还可得到一种副产品 。生产流程和溶解度曲线如
图,下列说法错误的是( )。
A. 固体从母液中析出时需控制温度在0~10℃
B.从母液中经过循环1进入沉淀池的主要是 、 和氨水
C.沉淀池中反应的化学方程式:
D.循环Ⅰ、Ⅱ的目的是提高原料的利用率、减少对环境的污染
8.工业上从废旧金属中回收金属Co时,有一步操作是加入碳酸氢钠或碳酸氢铵溶液“沉钴”,离子方程
式为: 。下列有关说法不正确的是( )。A.该反应之所以能发生,原因是 与 结合生成难溶电解质促进了 的电离
B.“沉钴”后,还要进行的操作为过滤、干燥
C.“沉钴”时不用 的原因是:防止碱性比较强时生成 ,降低产率
D.“沉钴”时通入适量 效果更好,是因为发生了反应:
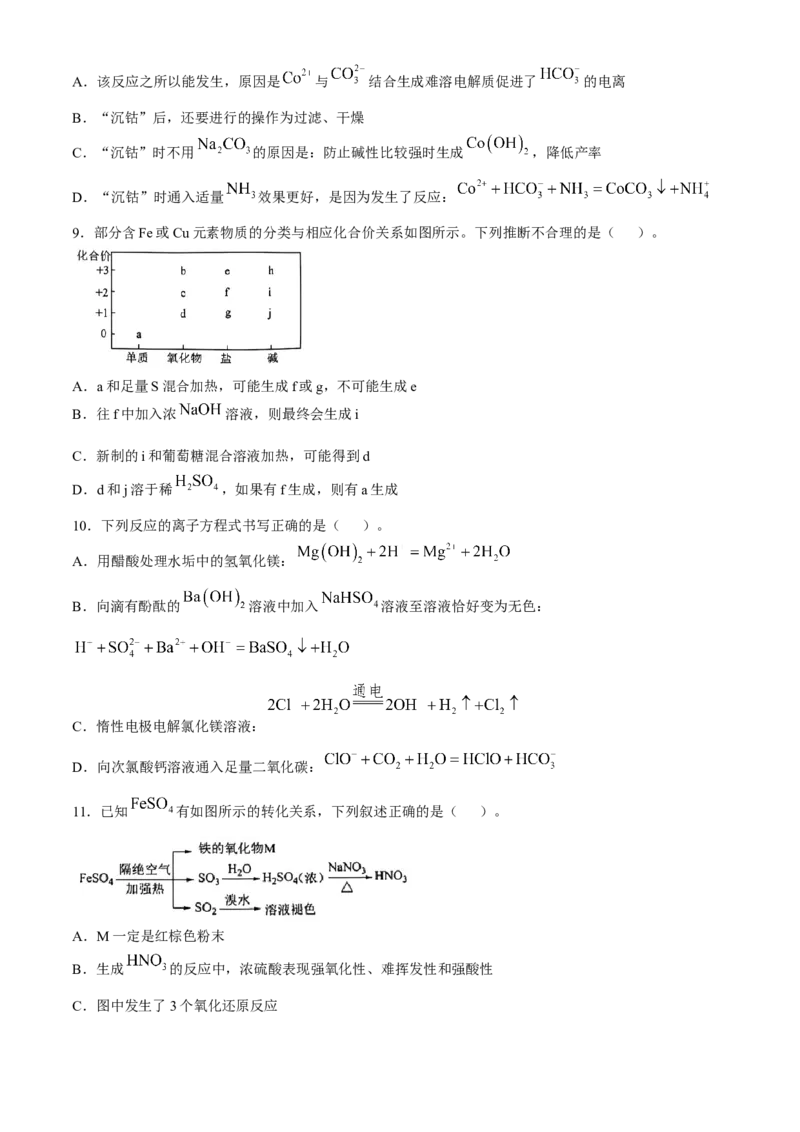
9.部分含Fe或Cu元素物质的分类与相应化合价关系如图所示。下列推断不合理的是( )。
A.a和足量S混合加热,可能生成f或g,不可能生成e
B.往f中加入浓 溶液,则最终会生成i
C.新制的i和葡萄糖混合溶液加热,可能得到d
D.d和j溶于稀 ,如果有f生成,则有a生成
10.下列反应的离子方程式书写正确的是( )。
A.用醋酸处理水垢中的氢氧化镁:
B.向滴有酚酞的 溶液中加入 溶液至溶液恰好变为无色:
C.惰性电极电解氯化镁溶液:
D.向次氯酸钙溶液通入足量二氧化碳:
11.已知 有如图所示的转化关系,下列叙述正确的是( )。
A.M一定是红棕色粉末
B.生成 的反应中,浓硫酸表现强氧化性、难挥发性和强酸性
C.图中发生了3个氧化还原反应D.“褪色”的原因是
12.下列各组离子能大量共存,通入 后,不能大量共存的是( )。
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
13.通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一。下列实验操作、现象和
解释或结论不正确的有( )。
序号 实验操作 实验现象 解释或结论
用大理石和稀硝酸反应制取 气 的酸性比
① 体,将制得的气体立即通入一定浓 出现白色沉淀
的酸性强
度的 溶液中
放出刺激性气味
向某溶液中加入浓 溶液后微
② 热,用蓝色石蕊试纸检验产生的气 气体且试纸变红 原溶液中一定含有
体
少量铝热剂(只有一种金属氧化 出现蓝色沉淀和 铝热剂中可能含有
③ 物)溶于足量稀盐酸后,分两份, 血红色
再分别滴加铁氰化钾和KSCN溶液
向某钾盐中滴加浓盐酸,产生的气
该钾盐为 与
④ 体再通入品红溶液 品红溶液褪色
至少有一种
pH试纸先变为 饱和新制氯水呈酸性且
⑤ 用pH试纸测量饱和新制氯水的pH 红色后褪色
具有漂白性
A.①③④ B.②④⑤ C.①②④⑤ D.①②③⑤
14.工业上常用纯碱溶液吸收尾气中的NO、 ,反应如下:
反应1:
反应2:
已知: 与水的反应类似 和 的反应。若 代表阿伏加德罗常数的值。
下列叙述正确的是( )。
A.反应1中放出 时,NO、 参与反应的总分子数为
B. 溶液恰好完全反应时,作氧化剂的分子数为
C.将反应2中 完全反应产生的 通入足量水中生成的 分子数为
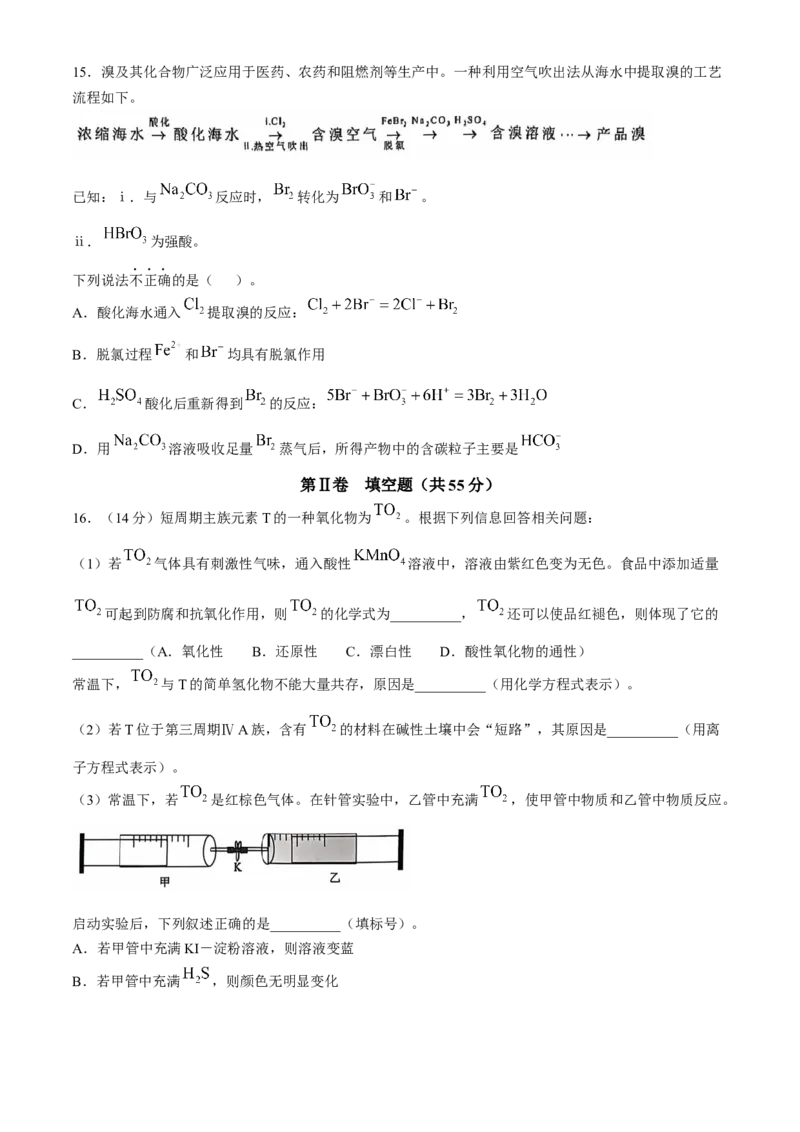
D.上述制备的化工品( 、 )中含N元素的质量为 ,则所含的 数一定为15.溴及其化合物广泛应用于医药、农药和阻燃剂等生产中。一种利用空气吹出法从海水中提取溴的工艺
流程如下。
已知:ⅰ.与 反应时, 转化为 和 。
ⅱ. 为强酸。
下列说法不正确的是( )。
A.酸化海水通入 提取溴的反应:
B.脱氯过程 和 均具有脱氯作用
C. 酸化后重新得到 的反应:
D.用 溶液吸收足量 蒸气后,所得产物中的含碳粒子主要是
第Ⅱ卷 填空题(共55分)
16.(14分)短周期主族元素T的一种氧化物为 。根据下列信息回答相关问题:
(1)若 气体具有刺激性气味,通入酸性 溶液中,溶液由紫红色变为无色。食品中添加适量
可起到防腐和抗氧化作用,则 的化学式为__________, 还可以使品红褪色,则体现了它的
__________(A.氧化性 B.还原性 C.漂白性 D.酸性氧化物的通性)
常温下, 与T的简单氢化物不能大量共存,原因是__________(用化学方程式表示)。
(2)若T位于第三周期ⅣA族,含有 的材料在碱性土壤中会“短路”,其原因是__________(用离
子方程式表示)。
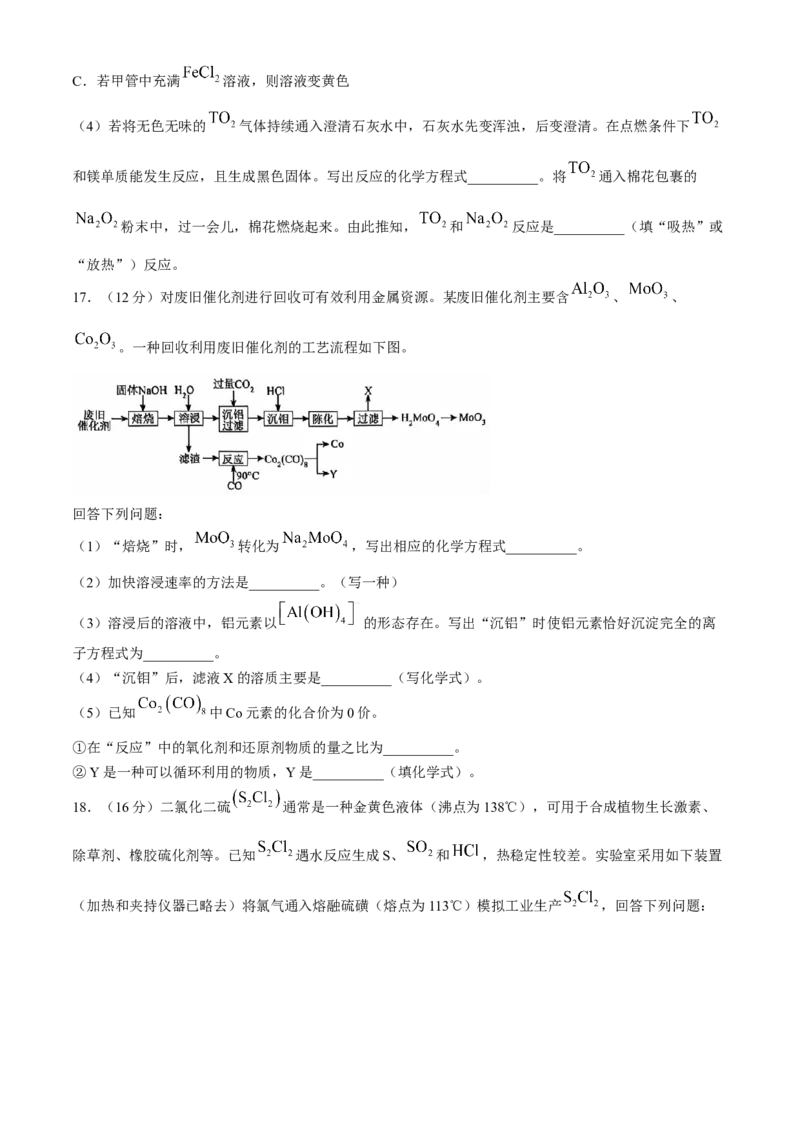
(3)常温下,若 是红棕色气体。在针管实验中,乙管中充满 ,使甲管中物质和乙管中物质反应。
启动实验后,下列叙述正确的是__________(填标号)。
A.若甲管中充满KI-淀粉溶液,则溶液变蓝
B.若甲管中充满 ,则颜色无明显变化C.若甲管中充满 溶液,则溶液变黄色
(4)若将无色无味的 气体持续通入澄清石灰水中,石灰水先变浑浊,后变澄清。在点燃条件下
和镁单质能发生反应,且生成黑色固体。写出反应的化学方程式__________。将 通入棉花包裹的
粉末中,过一会儿,棉花燃烧起来。由此推知, 和 反应是__________(填“吸热”或
“放热”)反应。
17.(12分)对废旧催化剂进行回收可有效利用金属资源。某废旧催化剂主要含 、 、
。一种回收利用废旧催化剂的工艺流程如下图。
回答下列问题:
(1)“焙烧”时, 转化为 ,写出相应的化学方程式__________。
(2)加快溶浸速率的方法是__________。(写一种)
(3)溶浸后的溶液中,铝元素以 的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离
子方程式为__________。
(4)“沉钼”后,滤液X的溶质主要是__________(写化学式)。
(5)已知 中Co元素的化合价为0价。
①在“反应”中的氧化剂和还原剂物质的量之比为__________。
②Y是一种可以循环利用的物质,Y是__________(填化学式)。
18.(16分)二氯化二硫 通常是一种金黄色液体(沸点为138℃),可用于合成植物生长激素、
除草剂、橡胶硫化剂等。已知 遇水反应生成S、 和 ,热稳定性较差。实验室采用如下装置
(加热和夹持仪器已略去)将氯气通入熔融硫磺(熔点为113℃)模拟工业生产 ,回答下列问题:(1)写出A中制取氯气的离子方程式__________。
(2)装置接口从左到右的顺序为:a→__________(填小写字母)。
(3)仪器m的名称是__________,所装碱石灰的作用是__________。
(4)打开 ,通一段时间 ,原因是__________;实验结束时,装置B中烧瓶底部有少量硫附着,可
用热的 浓溶液洗涤,该反应的离子方程式为__________。
(5)证明实验中有 生成的现象是__________。
(6)某同学查阅资料发现:采用 和 在95~100℃之间反应,也能得到 和一种常用作有机溶
剂的副产物,该反应的化学方程式为__________。
19.(13分) 、 为常见的空气污染物,会引起酸雨、光化学烟雾等污染问题。研究者以多种方
法进行“脱硫”“脱硝”。
(1)利用工业废碱渣(主要成分为 )来吸收含 的烟气,同时得到 粗品。其流程如
图所示:
①操作1和操作2中均包含的分离技术为__________。(1分)
② 被 溶液吸收时,会释放出一种无色无味气体,该气体是__________(填化学式)。
(2)利用含有 的烟气制备 。其流程如图所示:
①反应a的化学方程式为__________。②反应b中的氧化剂和还原剂的物质的量之比为__________。
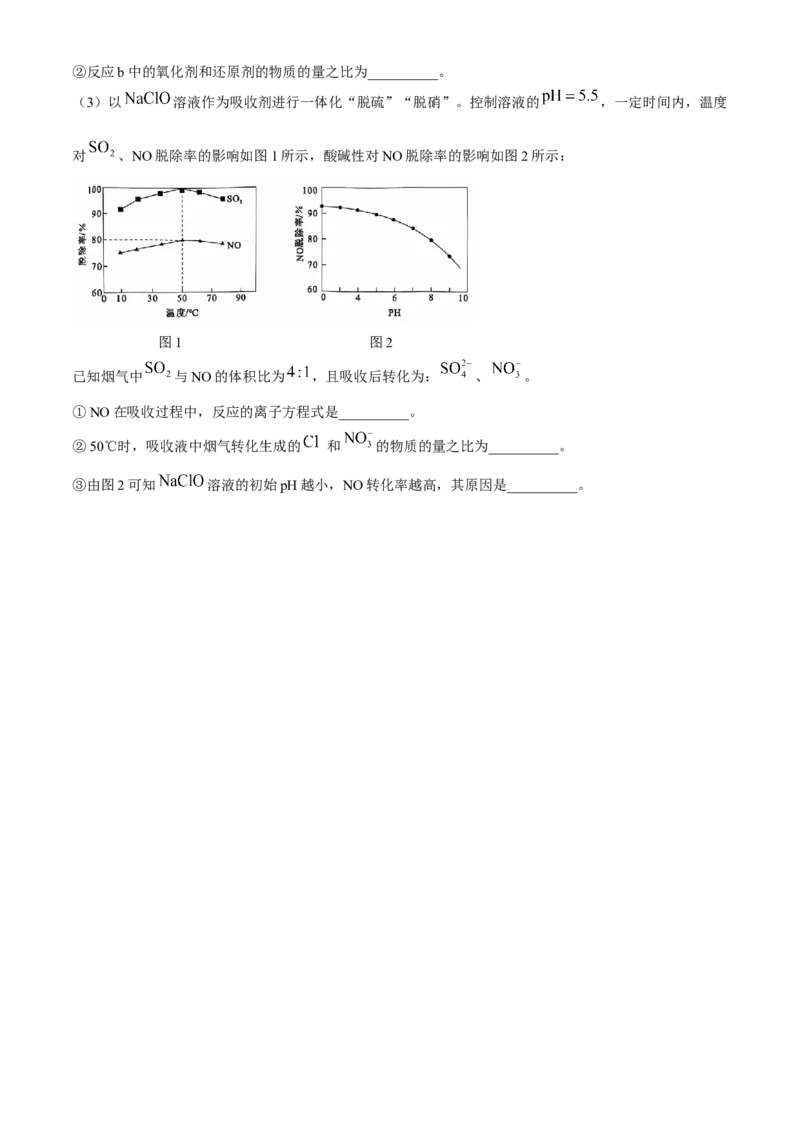
(3)以 溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的 ,一定时间内,温度
对 、NO脱除率的影响如图1所示,酸碱性对NO脱除率的影响如图2所示:
图1 图2
已知烟气中 与NO的体积比为 ,且吸收后转化为: 、 。
①NO在吸收过程中,反应的离子方程式是__________。
②50℃时,吸收液中烟气转化生成的 和 的物质的量之比为__________。
③由图2可知 溶液的初始pH越小,NO转化率越高,其原因是__________。2024~2025 学年度上学期郊联体高三 10 月月考
化学试题参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A B C A C C C B B D D D C B D
16.(14分)
(1) C
(2)
(3)AC
(4) 放热
17.(12分)
(1)
(2)适当升高溶液温度,搅拌等(答对一条即得满分,有错不得分)
(3)
(4)
(5) CO
18.(16分)
(1)
(2)hi→fg→bc→jk(或kj)→de
(3)球形干燥管 吸收多余的氯气,防止空气中的水蒸气进入装置,导攻产率下降(两点,每对一点
得1分)
(4)将整个装置中的空气排尽,避免加热时硫磺与氧气反应
(5)装置B或F中有金黄色液体生成
(6)19.(13分)
(1)过滤(1分)
(2)
(3)
溶液pH越小,溶液中 的浓度越大,氧化NO的能力越强