文档内容
(2)氮及其化合物—高一化学人教版暑假作业本
1.下列反应属于氮的固定的是( )
A.工业上用氮气与氢气合成氨 B. 和HCl反应制取
C.氯化铵与烧碱的复分解反应 D.空气中的氮氧化物转化成酸雨
2.硝酸被称为“国防工业之母”,是因为它是制取炸药的重要原料。下列实验事实与硝酸的
性质不相对应的是( )
A.浓硝酸使紫色石蕊溶液先变红后褪色——酸性和强氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液的红色褪去——强氧化性
3.如图所示,干燥烧瓶内有某种气体,烧杯和滴管内盛放某种溶液。挤压胶头滴管,与实验
事实不相符的是( )
A.HCl( 溶液)/白色喷泉 B. ( 中含酚酞)/红色喷泉
C. (NaOH溶液)/无色喷泉 D. ( 溶液)/无色喷泉
4.某化学兴趣小组用如图1装置探究氨气喷泉实验中三颈烧瓶内压强变化。图1中的三颈烧瓶
收集满氨气后关闭 ,用在冰水中浸泡后的湿毛巾敷在三颈烧瓶上,50s时拿走毛巾并打开
,整个过程中测得三颈烧瓶内压强变化曲线如图2。下列说法正确的是( )
A.固体X可选择 ,试剂a可选择浓氨水B.20s~50s时,氨气发生化学反应导致三颈烧瓶内压强减小
C.70s时,三颈烧瓶内的喷泉现象最明显
D.固体X和试剂a分别为锌片和稀硫酸时,实验过程中也能观察到喷泉现象
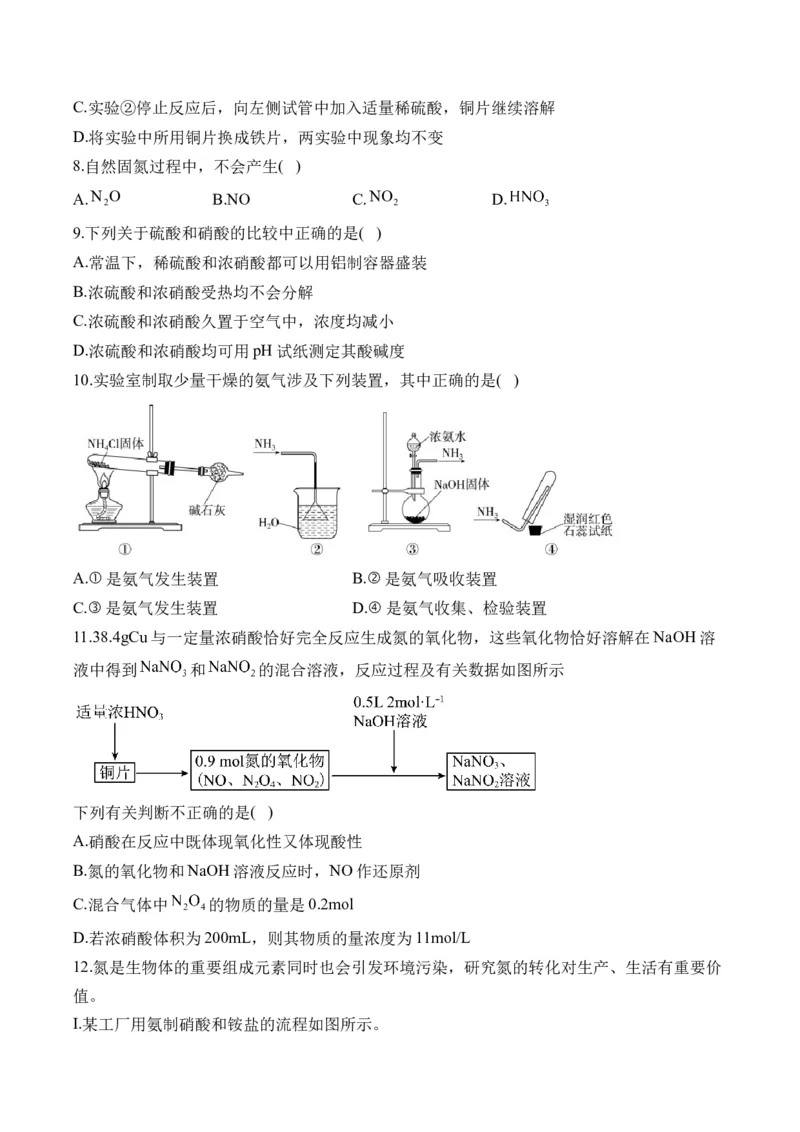
5.工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如下图所示:( )
下列说法错误的是
A.过程①属于氮的固定
B.氮气在足量氧气中也可以通过一步反应生成
C.过程④反应中氧化剂与还原剂的物质的量之比为1:2
D.反应①②③④都是氧化还原反应
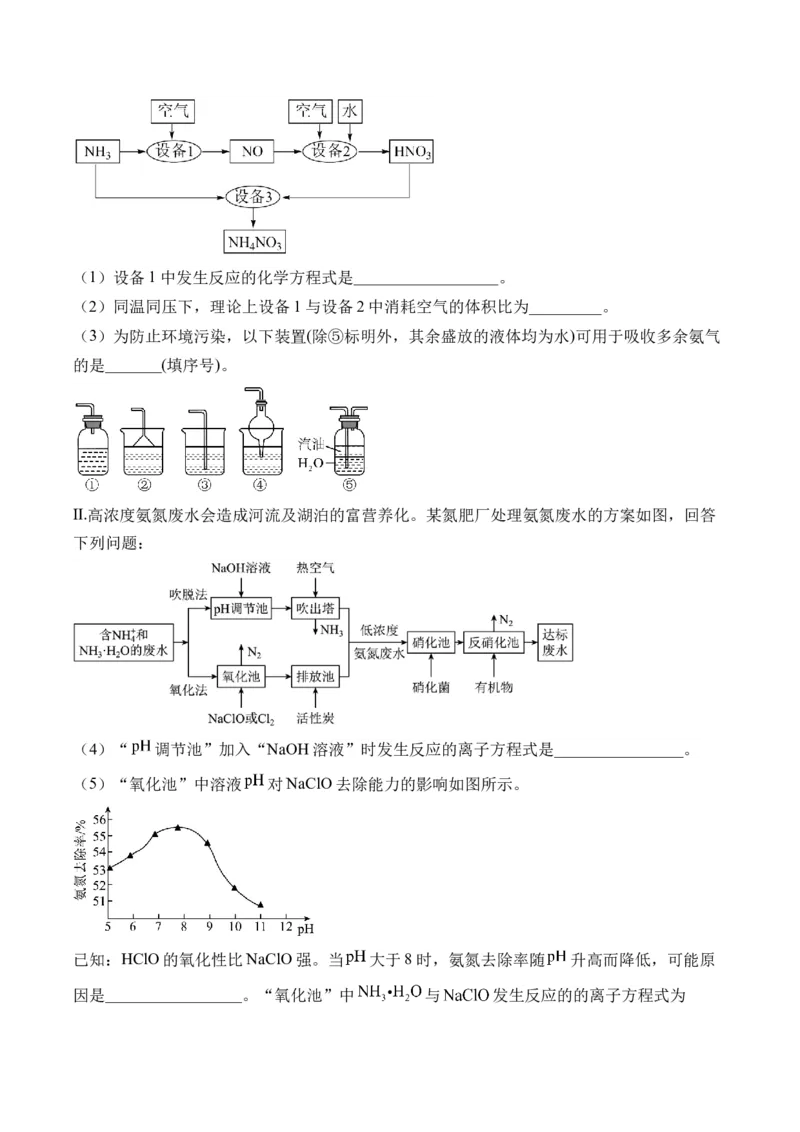
6.沸石分子筛选择性催化还原NO的循环过程如图所示。下列说法正确的是( )
A.反应过程中催化剂 未参与电子得失
B.步骤一中 与 的物质的量之比为2:1
C.每生成 理论上消耗
D.所有步骤均有氧化还原反应发生
7.化学兴趣小组按如图所示装置,用过量的铜分别与等物质的量的浓硝酸、稀硝酸反应(实
验前原试管中充满 ),下列叙述正确的是( )
A.实验①②生成气体的物质的量相等
B.实验②左侧试管中有红棕色气体生成C.实验②停止反应后,向左侧试管中加入适量稀硫酸,铜片继续溶解
D.将实验中所用铜片换成铁片,两实验中现象均不变
8.自然固氮过程中,不会产生( )
A.N O B.NO C.NO D.
2 2
9.下列关于硫酸和硝酸的比较中正确的是( )
A.常温下,稀硫酸和浓硝酸都可以用铝制容器盛装
B.浓硫酸和浓硝酸受热均不会分解
C.浓硫酸和浓硝酸久置于空气中,浓度均减小
D.浓硫酸和浓硝酸均可用pH试纸测定其酸碱度
10.实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )
A.①是氨气发生装置 B.②是氨气吸收装置
C.③是氨气发生装置 D.④是氨气收集、检验装置
11.38.4gCu与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶
液中得到 和 的混合溶液,反应过程及有关数据如图所示
下列有关判断不正确的是( )
A.硝酸在反应中既体现氧化性又体现酸性
B.氮的氧化物和NaOH溶液反应时,NO作还原剂
C.混合气体中 的物质的量是0.2mol
D.若浓硝酸体积为200mL,则其物质的量浓度为11mol/L
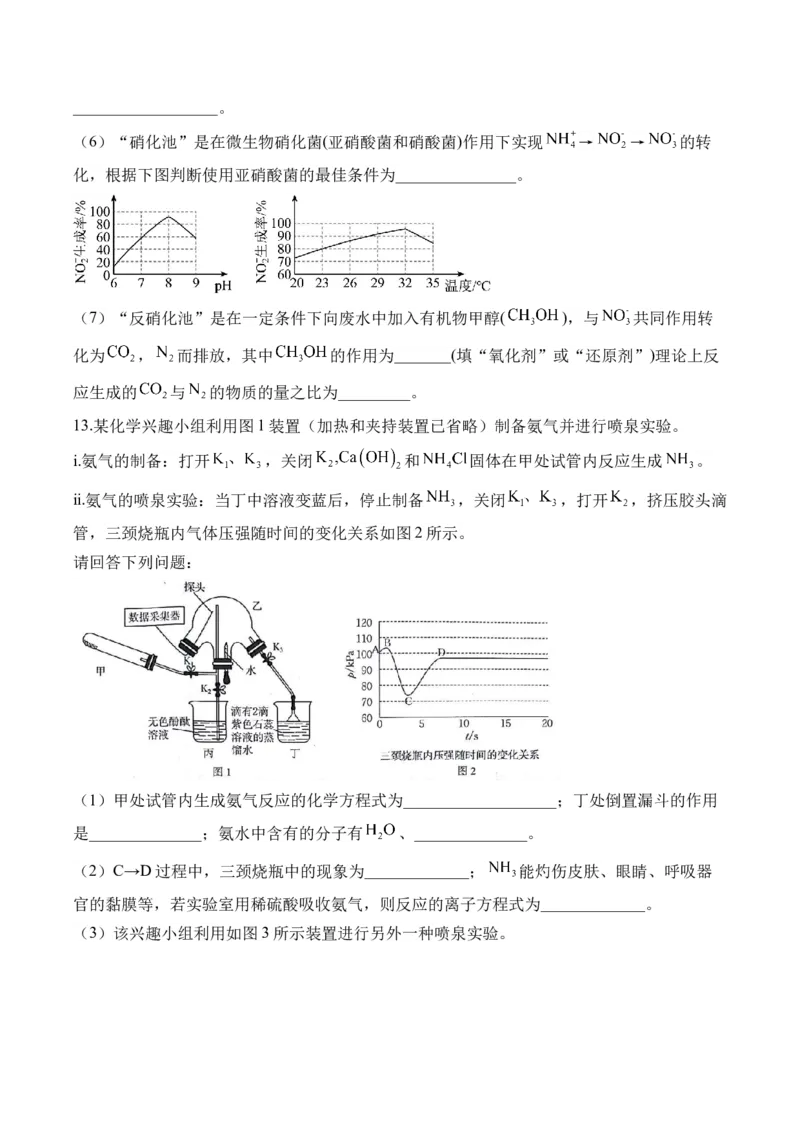
12.氮是生物体的重要组成元素同时也会引发环境污染,研究氮的转化对生产、生活有重要价
值。
I.某工厂用氨制硝酸和铵盐的流程如图所示。(1)设备1中发生反应的化学方程式是__________________。
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为_________。
(3)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气
的是_______(填序号)。
Ⅱ.高浓度氨氮废水会造成河流及湖泊的富营养化。某氮肥厂处理氨氮废水的方案如图,回答
下列问题:
(4)“ 调节池”加入“NaOH溶液”时发生反应的离子方程式是________________。
(5)“氧化池”中溶液 对NaClO去除能力的影响如图所示。
已知:HClO的氧化性比NaClO强。当 大于8时,氨氮去除率随 升高而降低,可能原
因是_________________。“氧化池”中 与 发生反应的的离子方程式为__________________。
(6)“硝化池”是在微生物硝化菌(亚硝酸菌和硝酸菌)作用下实现 → → 的转
化,根据下图判断使用亚硝酸菌的最佳条件为_______________。
(7)“反硝化池”是在一定条件下向废水中加入有机物甲醇( ),与 共同作用转
化为 , 而排放,其中 的作用为_______(填“氧化剂”或“还原剂”)理论上反
应生成的 与 的物质的量之比为_________。
13.某化学兴趣小组利用图1装置(加热和夹持装置已省略)制备氨气并进行喷泉实验。
i.氨气的制备:打开 ,关闭 和 固体在甲处试管内反应生成 。
ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备 ,关闭 ,打开 ,挤压胶头滴
管,三颈烧瓶内气体压强随时间的变化关系如图2所示。
请回答下列问题:
(1)甲处试管内生成氨气反应的化学方程式为___________________;丁处倒置漏斗的作用
是______________;氨水中含有的分子有 、______________。
(2)C→D过程中,三颈烧瓶中的现象为_____________; 能灼伤皮肤、眼睛、呼吸器
官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为_____________。
(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验。①锥形瓶中反应的离子方程式为_________________________。
②烧杯中发生反应 (未配平),该反应的氧化剂为
__________(填化学式),氧化产物和还原产物的物质的量之比为__________(填最简整数
比)。
14.A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的
转化关系如图所示(反应条件与部分反应的生成物略去)。
请回答下列问题:
(1)D的化学式为________,Y的化学式为________,E的化学式为________。
(2)Y与氧化铜反应,每生成1 mol B消耗3 mol氧化铜,该反应的化学方程式为
___________。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境
的污染,该反应的化学方程式为______________________________________________。
(4)气体F和气体 在通常条件下同时通入盛有 溶液的洗气瓶中(如图所示),洗气瓶中
是否有沉淀生成?________,理由是___________________________________________。答案以及解析
1.答案:A
2.答案:D
解析:向滴有酚酞的NaOH溶液中滴入硝酸,溶液红色褪去,利用的是硝酸的酸性。
3.答案:D
解析:A. ,AgCl为白色沉淀,能形成白色喷泉,故不选A;
B. 易溶于水,形成 , ,溶液呈碱性,能形成红色喷
泉,故不选B;
D. 与 不反应,烧瓶内的压强不变,不能形成喷泉,故选D;
答案选D。
4.答案:A
解析:A.CaO溶于水与水反应放出大量热,促使浓氨水分解放出大量氨气,故固体X可选择
,试剂a可选择浓氨水,A正确;
B.20s~50s时,氨气极易溶于水,导致三颈烧瓶内压强减小,为物理变化,B错误;
C.压强最小时,喷泉最剧烈,50s时压强最小,此时喷泉最剧烈,C错误;
D.锌片和稀硫酸反应生成氢气,氢气难溶于水且不和水反应,不能观察到喷泉现象,D错
误;
故选A。
5.答案:B
解析:过程①是 转化为 ,属于氮的固定,A正确;
在 中反应,只能生成NO,而不能直接产生 ,B错误;
过程④的反应为 ,该反应中 既作氧化剂,又作还原剂,由
化合价变化可知,氧化剂与还原剂的物质的量之比为1:2,C正确;
反应①②③④中都存在元素化合价变化,都属于氧化还原反应,D正确。
6.答案:C
7.答案:C解析:由反应 和
可知,当酸的物质的量相同时,生成气体的
物质的量:浓>稀,A项错误;实验②是铜片与稀硝酸反应,生成NO,NO为无色气体,B
项错误;实验②反应完全,向左侧试管中加入适量稀硫酸,补充 ,与溶液中剩余的 万
一起与铜片作用,铜片继续溶解,C项正确:将实验中所用铜片换成铁片,常温下,铁片遇
浓硝酸“钝化”,实验现象不同,D项错误。
8.答案:A
解析:自然固氮是指在闪电作用下,空气里的氮气转化为氮的化合物的过程,主要包括
放电
N O 2NO,NO遇到空气中的 : , 与空气中雨水接触:
2 2
O
2
,该过程中没有一氧化二氮的生成,A项符合题意;
故选A。
9.答案:C
解析:A.铝遇冷的浓硝酸发生钝化,因此可用铝制容器盛装,但稀硫酸可与铝发生置换反
应,A错误;
B.浓硫酸难分解,浓硝酸不稳定,受热会分解,B错误;
C.浓硫酸具有吸水性,久置于空气中浓度减小,浓硝酸具有挥发性,久置于空气中浓度也
减小,C正确;
D.浓硫酸具有脱水性,pH试纸无法测定其酸碱度,D错误;
故选C。
10.答案:C
解析:①装置在试管口处又生成 ,无法制得 ,A项错误;②装置漏斗插入水中,
不能防止倒吸,B项错误;③装置用浓氨水与NaOH固体作用,可制取 ,C项正确:利
用④装置收集 时,收集到的气体不纯,试管口应放一团干燥的棉花,D项错误。
11.答案:C
解析:A.铜与硝酸反应,部分硝酸中氮元素化合价降低,部分化合价不变,所以硝酸在反应
中既体现氧化性又体现酸性,故A正确;B.反应中一氧化氮中十2价氮元素化合价升高,所以一氧化氮为还原剂,故B正确;
C.氮的氧化物恰好溶解在NaOH溶液中得到 和 的混合溶液,氢氧化钠的物质的
量为1mol,氮氧化合物的物质的量为0.9mol,则收集的 物质的量为0.1mol,故C错
误;
D.铜和硝酸反应生成硝酸铜和氮的化合物, ,所以生成硝酸铜
0.6mol,含有硝酸根离子1.2mol,氮的化合物为0.9mol,与氢氧化钠怡好完全反应生成
和 ,根据原子守恒可知: ,则
硝酸的总量为 ,若浓硝酸体积为200mL,则其物质的量浓度为
,故D正确。
12.答案:(1)
(2)5:3
(3)② ④
(4)
(5)① 溶液碱性增强,HClO转化为氧化性弱的 ;
②
(6)pH=8、温度为32℃
(7)① 还原剂;② 5:3
解析:(1)设备1中发生反应氨气和氧气催化氧化生成NO和水,
;
(2)设备2中反应为: ,结合(1)分析,则同温同压下,理论
上设备1与设备2中消耗空气的体积比为5:3;
(3)氨气极易溶于水,氨气不能直接和水小面积接触防止倒吸,吸收氨气要有防止倒吸装
置,故选②④;
(4)“pH调节池”加入“ 溶液”时发生反应为铵根离子和氢氧根离子生成一水合氨,离子方程式是 ;
(5)溶液碱性增强,使得 和氢氧根离子反应转化为氧化性弱的 ,导致 大于8
时,氨氮去除率随 升高而降低;次氯酸根离子具有强氧化性,氧化一水合氨为氮气,同时
生成氯离子,反应中氮化合价由-3变为0、氯化合价由+1变为-1,结合
;
(6)由图可知, 、温度为 时,亚硝酸根离子的生成率最高,利于氮元素的转化
除去;
(7)有机物甲醇
CH OH
,与 共同作用转化为 , 而排放,反应中碳元素化合价升
3
高,故 的作用为还原剂;反应中碳化合价由-2变为+4、氮化合价由+5变为0,结合电
子守恒可知,理论上反应生成的 与 的物质的量之比为5:3。
13.答案:(1) ;防倒吸;
(2)产生红色喷泉;
(3)① ;② ;5:3
14.答案:(1) ; ;NO
(2)
(3)
(4)有;二氧化氮与水反应生成硝酸,硝酸可将二氧化硫或亚硫酸氧化成硫酸,硫酸与氯化钡
反应可生成硫酸钡沉淀
解析: E的相对分子质量比F小16,且F为红棕色,可确定E为NO,F为 ,C是 ,
综合题中信息知,Z是 ,G是 ,则D是 ,B是 ,Y是 ,A是 。
(2) 与CuO反应生成Cu、 和 ,每生成1 mol 消耗3 mol CuO,则反应的化学方
程式为 。
(4)二氧化氮与水反应生成硝酸,硝酸可将二氧化硫或亚硫酸氧化成硫酸,硫酸与氯化钡反应
生成硫酸钡沉淀。