文档内容
第 10 讲 酸碱中和滴定及其应用
模块一 思维导图串知识 1.知道滴定管的构造、用途以及使用方法。
模块二 基础知识全梳理 2.学会指示剂的选择并能判断滴定终点,能判断滴定过程中所
模块三 重点难点必掌握 产生的实验误差。
模块四 核心考点精准练 3.能通过酸碱中和滴定的方法测定酸或碱的浓度,掌握数据分
模块五 小试牛刀过关测 析与处理的方法,培养定量研究的意识。
一.酸碱中和滴定
概念 依据中和反应,用已知浓度的酸(或碱)来测定未知浓度的 碱 ( 或酸 )的方法
以HCl溶液为标准液,滴定待测液NaOH溶液为例:在中和反应中,酸提供的 H + 与碱提供的 OH -
原理
之间的物质的量相等,即c(测)=
①准确测定待测液NaOH溶液的体积。
关键
②选择合适的指示剂,准确判断滴定的终点。①精确度是百分之一。即
可精确到0.01 mL!
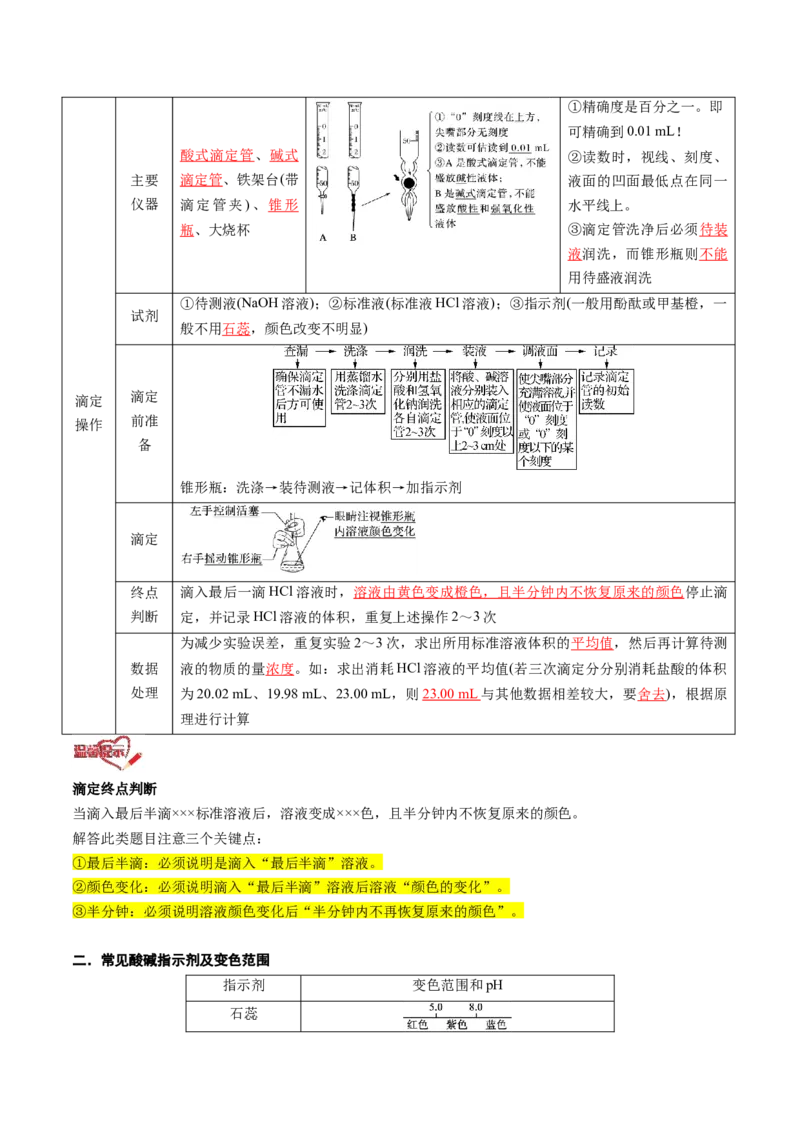
酸式滴定管、碱式 ②读数时,视线、刻度、
主要 滴定管、铁架台(带 液面的凹面最低点在同一
仪器 滴定管夹)、锥形 水平线上。
瓶、大烧杯 ③滴定管洗净后必须待装
液润洗,而锥形瓶则不能
用待盛液润洗
①待测液(NaOH溶液);②标准液(标准液HCl溶液);③指示剂(一般用酚酞或甲基橙,一
试剂
般不用石蕊,颜色改变不明显)
滴定
滴定
前准
操作
备
锥形瓶:洗涤→装待测液→记体积→加指示剂
滴定
终点 滴入最后一滴HCl溶液时,溶液由黄色变成橙色,且半分钟内不恢复原来的颜色停止滴
判断 定,并记录HCl溶液的体积,重复上述操作2~3次
为减少实验误差,重复实验2~3次,求出所用标准溶液体积的平均值,然后再计算待测
数据 液的物质的量浓度。如:求出消耗HCl溶液的平均值(若三次滴定分分别消耗盐酸的体积
处理 为20.02 mL、19.98 mL、23.00 mL,则23.00 mL 与其他数据相差较大,要舍去),根据原
理进行计算
滴定终点判断
当滴入最后半滴×××标准溶液后,溶液变成×××色,且半分钟内不恢复原来的颜色。
解答此类题目注意三个关键点:
①最后半滴:必须说明是滴入“最后半滴”溶液。
②颜色变化:必须说明滴入“最后半滴”溶液后溶液“颜色的变化”。
③半分钟:必须说明溶液颜色变化后“半分钟内不再恢复原来的颜色”。
二.常见酸碱指示剂及变色范围
指示剂 变色范围和pH
石蕊甲基橙
酚酞
指示剂 酚酞 甲基橙 温馨提醒
强酸滴定强碱 粉红色变为无色 黄色变为橙色 ①石蕊不用作指示剂;②终点颜色变
强碱滴定强酸 无色变为粉红色 红色变为橙色 化后要强调“半分钟内不褪色或不变
色”
说明:NaCO 与H+反应,选用的指示剂不同,发生的反应也不同:NaCO 盐酸—酚 NaHCO 、NaCO 盐酸—甲基
2 3 2 3——— 酞 3 2 3———橙
CO。
2
三.中和滴定的误差分析
以标准盐酸滴定NaOH溶液为例,根据中和滴定原理,分析所产生的误差:
操作不当 具 体 内 容 误差 判断方法
1 酸式滴定管未用HCl润洗 偏高
2 碱式滴定管未用NaOH润洗 偏低 c(H)V(H)
仪器洗涤 c(OH—)=
3 锥形瓶用NaOH润洗 偏高 V(OH)
4 锥形瓶用蒸馏水洗后未干燥 不变
想一想:以上三个量中,什么是
5 滴定前有气泡滴定后无气泡 偏高
记录量(不变量)、滴定量(可变
气泡处理
6 滴定前无气泡滴定有无气泡 偏低 量)
7 HCl漏滴出锥形瓶外 偏高 关键:看滴定量有无改变!
滴定过程
8 振荡时瓶内溶液溅出 偏低
9 滴定前仰视,滴定后平视 偏低
10 滴定前平视,滴定后仰视 偏高
读数方法
11 滴定前俯视,滴定后仰视 偏高
12 滴定前仰视,滴定后俯视 偏低
13 滴HCl终点时尖咀悬一滴溶液 偏高
14 指示剂变色即停止滴定 偏低
其他 15 滴定结束立即读数 偏高
16 锥形瓶中待测液加水稀释 无影响
17 一滴标准液附在锥形瓶壁上未流下 偏高
四.图示强酸与强碱滴定过程中pH曲线
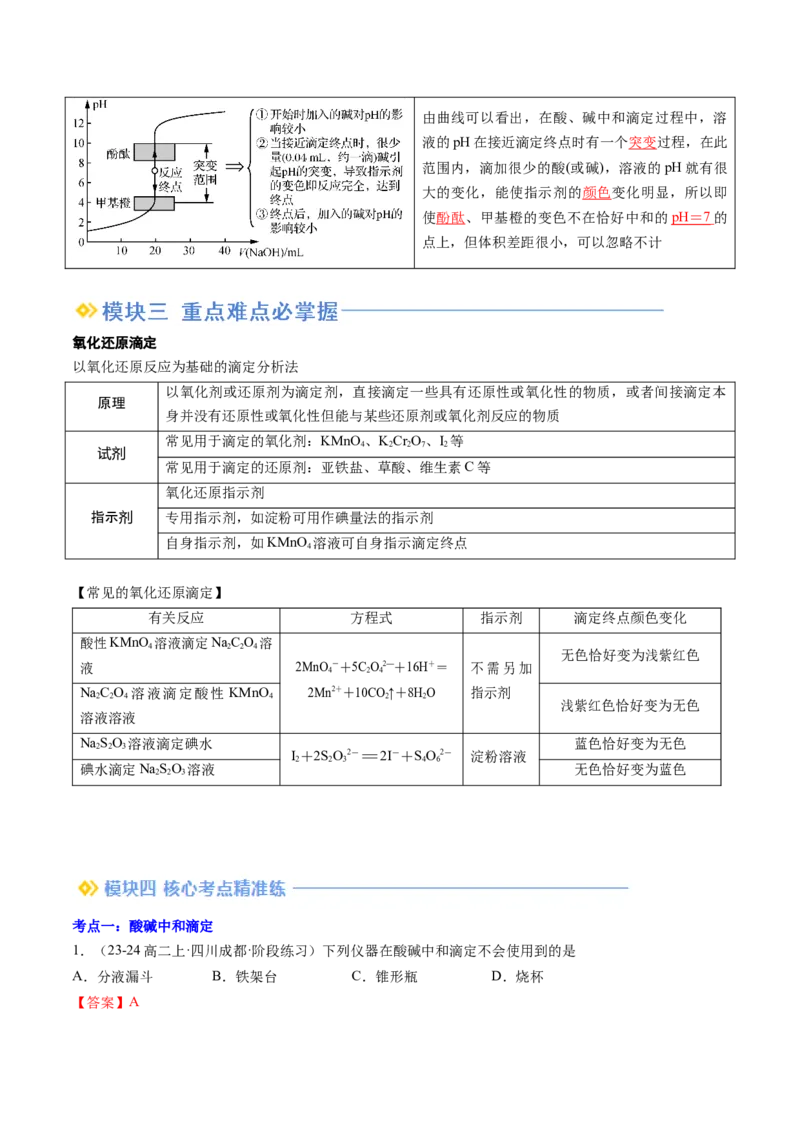
以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 盐酸为例由曲线可以看出,在酸、碱中和滴定过程中,溶
液的pH在接近滴定终点时有一个突变过程,在此
范围内,滴加很少的酸(或碱),溶液的pH就有很
大的变化,能使指示剂的颜色变化明显,所以即
使酚酞、甲基橙的变色不在恰好中和的 pH = 7 的
点上,但体积差距很小,可以忽略不计
氧化还原滴定
以氧化还原反应为基础的滴定分析法
以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定本
原理
身并没有还原性或氧化性但能与某些还原剂或氧化剂反应的物质
常见用于滴定的氧化剂:KMnO 、KCr O、I 等
4 2 2 7 2
试剂
常见用于滴定的还原剂:亚铁盐、草酸、维生素C等
氧化还原指示剂
指示剂 专用指示剂,如淀粉可用作碘量法的指示剂
自身指示剂,如KMnO 溶液可自身指示滴定终点
4
【常见的氧化还原滴定】
有关反应 方程式 指示剂 滴定终点颜色变化
酸性KMnO 溶液滴定NaCO 溶
4 2 2 4
无色恰好变为浅紫红色
液 2MnO-+5CO2—+16H+= 不需另加
4 2 4
NaC O 溶液滴定酸性 KMnO 2Mn2++10CO↑+8HO 指示剂
2 2 4 4 2 2
浅紫红色恰好变为无色
溶液溶液
NaSO 溶液滴定碘水 蓝色恰好变为无色
2 2 3
I+2SO2-=2I-+SO2- 淀粉溶液
2 2 3 4 6
碘水滴定NaSO 溶液 无色恰好变为蓝色
2 2 3
考点一:酸碱中和滴定
1.(23-24高二上·四川成都·阶段练习)下列仪器在酸碱中和滴定不会使用到的是
A.分液漏斗 B.铁架台 C.锥形瓶 D.烧杯
【答案】A【解析】酸碱中和滴定实验中需要用到滴定管、锥形瓶、烧杯、铁架台,不会使用到分液漏斗,故选A。
2.(23-24高二下·安徽淮北·开学考试)利用NaOH标准溶液滴定食醋中醋酸的浓度,下列操作正确的是
A.锥形瓶洗净后需要用待测食醋润洗
B.碱式滴定管用NaOH标准溶液润洗后,润洗液应从滴定管上口倒出
C.滴定读数时,应双手一上一下持滴定管
D.在使用前,若酸式滴定管旋塞处存在轻微漏水现象;可在旋塞处涂抹适量凡士林
【答案】D
【解析】A.锥形瓶洗净后不需要用待测食醋润洗,如果润洗,消耗的NaOH标准溶液偏大,使测定结果
偏大,A错误;
B.滴定管润洗后,润洗液应从下端流出,B错误;
C.滴定读数时,应单手持滴定管上端,使滴定管垂直向下,C错误;
D.凡士林是一种软膏状有机物,有滑腻感,旋塞处涂抹凡士林可以润滑、防水渗出,若滴定管旋塞处存
在轻微漏水现象,可在旋塞处涂抹适量凡士林,D正确;
故选D。
3.(23-24高二上·四川广安·阶段练习)量程为50.00mL的酸式滴定管,滴定前凹液面停留在20.00mL,
若把里面的液体全部放完,放出液体的体积
A.大于30.00mL B.小于30.00mL C.等于20.00mL D.等于30.00mL
【答案】A
【解析】滴定管的0刻线在上部,最大刻线在下面,最大刻线的下面还有一部分没有刻线,该部分也装有
液体,滴定前凹液面停留在20.00mL,若把里面的液体全部放完,放出液体的体积大于30.00mL,故选
A。
4.(23-24高二上·山东青岛·期末)碳酸钠俗称纯碱,是一种重要的化工原料。工业制备的碳酸钠产品中
通常含有少量碳酸氢钠,某兴趣小组测定碳酸钠中碳酸氢钠含量的实验步骤如下:
步骤一:称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
步骤二:移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定至终点(第
一滴定终点),消耗盐酸 ;
步骤三:在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终点),
又消耗盐酸 ;
平行测定三次, 平均值为22.45, 平均值为23.51。
下列有关上述实验或滴定管的描述错误的是
A.指示剂M可能为酚酞,N可能为甲基橙
B.酸性高锰酸钾溶液、碘水均需用酸式滴定管
C.碱式滴定管可以通过挤压玻璃球下方的乳胶管放液
D.滴定管中装液时,应由试剂瓶直接灌入,不得借用任何别的器皿
【答案】C【解析】A.用盐酸滴定碳酸钠溶液,滴定终点时,得到NaHCO 溶液,NaHCO 溶液呈碱性,M可能为酚
3 3
酞,继续用盐酸滴定,滴定终点时,得到HCO 溶液,N可能为甲基橙,A正确;
2 3
B.酸性高锰酸钾溶液、碘水具有氧化性,需用酸式滴定管,B正确;
C.碱式滴定管应用拇指和食指捏住胶管中玻璃珠所在部位稍上处,捏挤胶管使其与玻璃珠之间形成一条
缝隙,溶液即可流出,C错误;
D.滴定管中装液时,应由试剂瓶直接灌入,不得借用任何别的器皿,D正确;
故选C。
5.(23-24高二上·山西朔州·阶段练习)关于下列各实验或装置的叙述中,不正确的是
A.①可用于测溶液pH
B.②是用酸性KMnO 溶液滴定NaSO 溶液
4 2 3
C.③是滴定操作时手的操作
D.④中滴入最后半滴NaOH标准液使溶液由无色变为红色,即达到滴定终点
【答案】D
【解析】A.测溶液pH的方法:将pH试纸放在玻璃片或点滴板上,将待测液滴到pH试纸上,将试纸显
示的颜色与标准比色卡对照,图示操作方法合理,A项正确;
B.酸性高锰酸钾溶液具有强氧化性,能够氧化碱式滴定管的橡胶,应用酸式滴定管盛放,图示操作方法
合理,B项正确;
C.滴定操作,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视锥形瓶内溶液颜色变化,
图示操作方法合理,C项正确;
D.用氢氧化钠溶液滴定盐酸,可选用酚酞作指示剂,滴定终点现象为:最后半滴NaOH标准液使溶液由
无色变为红色,且30s不恢复,该说法不合理,D项错误;
答案选D。
6.(22-23高二上·上海闵行·期末)常温下,用氢氧化钠溶液滴定 稀盐酸时,溶液 随 溶
液的体积变化如图所示。下列说法正确的是A.一般用蓝色手柄滴定管量取稀盐酸 B.一般选用甲基橙试液作终点指示剂
C.稀盐酸的浓度为 D.氢氧化钠溶液的浓度为
【答案】D
【解析】A.蓝色手柄滴定管用于盛放碱性物质,盐酸为酸性,A错误;
B.甲基橙变色范围为酸性,氢氧化钠和盐酸生成中性氯化钠,氢氧化钠能使酚酞试液变红色,故指示剂
选酚酞,B错误;
C.由图可知,起点pH=1,氢离子浓度为0.1mol/L,盐酸为强酸,则稀盐酸的浓度为 ,C错误;
D.HCl和 反应关系为 ,则氢氧化钠溶液的浓度为 ,
D正确;
故选D。
考点二:酸碱中和滴定的误差分析
7.(23-24高二上·浙江杭州·期末)下列有关滴定操作的说法正确的是
A.酸碱中和滴定实验时,滴定管和锥形瓶水洗后都需要用待装液润洗
B.用标准 溶液滴定未知浓度的盐酸,配制标准溶液的固体 中含有 杂质,则测定结果偏
低
C.可用量筒量取 待测液置于锥形瓶中
D.用盐酸标准液滴定 待测液时,选择酚酞指示反应终点,误差比甲基橙的大
【答案】B
【解析】A.锥形瓶用蒸馏水洗后,不能用待测液润洗,否则待测液的物质的量增加,滴定时标准液所用
体积增加,导致测定结果偏大,A错误;
B.等质量的氢氧化钠的物质的量大于氢氧化钾,导致标准碱液中氢氧根离子浓度过大,使得标准液用量
偏小,导致测定结果偏低,B正确;
C.不可用量筒量取 待测液置于锥形瓶,应该使用移液管或碱式滴定管,C错误;
D.用盐酸标准液滴定 待测液时,由于反应产物为NaCl,滴定终点时溶液呈中性,因此指示剂即可
选酚酞,也可以选甲基橙,D错误;
故选B。
8.(23-24高二上·陕西西安·阶段练习)用标准盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验
误差的是
A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定
C.用蒸馏水洗净锥形瓶后,装入20.00mLNaOH溶液,加入少量的蒸馏水再进行滴定
D.用酚酞作指示剂滴至红色刚变无色时,立即停止加盐酸并读数
【答案】C
【解析】A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定会使消耗盐酸溶液的体积偏大,导致测
定结果偏大,故A不合题意;
B.用蒸馏水洗净锥形瓶后,再用氢氧化钠溶液润洗,后装入氢氧化钠溶液进行滴定会使氢氧化钠的物质
的量增大,消耗盐酸溶液的体积偏大,导致测定结果偏大,故B不合题意;
C.用蒸馏水洗净锥形瓶后,装入20.00mL氢氧化钠溶液,加入少量的蒸馏水再进行滴定对氢氧化钠的物
质的量和盐酸溶液的体积无影响,对测定结果无影响,不会引起实验误差,故C符合题意;
D.用酚酞作指示剂滴至红色刚变无色时,立即停止加盐酸并读数会使消耗盐酸溶液的体积偏小,导致测
定结果偏小,故D不合题意;
故选C。
9.(23-24高二上·湖北·期末)下列有关滴定操作的说法正确的是
A.用标准KOH溶液滴定未知浓度的盐酸,洗净碱式滴定管后直接取标准KOH溶液进行滴定,则测定结
果偏高
B.用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL
C.用标准KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中含有NaOH杂质,则测定结果偏
高
D.用未知浓度的盐酸滴定标准KOH溶液时,若读取盐酸体积时,滴定前仰视,滴定到终点后俯视,会导
致测定结果偏低
【答案】A
【解析】A.用标准KOH溶液滴定未知浓度的盐酸,洗净碱式滴定管后直接取标准KOH溶液进行滴定,
由于没有润洗,标准液浓度减小,消耗标准液体积增加,则测定结果偏高,A正确;
B.滴定管精确值为0.01mL,读数应保留小数点后2位,B错误;
C.所用的固体KOH中混有NaOH,相同质量的氢氧化钠和氢氧化钾,氢氧化钠的物质的量大于氢氧化钾
的物质的量,故所配的溶液的OH-浓度偏大,导致消耗标准液的体积偏小,测定结果偏低,C错误;
D.用未知浓度的盐酸滴定标准的KOH溶液时,若滴定前仰视读数,滴定至终点后俯视读数,导致消耗的
盐酸体积偏小,测定结果偏高,D错误;
故选A。
10.(23-24高二上·安徽·期末)用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列
操作会导致测定结果偏低的是
A.酸式滴定管未润洗就装标准液滴定
B.锥形瓶未用待测液润洗
C.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失
D.读取标准液读数时,滴前仰视,滴定到终点后俯视
【答案】D【解析】A.酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定,标准液浓度偏小,造成V(标准)偏
大,根据c(待测) 知c(待测)偏高,A错误;
B.锥形瓶未用待测液润洗,待测液的物质的量不变,标准液的体积不变,结果不变,B错误;
C.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失,造成V(标准)偏大,根据c(待测)
知c(待测)偏高,C错误;
D.读取标准液读数时,滴前仰视,滴定到终点后俯视,造成V(标准)偏小,根据c(待测)
知c(待测)偏低,D正确;
故选D。
11.(22-23高二上·湖北·阶段练习)某学生以酚酞为指示剂,用已知物质的量浓度的盐酸来测定未知物质
的量浓度的氢氧化钠溶液,三次实验分别记录有关数据如下表:
盐酸的体积
滴定次数 待测氢氧化钠溶液的体积
滴定前刻度 滴定后刻度
第一次 25.00 0.00 27.45
第二次 25.00 0.00 30.30
第三次 25.00 0.00 17.55
下列说法正确的是
A.该氢氧化钠溶液中
B.当滴入最后半滴标准液时溶液从粉红色刚好变成无色时,即达到滴定终点
C.达滴定终点时,滴定管尖嘴有悬液,则测定结果偏低
D.实验中雉形瓶若用待测氢氧化钠溶液润洗,则测定结果偏低
【答案】A
【解析】A.可知第三次实验所耗盐酸体积误差较大,取前两组实验的平均值,可知平均所耗盐酸体积为
28.875mL,该氢氧化钠溶液中 ,A正确;
B.当滴入最后半滴标准液时溶液从粉红色刚好变成无色且半分钟内不恢复原色时,即达到滴定终点,B
错误;
C.达滴定终点时,滴定管尖嘴有悬液,读取示数时因将悬滴的体积考虑在内,使得盐酸体积偏高,则测
定结果偏高,C错误;
D.实验中雉形瓶若用待测氢氧化钠溶液润洗,使需要滴定的盐酸偏多,则测定结果偏高,D错误。
故选A。1.(23-24高二上·四川泸州·期末)酸碱中和滴定实验中不需要的仪器是
A. B.
C. D.
【答案】B
【解析】酸碱中和滴定用到的仪器有:酸式滴定管、碱式滴定管、滴定管夹、铁架台、胶头滴管、烧杯、
锥形瓶等仪器,用不到分液漏斗,故选B。
2.(23-24高二上·陕西宝鸡·期中)要精确量取20.00mL酸性高锰酸钾溶液,可选用的仪器是
A.100mL容量瓶 B.100mL烧杯 C.25mL碱式滴定管 D.25mL酸式滴定管
【答案】D
【解析】酸性高锰酸钾溶液具有强氧化性,会腐蚀碱式滴定管中的橡胶管,所以应用25mL酸式滴定管确
量取20.00mL酸性高锰酸钾溶液,故选D。
3.(23-24高二上·山东青岛·期末)碳酸钠俗称纯碱,是一种重要的化工原料。工业制备的碳酸钠产品中
通常含有少量碳酸氢钠,某兴趣小组测定碳酸钠中碳酸氢钠含量的实验步骤如下:
步骤一:称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
步骤二:移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定至终点(第
一滴定终点),消耗盐酸 ;
步骤三:在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终点),
又消耗盐酸 ;
平行测定三次, 平均值为22.45, 平均值为23.51。
下列关于滴定分析的操作,正确的是
A.滴定时应一直观察滴定管中溶液体积的变化
B.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以上某固定位置
C.滴定时自始至终应匀速滴加
D.读数时应捏住滴定管上端无刻度处,使管保持垂直
【答案】D
【解析】A.滴定时应一直观察锥形瓶中溶液颜色变化确定滴定终点,A错误;B.平行滴定时,需要确定的是消耗标准液的体积,无须重新装液并调节液面至“0”刻度或“0”刻度以上
某固定位置,B错误;
C.滴定时初始可以稍快,接近滴定终点时应该逐滴滴加,C错误;
D.读数时应捏住滴定管上端无刻度处,使管保持垂直,便于正确读数,D正确;
故选D。
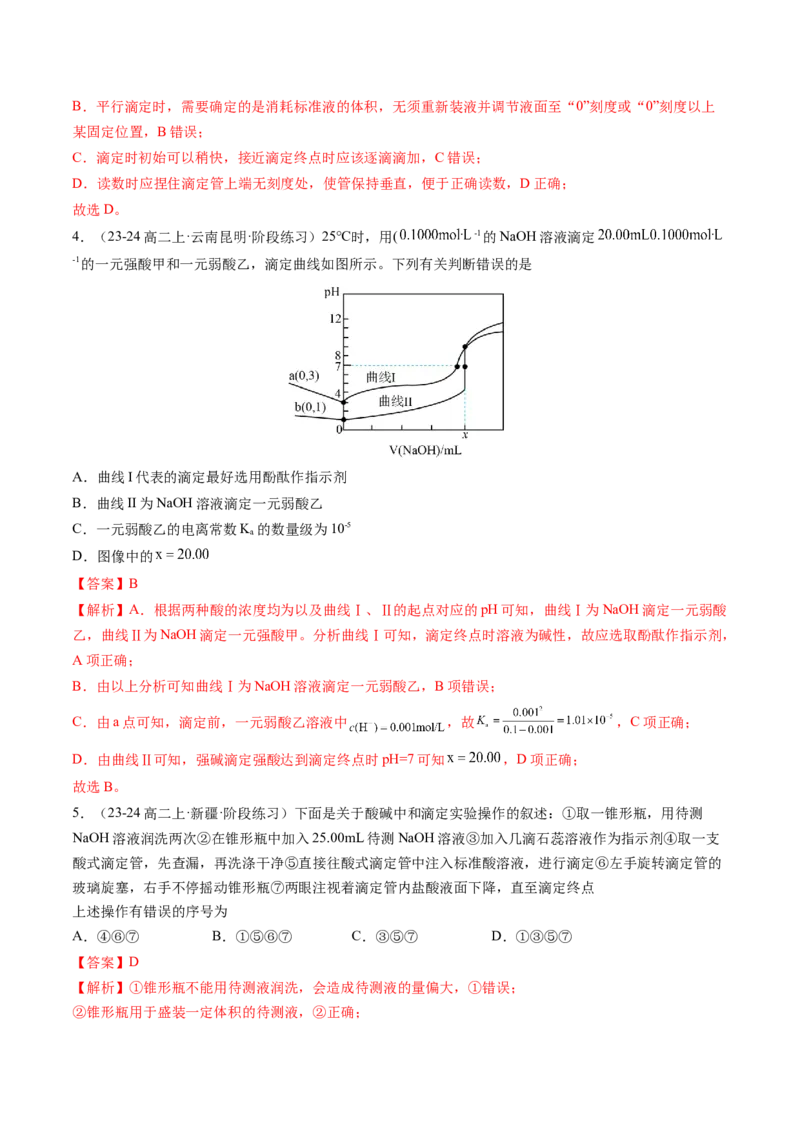
4.(23-24高二上·云南昆明·阶段练习)25℃时,用( -1的NaOH溶液滴定
-1的一元强酸甲和一元弱酸乙,滴定曲线如图所示。下列有关判断错误的是
A.曲线I代表的滴定最好选用酚酞作指示剂
B.曲线II为NaOH溶液滴定一元弱酸乙
C.一元弱酸乙的电离常数Kₐ的数量级为10-5
D.图像中的
【答案】B
【解析】A.根据两种酸的浓度均为以及曲线Ⅰ、Ⅱ的起点对应的pH可知,曲线Ⅰ为NaOH滴定一元弱酸
乙,曲线Ⅱ为NaOH滴定一元强酸甲。分析曲线Ⅰ可知,滴定终点时溶液为碱性,故应选取酚酞作指示剂,
A项正确;
B.由以上分析可知曲线Ⅰ为NaOH溶液滴定一元弱酸乙,B项错误;
C.由a点可知,滴定前,一元弱酸乙溶液中 ,故 ,C项正确;
D.由曲线Ⅱ可知,强碱滴定强酸达到滴定终点时pH=7可知 ,D项正确;
故选B。
5.(23-24高二上·新疆·阶段练习)下面是关于酸碱中和滴定实验操作的叙述:①取一锥形瓶,用待测
NaOH溶液润洗两次②在锥形瓶中加入25.00mL待测NaOH溶液③加入几滴石蕊溶液作为指示剂④取一支
酸式滴定管,先查漏,再洗涤干净⑤直接往酸式滴定管中注入标准酸溶液,进行滴定⑥左手旋转滴定管的
玻璃旋塞,右手不停摇动锥形瓶⑦两眼注视着滴定管内盐酸液面下降,直至滴定终点
上述操作有错误的序号为
A.④⑥⑦ B.①⑤⑥⑦ C.③⑤⑦ D.①③⑤⑦
【答案】D
【解析】①锥形瓶不能用待测液润洗,会造成待测液的量偏大,①错误;
②锥形瓶用于盛装一定体积的待测液,②正确;③用石蕊试液做指示剂,变色不明显,不便于观察判断滴定终点,应使用酚酞或甲基橙做指示剂,③错误;
④滴定管使用前需查漏,再洗涤干净,④正确;
⑤滴定管经过查漏、水洗后还要用标准液润洗,才能加注标准液,不能接往酸式滴定管中注入标准酸溶液,
⑤错误;
⑥滴定时左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶,⑥正确;
⑦滴定过程中目光应注视锥形瓶内溶液颜色的变化,⑦错误。
综上所述,错误的是①③⑤⑦,故选D。
6.(23-24高二上·山东菏泽·阶段练习)实验室用标准盐酸测定某NaOH溶液的浓度,用甲基橙作指示剂,
下列操作中可能使测定结果偏高的是
A.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
B.酸式滴定管在装酸液前用标准盐酸润洗2~3次
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前未用NaOH溶液润洗2~3次
【答案】A
【解析】A.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
可知c(标准)偏高,A正确;
B.酸式滴定管在装酸液前用标准盐酸溶液润洗2~3次,该操作方法合理,不影响测定结果,B错误;
C.滴定过程中,锥形瓶内溶液颜色由黄色变为橙色,立即记下滴定管内液面所在刻度,造成V(标准)
偏小,根据c(待测)= 可知c(标准)偏低,C错误;
D.盛NaOH溶液的锥形瓶滴定不用NaOH溶液润洗,该操作方法合理,不影响测定结果,D错误;
故选A。
7.(23-24高二上·山西朔州·期末)下列有关实验说法正确的是
A.用广泛pH试纸测得某浓度的NaClO溶液pH=10
B.中和热的测定实验中,应用同一支温度计测量溶液的温度
C.用NaOH标准溶液滴定盐酸,若滴定前仰视读数,滴定后俯视读数,则所测盐酸的浓度偏高
D.中和滴定时为了更清楚观察到锥形瓶内溶液颜色的变化,可以加多2~3mL指示剂
【答案】B
【解析】A.NaClO溶液具有漂白性,漂白pH试纸,A错误;
B.中和热的测定实验中,为避免出现仪器误差,应用同一支温度计测量酸液和碱液的温度,B正确;
C.若滴定前仰视读数,滴定后俯视读数,测得消耗标准液体积偏小,则盐酸浓度偏低,C错误;
D.指示剂加入过多会影响实验结果,D错误;
答案选B。
8.(23-24高二上·浙江绍兴·期末)实验小组用 的NaOH溶液滴定20.00mL未知浓度的
溶液。下列说法正确的是A.可以用如图甲所示装置和操作进行滴定
B.滴定结束时俯视滴定管读数,测量结果偏低
C.图乙所示滴定管中液面的读数为18.20mL
D.图丙可以表示滴定过程中溶液的pH与滴加NaOH溶液体积的关系
【答案】B
【解析】A.盛装氢氧化钠溶液应该为碱式滴定管,A错误;
B.滴定结束时俯视滴定管读数,导致最后体积消耗偏小,因此浓度偏低,B正确;
C.滴定管从上到下,读书依次变大,因此读数为19.80mL,C错误;
D.氢氧化钠溶液滴定醋酸,滴定终点溶液呈碱性,D错误;
故选B。
9.(23-24高二上·江苏苏州·期末)关于滴定管装液,正确的是
A.装液后,检查气泡时需注意,碱式滴定管的气泡在尖嘴处和橡胶管内都会存在
B.可将待装溶液倒入一洁净烧杯中,再加入滴定管
C.待装溶液需直接从其容器中加入滴定管,中间避免使用其他仪器
D.装液时,要保持滴定管垂直
【答案】AC
【解析】A.装液后,检查气泡时需注意,乳胶管内及出口管内是否有气泡或有未充满的地方,故A正确;
B.待测溶液直接倒入滴定管中,不得用其他容器(如烧杯、漏斗等)来转移,防止污染待测液或使待测液挥
发,故B错误;
C.待测溶液直接倒入滴定管中,不得用其他容器(如烧杯、漏斗等)来转移,故C正确;
D.左手前三指持滴定管上部无刻度处,并可稍微倾斜,右手拿住细口瓶往滴定管中倒溶液,故D错误;
故选:AC。
10.(22-23高二上·山东聊城·期中)下列实验操作会使结果偏大的是
A.用玻璃棒蘸取少量氯化钠溶液滴在湿润的pH试纸上
B.中和滴定时,溶液颜色刚刚变色便立即读数
C.用已知浓度的盐酸滴定未知浓度的氢氧化钠时,碱式滴定管未润洗
D.用已知浓度的盐酸滴定未知浓度的氢氧化钠时,酸式滴定管刚开始有气泡,读数时,气泡消失
【答案】D
【解析】A.氯化钠溶液中性,湿润的pH试纸对结果无影响,A错误;
B.颜色褪去立即读数,导致滴入的标准溶液体积偏小,会使测量结果偏小,B错误;C.碱式滴定管未润洗,量取的氢氧化钠物质的量变小,测量结果偏小,C错误;
D.该操作会导致读取的盐酸体积偏大,导致测量结果偏大,D正确;
答案选D。
11.(23-24高二上·江西上饶·阶段练习)某小组拟用标准 溶液滴定某浓度的草酸溶液,下列有关
说法正确的是
A.标准 溶液和草酸溶液分别用滴定管Ⅰ、Ⅱ盛装或量取
B.检漏后即可将标准 溶液直接倒入滴定管中
C.滴定后液面(图Ⅳ)读数约为21.30 mL
D.本次实验消耗标准 溶液的体积约为21.30 mL
【答案】D
【解析】A.标准 溶液应用酸式滴定管盛装或量取,选项A错误;
B.在使用滴定管前,首先要检查活塞是否漏水,之后用要盛装的溶液润洗2-3遍,然后才加入相关溶液,
选项B错误;
C.滴定管读数视线应平视凹液面的最低点,滴定后液面读数为22.70mL,选项C错误;
D.根据滴定前和滴定后的读数可知本实验消耗标准 溶液的体积约为21.30mL,选项D正确;
答案选D。
12.(23-24高二下·江苏无锡·阶段练习)如图所示为常温下用0.1000mol·L-1NaOH溶液滴定10.00mL未知
浓度的硫酸(用酚酞作指示剂)的滴定曲线。下列说法正确的是
A.水电离出的氢氧根离子浓度:a>b
B.硫酸的物质的量浓度为0.2000mol·L-1
C.指示剂变色时,说明硫酸与NaOH恰好完全反应D.当滴加NaOH溶液的体积为10.00mL时,该混合液的 =0.05mol·L-1
【答案】D
【解析】A.酸、碱抑制水的电离,a点剩余硫酸的浓度比b点大,a点对水电离的抑制作用比b点大,所
以水电离出的氢氧根离子浓度:a<b,故A错误;
B.当滴加NaOH的体积为20.00mL时,硫酸与NaOH刚好完全反应,则2c(HSO )
2 4
×10.00mL=0.1000mol/L×20mL,c(HSO )=0.1000mol⋅L-1,故B错误;
2 4
C.当最后半滴标准NaOH溶液滴入,溶液恰好由无色变成粉红色,且在半分钟内不变色时,达到了滴定
终点,但酚酞变红,NaOH稍过量,故C错误;
D.当滴加NaOH溶液为10.00mL时,该混合液的c(H+)=
=0.05mol/L,故D正确;
故选D。
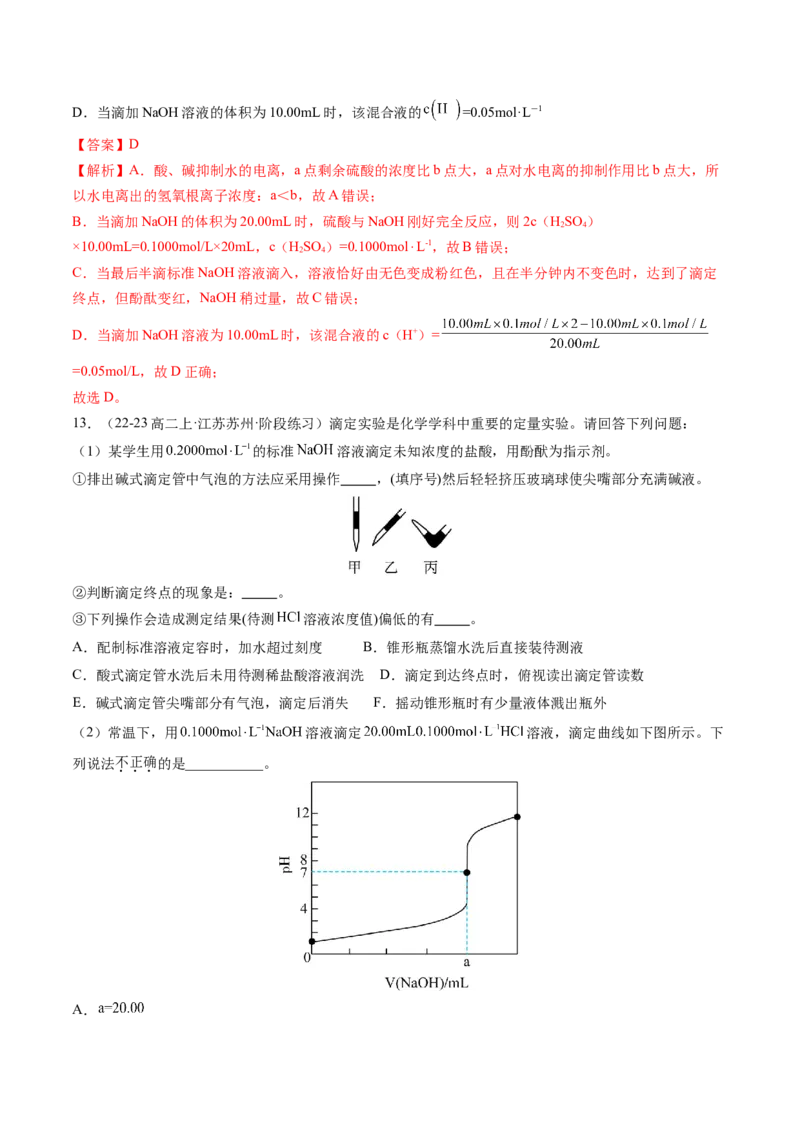
13.(22-23高二上·江苏苏州·阶段练习)滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)某学生用 的标准 溶液滴定未知浓度的盐酸,用酚䣭为指示剂。
①排出碱式滴定管中气泡的方法应采用操作 ,(填序号)然后轻轻挤压玻璃球使尖嘴部分充满碱液。
②判断滴定终点的现象是: 。
③下列操作会造成测定结果(待测 溶液浓度值)偏低的有 。
A.配制标准溶液定容时,加水超过刻度 B.锥形瓶蒸馏水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗 D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失 F.摇动锥形瓶时有少量液体溅出瓶外
(2)常温下,用 溶液滴定 溶液,滴定曲线如下图所示。下
列说法不正确的是___________。
A.B.滴定过程中,可能存在:
C.若用甲基橙作指示剂,滴定终点的颜色变化为红色变为橙色
D.若将盐酸换成相同浓度 醋酸,则滴定到 时,
(3)样品中亚硝基硫酸质量分数的测定
称取 产品放入 的锥形瓶中,加入 的 溶液和少量稀 ,发
生反应: ,产品中其他杂质不与
反应。反应完全后,用 的 标准溶液滴定过量的 ,发生反应:
,消耗 标准溶液 。
请确定样品中亚硝基硫酸(相对分子质量为127)的质量分数 ,并写出计算过程。
【答案】(1)丙 滴入最后半滴NaOH溶液后,溶液由无色变为粉红色,且半分钟内不褪色
CDF
(2)CD
(3)
【解析】(1)①排出碱式滴定管中气泡时尖嘴略向上倾斜,则应采用操作丙;
②用酚䣭作指示剂,酚酞遇碱变红色,判断滴定终点的现象是:滴入最后半滴NaOH溶液后,溶液由无色
变为粉红色,且半分钟内不褪色;
③A.配制标准溶液定容时,加水超过刻度,则所配标准溶液浓度偏低,滴定时消耗标准液体积偏大,导
致所测盐酸浓度偏高,A不符合题意;
B.锥形瓶蒸馏水洗后直接装待测液,锥形瓶中HCl的物质的量不变,消耗NaOH标准液体积不变,对实
验无影响,B不符合题意;
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗,盐酸被稀释浓度偏低,消耗的NaOH标准液体积减小,
所测盐酸浓度偏低,C符合题意;
D.滴定到达终点时,俯视读出滴定管读数,导致所读取的标准液体积偏小,则消耗标准液体积偏小,所
测盐酸浓度偏低,D符合题意;
E.碱式滴定管尖嘴部分有气泡,滴定后消失,导致滴定前读取的标准液体积偏小,则消耗标准液体积偏
大,所测盐酸浓度偏高,E不符合题意;
F.摇动锥形瓶时有少量液体溅出瓶外,盐酸溶质有损失,消耗标准液体积减小,所测盐酸浓度偏低,F符
合题意;
故选CDF。
(2)A.常温下,用0.1000mol·L−1NaOH溶液滴定20.00mL0.1000mol·L−1HCl溶液至呈中性时,消耗
NaOH溶液体积为20mL,则a=20mL,A正确;
B.由电荷守恒得 ,则可能存在 ,且此时所
加NaOH溶液体积小于10mL,B正确;
C.若用甲基橙作指示剂,溶液由红色变为橙色时,pH约为3.1,不是滴定终点,C错误;
D.将盐酸换成相同浓度0.1000mol·L−1醋酸,滴加NaOH溶液至呈中性时,消耗NaOH溶液体积小于20mL,则滴定到pH=7时,a<20.00,D错误;
故选CD。
(3)与亚硝基硫酸反应后剩余的KMnO 物质的量为 ,则与亚
4
硝基硫酸参加反应的KMnO 物质的量为 ,所以
4
,样品中亚硝基硫酸质量分数为 。
14.(23-24高二下·四川雅安·开学考试)电解质的水溶液中存在电离平衡。
(1)NH ·H O是常见的弱碱。
3 2
①NH ·H O在水溶液中的电离方程式为 。
3 2
②下列方法中,可以使氨水中NH ·H O电离程度减小的是(填字母序号) 。
3 2
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为 、浓度均为0.1000mol/L的盐酸
和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
①滴定开始前,Ⅰ图中水电离出的c(H+)是 。
②滴定醋酸的曲线是 (填“I”或“Ⅱ”),则V V(填“>”、 “<”“或“=”)。
1 2
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为 mL。
(4)酸碱中和滴定可用于测定酸或碱的物质的量浓度,取 未知浓度的醋酸放入锥形瓶中,用
0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编
NaOH溶液的浓度(mol·L-1) 滴定完成时,NaOH溶液滴入的体积(mL) 待测醋酸的体积(mL)
号
1 0.1000 22.48 20.00
2 0.1000 25.72 20.003 0.1000 22.52 20.00
①该滴定过程应选择 (填“甲基橙”或“酚酞”)为指示剂,根据上述数据,可计算出该醋酸的
浓度约为 。
②在上述实验中,下列操作会造成测定结果偏大的有 。(填字母序号)。
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
【答案】(1) d
(2)10-11mol/L Ⅰ <
(3)22.80
(4)酚酞 0.1125 BE
【解析】(1)① 在水溶液中电离出铵根离子和OH-,电离方程式为: ;
②a.微热溶液,电离平衡正向移动, 电离程度增大,a不符合题意;
b.滴加浓盐酸,电离平衡正向移动, 电离程度增大,b不符合题意;
c.加水稀释,根据电离规律“越稀越电离”, 电离程度增大,c不符合题意;
d.加入氯化铵晶体, 浓度增大,电离平衡逆向移动, 电离程度减小,d符合题意;
故选d;
(2)①滴定开始前,Ⅰ图中pH为3,即 ,水电离出的H+浓度与水电离出的OH-浓度相
等: ;
②浓度均为0.1000mol/L的盐酸和醋酸溶液,由于盐酸是强酸,醋酸是弱酸,因此滴定开始前,盐酸溶液
pH=1,醋酸溶液pH>1,即滴定醋酸的曲线为Ⅰ,盐酸与NaOH完全反应产物为NaCl,溶液呈中性,醋
酸与NaOH完全反应产物为醋酸钠,溶液呈碱性,因此V<V;
1 2
(3)由图可知,读数为22.80mL;
(4)①醋酸与NaOH完全反应产物为醋酸钠,溶液呈碱性,酚酞的变色范围是 ,选用酚酞作为指
示剂;实验编号2的数据误差过大舍去,消耗NaOH溶液的平均体积为: ,
醋酸的浓度为: ;
②A.滴定前仰视读数,滴定后俯视读数,导致计算的所用NaOH标准液体积偏小,测定结果偏小,A不
符合题意;B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗,NaOH溶液被稀释,所需要的NaOH溶液体
积变大,测定结果偏大,B符合题意
C.滴定过程中,溶液刚出现变色,立即停止滴定,导致计算的所用NaOH标准液体积偏小,测定结果偏
小,C不符合题意;
D.锥形瓶水洗后未干燥,不影响醋酸总物质的量,因此滴入NaOH的量也不变,对结果无影响,D不符
合题意
E.碱式滴定管尖嘴部分有气泡,滴定后消失,导致计算的所用NaOH标准液体积偏大,测定结果偏大,E
符合题意;
故选BE。