文档内容
(八)离子液体 超分子
(选择题1~5题,每小题6分,共30分)
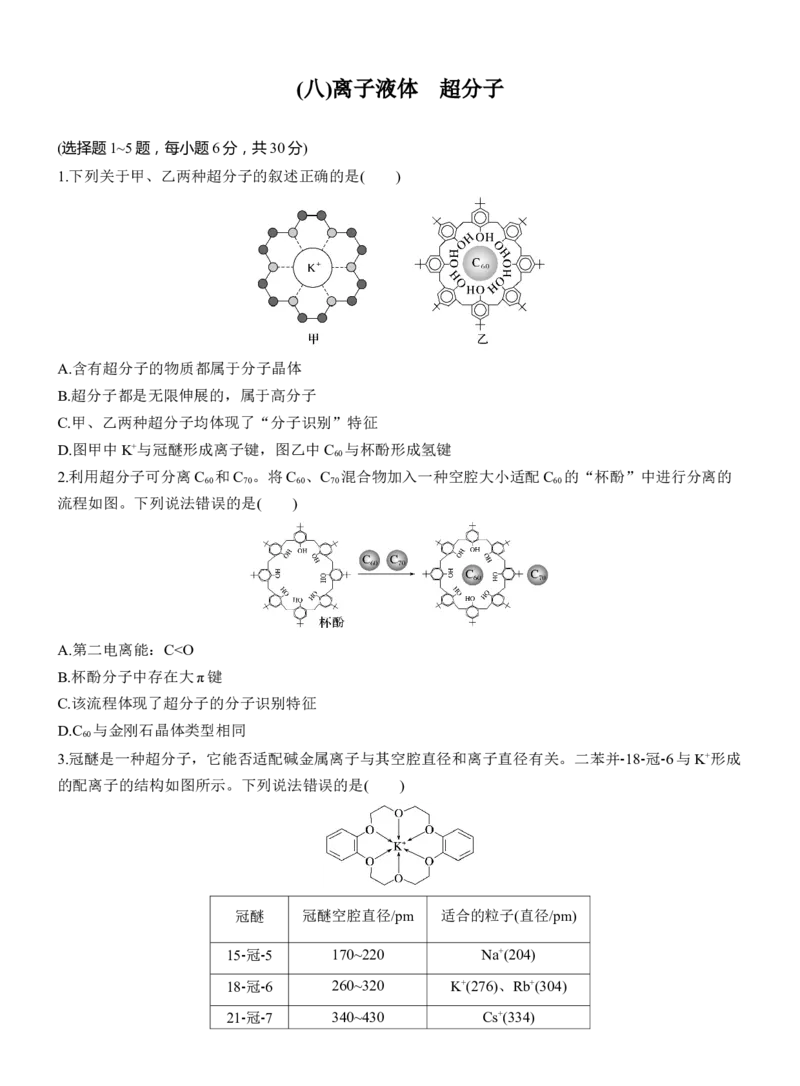
1.下列关于甲、乙两种超分子的叙述正确的是( )
A.含有超分子的物质都属于分子晶体
B.超分子都是无限伸展的,属于高分子
C.甲、乙两种超分子均体现了“分子识别”特征
D.图甲中K+与冠醚形成离子键,图乙中C 与杯酚形成氢键
60
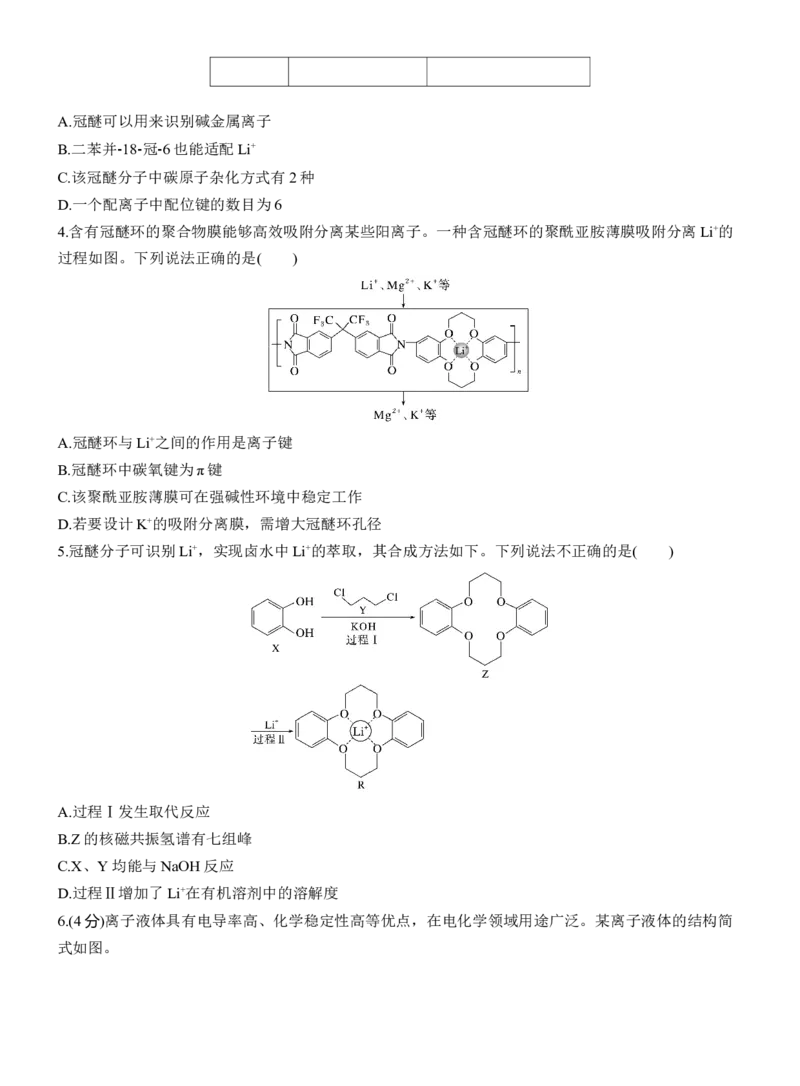
2.利用超分子可分离C 和C 。将C 、C 混合物加入一种空腔大小适配C 的“杯酚”中进行分离的
60 70 60 70 60
流程如图。下列说法错误的是( )
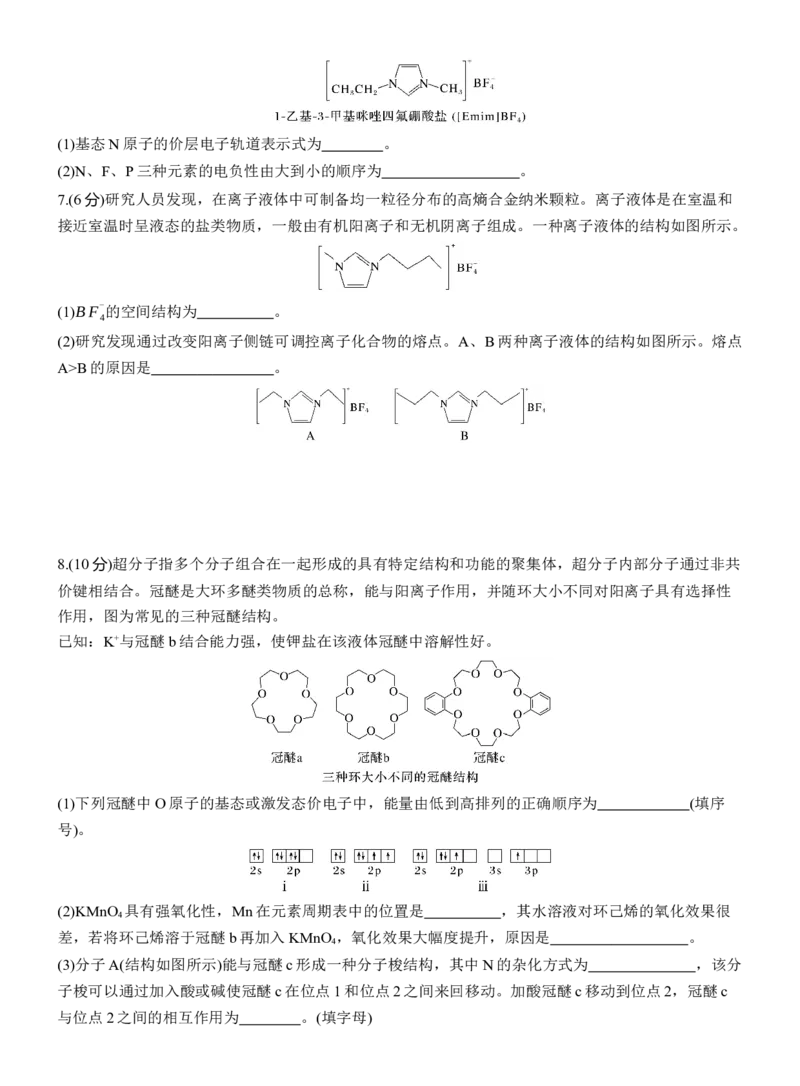
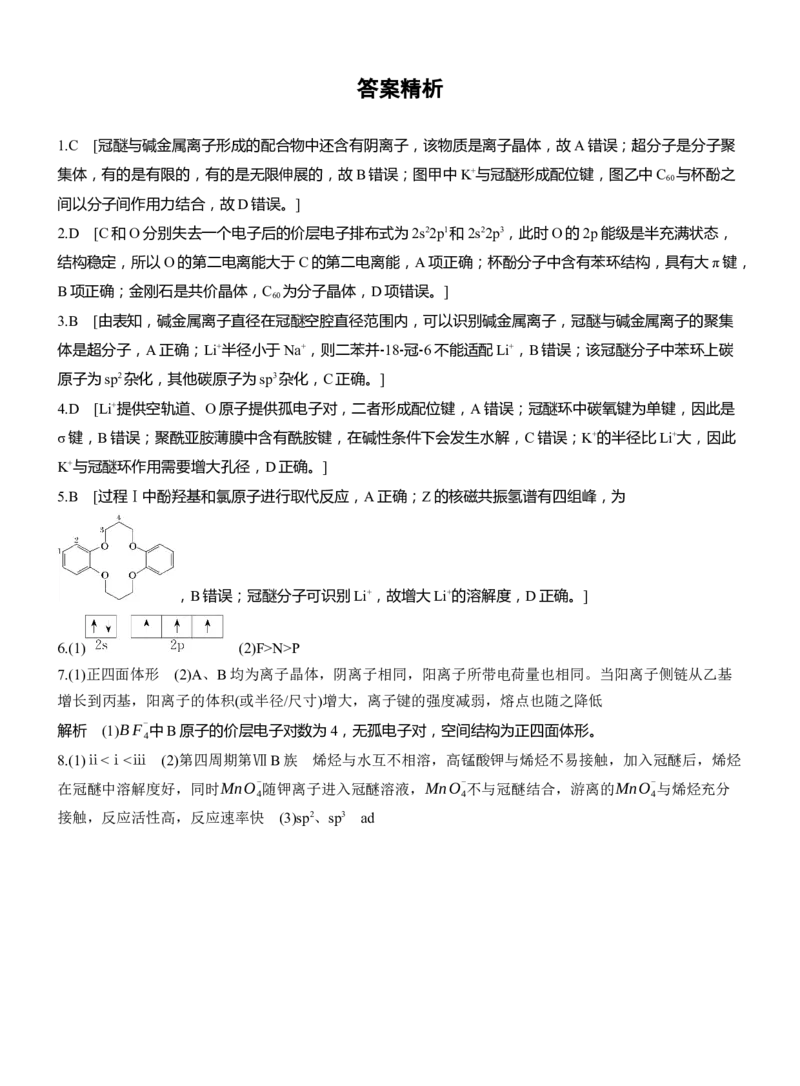
A.第二电离能:CB的原因是 。
8.(10分)超分子指多个分子组合在一起形成的具有特定结构和功能的聚集体,超分子内部分子通过非共
价键相结合。冠醚是大环多醚类物质的总称,能与阳离子作用,并随环大小不同对阳离子具有选择性
作用,图为常见的三种冠醚结构。
已知:K+与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好。
(1)下列冠醚中O原子的基态或激发态价电子中,能量由低到高排列的正确顺序为 (填序
号)。
(2)KMnO 具有强氧化性,Mn在元素周期表中的位置是 ,其水溶液对环己烯的氧化效果很
4
差,若将环己烯溶于冠醚b再加入KMnO ,氧化效果大幅度提升,原因是 。
4
(3)分子A(结构如图所示)能与冠醚c形成一种分子梭结构,其中N的杂化方式为 ,该分
子梭可以通过加入酸或碱使冠醚c在位点1和位点2之间来回移动。加酸冠醚c移动到位点2,冠醚c
与位点2之间的相互作用为 。(填字母)a.静电相互作用 b.离子键
c.共价键 d.氢键答案精析
1.C [冠醚与碱金属离子形成的配合物中还含有阴离子,该物质是离子晶体,故A错误;超分子是分子聚
集体,有的是有限的,有的是无限伸展的,故B错误;图甲中K+与冠醚形成配位键,图乙中C 与杯酚之
60
间以分子间作用力结合,故D错误。]
2.D [C和O分别失去一个电子后的价层电子排布式为2s22p1和2s22p3,此时O的2p能级是半充满状态,
结构稳定,所以O的第二电离能大于C的第二电离能,A项正确;杯酚分子中含有苯环结构,具有大π键,
B项正确;金刚石是共价晶体,C 为分子晶体,D项错误。]
60
3.B [由表知,碱金属离子直径在冠醚空腔直径范围内,可以识别碱金属离子,冠醚与碱金属离子的聚集
体是超分子,A正确;Li+半径小于Na+,则二苯并⁃18⁃冠⁃6不能适配Li+,B错误;该冠醚分子中苯环上碳
原子为sp2杂化,其他碳原子为sp3杂化,C正确。]
4.D [Li+提供空轨道、O原子提供孤电子对,二者形成配位键,A错误;冠醚环中碳氧键为单键,因此是
σ键,B错误;聚酰亚胺薄膜中含有酰胺键,在碱性条件下会发生水解,C错误;K+的半径比Li+大,因此
K+与冠醚环作用需要增大孔径,D正确。]
5.B [过程Ⅰ中酚羟基和氯原子进行取代反应,A正确;Z的核磁共振氢谱有四组峰,为
,B错误;冠醚分子可识别Li+,故增大Li+的溶解度,D正确。]
6.(1) (2)F>N>P
7.(1)正四面体形 (2)A、B均为离子晶体,阴离子相同,阳离子所带电荷量也相同。当阳离子侧链从乙基
增长到丙基,阳离子的体积(或半径/尺寸)增大,离子键的强度减弱,熔点也随之降低
解析
(1)BF-
中B原子的价层电子对数为4,无孤电子对,空间结构为正四面体形。
4
8.(1)ⅱ<ⅰ<ⅲ (2)第四周期第ⅦB族 烯烃与水互不相溶,高锰酸钾与烯烃不易接触,加入冠醚后,烯烃
在冠醚中溶解度好,同时MnO- 随钾离子进入冠醚溶液,MnO- 不与冠醚结合,游离的MnO-
与烯烃充分
4 4 4
接触,反应活性高,反应速率快 (3)sp2、sp3 ad