文档内容
(六)关注创新电源
(选择题1~3题,每小题5分,4~8题,每小题7分,共50分)
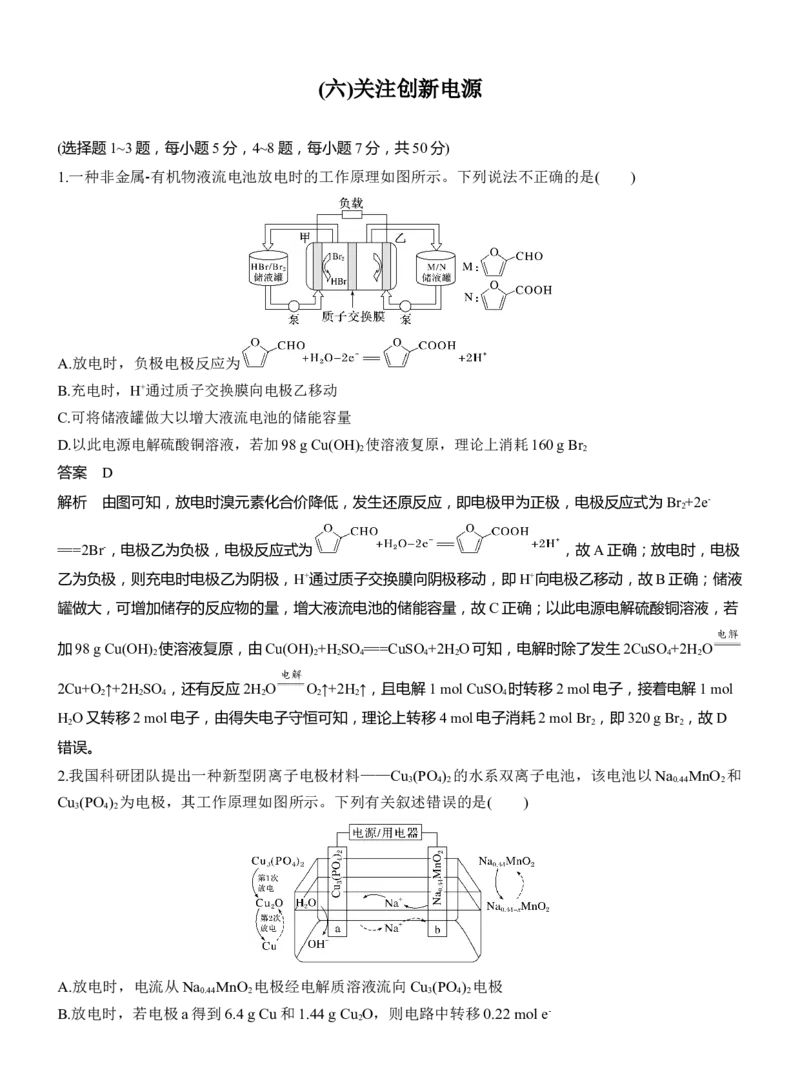
1.一种非金属 ⁃ 有机物液流电池放电时的工作原理如图所示。下列说法不正确的是( )
A.放电时,负极电极反应为
B.充电时,H+通过质子交换膜向电极乙移动
C.可将储液罐做大以增大液流电池的储能容量
D.以此电源电解硫酸铜溶液,若加98 g Cu(OH) 使溶液复原,理论上消耗160 g Br
2 2
答案 D
解析 由图可知,放电时溴元素化合价降低,发生还原反应,即电极甲为正极,电极反应式为Br +2e-
2
===2Br-,电极乙为负极,电极反应式为 ,故A正确;放电时,电极
乙为负极,则充电时电极乙为阴极,H+通过质子交换膜向阴极移动,即H+向电极乙移动,故B正确;储液
罐做大,可增加储存的反应物的量,增大液流电池的储能容量,故C正确;以此电源电解硫酸铜溶液,若
加98 g Cu(OH) 使溶液复原,由Cu(OH) +H SO ===CuSO +2H O可知,电解时除了发生2CuSO +2H O
2 2 2 4 4 2 4 2
2Cu+O ↑+2H SO ,还有反应2H O O ↑+2H ↑,且电解1 mol CuSO 时转移2 mol电子,接着电解1 mol
2 2 4 2 2 2 4
H O又转移2 mol电子,由得失电子守恒可知,理论上转移4 mol电子消耗2 mol Br ,即320 g Br ,故D
2 2 2
错误。
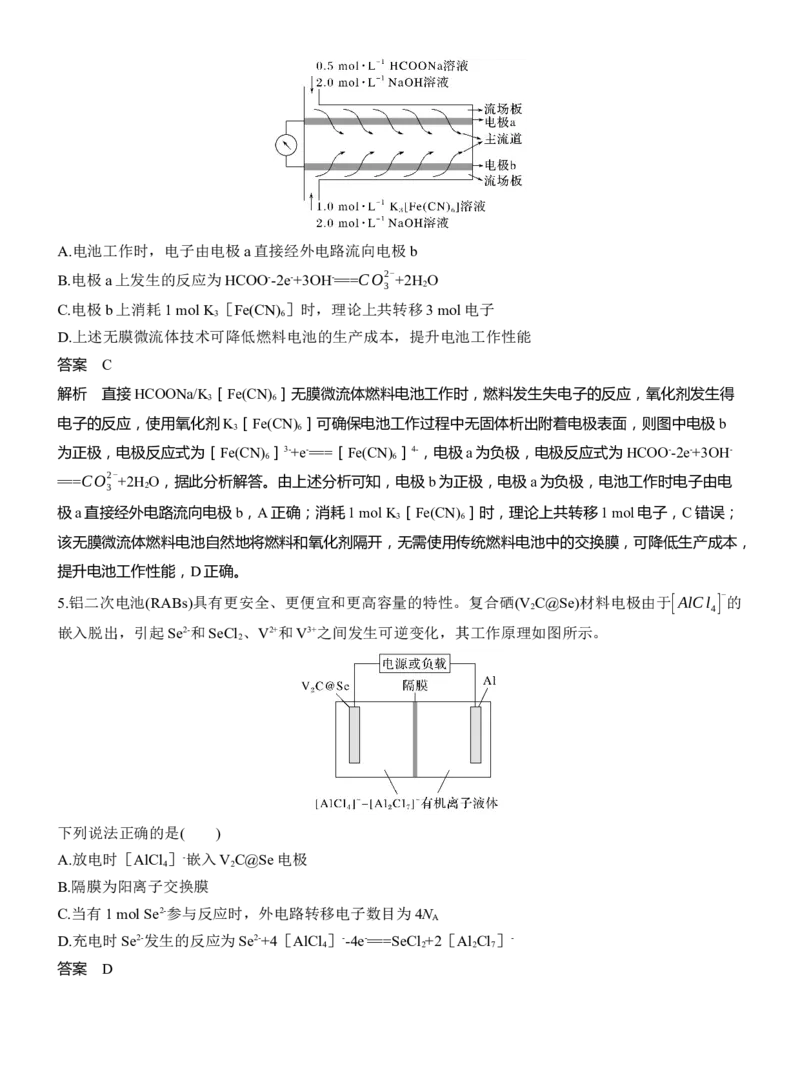
2.我国科研团队提出一种新型阴离子电极材料——Cu (PO ) 的水系双离子电池,该电池以Na MnO 和
3 4 2 0.44 2
Cu (PO ) 为电极,其工作原理如图所示。下列有关叙述错误的是( )
3 4 2
A.放电时,电流从Na MnO 电极经电解质溶液流向Cu (PO ) 电极
0.44 2 3 4 2
B.放电时,若电极a得到6.4 g Cu和1.44 g Cu O,则电路中转移0.22 mol e-
2C.充电时,电极b的电极反应式为Na MnO +xNa++xe-===Na MnO
0.44-x 2 0.44 2
D.为消除第一次放电的不可逆,可将Cu (PO ) 彻底放电转化为Cu O后再充电
3 4 2 2
答案 B
解析 由图可知,放电时为原电池,a极上Cu (PO ) →Cu O→Cu,发生得电子的还原反应,b极上
3 4 2 2
Na MnO →Na MnO ,发生失电子的氧化反应,则a极为正极,b极为负极,负极反应式为Na MnO -
0.44 2 0.44-x 2 0.44 2
xe-===Na MnO +xNa+,充电时为电解池,即a极为阳极,b极为阴极,据此分析解答。放电时,电流从
0.44-x 2
正极沿导线流向负极,再经电解质溶液到正极,A正确;放电时,电子转移情况为Cu~2e-、Cu O~2e-,若
2
电极a得到6.4 g Cu(为0.1 mol)和1.44 g Cu O(为0.01 mol),则电路中转移0.1 mol×2+0.01 mol×2=0.22 mol
2
电子,原电池的a极还发生2H O+2e-===H ↑+2OH-,因此无法判断转移多少电子,B错误;充电时,电极b
2 2
的电极反应式为Na MnO +xNa++xe-===Na MnO ,C正确;若将Cu (PO ) 彻底放电转化为Cu O,再充
0.44-x 2 0.44 2 3 4 2 2
电时Cu O可单向转化生成Cu (PO ) ,D正确。
2 3 4 2
3.如图为一种酶生物电池,可将葡萄糖(C H O )转化为葡萄糖内酯(C H O ),两个碳纳米管电极材料由
6 12 6 6 10 6
石墨烯片层卷曲而成。下列说法不正确的是( )
A.图中的离子交换膜为阳离子交换膜
B.负极区发生的电极反应主要为C H O -2e-===C H O +2H+
6 12 6 6 10 6
C.碳纳米管有良好导电性能,且能高效吸附气体
D.理论上消耗标准状况下2.24 L O ,可生成葡萄糖内酯0.2 mol
2
答案 D
解析 由图可知,右侧碳纳米管为正极,电极反应式为O +4e-+4H+===2H O,左侧碳纳米管为负极,电极
2 2
反应式为C H O -2e-===2H++C H O ,H -2e-===2H+,据此作答。图中离子交换膜能让氢离子通过,故离
6 12 6 6 10 6 2
子交换膜为阳离子交换膜,故A正确;碳纳米管电极材料由石墨烯片层卷曲而成,有良好导电性能,且能
高效吸附气体,故C正确;理论上消耗标准状况下2.24 L O ,得到0.4 mol e-,由于负极区有H 和C H O
2 2 6 12 6
两种物质失电子,所以生成的葡萄糖内酯小于0.2 mol,故D错误。
4.直接HCOONa/K [Fe(CN) ]无膜微流体燃料电池(结构如图所示)利用多股流体在微通道内平行层流
3 6
的特性,自然地将燃料和氧化剂隔开,无需使用传统燃料电池中的交换膜,且使用氧化剂K
3
[Fe(CN) ]可确保电池工作过程中无固体析出附着电极表面。下列有关说法不正确的是( )
6A.电池工作时,电子由电极a直接经外电路流向电极b
B.电极a上发生的反应为HCOO--2e-+3OH-===CO2-
+2H O
3 2
C.电极b上消耗1 mol K [Fe(CN) ]时,理论上共转移3 mol电子
3 6
D.上述无膜微流体技术可降低燃料电池的生产成本,提升电池工作性能
答案 C
解析 直接HCOONa/K [Fe(CN) ]无膜微流体燃料电池工作时,燃料发生失电子的反应,氧化剂发生得
3 6
电子的反应,使用氧化剂K [Fe(CN) ]可确保电池工作过程中无固体析出附着电极表面,则图中电极b
3 6
为正极,电极反应式为[Fe(CN) ]3-+e-===[Fe(CN) ]4-,电极a为负极,电极反应式为HCOO--2e-+3OH-
6 6
===CO2-
+2H O,据此分析解答。由上述分析可知,电极b为正极,电极a为负极,电池工作时电子由电
3 2
极a直接经外电路流向电极b,A正确;消耗1 mol K [Fe(CN) ]时,理论上共转移1 mol电子,C错误;
3 6
该无膜微流体燃料电池自然地将燃料和氧化剂隔开,无需使用传统燃料电池中的交换膜,可降低生产成本,
提升电池工作性能,D正确。
-
5.铝二次电池(RABs)具有更安全、更便宜和更高容量的特性。复合硒(V C@Se)材料电极由于[AlCl ] 的
2 4
嵌入脱出,引起Se2-和SeCl 、V2+和V3+之间发生可逆变化,其工作原理如图所示。
2
下列说法正确的是( )
A.放电时[AlCl ]-嵌入V C@Se电极
4 2
B.隔膜为阳离子交换膜
C.当有1 mol Se2-参与反应时,外电路转移电子数目为4N
A
D.充电时Se2-发生的反应为Se2-+4[AlCl ]--4e-===SeCl +2[Al Cl ]-
4 2 2 7
答案 D解析 由图示可知,该电池放电时,Al为负极,电极反应式为Al+7[AlCl ]--3e-===4[Al Cl ]-,
4 2 7
V C@Se为正极,SeCl 发生的反应为SeCl +2[Al Cl ]-+4e-===Se2-+4[AlCl ]-,V3+发生的反应为V3++e-
2 2 2 2 7 4
===V2+ ;充电时,Al为阴极,电极反应式为4[Al Cl ]-+3e-===Al+7[AlCl ]-,V C@Se为阳极,Se2-发
2 7 4 2
生的反应为Se2-+4[AlCl ]--4e-===SeCl +2[Al Cl ] - ,V2+发生的反应为V2+ -e-===V3+,据此分析答题。
4 2 2 7
电池放电时,V C@Se为正极,SeCl 发生的反应为SeCl +2[Al Cl ]-+4e-===Se2-+4[AlCl ]-,[AlCl ]-
2 2 2 2 7 4 4
脱出V C@Se电极,A错误;[AlCl ]-、[Al Cl ]-通过离子交换膜嵌入和脱出,隔膜为阴离子交换膜,
2 4 2 7
B错误;当有1 mol Se2-参与反应时,V3+也同时发生反应,外电路转移电子数目大于4N ,C错误。
A
6.我国科学家开发出Mo
2
C/NiCu@C催化剂,设计了新型Zn⁃NH
3
电池,实现高效、连续的NH
3
到H
2
的
转化,装置如图所示。下列叙述错误的是( )
A.放电时,电极电势:a>b
B.充电时,a极反应式为2NH +6OH--6e-===N +6H O
3 2 2
C.放电时,生成11.2 L H (标准状况)时,有2 mol OH-向a极迁移
2
D.充电时,b极净增39 g时,电路中转移1.2 mol电子
答案 C
解析 由图可知,放电时,a电极为原电池的正极,水在正极得到电子,发生还原反应,生成氢气和氢氧
根离子,b电极为负极,碱性条件下锌失去电子,发生氧化反应,生成四羟基合锌离子,氢氧根离子通过
阴离子交换膜进入负极区;充电时,与直流电源正极相连的a电极为电解池的阳极,碱性条件下氨气在阳
极失去电子发生氧化反应,生成氮气和水,b电极为阴极,四羟基合锌离子在阴极得到电子发生还原反应,
生成锌和氢氧根离子,氢氧根离子通过阴离子交换膜进入阳极区。放电时,a极为正极,b极为负极,正极
电势高于负极,A项正确;放电时,a极为正极,电极反应式为2H O+2e-===2OH-+H ↑,n(H )=0.5 mol,则
2 2 2
有1 mol OH-向b极迁移,C项错误;充电时,b极为阴极,电极反应式为[Zn(OH) ]2-+2e-===Zn+4OH-,
4
39 g
n(Zn)= =0.6 mol,电路中转移1.2 mol电子,D项正确。
65 g·mol-1
7.储氢合金LaNi 储氢时的化学式为LaNi H (设各元素的价态均为0)。以LaNi H (m)和NiO(OH)(n)为电
5 5 6 5 6
极,KOH溶液为电解质溶液的二次电池结构如图所示(已知电池工作之前隔膜两侧电解质溶液的质量相
等)。下列说法正确的是( )
A.充电时,n极发生还原反应
B.充电时,电子流向:n→交换膜→m
C.放电时,m极的电极反应式为LaNi H -6e-+6OH-===LaNi +6H O
5 6 5 2
D.放电时,若转移1 mol e-,隔膜左侧电解质溶液的质量减少39 g
答案 C
解析 由题干图示信息可知,图中实线代表放电过程,放电时n极为正极,电极反应为6NiO(OH)+6e-
+6H O===6Ni(OH) +6OH-,m极为负极,电极反应为 LaNi H -6e-+6OH-===LaNi +6H O,虚线代表充电过
2 2 5 6 5 2
程,充电时n极为阳极,发生氧化反应,A错误;电子不能经过电解质溶液,B错误;放电时左侧为负极
室,右侧为正极室,原电池中电解质溶液中的阳离子移向正极,若转移1 mol e-,则有1 mol K+从左侧移向
右侧,即左侧溶液质量减少1 mol×39 g·mol-1=39 g,但同时根据电极反应LaNi H -6e-+6OH-===LaNi +6H O
5 6 5 2
可知,左侧溶液质量又增加1 mol H即增重1 g,故隔膜左侧电解质溶液的质量减少(39-1)g=38 g,D错误。
8.(2023·杭州第二中学高三模拟)由我国科学家设计的Mg⁃Li双盐电池的工作原理如图所示,下列说法错
误的是( )
A.放电时,正极电极反应式为FeS+2e-+2Li+===Fe+Li S
2
B.充电时,Mg电极发生还原反应
C.充电时,每生成1 mol Mg,电解质溶液质量减少24 g
D.电解液含离子迁移速率更快的Li+,提高了电流效率
答案 C
解析 放电时Mg转化为Mg2+,所以右侧电极为负极,左侧电极为正极,FeS得电子生成Fe和Li S,电极
2
反应式为FeS+2e-+2Li+===Fe+Li S,A正确;充电时Mg2+转化为Mg,被还原,Mg电极发生还原反应,B
2
正确;充电时阳极反应式为Fe+Li S-2e-===FeS+2Li+,每生成1 mol Mg,消耗1 mol Mg2+,转移2 mol电子,
2同时生成2 mol Li+,所以电解质溶液质量减少24 g-2×7 g=10 g,C错误;电解液中含离子迁移速率更快的
Li+,增强了导电性,提高了电流效率,D正确。